托法替布治疗难治性类风湿关节炎的分析
2022-06-06张娟余雅坤田晶晶黄逸晨朵瑞雪沈海丽
张娟 余雅坤 田晶晶 黄逸晨 朵瑞雪 沈海丽
1兰州大学第二医院风湿免疫科(兰州 730030);2兰州大学第二临床医学院(兰州 730030)
类风湿关节炎(rheumatoid arthritis,RA)是一种以侵袭性关节炎为特点的慢性炎症性疾病,常伴随严重残疾和多种并发症[1]。生物DMARDs的出现显著改善了RA 疗效,但仍有20%患者未达到低疾病活动度或临床缓解的治疗目标[2-4]。以往将经过传统DMARDs 规范治疗≥6 个月或生物DMARDs 治疗≥3 个月,病情仍处于中高疾病活动度的RA 定义为难治性RA(difficult⁃to⁃treat rheu⁃matoid arthritis,D2T RA)[2-3,5]。难治性RA 临床疗效差、骨质破坏和关节畸形率高,既往多采用3 种以上传统DMARD 联用、生物DMARD 联合传统DMARDs、免疫吸附和造血干细胞移植等方法治疗[6-10],6 个月的改善率在36.9%~57.5%,但存在胃肠道副反应明显、经济负担重、肝肾损伤等弊端,限制了上述方案的临床推广。托法替布(tofacitinib)是一种新型口服小分子Janus 激酶(JAKs)抑制剂,是首个获批用于RA 治疗的靶向合成DMARDs。研究显示托法替布对既往甲氨蝶呤(MTX)或肿瘤坏死因子拮抗剂(TNFi)不应答的患者有一定疗效[11-12]。由于托法替布在我国上市较晚且上市初期经济费用较高等原因,中国人群真实世界关于托法替布治疗难治性RA 疗效及安全性报道较少。本研究拟分析单中心托法替布治疗难治性RA 患者的疗效及安全性,以期为难治性RA 的临床治疗提供新的治疗策略。
1 对象与方法
1.1 研究对象 收集2019年11月至2021年2月就诊于兰州大学第二医院风湿免疫科门诊或住院经托法替布治疗的难治性RA 患者临床资料。纳入标准:(1)RA 诊断符合1987年ACR 制定RA 分类标准或2010年ACR/EULAR 关于RA 分类标准[13];(2)所有患者既往经历至少2 种传统DMARDs[其中一种为MTX 或来氟米特(LEF)]治疗≥6 个月或生物DMARDs 联合传统DMARDs 治疗≥3 个月疾病仍然处于中高度活动(DAS28CRP ≥3.2)。排除标准:(1)临床资料不完整者;(2)合并严重心、肺、肾等基础疾病者;(3)合并结核、带状疱疹等感染性疾病者;(4)合并关节外表现需联用泼尼松15 mg(或甲泼尼龙12 mg)以上及免疫抑制剂者。本研究方案获得兰州大学第二医院伦理委员会批准(伦理批件号:2021A⁃405)。本研究为回顾性研究,经伦理委员会批准免签知情同意书。
1.2 治疗方案 托法替布(正大天晴药业集团股份有限公司,规格5 mg/片,批准文号:国药准字H20193281)1次5 mg,1日2次,单药治疗或联合1种传统DMARDs,连续治疗24周。原服用泼尼松或甲泼尼龙者维持不变,4~6 周复查按每2 周减2.5 mg直至停用;治疗开始4 周内均联用萘普生0.5 g qd或依托考昔60 mg qd,后调整为按需服用;全程未联用生物DMARDs。
1.3 临床资料收集 收集患者的基线资料,包括性别、年龄、病程、合并症、并发症、既往用药以及基线、治疗后4、12 和24 周的28 个肿胀关节数、28 个压痛关节数、患者VAS疼痛指数、实验室指标等。
1.4 观察指标
1.4.1 疾病活动性指标 治疗前、治疗后4、12 和24 周的DAS28CRP、DAS28ESR、CRP、ESR、28 个肿胀关节数、28 个压痛关节数和患者VAS 疼痛指数。
1.4.2 安全性指标 血常规白细胞计数(WBC)、血红蛋白(Hb)、血小板计数(PLT);肝功能丙氨酸氨基转移酶(ALT)和门冬氨酸氨基转移酶(AST);肾功能血肌酐(Scr)。
1.5 统计学方法 采用SPSS 23.0 统计软件包进行统计学处理。计量资料不服从正态分布,采用M(P25,P75)进行统计描述,采用FriedmanM检验和两两比较的q检验进行统计推断;计数资料采用例(%)进行统计描述,采用χ2检验进行统计推断,检验水准α=0.05。
2 结果
2.1 基线资料 符合入排标准患者51 例,均完成24 周随访。治疗全程中MTX 用量维持在10~12.5 mg qw,LEF 用量为20 mg qd,原使用糖皮质激素患者中4 例在24 周随访结束时仍维持泼尼松2.5 mg qd 治疗,一般特征见表1。
表1 51 例难治性类风湿关节炎患者一般特征Tab.1 Basic characteristics of 51 patients with D2T RA ±s
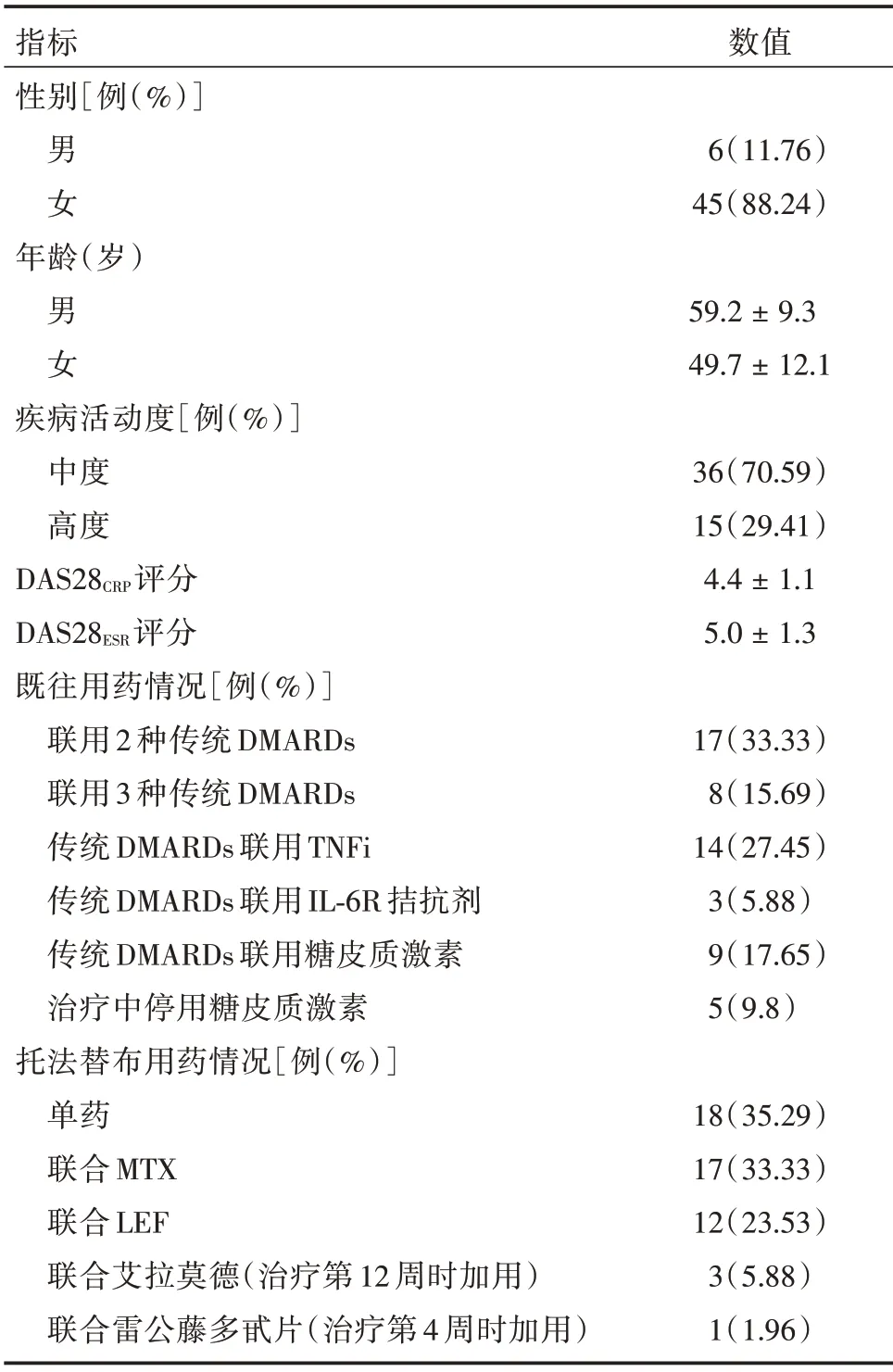
表1 51 例难治性类风湿关节炎患者一般特征Tab.1 Basic characteristics of 51 patients with D2T RA ±s
指标性别[例(%)]男 女年龄(岁)男 女疾病活动度[例(%)]中度高度DAS28CRP评分DAS28ESR评分既往用药情况[例(%)]联用2 种传统DMARDs联用3 种传统DMARDs传统DMARDs 联用TNFi传统DMARDs 联用IL⁃6R 拮抗剂传统DMARDs 联用糖皮质激素治疗中停用糖皮质激素托法替布用药情况[例(%)]单药联合MTX联合LEF联合艾拉莫德(治疗第12 周时加用)联合雷公藤多甙片(治疗第4 周时加用)数值6(11.76)45(88.24)59.2±9.3 49.7±12.1 36(70.59)15(29.41)4.4±1.1 5.0±1.3 17(33.33)8(15.69)14(27.45)3(5.88)9(17.65)5(9.8)18(35.29)17(33.33)12(23.53)3(5.88)1(1.96)
2.2 疗效分析
2.2.1 托法替布治疗疗效分析 相比治疗前,托法替布 治 疗4、12 和24 周 后DAS28CRP、DAS28ESR、CRP、ESR、28个肿胀关节数、28个压痛关节数、VAS疼痛指数均明显下降,差异有统计学意义(P<0.05);治疗12 和24 周相比治疗4 周,DAS28CRP、DAS28ESR、28 个肿胀关节数、28 个压痛关节数、VAS疼痛指数均明显下降,差异有统计学意义(P<0.05);ESR 在治疗24 周相比治疗4 周明显下降,差异有统计学意义(P<0.05,表2)。
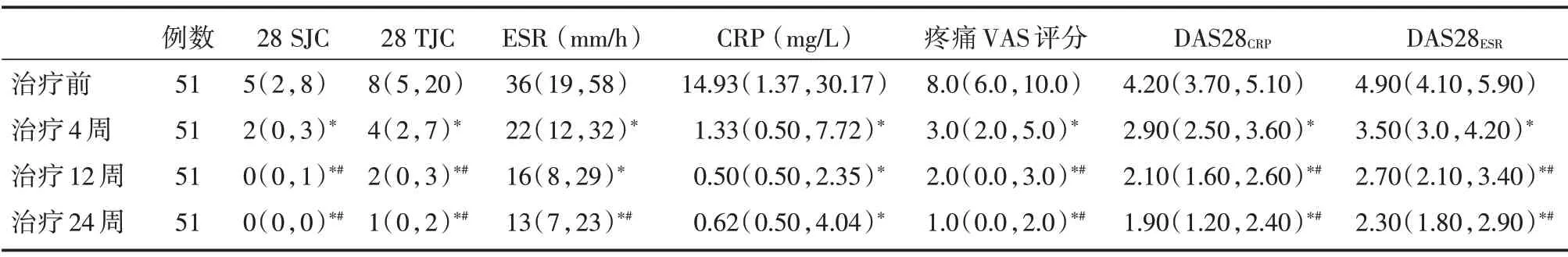
表2 难治性RA 经托法替布治疗前后各项指标变化Tab.2 The changes of indicators in patients with D2T RA after treat with tofacitinib M(P25,P75)
2.2.2 托法替布治疗后低疾病活动度和临床缓解达标率对比分析 托法替布治疗4、12 和24 周,DAS28CRP和DAS28ESR的低疾病活动度和临床缓解达标率略有不同,但二者临床缓解达标率差异有统计学意义(P<0.001,表3)。
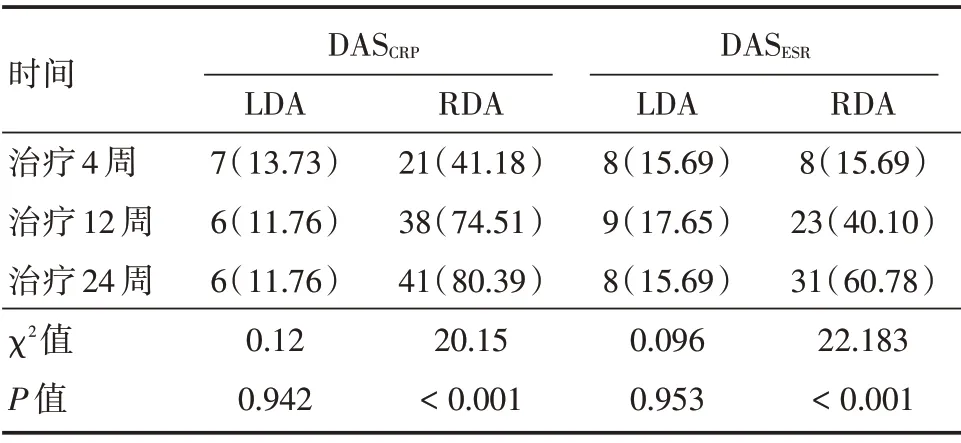
表3 托法替布治疗后DAS28CRP和DAS28ESR达标率比较Tab.3 Comparison of DAS28CRP and DAS28ESR control rate after treatment 例(%)
2.2.3 托法替布治疗后24 周不同分组临床缓解达标率比较 托法替布治疗后24 周,既往传统DMARDs 不应答组和既往生物DMARDs 不应答组的DAS28CRP的临床缓解达标率分别为82.35%和76.47%,DAS28ESR的临床缓解达标率分别为55.88%和70.59%,二者差异均无统计学意义(P>0.05,表4)。

表4 托法替布治疗24 周既往传统DMARDs 治疗组和生物DMARDs 治疗组间患者临床缓解达标率比较Tab.4 Comparison proportion of target between Pre⁃csDMARDs group and Pre⁃bDMARDs group after treatment例(%)
2.3 达标率生存分析比较 托法替布治疗4、12、24 周的低疾病活动度和临床缓解的达标率生存分析显示,DAS28CRP临床缓解在治疗4 周改善最为明显,DAS28ESR临床缓解在治疗12 周改善最为明显,随着治疗时间的延长,低疾病活动度和临床缓解改善呈持续下降趋势(图1)。
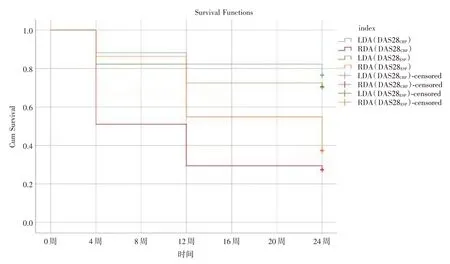
图1 托法替布治疗后低疾病活动度和临床缓解的达标率生存分析Fig.1 LDA and RDA survival analysis after tofacitinib treatment
2.4 安全性分析 血红蛋白、血小板和血肌酐治疗4、12 和24 周相比治疗前差异无统计学意义(P>0.05,表5);其中3 例患者治疗24 周时出现轻度肝损害,ALT 分别是54、73、76 U/L,AST 分别是51、57、69 U/L,给予保肝治疗后恢复正常;1 例出现呼吸道感染,经抗感染治疗后恢复。无带状疱疹、血栓、贫血和恶性肿瘤的发生。
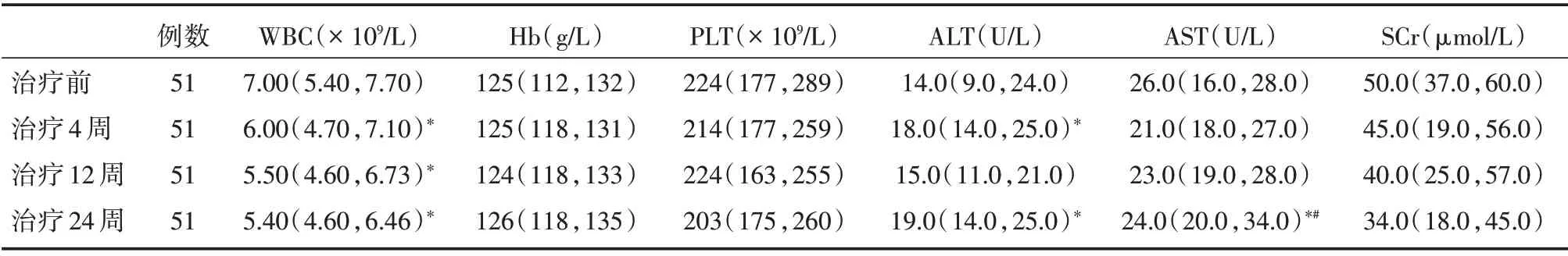
表5 难治性RA 患者经托法替布治疗前后安全性指标变化Tab.5 The changes of security indexes in patients with D2T RA after treat with tofacitinib M(P25,P75)
3 讨论
RA 是一种常见关节炎,随着对其发病机制认识的不断深入,治疗药物也在不断增加,但其达标现状却不容乐观。我国RA 横断面调查显示仅有14.88%可达到DAS28CRP缓解[14],临床缓解达标率仅为20%[15],仍有相当多患者属于难治性RA范畴。EULAR最新关于难治性RA的定义是传统DMARDs治疗失败后(除非有禁忌证),≥2 种作用机制不同的生物DMARDs/靶向DMARDs 治疗失败,但症状和(或)体征持续存在的患者[16-17]。苏茵教授团队结合我国临床实践,将2 种或2 种以上传统DMARDs(至少一种为MTX或LEF)治疗至少6个月或生物DMARDs 联合传统DMARDs 治疗至少3 个月,病情仍处于高疾病活动度的RA 定义为难治性RA[18];本研究中纳入的患者,受地域和经济条件的限制,生物制剂使用率低,未能满足我国和EU⁃LAR 最新关于难治性RA 的诊断标准,但均符合传统难治性RA 标准,并具有女性居多、长病程(平均4.48年)的特点,与文献报道[14]临床特点基本相符。
近年来,难治性RA 的治疗方法一直在不断的探索中,针对多重耐药的优化治疗策略是更换治疗靶点[19],2021 ACR 关于RA 的诊治指南中建议初始治疗未达标者换用JAKi[20]。托法替布是一种JAK1/JAK3 选择性抑制剂,通过抑制JAK⁃STAT 通路直接或间接的阻断多种细胞因子从而抑制RA炎症反应、减轻关节损伤。临床实践证明托法替布可有效控制RA 疾病活动,但对难治性RA 的疗效国内鲜有报道。本研究回顾性分析托法替布治疗难治性RA 的疗效,结果显示托法替布可有效改善患者关节肿痛症状和体征,降低VAS 评分和疾病活动度,短期内(4 周)即可降低患者CRP 和ESR,与文献报道基本一致[12,22-23]。此外,本研究还评估了托法替布治疗难治性RA 的安全性,旨为真实世界托法替布在难治性RA 的应用提供一定的参考价值。
既往研究报道托法替布治疗TNFi 反应不充分(TNFi⁃IR)的难治性RA 的患者,症状、体征以及身体功能均快速改善且安全性可控,57.5%的患者在治疗6 个月内达到CDAI50 应答[24];本研究对比托法替布治疗4、12、24 周DAS28CRP和DAS28ESR的达标率,结果显示治疗4 周54.55%患者实现DAS28CRP达标,治疗24 周达标率可达80.39%,肿胀关节数、压痛关节数等体征和CRP、ESR 炎性指标均有明显改善;采用生存分析方法比较不同时间节点难治性RA 的缓解率,发现疾病活动度在治疗4 周即出现明显下降,缓解率随治疗时间延长而持续下降至24周。同时,本研究还评估了既往不同治疗经历患者对托法替布的治疗反应,既往未使用过生物DMARDs 的难治性RA 相比使用过的患者更容易达标(82.35%vs.76.47%),但缓解率二者差异无统计学医院,考虑与基础样本量过少有关(既往生物DMARDs 治疗不答应组仅有17 例),与文献报道的未使用过生物制剂的难治性RA 患者DAS28CRP改善更明显(5.16 降至2.14)的研究结果相近[25]。本研究说明托法替布可快速改善难治性RA 患者的症状、炎性指标和疾病活动度,疗效持续稳定。
除了疗效,JAKi 的安全性是临床关注的另一个重点,JAK⁃STAT 通路对淋巴细胞生成和红细胞生成等细胞稳态非常重要[26],抑制该通路最常见的不良反应为感染、造血功能异常、恶性肿瘤风险等。托法替布主要选择性抑制JAK3,其次是JAK1,对JAK2 的抑制作用较弱,目前报道的亚洲人群中不良反应以上呼吸道感染和带状疱疹病毒再激活多见,日本和韩国的风险最高[27-28]。本研究中主要不良反应为上呼吸道感染和轻度肝损伤,无严重感染、血栓、贫血和恶性肿瘤的发生,安全性相对较好,考虑一方面观察时间较短,另一方面托法替布对JAK2 的影响较小有关。
综上所述,难治性RA 临床疗效差、达标率低,是RA 的治疗难点。本研究结果初步说明托法替布可有效改善难治性RA 患者症状、体征和炎性指标,短期内降低疾病活动度且安全性良好,既往未使用生物制剂的难治性RA 患者更容易达到低疾病活动度或临床缓解。不良反应为可控制的上呼吸道感染和肝功能异常。但由于本研究为单中心的回顾性分析,仍存在如下不足:(1)治疗24 周DAS28 的临床缓解和低疾病活动度达标率相比文献报道略高,可能与回顾性研究方法有关,在病例纳入方面因临床资料不全会排除部分未按时复查、疗程尚不足24 周的患者,导致样本量较小,影响了达标率结果;(2)影像学、类风湿因子、抗环瓜氨酸肽以及IL⁃6、TNF⁃α 等非常规检查项目因资料不全故未纳入研究,影响了病情评估的全面性;(3)随访时间相对较短。因此,托法替布在真实世界对难治性RA 的疗效有待在未来的多中心、大样本、长期前瞻性研究进一步观察。
