酸化水玻璃对重晶石与白云石浮选分离行为的影响
2022-06-05蒋海勇张发明陈志杰张辉齐越超
蒋海勇,张发明,陈志杰,张辉,齐越超
(广东省科学院资源利用与稀土开发研究所,广州粤有研矿物资源科技有限公司,稀有金属分离与综合利用国家重点实验室,广东省矿产资源开发和综合利用重点实验室,广东 广州 510650)
重晶石具有比重大,无毒、无磁性、易吸收χ 和γ 射线等特性,因而广泛应用于石油、化工、油漆等工业部门,其中80%~90%被用作石油旋转井中的泥浆加重剂[1]。在一些矿床中,白云石通常与重晶石共生嵌布,重晶石与白云石都含有Ba2+、Ca2+和Mg2+同一族元素离子,他们的可浮性非常接近,由于白云石的存在导致重晶石浮选回收的过程中存在很大的困难[2-3]。本文在十二烷基磺酸钠浮选体系中,采用重晶石与白云石单矿物研究不同酸化程度的水玻璃对重晶石和白云石浮选分离行为的影响,并对其可能的作用机理进行分析,为实现低品位重晶石和白云石的高效分离提供系统的技术支持和理论依据。
1 原料、试剂及仪器和实验方法
1.1 原 料
实验所用重晶石和白云石单矿物分别产自广西和河北某矿山。将经手选挑出的品质较好的重晶石和白云石矿石敲碎,采用陶瓷球磨机细磨后,筛分出-0.075+0.038 mm 和-0.038 mm 两个粒级的矿物颗粒,再用淘盘除去微量杂质,最后经蒸馏水多次洗涤、自然晾干获得了重晶石和白云石单矿物试样。经矿物学分析检测知重晶石和白云石的纯度分别为98.85%、99.98%,XRD 分析结果见图1 和图2。
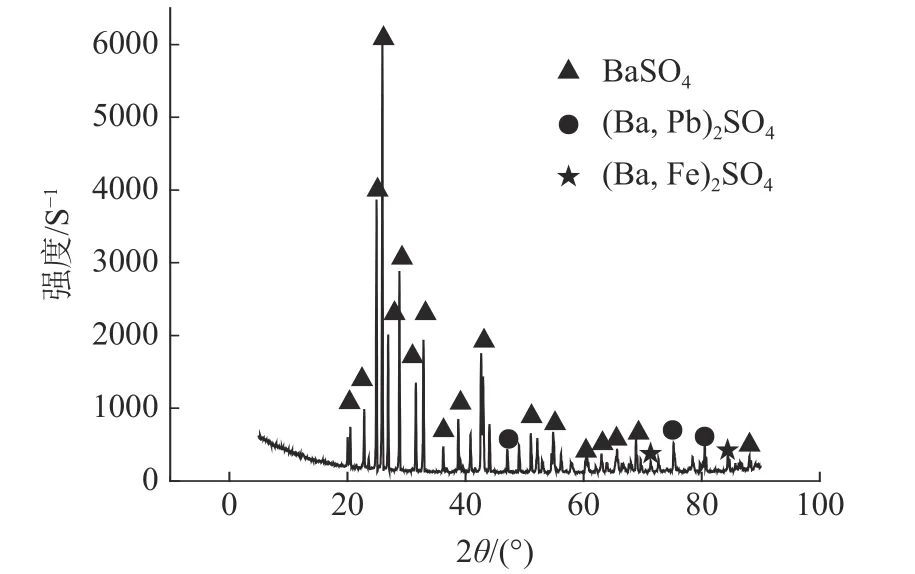
图1 重晶石的XRDFig.1 X-ray diffraction of barite

图2 白云石的XRDFig.2 X-ray diffraction of dolomite
1.2 试剂及设备
氢氧化钠、硫酸、盐酸、水玻璃、十二烷基磺酸钠等药剂,均采用分析纯;PANalytical X’pert PRO 型X 射线衍射仪(Cu 靶,最大功率2.2 kW),XJM-100 陶瓷球磨机,RexpHS-3C 型pH 计,JE502 型电子天平,DF-2 磁力搅拌器,DL5C 型真空抽滤机,XFG 挂槽式浮选机,SK200H 超声波清洗仪,101A-1 型远红外快速恒温干燥箱,DELSA44OSX 型精密Zeta-电位测定仪,WPF-520A 红外光谱仪,WPF-520A 视频接触角测定仪。
1.3 实验方法
在常温条件下,采用主轴转速为1750 r/min的XFG-76 型浮选机进行单矿物浮选实验:每次实验加2 g 矿样进浮选槽内,然后再加30 mL 的去离子水,搅拌1 min 后再采用氢氧化钠和盐酸进行矿浆pH 值调整;加入酸碱后搅拌2 min,采用RexpHS-3C 型pH 计测定浮选环境中的pH 值;浮选环境中的pH 值稳定后加入抑制剂,搅拌2 min;搅拌时间完成后再加入捕收剂,并搅拌2 min;最后浮选刮泡,获得的泡沫精矿与尾矿分别过滤、低温烘干、称量,计算出浮选回收率。
通过利用WPF-520A 视频接触角测定仪、DELSA44OSX 型精密Zeta-电位测定仪和WPF-520A 红外光谱仪对重晶石和白云石单矿物分别进行接触角的测量、Zeta 电位的测试以及红外光谱的分析,然后根据实验结果对TS11 可能的作用原理进行分析和研究。
2 实验结果与讨论
2.1 单矿物浮选条件实验
通过进行单矿物浮选实验,探索出不同pH 值以及不同十二烷基磺酸钠浓度的条件下对重晶石与白云石浮选行为的影响,实验结果见图3。

图3 十二烷基磺酸钠浓度和pH 对回收率的影响Fig.3 Effect on recovery of sodium dodecyl sulfonate concentration and pH
图3 中曲线3 和曲线4 表明,十二烷基磺酸钠浓度为8 mg/L 的条件下,不同的pH 值对重晶石与白云石回收率的影响。随着pH 值的增大重晶石与白云石两者的回收率均先升高而后趋于平稳,拐点在pH=10 左右,当pH≥10 以后,两者的回收率增幅逐渐趋向于零。曲线1、2 分别表示矿浆在pH 值为9.5 的条件下,十二烷基磺酸钠浓度对重晶石、白云石回收率的影响。重晶石、白云石两种矿物的回收率都随十二烷基磺酸钠浓度增大而升高,并且浓度大于8 mg/L 后,重晶石的回收率增加趋向于平缓并最终稳定在95%以上,同时白云石的回收率也最终稳定在70%以上。因此选定十二烷基磺酸钠浮选重晶石与白云石的后续实验条件为:十二烷基磺酸钠固定用量为8 mg/L,浮选环境pH 值为9.5。
2.2 水玻璃酸化程度实验
李沛伦等发现将硫酸与水玻璃混合可以提高水玻璃的抑制能力[4]。所以,在酸化水玻璃的用量(80 mg/L)一定的前提下通过改变硫酸(H2SO4)的加入量,改变酸化水玻璃的酸化程度,然后通过单矿物浮选实验考察酸化水玻璃的酸化程度对重晶石与白云石回收率的影响,实验结果见图4。
从图4 可以看出,随着水玻璃的酸化程度(硫酸Mg/L:水玻璃Mg/L)增大,重晶石的回收率的先增加后逐渐下降;水玻璃的酸化程度与白云石的回收率呈正相关。当酸化程度高于1 后,重晶石的回收率逐渐下降,然而白云石的回收率却逐渐升高。当水玻璃的酸化程度为1 时,重晶石的回收率抵达峰值,此时回收率为89.72%,而白云石此时的回收率只有9.35%,显示出对两种矿物良好的选择性抑制。因此选择水玻璃的酸化程度为1 的配比进行下面实验,此时的浮选环境pH 值为6.5 左右,并将其命名为TS11。

图4 水玻璃酸化程度对回收率的影响Fig.4 Effect on recovery of water glass acidification degree
2.3 TS11 药剂用量实验
十二烷基磺酸钠用量固定为8 mg/L 的条件中,为研究TS11 用量对重晶石和白云石浮选分离行为的影响,进行了TS11 用量条件实验,实验结果见图5。
从图5 表明,随着TS11 的用量增加重晶石与白云石的回收率均逐渐下降,当TS11 用量超过80 mg/L 后,白云石的回收率逐渐趋于平缓但重晶石的回收率仍在逐渐下降。当TS11 用量为80 mg/L时,测得此时矿浆pH 值为6~6.5,重晶石的回收率为89.72%,而此时白云石的回收率仅为9.35%。由此表明,当TS11 用量为80 mg/L 时,TS11 对白云石表现出较好的抑制效果,但对重晶石的可浮性影响较小。

图5 TS11 用量对回收率的影响Fig.5 Effect on recovery of TS11 dosage
2.4 接触角测量实验
矿物接触角θ 能直接反映出矿物对水的亲疏程度,重晶石和白云石与不同用量的TS11 作用后其矿物接触角θ 会发生改变,因此能表征矿物可浮性大小的指标(1-cosθ)也必然会发生改变。为了研究TS11 用量对重晶石与白云石可浮性的影响,固定十二烷基磺酸钠用量为8 mg/L,随着TS11 用量的改变两种矿物的接触角θ 和可浮性(1-cosθ)的变化见表1。

表1 TS11 用量对接触角的影响Table 1 Effect on contact angle of TS11 dosage
从表1 表明,TS11 用量为0 mg/L 时,重晶石和白云石经十二烷基磺酸钠作用后疏水性都较好,可浮性分别为1.57 和0.74。随着TS11 用量的增加80 mg/L,重晶石的可浮性从1.57 下降到1.42,相对TS11 为0 mg/L 时下降9.55%,表明重晶石的可浮性变化不大;但是白云山的可浮性从0.74 下降到0.07,相对TS11 为0 mg/L 时下降90.54%,这表明对白云石的可浮性的变化影响非常大。TS11 可能在白云石表面与发生竞争吸附导致白云石的可浮性随着TS11 用量的增加逐渐降低,具有强烈的亲水性。在TS11 的用量超过80 mg/L 后,白云石的可浮性降到0.07 以下,白云石此时表现为强烈的亲水性,与重晶石的可浮性相差甚大,从而能使重晶石与白云石实现高效分离,这与TS11 用量浮选实验的结果相符。
2.5 Zeta 电位实验
水玻璃主要成分为硅酸钠(Na2O•RSiO2),水解后显强碱弱酸盐[5]。在浮选中起到抑制效果的成分是其水解生产的,水玻璃在水中具有以下水解平衡:

由公式1~7 可以计算出水玻璃各组分的ωpH 关系(见图6)。由图6 可知,当pH<9.4 时,Si(OH)4的含量占绝对优势,当9.4≤pH≤12.6 时,的含量最多,pH≥ 12.6 时,为最优组分。虽然水玻璃的各种水解组分均可能抑制白云石的可浮性,但必须是该pH 值条件下介质中的最优组分起到主要抑制作用[5]。根据上述的酸化程度实验知TS11 的pH=6.5,因此Si(OH)4是S11 的优势组分。在弱碱与弱酸性环境中,Si(OH)4主要以胶体形式存在,矿浆中的存在可能使Si(OH)4以亲水性更强的{(SiO2·yH2O)m·的形式存在[6]。通过Zeta电位的变化分析TS11 的作用原理,TS11 的加入对十二烷基磺酸钠作用下的重晶石与白云石Zeta 电位的影响见图7。
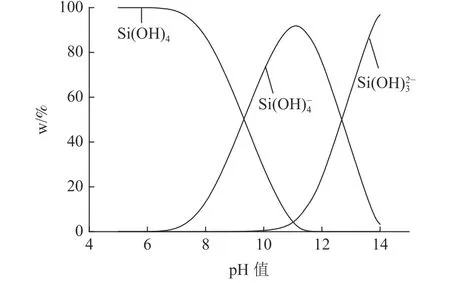
图6 水玻璃各组分的ω-pH 关系Fig.6 ω-pH relation chart of water glass each component
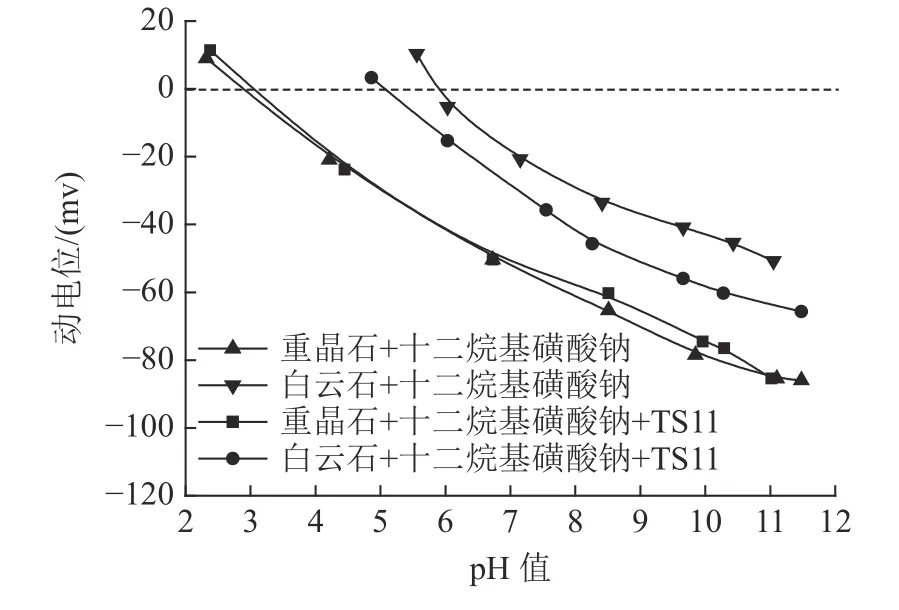
图7 TS11 对矿物Zeta 电位的影响Fig.7 Effect on mineral Zeta potential of TS11
由图7 可知,在十二烷基磺酸钠浮选体系下,TS11 加入后重晶石Zeta 电位几乎没有负向移动,分析可能是由于十二烷基磺酸钠在重晶石表面有具较强的表面吸附,TS11 水解组分Si(OH)4对于十二烷基磺酸钠在重晶石表面吸附影响较少,但TS11 的加入使白云石的Zeta 动电位向负方向移动较大。分析可能是TS11 水解组分Si(OH)4与白云石表面的Ca2+发生了强烈的表面吸附作用,从而抑制白云石表面吸附,致使其Zeta 电位向负方向大幅度移动,这与上面单矿物实验相吻合。
2.6 红外光谱实验
采用红外光谱仪分析化学键的特征波数来鉴别TS11 与十二烷基磺酸钠体系中重晶石与白云石矿物表面与药剂相互作用的结果[7],实验结果见图8。
从图8 可以发现,十二烷基磺酸钠红外光谱(a)中,(2950.40、2919.40 和2850.35)cm-1为烷基-CH3和-CH2-的3 个削峰的伸缩振动吸收峰,磺酸盐(S=O=S)反对称伸缩振动吸收峰位于(1295.93、1240.00、1205.30 和1170.58 )cm-1处,而位于(1166.44 和1041.37)cm-1处为对称伸缩振动吸收峰;白云石红外光谱(b)中,反对称伸缩振动吸收峰位于1445.06 cm-1,面外弯曲振动吸收峰位于880.01 cm-1处,面内弯曲振动吸收峰位于727.27 cm-1处;重晶石红外光谱(c)中,SO42-较强对称伸缩振动吸收峰位于(1080.06和1180.08)cm-1处,SO42-较弱的不对称变角吸收峰则位于(610.57、632.81 和 980.93 )cm-1。
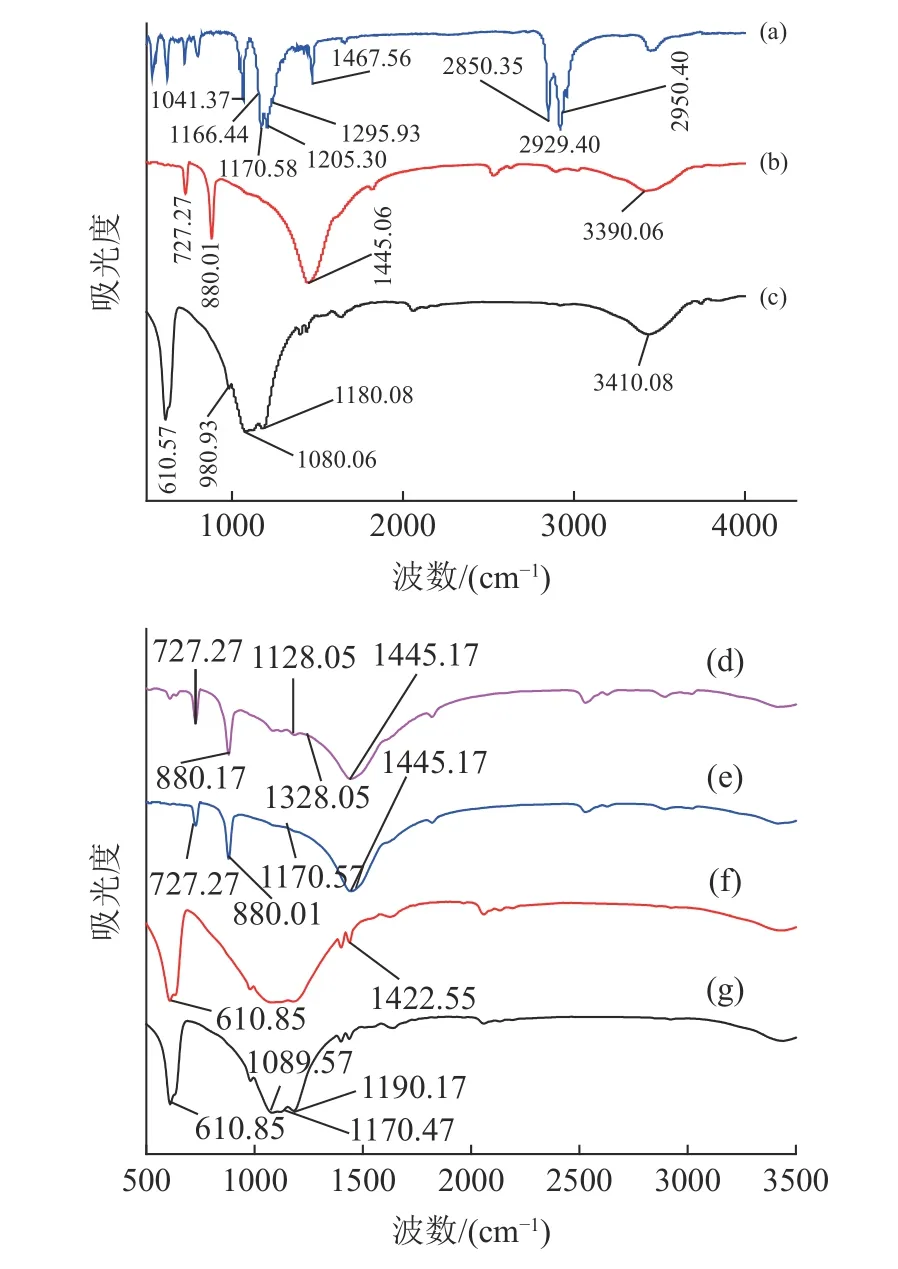
图8 矿物与TS11 相互作用前后红外光谱Fig.8 I Infrared spectrum of TS11 and mineral effects before and after
重晶石+十二烷基磺酸钠作用后红外光谱(g)表明,位于(1089.57 和1190.17 )cm-1处的对称伸缩振动吸收峰于重晶石红外光谱(c)分别发生了 8 cm-1与10 cm-1的位移,并在1170.47 cm-1处有新吸收峰生成,表明重晶石表面裸露的Ba2+与发生化学吸附,并在矿物表面生成相对稳定的十二烷基磺酸钡。白云石+十二烷基磺酸钠作用后红外光谱(e)表明,在1170.57 cm-1处有新吸收峰生成,可能是与白云石表面暴露的Ca2+发生化学反应生成稳定的十二烷基磺酸钙。重晶石+十二烷基磺酸钠+TS11 红外光谱(f)与重晶石+十二烷基磺酸钠红外光谱(g)相比吸附基本没有变化,说明Si(OH)4对重晶石的可浮性影响不大。重晶石+十二烷基磺酸钠+TS11 红外光谱(d)与白云石+十二烷基磺酸钠(e)相比在1100~1450 cm-1范围内出现了Si(OH)4的Si-OH 特征吸收峰,说明硅酸胶粒Si(OH)4凭借着更强劲的竞争吸附能力与亲水性挤走了在重晶石表面吸附的,从而使白云石亲水受到抑制。
3 结论
(1)在十二烷基磺酸钠浮选体系中进行重晶石与白云石的浮选分离行为研究表明,TS11(pH=6.5)能高效地实现对白云石的选择性抑制,而对重晶石的可浮性影响较小。
(2)酸化程度过低或者过高的水玻璃对重晶石和白云石的分选效果都不佳,酸化程度为1 的水玻璃(TS11)的分选效果最好。
(3)TS11 水解生成亲水性很强的硅酸胶粒Si(OH)4与白云石表面的Ca2+发生较强的化学吸附,并通过竞争吸附阻止白云石表面吸附,从而导致白云石的可浮性急剧降低,表现出强烈的亲水性;但对经十二烷基磺酸钠作用后的重晶石的可浮性影响较少。因此在十二烷基磺酸钠浮选体系下,TS11 对重晶石与白云石浮选分离行为具有良好的选择性抑制作用。
