纳豆软胶囊功效成分安全性及免疫功能研究
2022-06-05潘钰夏海华叶阳曲晓军于冲
潘钰,夏海华,叶阳,曲晓军,于冲
(黑龙江省科学院微生物研究所,哈尔滨 150010)
纳豆是一种日本传统的发酵大豆食品,众所周知,纳豆营养丰富,具有辅助降血脂、调节血糖、增强免疫力等功效,对健康有益,它的主要活性成分纳豆激酶具有很强的溶解血栓功能[1-2],Oba Mami等[3]最新研究发现纳豆提取物含有一种蛋白酶,能通过水解病毒蛋白质抑制病毒感染,纳豆激酶粉末可与其他辅助成分复合,作为保健食品开发,预防和治疗心血管疾病[4-5]。
本研究在前期研究[6-7]的基础上,探索以纳豆冻干粉、低聚果糖、亚麻籽油为主要功效成分复配成的纳豆软胶囊的安全性及功能,通过对胶囊内容物进行急性毒性试验与30 d喂养试验对其安全性进行评价,并研究其对小鼠细胞免疫、体液免疫、单核-巨噬细胞功能和自然杀伤细胞(natural killer cell,NK)活性的影响,为纳豆软胶囊作为保健食品的研究和开发提供了理论及试验依据。
1 材料和方法
1.1 材料
样品:纳豆软胶囊,由黑龙江省科学院微生物研究所提供,规格为0.5 g/粒,储存条件为密封,口服,按60 kg体重计算,推荐剂量为成人3次/d,每次2粒。取纳豆软胶囊内容物作为试验的样品。
1.2 试剂
试验动物:ICR小鼠SPF级、Wistar大鼠及饲料:长春市亿斯实验动物技术有限责任公司;试验动物使用许可证号:SYXK-(吉)2010-0011;试验条件合格证:吉动设字10-1005;饲养条件:温度20~22 ℃,相对湿度40%~70%。绵阳红细胞(SRBC)、生理盐水、Hank's液、RPMI1640培养液、Giemsa染液等:深圳迈瑞生物医疗电子股份有限公司。
1.3 主要仪器与设备
Olympus-CH显微镜 日本奥林巴斯株式会社;HPP110恒温培养箱、PURA22电热恒温水浴箱 瑞轩电子科技(上海)有限公司;SYSMEX XT-1800i全自动血液分析仪 上海涵飞医疗器械有限公司;JE203GE电子天平 梅特勒-托利多仪器(上海)有限公司;Infinite M200 Pro酶标仪 帝肯(上海)贸易有限公司;ZHJH-C1115C超净工作台 北京中仪友信科技有限公司。
1.4 方法
1.4.1 急性毒性试验[8]
采用最大耐受剂量法,剂量为24.8 g/kg BW,取31.0 g样品溶于植物油至50.0 mL,小鼠禁食不禁水16 h后,间隔4 h灌胃2次,每次灌胃量0.2 mL/10 g BW,灌胃后观察14 d并记录下小鼠的中毒情况,在第14天称量体重,计算增重,试验结束后对小鼠做大体解剖,根据毒性分级标准评价受试物的急性毒性。
1.4.2 骨髓细胞微核试验
采用间隔24 h两次经口灌胃法,各组每次灌胃量为0.2 mL/10 g BW,试验设高(10.0 g/kg BW)、中(5.0 g/kg BW)、低(2.5 g/kg BW)3个剂量组,植物油为阴性对照,40 mg/kg BW剂量的环磷酰胺为阳性对照,于末次灌胃后6 h,处死小鼠,制备骨髓液并涂片,经固定和染色后,于光学显微镜下计数。
1.4.3 精子畸变试验
采用经口灌胃方式给予小鼠受试物[9],连续5 d每天灌胃一次,灌胃量及分组同1.4.2,经过一定时间后处死小鼠,取其附睾制备涂片,经固定、染色,显微镜下计数畸形精子。
1.4.4 Ames试验
Ames试验即沙门氏菌回复突变试验,采用平板掺入法,选取5000,1000,200,40,8 μg/皿5个受试物剂量,利用4株鼠伤寒沙门氏菌组氨酸营养缺陷型菌株,具体操作详见文献[10]。
1.4.5 30 d喂养试验[11]
采用经口灌胃给予受试物,将高、中、低3个试验组(分别取样50.0,37.5,25.0 g至100 mL植物油中)及对照组均按1.0 mL/100 g BW的量灌胃,对照组给予植物油。观察大鼠一般情况,检测大鼠血液学指标、血液生化指标,大体解剖后称量脏器质量,对大鼠主要脏器进行组织病理学观察。
1.4.6 免疫功能学评价检验
按照卫生部颁发的《保健食品检验与评价技术规范》中增强免疫力功能检验方法操作[12],包括测定脏器/体重比值、迟发型变态反应、半数溶血值(HC50)、NK细胞活性、小鼠碳廓清试验、小鼠腹腔巨噬细胞吞噬鸡红细胞试验。
1.4.7 试验数据统计
采用SPSS统计分析软件处理数据,进行单因素方差分析,试验分析结果用平均数±标准差(x±s)形式表示,以P<0.05为差异显著性判断标准。
2 结果与分析
2.1 急性毒性试验结果
小鼠经最大耐受剂量灌胃后14 d内,雌性、雄性小鼠均未观察到异常症状,无死亡,最大耐受剂量(MTD)均>24.80 g/kg BW。根据急性毒性半数致死剂量分级,判断纳豆软胶囊内容物属无毒级。
2.2 骨髓细胞微核试验结果
微核试验是用于染色体损伤和干扰细胞有丝分裂的化学毒物的快速检测方法。3个剂量组微核率与阴性对照相比,差异均无显著性(P>0.05);阳性对照与阴性对照的微核率比较,差异极显著(P<0.01),各剂量组PCE与NCE的比值均高于对照组的20%,结果见图1。纳豆软胶囊内容物小鼠骨髓细胞微核试验为阴性。

图1 小鼠骨髓细胞微核试验结果(x±s, n=5)Fig.1 The results of mice bone marrow micronucleus test (x±s, n=5)
2.3 精子畸变试验结果
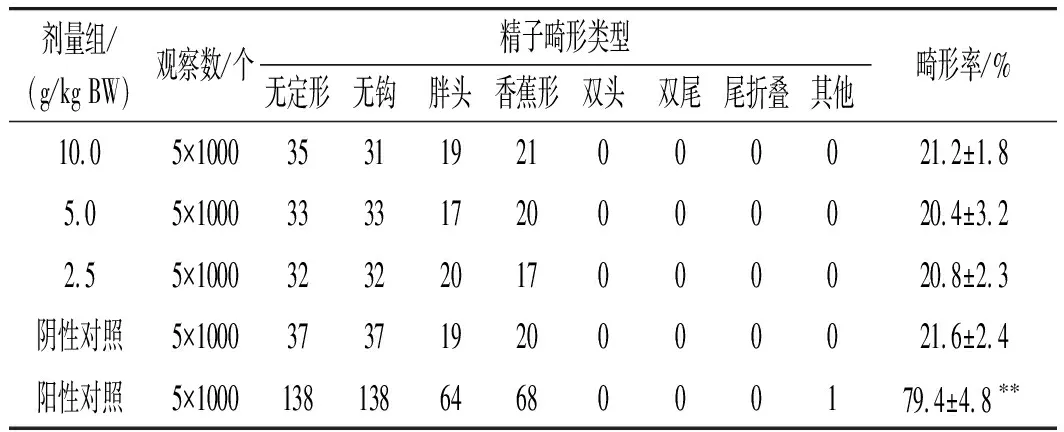
表1 纳豆软胶囊对小鼠精子畸形发生率的影响(x±s, n=5)Table 1 Effect of natto soft capsules on the sperm malformation rate of mice (x±s, n=5)
经统计学分析,由表1可知,各剂量组精子畸形发生率与阴性对照比较无显著性差异(P>0.05);阳性对照与阴性对照比较差异极显著(P<0.01)。纳豆软胶囊内容物小鼠精子畸变试验结果为阴性。
2.4 Ames试验结果
将纳豆软胶囊内容物在4株TA97、TA98、TA100、TA102鼠伤寒沙门氏菌组氨酸营养缺陷型突变株中进行平板掺入试验,无论加与不加S9,不同纳豆胶囊内容物含量组均未显著增加试验菌株回复突变菌落数,判定沙门氏菌回复突变试验结果为阴性。
2.5 30 d喂养试验结果
2.5.1 纳豆软胶囊对大鼠体重的影响
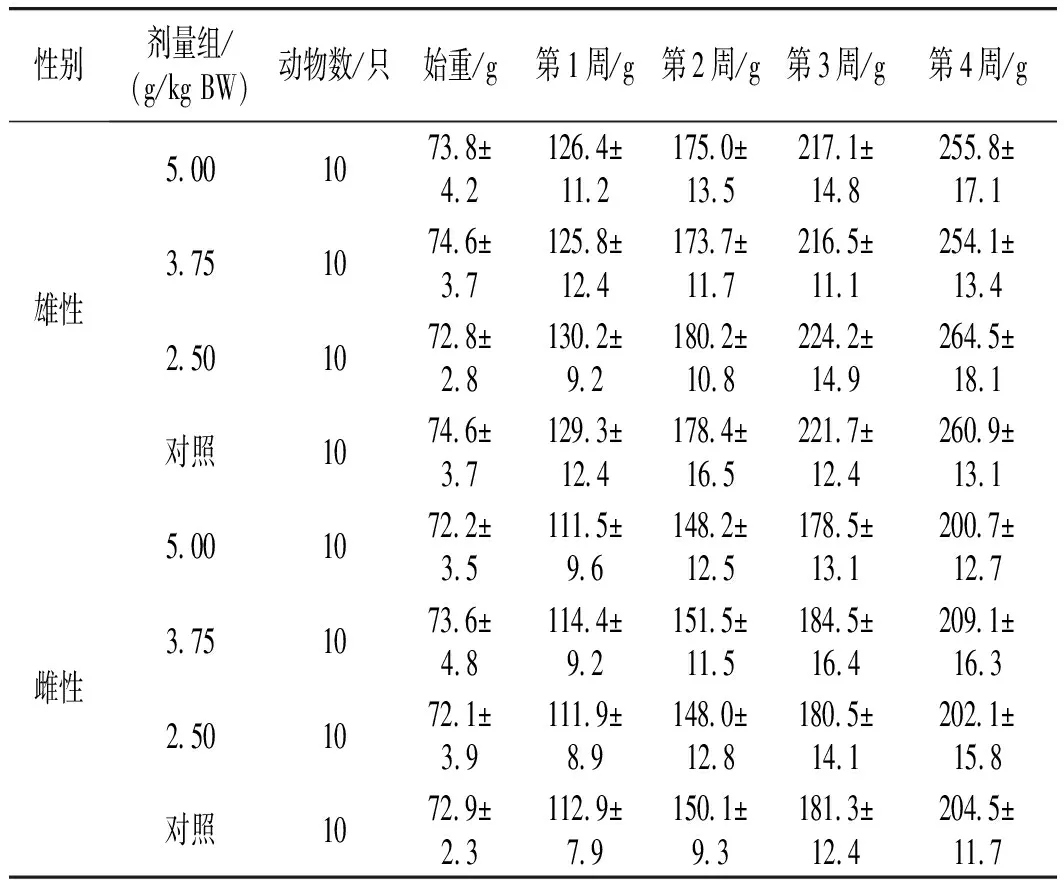
表2 纳豆软胶囊对大鼠体重的影响(x±s, n=10)Table 2 Effect of natto soft capsules on the body weight of rats (x±s, n=10)
由表2可知,各剂量组不同性别大鼠生长活动正常,未见异常,各组大鼠体重与对照组比较无显著差异(P>0.05),说明不同含量纳豆胶囊内容物未对大鼠的体重产生明显影响。
2.5.2 纳豆软胶囊对大鼠食物利用率的影响
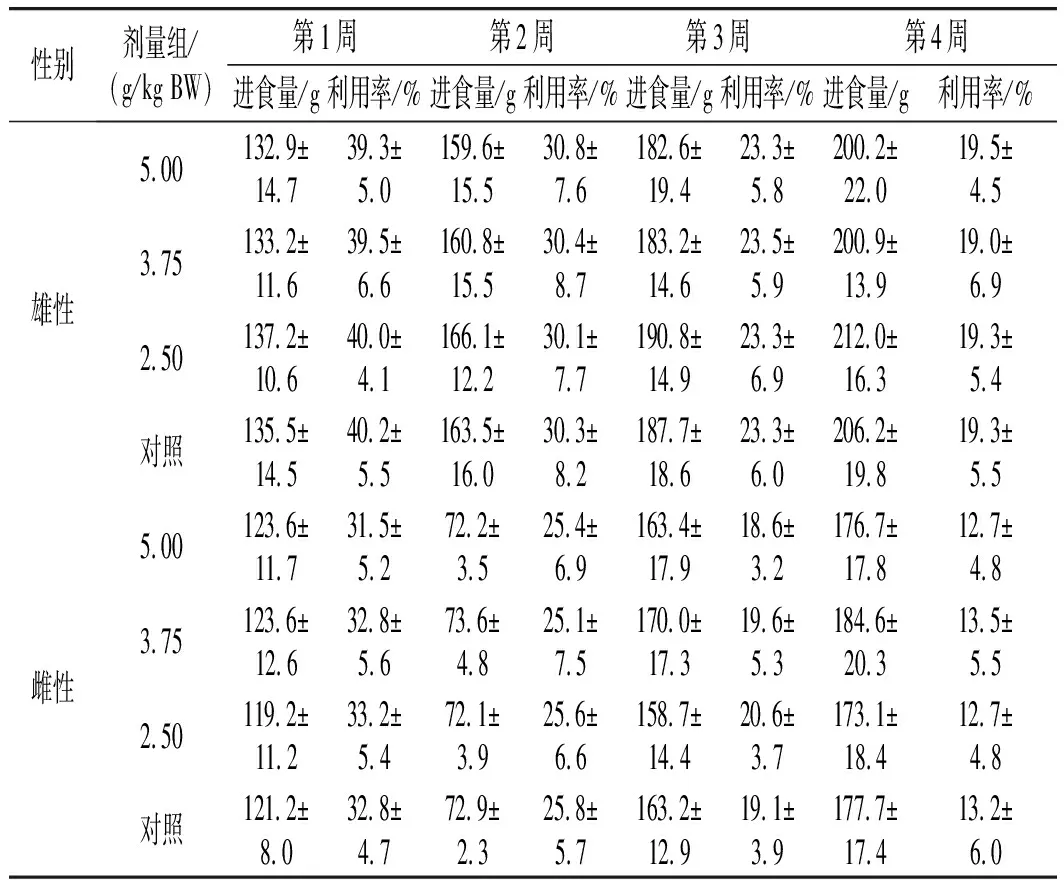
表3 纳豆软胶囊对大鼠进食量及食物利用率的影响(x±s, n=10)Table 3 Effect of natto soft capsules on food intake amount and food utilization rates of rats (x±s, n=10)
由表3可知,给予不同含量纳豆软胶囊内容物进行灌胃后,各剂量组雌性、雄性大鼠食物利用率与对照组比较无显著性差异(P>0.05),纳豆软胶囊内容物没有对动物的进食量和食物利用率造成明显影响。
2.5.3 血液学检查结果
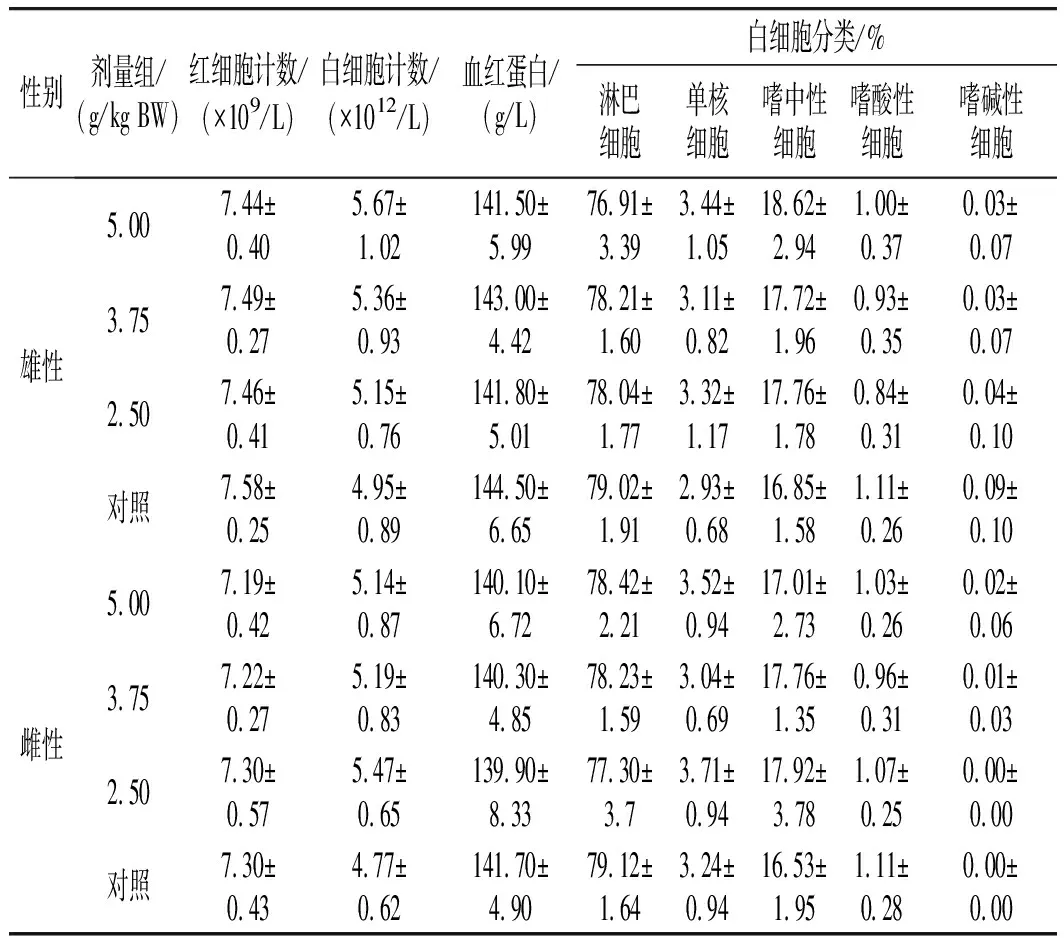
表4 纳豆软胶囊对大鼠血常规的影响(x±s, n=10)Table 4 Effect of natto soft capsules on blood routine parameters of rats (x±s, n=10)
由表4可知,各剂量组动物的血液学检查结果中,红、白细胞计数、血红蛋白含量及白细胞分类与对照组比较接近,差异不显著(P>0.05),各项数值均在正常范围内,说明纳豆软胶囊内容物对动物的血常规指标无明显影响。
2.5.4 血清生化检验结果

表5 血液生化指标结果(x±s, n=10)Table 5 The results of blood biochemistry indexes (x±s, n=10)
由表5可知,受试物各剂量组与空白对照组大鼠各项血液生化指标无明显差异(P>0.05),且血液生化指标各项数值处于大鼠血液指标正常参考值范围内。
2.5.5 纳豆软胶囊对大鼠脏器重量和脏体比的影响
受试物各剂量组重要脏器的重量和脏体比见表6。
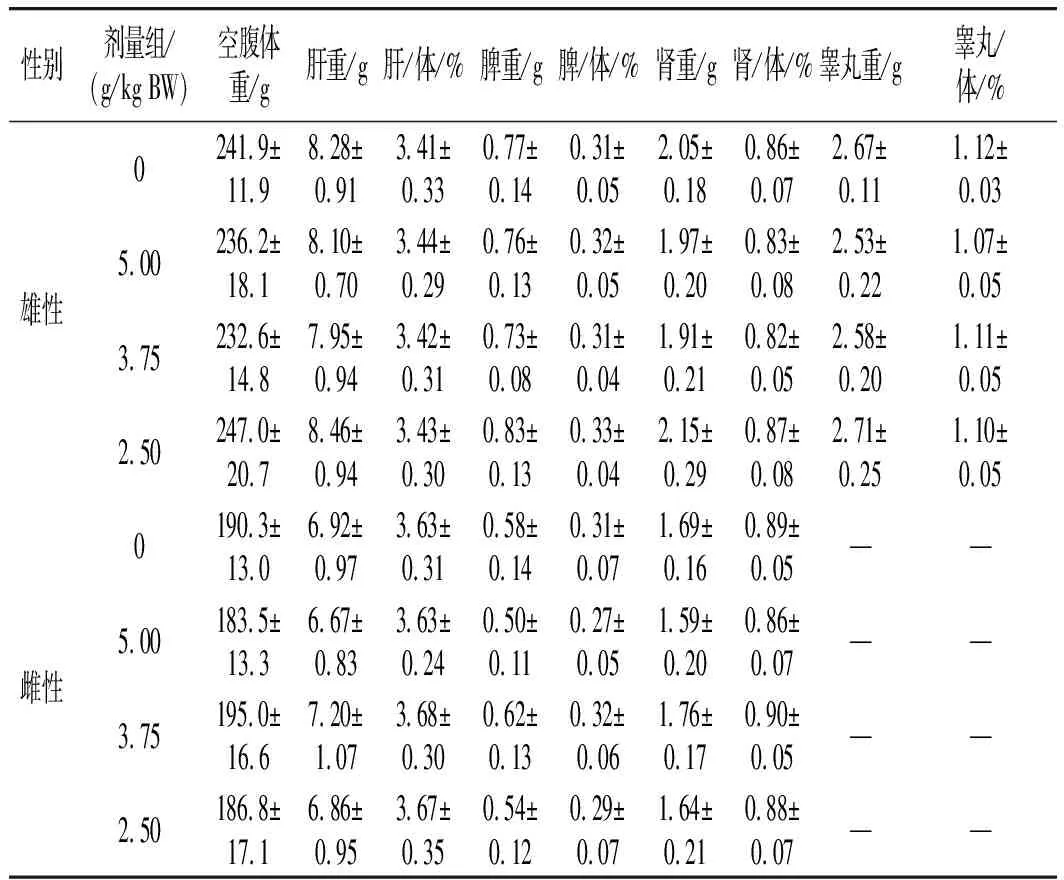
表6 纳豆软胶囊对大鼠脏器重量及脏体比的影响(x±s, n=10)Table 6 Effect of natto soft capsules on viscera weight and viscera-body ratio of rats (x±s, n=10)
由表6可知,雄性、雌性大鼠各剂量组肝、脾、肾、睾丸(雄鼠)的重量和各脏器系数与阴性对照组比较均无显著性差异(P>0.05)。
2.5.6 病理组织学检查
3个剂量组与对照组雌性、雄性大鼠在试验期内各组间动物体重无显著差异,生长活动均正常,排泄物无异常。大体检查各组动物脏器均未见病变,高剂量组与对照组雌性、雄性动物的主要脏器经组织病理学检查只发现个别轻微程度病变且没有特异性分布,考虑为个体化因素,故总结为未发现明显病理性改变,中、低剂量组动物未进行组织病理学检查。
2.6 增强免疫力功能试验结果
2.6.1 对小鼠脏器/体重值的影响
胸腺和脾脏是身体的中心免疫器官,是T淋巴细胞定居、分化及成熟的器官,它们与体重的比值可粗略估计机体的免疫水平[13],脾脏指数指脾脏与体重的比值,胸腺指数指胸腺与体重的比值。
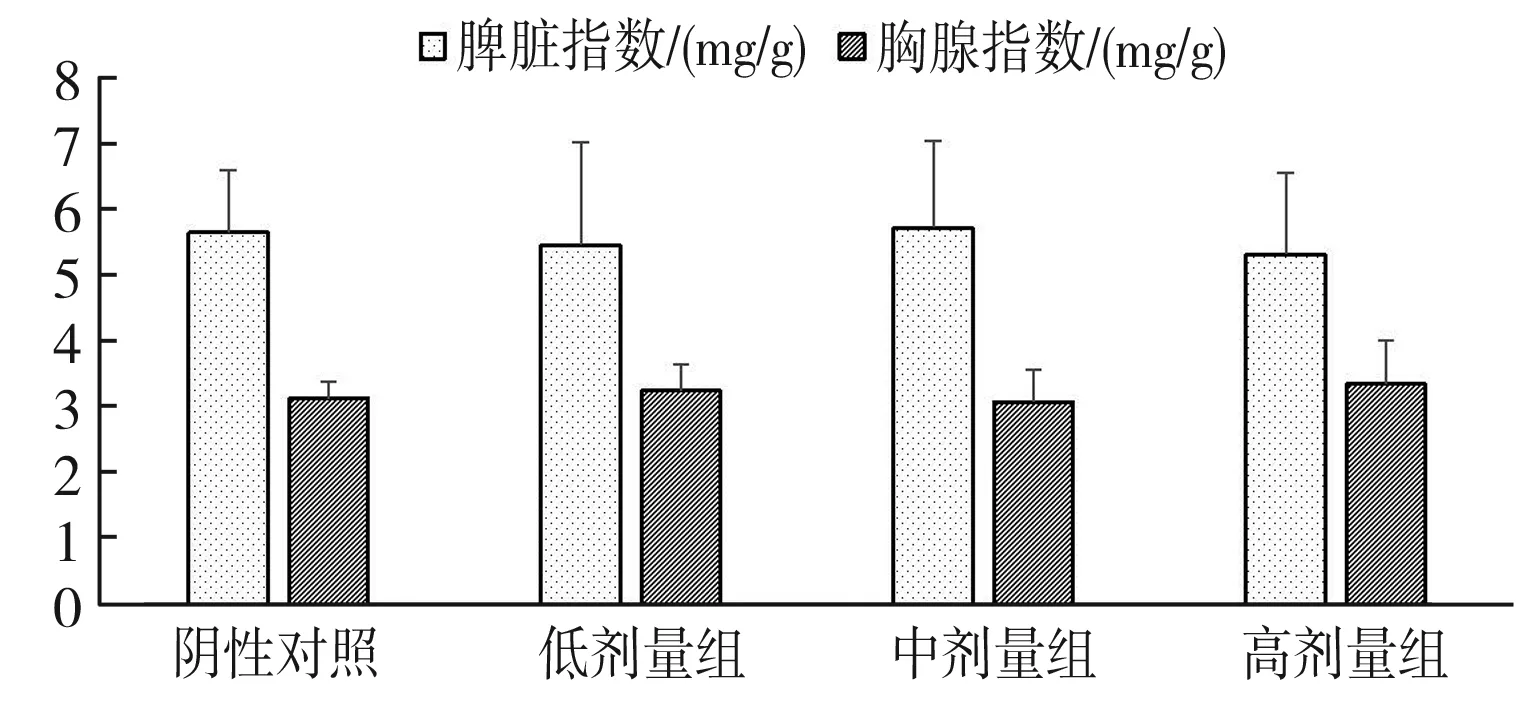
图2 小鼠免疫器官脏器指数测定结果(x±s, n=12)Fig.2 The test results of viscera indexes of immune organs of mice (x±s, n=12)
由图2可知,经口给予小鼠不同剂量受试物30 d,各剂量组脾脏指数和胸腺指数基本无差异且与阴性对照组间比较差异无显著性(P>0.05),表明受试物未对小鼠脾脏和胸腺产生影响。
2.6.2 小鼠迟发型变态反应(DTH)试验结果
迟发型变态反应是由致敏T细胞介导的以单核细胞浸润和细胞变性坏死为特征的损伤性炎症反应,炎症反应的强度可间接体现细胞免疫能力[14]。
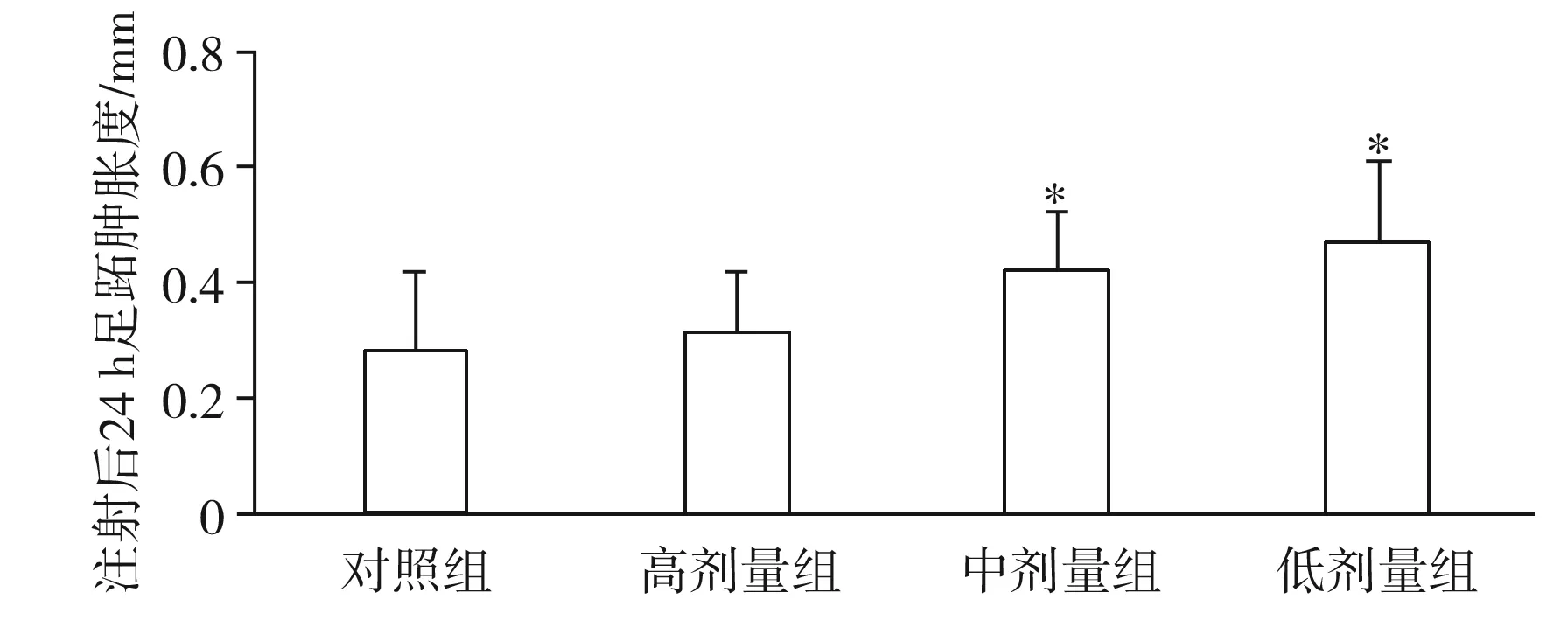
图3 受试物对小鼠迟发型变态反应的影响Fig.3 Effect of tested substances on delayed allergy of mice
由图3可知,小鼠的足跖肿胀度随着剂量的增加而升高,且数值均高于对照组。与对照组比较,中、高剂量组对小鼠足跖肿胀度的影响达到显著水平(P<0.05),即对小鼠迟发型变态反应能力有显著影响。
2.6.3 对小鼠半数溶血值(HC50)的影响
半数溶血值,是指血清中溶血素的含量,是体外检测体液免疫最佳的方法,小鼠血清中溶血素抗体的生成量能直观清晰地反映出体液免疫功能的强弱[15]。当用绵羊红细胞(SRBC)免疫小鼠淋巴细胞后,会产生溶血素,通过检测释放到血清中的溶血素抗体水平来评估个体特异性免疫功能。
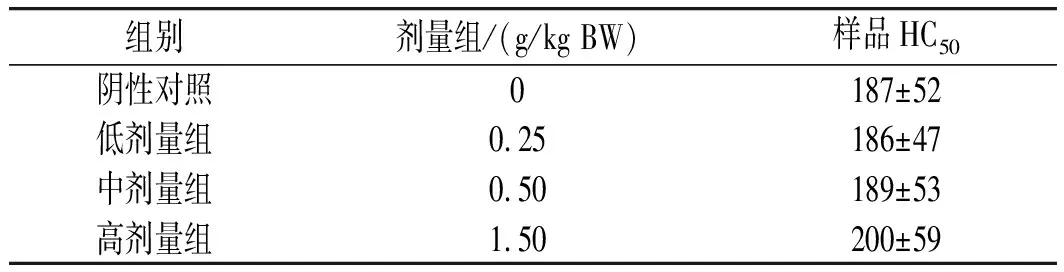
表7 受试物对小鼠半数溶血值HC50的影响(x±s, n=12)Table 7 Effect of tested substances on half hemolysis value (HC50) of mice (x±s, n=12)
由表7可知,中、高剂量组小鼠半数溶血值有增高趋势,但没有显著性差异(P>0.05),即受试物对小鼠HC50无明显影响。
2.6.4 对小鼠巨噬细胞吞噬鸡红细胞的影响
采用小鼠腹腔巨噬细胞吞噬鸡红细胞试验测定单核-巨噬细胞功能,巨噬细胞是机体发挥先天性免疫反应的主要免疫细胞,它能对细胞残片及病原体进行噬菌作用,是机体免疫系统的第一道防线,评估小鼠腹腔巨噬细胞的吞噬能力能够衡量机体先天性免疫和细胞免疫功能[16]。
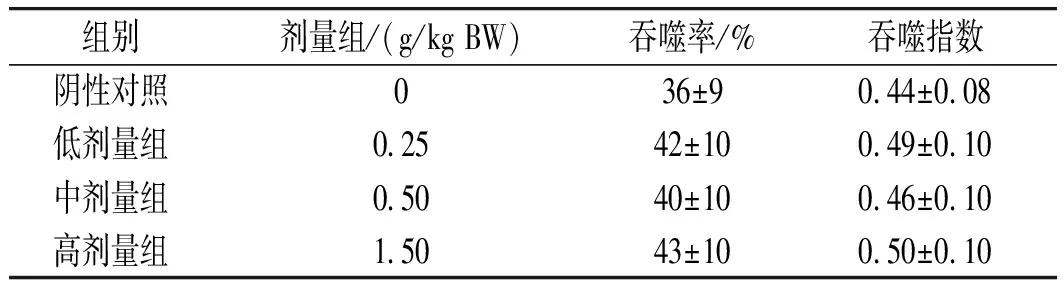
表8 小鼠单核-巨噬细胞功能的测定结果(x±s, n=12)Table 8 The testing results of mice monocyte-macrophage function (x±s, n=12)
由表8可知,经统计学分析,经口给予受试物30 d,各剂量组小鼠单核-巨噬细胞吞噬率和吞噬指数与阴性对照比较均有不同程度升高,无显著性差异(P>0.05),即受试物对小鼠巨噬细胞吞噬鸡红细胞的能力无影响。
2.6.5 小鼠碳廓清试验吞噬指数结果

图4 小鼠碳廓清试验吞噬指数结果Fig.4 The results of phagocytic indexes of mice carbon clearance test
经口给予小鼠不同剂量受试物30 d,由图4可知,中、高剂量组与阴性对照组比较差异有显著性(P<0.05),即中、高剂量组受试物能提高小鼠单核-巨噬细胞的碳廓清能力。
2.6.6 小鼠自然杀伤(NK)细胞活性试验结果
NK细胞是机体重要的免疫细胞,具有天然防御功能,能够识别靶细胞,杀伤介质,其杀伤能力和范围远大于T细胞,无需预先致敏也能发挥免疫功能,杀伤多数受感染细胞和肿瘤细胞,维护机体免受感染[17]。
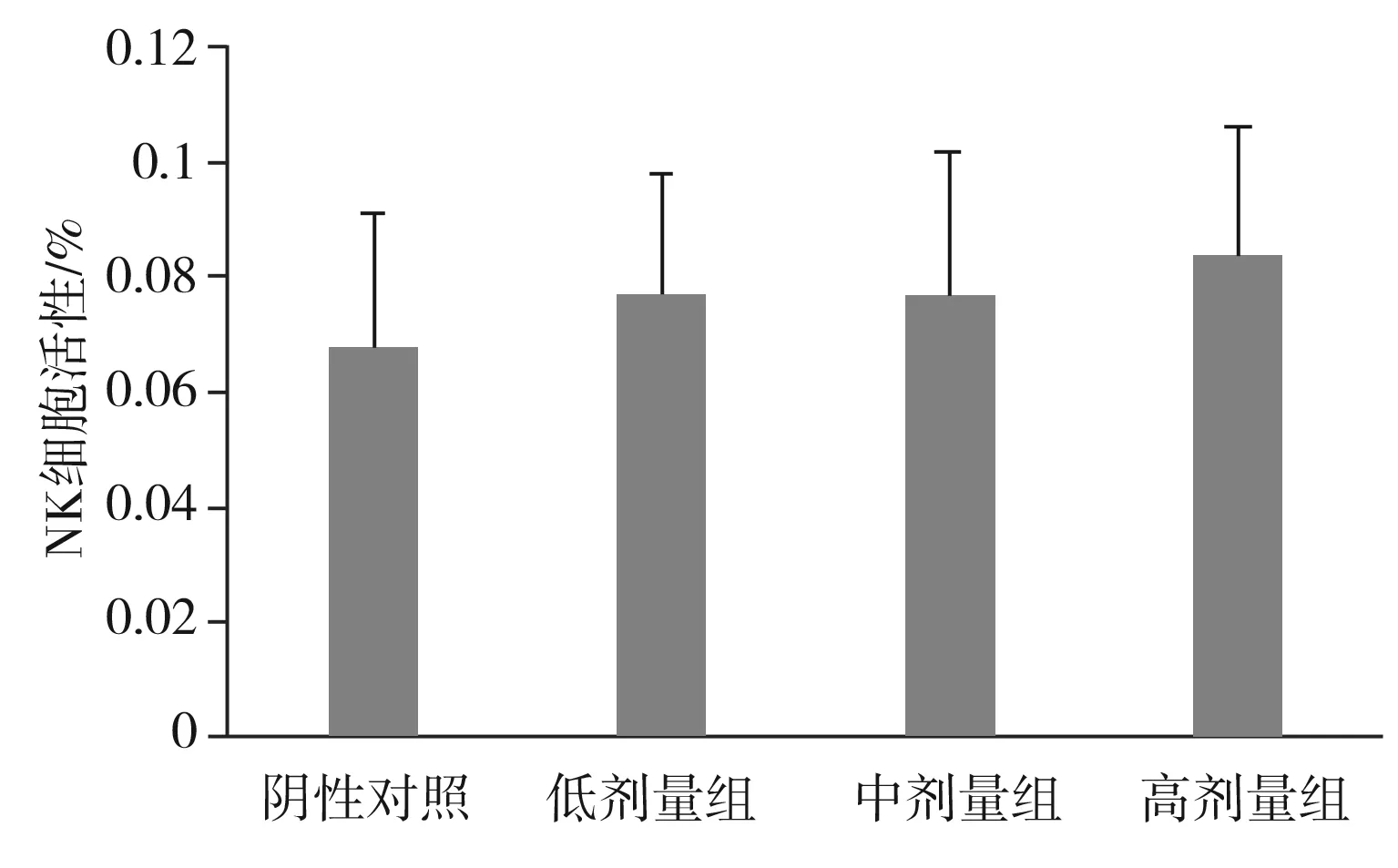
图5 小鼠NK细胞活性试验结果Fig.5 The results of mice NK cell activity test
采用乳酸脱氢酶测定法测定NK细胞活性,由图5可知,经口给予小鼠不同剂量的受试物30 d,经统计学处理,各剂量组NK细胞活性与对照相比均有所提高,但无显著性差异(P>0.05),说明受试物对小鼠的NK细胞活性无明显影响。
3 结论
急性经口毒性试验是最基础的毒理学安全性评价试验,能够初步评估毒性作用的靶器官和作用机制,为以后的亚急(慢)性等毒性试验提供毒性作用和剂量选择的依据[18]。本研究中纳豆软胶囊内容物急性经口毒性试验最大耐受剂量MTD>24.8 g/kg BW,属无毒级;骨髓细胞微核试验能检测染色体和染色体组畸变,精子畸形试验通过评估受试物是否对精子生成、发育产生影响,判断其对体内生殖细胞是否具有遗传毒性作用,Ames试验是从原核细胞水平检测受试物是否具有诱发基因突变能力[19]。 本研究中以上3项试验结果均为阴性,表明纳豆软胶囊没有致突变性。
本试验纳豆软胶囊内容物以2.50,3.75,5.00 g/kg BW的剂量(相当于人体推荐摄入量的50,75,100倍),连续喂养30 d,各剂量组动物生长情况良好,未见异常,试验期间各剂量组动物体重、进食情况、血液指标与对照组比较均无显著性差异(P>0.05);动物的各内脏器官的大体观察和高剂量组动物内脏病理组织学检查均未见与受试物有关的病理学改变,初步估计纳豆激酶软胶囊在本试验剂量范围内,作为保健食品是安全的。
分别从细胞免疫、体液免疫、单核-巨噬细胞和NK细胞活性方面测定研究了纳豆软胶囊对小鼠免疫功能的调节作用。细胞免疫试验发现,在迟发型免疫反应中,中、高剂量组足跖肿胀度显著高于对照组(P<0.05),表明其具有增强细胞免疫功能作用。单核-巨噬细胞功能试验表明,其能够显著调节碳廓清能力。纳豆软胶囊对小鼠体重增长、小鼠半数溶血值、脏器/体重比值、小鼠腹腔巨噬细胞吞噬鸡红细胞能力、NK细胞活性没有显著性影响。参照《保健食品检验与评价技术规范》,试验结果符合评价程序中“具有增强免疫力”的评价标准,因此可判断纳豆软胶囊具有增强免疫力的功能。
随着时代的进步和人们生活方式的变迁,人口老龄化问题日益凸显,居民疾病谱已然发生重大变化,未来医学将进入预防医学年代,从单纯的治疗向预防保健方向转化[20],本研究初步验证了纳豆软胶囊功效成分无毒无害且具有增强免疫力的功效,加上纳豆激酶本身具有良好的溶血栓作用,为开发出安全性高、可供正常人群食用的增强免疫力的保健食品奠定了基础。
