香薷精油与多酚的提取及抗氧化活性研究
2022-06-05陈林林张佳欣吴嘉树李伟范天娇杨茜瑶郑凤鸣
陈林林,张佳欣,吴嘉树,李伟,范天娇,杨茜瑶,郑凤鸣
(哈尔滨商业大学 食品工程学院,哈尔滨 150028)
香薷全草可入药,是一种药食同源的植物,主要生长在丘陵和路边[1]。香薷富含化合物,目前已鉴定出60多种,主要为萜烯、酯、醇、酚、醛等[2]。在食品中可以作为调味品、添香剂[3]。香薷通过萃取得到的精油能够延缓甚至抑制微生物对食品的作用,可以作为一种天然抗菌剂,用于食品保鲜[4-5]。因香薷精油特有的风味,可应用于饮料、糕点等食品行业中[6]。
多酚作为香薷次生代谢产生的一类天然有机化合物,存在于香薷的各种组织中[7],可以减少细胞和组织中的氧化损伤,是一种天然的抗氧化剂,主要应用在医药、食品等领域[8]。郭彩慧等[9]测定了青花椒中多酚的抗氧化能力,结果表明多酚是一种有效的抗氧化剂。陈仕学等[10]从不同类型的茶叶中提取茶多酚,并对其抗氧化能力进行检测,实验结果表明不同茶叶中的茶多酚清除自由基的能力不同。
本文利用水蒸气蒸馏提取香薷中的精油,并用有机溶剂提取残渣中的多酚。利用气相色谱-质谱联用(GC-MS)技术分析精油成分组成,高效液相色谱法确定多酚溶液中成分组成并对精油以及残渣中的多酚进行了抗氧化活性研究,为香薷的利用提供了依据。
1 实验部分
1.1 材料与仪器
香薷:黑龙江省牡丹江市;乙酸钠:天津市福晨化学试剂厂;冰醋酸:天津市永大化学试剂有限公司;三氯化铁:天津市双船化学试剂厂;抗坏血酸(VC):西陇化工股份有限公司;邻苯三酚(焦性没食子酸):天津市光复精细化工研究所;2,6-二叔丁基-4-甲基苯酚(BHT)、2,4,6-三吡啶基三嗪(TPTZ):萨恩化学技术(上海)有限公司;1,1-二苯基-2-三硝基苯肼(DPPH):东京化成工业株式会社;三羟甲基氨基甲烷(Tris):天津市泰兴试剂厂;2,2-联氮-双-3-乙基苯并噻唑啉-6-磺酸(ABTS)。
UV 5100B型紫外可见分光光度计 上海元析仪器有限公司;TU-1900型紫外分光光度计 北京普析通用仪器有限责任公司;DHG-9070A型电热恒温鼓风干燥箱 上海一恒科技有限公司;DC-2006型低温恒温槽 宁波海曙天恒仪器厂;GC7890B/MS5977B型气相色谱-质谱联用仪 美国Agilent公司;Ultimate 3000型高效液相色谱仪 美国赛默飞世尔公司;XT 220A型精密电子天平 瑞士普利赛斯仪器公司;W501型升降恒温水浴锅 上海申胜生物技术有限公司;R-1001型旋转蒸发仪 郑州长城科工贸有限公司。
1.2 香薷精油的提取
取干燥的香薷籽粒150 g放于3 L的三颈烧瓶中,通过水蒸汽蒸馏从香薷中提取精油。加入体积为2 L的蒸馏水,使其完全浸泡,并放置在油浴锅中在115 ℃油浴加热。加热5~7 h,当回流管中不再馏出精油,停止加热,降至室温后,收集从回流管蒸馏的精油,并将该混合物于4 ℃冷藏16 h,收集精油,称取质量,平行3次[11-12],按公式(1)计算精油得率:

(1)
式中:m为收集的精油质量,g;m0为香薷籽粒总质量,g。
1.3 残渣中多酚含量的计算
用纱布包裹提取精油后的香薷残渣,挤压除去大部分水分,再置于烘箱中烘干,除去残渣中的水分并用粉碎机粉碎。取2 g粉碎后的残渣置于锥形瓶中,采用超声波辅助法,加入60%的乙醇溶液20 mL,采用层析分离法[13]使多酚溶液浓度为29.46 mg/mL。用预处理后的AB-8大孔树脂并加入10 mL的多酚溶液,采用pH为6的50%乙醇对多酚纯化,吸附时间为6 h,得到多酚提取液,于45 ℃在60 min时测定上层清液的吸光度。
制备浓度为0.1 mg/mL的没食子酸溶液,随后称取0.25 g硫酸亚铁和1.25 g酒石酸钠,用蒸馏水溶解定容至250 mL,得到酒石酸亚铁显色剂。准确称量0.1362 g磷酸二氢钠,2.0315 g磷酸氢二钠,溶解稀释至100 mL,制得pH为7.5的缓冲溶液[14]。
量取0,0.1,0.2,0.4,0.6,0.8,1.0 mL的没食子酸溶液,加入2 mL着色剂和5 mL缓冲液,定容至10 mL,并于540 nm处测量吸光值,按公式(2)计算多酚得率:

(2)
式中:C0为多酚浓度,mg/mL;V0为提取后溶液体积,mL;m0为加入残渣质量,g。
1.4 GC-MS分析香薷精油成分组成
采用GC-MS对香薷精油的组成成分及对应的含量进行分析检测,方法测定的条件如下:
GC分析条件:色谱柱:弹性石英毛细管柱HP-5MS(30 m×250 μm×0.25 μm);载气为氦气,氦气流量:1 mL/min;进样口的温度为250 ℃,进样分流,进样分流比为100∶1;程序升温:柱温在60 ℃保持1 min,随后以8 ℃/min升至240 ℃,并保持5 min。
MS分析条件:电离方式为EI离子源;离子源温度是230 ℃;质量扫描范围:33~550 amu;四级杆温度:150 ℃;电离电压:70 eV[15]。
1.5 HPLC确定多酚提取液的成分组成
对残渣中多酚的提取液进行液相色谱分析,分析条件:色谱柱:XDB-C18(4.6 mm×250 mm,5 μm);流动相是色谱级别的甲醇(A)-纯水(B)进行梯度洗脱:0~10 min:26% A,74% B;10~10.1 min:50% A,50% B;10.1~25 min:50% A,50% B。流速为1 mL/min;柱温为25 ℃;检测波长为280 nm;每次进样10 μL[16]。
1.6 香薷精油及多酚提取液抗氧化能力测定
1.6.1 清除DPPH自由基能力
以无水乙醇为溶剂,制备不同浓度梯度的香薷精油溶液,制得的香薷精油质量浓度分别为0.1,0.5,1,3,5,7,9 mg/mL,以同样浓度的VC溶液和BHT溶液作为样品对照溶液。将无水乙醇作为对照溶液,量取1 mL待测液,4 mL DPPH溶液(2×10-4mol/L),放于避光处,室温下静置30 min,于517 nm测吸光度A。同样条件下测定1 mL待测液,4 mL无水乙醇的吸光度记为A0;1 mL无水乙醇,4 mL DPPH的吸光度记为A1[17],按公式(3)计算清除率:

(3)
1.6.2 清除超氧阴离子自由基能力
量取体积为0.1 mL不同浓度梯度的待测液,添加0.5 mL吐温80溶液和6 mL Tris盐酸缓冲溶液(50 mmol/L,pH 8.2),25 ℃反应20 min后加入体积为0.1 mL 25 ℃的邻苯三酚溶液(10 mmol/L)反应4 min,再加入6 mol/L的盐酸溶液。将待测溶液放于420 nm处测定吸光值A,用蒸馏水替代样品,取同组的相同样品溶液,加入6 mL缓冲溶液,加蒸馏水使体积与样品组一致,然后测量其吸光度A1。将VC、BHT配成浓度梯度与待测样品一样的溶液,替代香薷精油和多酚提取液加入试管中,其他具体操作步骤相同,分别测得A、A0、A1[18-19],按公式(3)计算清除率。
1.6.3 清除ABTS+自由基能力
准确称取0.1921 g ABTS与0.0331 g过硫酸钾混合,并用蒸馏水稀释体积至50 mL,ABTS溶液为7 mmol/L,室温条件下避光静置12~16 h后加入磷酸盐缓冲液(0.01 mol/L,pH 7.4),734 nm处该混合溶液的吸光值为0.70。随后,将1 mL不同浓度的待测溶液和5 mL制得的ABTS反应液振荡使其混合均匀,放置在室温下静置10 min后在734 nm处测吸光值记为As。在相同条件下,以不加入样品的ABTS溶液为对照组,测其吸光值记为A0[20-21],按公式(4)计算清除率:
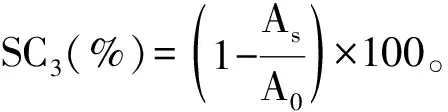
(4)
1.6.4 FRAP总抗氧化能力
准确称取4.0678 g乙酸钠,加4 mL冰醋酸,定容至250 mL;准确称取0.0781 g TPTZ粉末,加83 μL浓盐酸,并用蒸馏水定容至25 mL;精准称取0.1621 g的FeCl3,加入30 mL蒸馏水,充分摇晃使其均匀。将制备的溶液按照10∶1∶1进行混合,得到FRAP溶液。量取1 mL不同梯度浓度的待测液加入FRAP溶液6 mL,在37 ℃的水浴中摇匀,加热10 min,并在593 nm处测量吸光值A[22]。
2 结果与讨论
2.1 GC-MS分析香薷精油成分
采用水蒸气蒸馏法对香薷籽粒进行蒸馏,共计3次,结果见表1。

表1 香薷中精油得率Table 1 The extraction rate of essential oils from Elsholtzia ciliata
由表1可知,通过水蒸气蒸馏法从香薷中得到的精油平均得率为0.4135%。香薷精油相对标准偏差为4.7400%,相对标准偏差小于5%,说明精油产率数据符合实验要求,实验操作误差小,重复性好,收集的精油可以用于接下来抗氧化活性的研究。
2.2 没食子酸标准曲线的绘制
按照1.3中的步骤在没食子酸浓度和吸光度值之间建立标准曲线,结果见图1。

图1 没食子酸标准曲线Fig.1 The standard curve of gallic acid
回归方程为Y=0.0141X+0.0006,r=0.9981,浓度范围在0~10 μg/mL,线性关系良好,可以将没食子酸用作对照,用于计算提取液中多酚的浓度。
2.3 GC-MS测定香薷精油成分

图2 香薷精油的GC-MS总离子流谱图Fig.2 GC-MS total ion chromatogram of Elsholtzia ciliataessential oils
由图2可知,在香薷精油中检测到25种成分。使用NIST 98质谱数据库作为对照,定性分析这25种成分,并使用峰面积归一化方法定量分析了香薷精油的成分,结果见表2。

表2 香薷精油成分GC-MS解析结果Table 2 GC-MS analysis results of Elsholtzia ciliataessential oil components

续 表
由表2可知,所鉴定的香薷精油共有25种成分,其中,香薷酮相对含量最高(46.50%),其次是1-甲基-3-(1-甲基乙烯基)环己烯(43.08%),蛇麻烯的相对含量为2.79%,芳樟醇为1.61%。通过计算得知,这4种物质占香薷精油总含量的93.98%,可以认为是香薷精油香气的主要成分。
2.4 高效液相色谱法确定多酚提取液成分
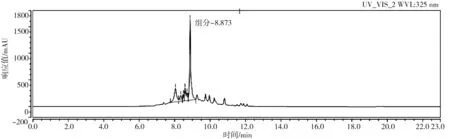
图3 多酚提取液的液相色谱图Fig.3 The liquid chromatogram of polyphenol extract
根据图3中峰面积的计算,多酚提取液中多酚的相对含量为41.24%。其中保留时间为8.870 min的组分峰值最高,故而可认为该组分为香薷多酚的主要组成成分。计算出多酚提取液中的多酚含量为45.5125 mg/mL。
2.5 香薷精油及多酚提取液抗氧化能力测定
2.5.1 清除DPPH自由基能力
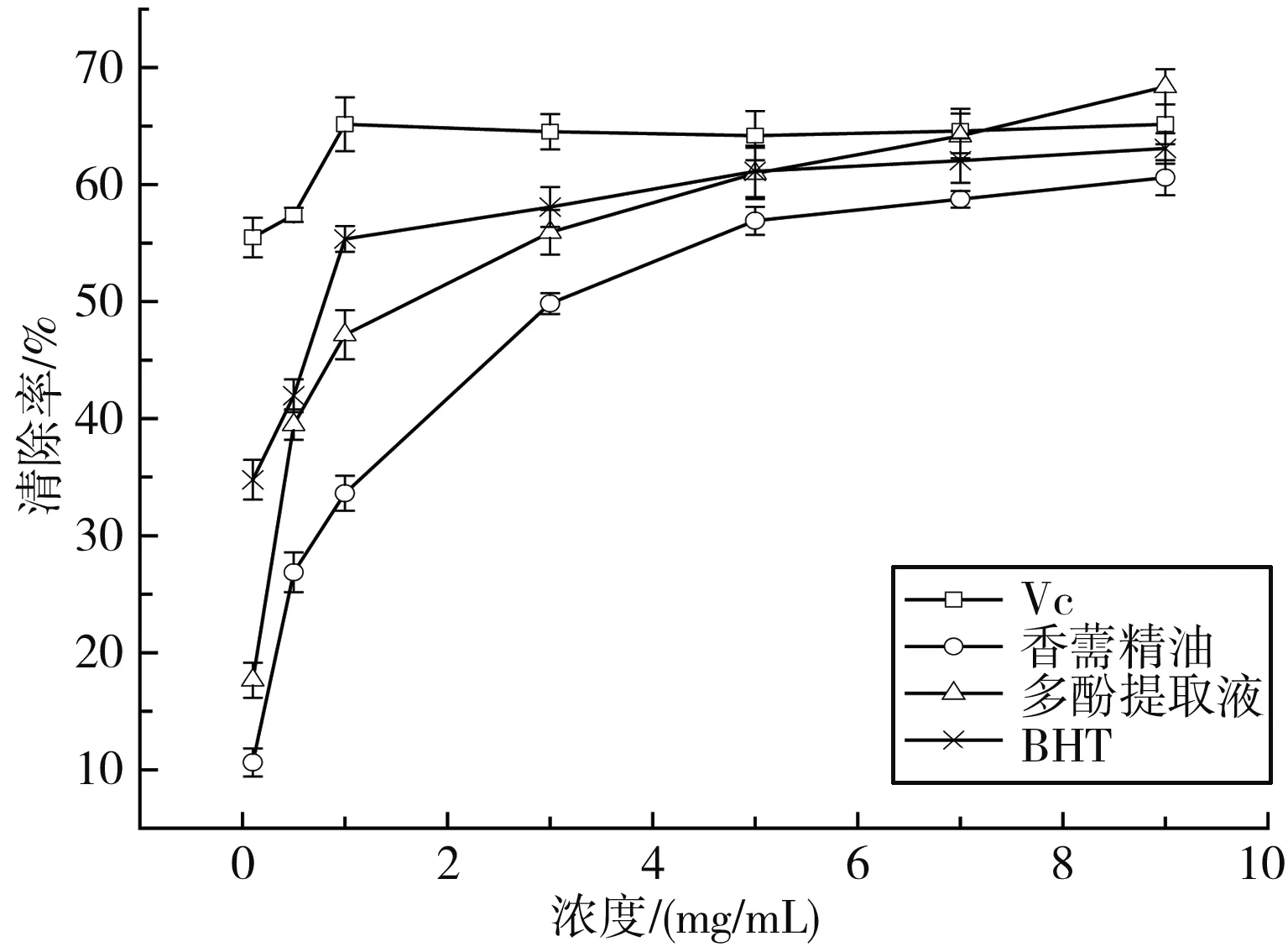
图4 清除DPPH自由基能力Fig.4 The DPPH free radical scavenging ability
由图4可知,在0~9.0 mg/mL的浓度范围内,每个样品的DPPH自由基的清除率均呈现上升趋势(P<0.05),其中VC的上升趋势相对平缓。在该浓度范围内VC的最大清除率为65.16%,BHT的最大清除率为63.09%。多酚提取液清除率在浓度为5 mg/mL时超过BHT,当浓度超过7 mg/mL时,多酚提取液清除率超过VC,在9.0 mg/mL时,达到最大值68.36%,随着浓度的继续增加,对DPPH自由基的清除能力保持上升的趋势(P<0.01);对于DPPH自由基的清除能力,香薷精油小于VC、多酚提取液和BHT,清除率在浓度为9.0 mg/mL时达到最大值60.59%,是同浓度下BHT的96.04%,香薷精油随着浓度的增加,清除率接近BHT(P<0.01)。
2.5.2 清除超氧阴离子自由基能力
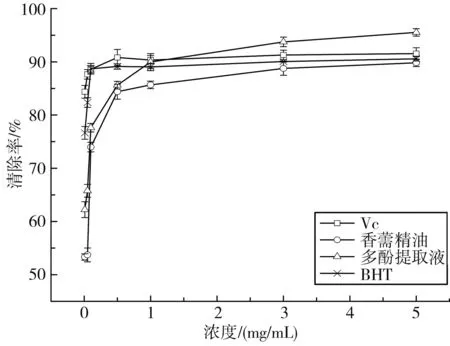
图5 超氧阴离子自由基清除能力Fig.5 The superoxide anion free radical scavenging ability
由图5可知,样品浓度在0~1.0 mg/mL范围内时,每个样品都呈现出急剧上升的趋势(P<0.05),在1.0~5.0 mg/mL浓度范围内VC、香薷精油和BHT的清除能力逐渐趋于平缓,多酚提取液的清除率保持上升的趋势(P<0.05)。在该浓度范围中VC的最大清除率为91.55%,BHT的最大清除率为90.57%。当浓度超过1.0 mg/mL时,多酚提取液对超氧阴离子自由基的清除能力开始超过BHT,并在3 mg/mL时超过VC,在5.0 mg/mL时清除率最高,达到95.54%,而且多酚提取液的清除能力随着浓度的增加而增大(P<0.01);对于超氧阴离子自由基的清除能力,香薷精油低于VC、多酚提取液和BHT,在5.0 mg/mL可达到最大值89.82%,是同浓度下BHT清除率的99.17%,随着浓度的增加,清除能力逐渐接近于BHT(P<0.01)。
2.5.3 清除ABTS+自由基能力

图6 ABTS+自由基清除能力Fig.6 The ABTS+ free radical scavenging ability
由图6可知,当浓度在0~0.5 mg/mL范围内,各样品对ABTS+自由基清除能力均有明显增强的趋势(P<0.05),当浓度高于0.1 mg/mL时各样品的抗氧化能力增加的趋势变得缓慢。在该浓度范围中VC的最大清除率为87.40%,BHT的最大清除率为69.20%。对于ABTS+自由基的清除能力,多酚提取液>VC>BHT>香薷精油。多酚提取液的最大清除率在0.5 mg/mL时达到最大值,是同浓度下VC的104.92%,BHT的132.51%;香薷精油的最大清除能力在0.5 mg/mL时达到最大值,是同浓度下BHT清除能力的94.94%,随着浓度的增加,清除能力逐渐接近BHT(P<0.05)。
2.5.4 FRAP总抗氧化能力

图7 FRAP总抗氧化能力Fig.7 FRAP total antioxidant capacity
由图7可知,当浓度在0~0.09 mg/mL范围内,各样品FRAP总抗氧化能力随浓度增长明显增强(P<0.05);多酚提取液的FRAP总抗氧化能力高于BHT,小于VC和香薷精油,在0.09 mg/mL时对FRAP总抗氧化能力最强,是同浓度下BHT的102.21%,VC的95.15%,并且随浓度的升高呈现稳定上升的趋势;在浓度大于0.03 mg/mL时,香薷精油的FRAP总抗氧化能力>VC>多酚提取液>BHT,在0.09 mg/mL时FRAP总抗氧化能力是VC的100.31%,BHT的107.75%。
2.5.5 抗氧化活性间的相关性分析
数据采用SPSS 17.0进行相关性分析,采用Pearson进行显著性检验,以P<0.05为显著性检验标准。

表3 香薷精油的4种抗氧化性评价方法的相关性Table 3 The correlation of four antioxidant evaluation methods of Elsholtzia ciliata essential oils
由表3可知,在测定香薷精油的抗氧化活性中,香薷精油对DPPH自由基的清除能力与超氧阴离子自由基、ABTS+自由基的清除能力、FRAP的总还原能力之间的线性关系非常显著(P<0.01);对于超氧阴离子自由基的清除能力和FRAP的总还原能力之间同样存在非常显著的线性关系(P<0.01),香薷精油对于其他抗氧化活性基团指标之间的相关程度并不明显。

表4 香薷多酚提取液的4种抗氧化性评价方法的相关性Table 4 The correlation of four antioxidant evaluation methods of Elsholtzia ciliata polyphenol extract
由表4可知,在4种用于测定香薷残渣中多酚提取液抗氧化活性的评价方法中,多酚对于DPPH自由基与超氧阴离子自由基、ABTS+自由基、FRAP总还原能力存在的线性关系非常显著(P<0.01);超氧阴离子自由基的清除能力与FRAP总还原能力之间线性关系非常显著(P<0.01),超氧阴离子自由基还与ABTS+自由基呈现线性相关(P<0.05);对于ABTS+自由基的清除能力与FRAP总还原能力线性关系显著(P<0.05),多酚提取液对于其他抗氧化活性基团指标之间的相关程度并不明显。
3 结论
利用水蒸气蒸馏法提取香薷中的精油并对残渣中的多酚进行有机溶剂提取,分别采用GC-MS和HPLC分析精油和多酚提取液的组分。所鉴定的香薷精油4种主要成分是香薷酮(46.5%)、1-甲基-3-(1-甲基乙烯基)环己烯(43.08%)、葎草烯(2.79%)和芳樟醇(1.61%)。这4种物质占香薷精油总含量的93.98%,可以认为是香薷精油香气的主要来源。研究发现香薷精油和多酚提取液清除DPPH·与O2-·、ABTS+·、FRAP的总还原能力线性关系呈现非常显著相关(P<0.01),对超氧阴离子自由基的清除能力与FRAP的总还原能力的线性关系同样非常显著(P<0.01)。香薷精油及香薷残渣中的多酚具有一定的抗氧化能力,可以作为食品防腐剂与抗氧化剂,为香薷的开发和利用提供了一定的理论依据。
