离子液体复合体系改性PEO制备新型固态聚合物电解质*
2022-06-02赵相峰陈前林
赵相峰,陈前林,郭 妤
(贵州大学 化学与化工学院,贵阳 550025)
0 引 言
固态锂电池主要由锂金属、正极材料及固态电解质组成,其具有能量密度高、电解质不可燃、无挥发性等特性,可以解决目前商业锂电池的能量密度低和安全性差等问题,也是未来锂电池的主要发展方向之一[1-2]。其中固态电解质的研发是影响和制约固态锂电池发展的主要问题[3]。在大量关于固态电解质的研究中,以PEO为基体的聚合物电解质由于具有电化学稳定、界面稳定等优点,一直被广泛研究[4-5]。然而,PEO在室温下结晶度较高,导致其离子电导率较低,通常在60 ℃以上才能表现出较好的导电性,这极大的限制了这类电解质的应用[6-7]。因此,如何有效降低PEO基固态聚合物电解质在常温下的结晶度、提高较低温度下锂盐迁移速率,是当前PEO基固态聚合物电解质的主要研究方向。
离子液体作为一种室温有机熔盐,其特殊的结构和性能,比如电导率高、热稳定性和电化学稳定性好等优点[8-9],能有效改善固态电解质的电化学性能,受到越来越多的关注。目前已应用于锂电池研究的离子液体主要有咪唑类、季铵类和吡咯类等,其中咪唑类离子液体因其黏度小、电导率高,且易调控等优点成为研究热点[10]。Balo[11]等将1-乙基-3-甲基咪唑双三氟甲烷磺酰亚胺盐(EMIMTFSI)掺杂入PEO制备出柔性凝胶聚合物电解质(GPE),表现出较高的室温离子电导率,组装的LiMn2O4/Li电池在0.1 C倍率下可以达到120 mAh·g-1放电容量,但在循环25圈后容量逐渐下降,循环稳定性不高。同时,目前常用的咪唑类离子液体,阳离子主要都是C(1)、C(3)位烷基取代,C(2)位上是氢原子的结构[12-13],其中C(2)位上质子具有较强的还原性,容易导致电解质的电化学窗口不高[14],无法适配高压充放电的正极材料。为了提高离子液体的电化学窗口,Li[15]等采用原位聚合技术将离子液体在PEO体系中聚合形成了一种半互穿聚合网络结构,电化学窗口明显提升,但该电解质仍然需要在55 ℃以上才能正常工作。
在已有研究的基础上,我们合成出一种1,2,3位烷基取代的新型咪唑离子液体及聚离子液体,并将其复配后应用于改性PEO聚合物电解质体系,力求在电导率和电化学窗口上均得到提升,并有效降低电池的运行温度。
1 实 验
1.1 实验试剂
聚环氧乙烷(PEO, MW=300000),双三氟甲烷磺酰亚胺锂(LiTFSI,99.9%),偶氮二异丁腈(AIBN,99%),N-甲基吡咯烷酮(NMP,≥99.9%),无水乙腈购于阿拉丁。1-乙烯基咪唑(VIM,99%),聚(乙二醇)甲基丙烯酸酯(PEGMA,MW=400)和溴乙烷购于麦克林。聚偏二氟乙烯(PVDF)购于赛博电化学。磷酸铁锂(LiFePO4)和炭黑采购于深圳市天成和科技有限公司。
1.2 PIL和IL的合成
依次将VIM、PEGMA、AIBN加入无水乙醇中,氮气保护下,升温回流反应6 h,采用乙酸乙酯洗涤过滤,随后加入溴乙烷,常温反应12 h后减压蒸馏,得到固体产品。最后将其与LiTFSI在无水乙醇中阴离子交换12 h,无水乙醚洗涤后得到PIL。
参考文献[16],合成出2-乙基-1,3-二丁基咪唑溴盐,然后将其与LiTFSI在去离子水中阴离子交换12 h,下层油状物即为交换后的IL,去离子水多次洗涤即可得到产品。
1.3 SPE的制备
采用常见的溶液浇铸技术制备固态聚合物电解质,具体过程如下:称取一定量的PEO、PIL、IL和LiTFSI(表1),溶于无水乙腈中,室温搅拌直至形成均匀透明的粘性溶液后,然后将其均匀的倒入聚四氟乙烯板中,待溶剂挥发后转移到60 ℃真空干燥箱干燥,最后使用21 mm冲头切成大小相同的膜片,并转移置手套箱中保存,并分别命名为PEO/PIL/IL SPE-10%,PEO/PIL/IL SPE-20%,PEO/PIL/IL SPE-30%,PEO SPE。
1.4 样品的表征
采用Nicolet iS50衰减全反射红外光谱仪(ATR)和BRUKER AVANCE 400M核磁氢谱仪(1H NMR)检测样品的分子结构;采用SmartLab9KW型X射线衍射仪(XRD)检测电解质膜的物相组成;采用STA449F1型热重分析仪(TG)检测电解质膜的热稳定性。
1.5 电化学性能测试
1.5.1 离子电导率
在手套箱中组装不锈钢(SS)/SPE/SS扣式对称电池,通过上海辰华CHI760E电化学工作站测试电池在不同温度下的阻抗(频率0.1 Hz~106Hz),电解质膜的离子电导率采用如下公式计算:
σ=L/RbS
式中,Rb代表电解质的体电阻,L和S分别是电解质膜的厚度(cm)和面积(cm2)。
1.5.2 电化学窗口
组装Li/SPE/SS扣式电池,通过美国普林斯顿Versa STAT 3型电化学工作站测试电池在40 ℃下的窗口(电压0~7 V)。
1.5.3 锂离子迁移数
组装Li/SPE/Li扣式对称电池,通过美国普林斯顿Versa STAT 3型电化学工作站进行电化学阻抗(EIS,0.1~106Hz)与计时电流(CA,0.01 V,3000 s)测试,电解质膜的锂离子迁移数通过以下公式计算:
tLi+=Is(ΔV-IoRo)/Io(ΔV-IsRs)
式中,I0,Is分别代表极化初始电流和极化稳态电流,R0,Rs分别代表极化前后的阻抗值,ΔV为极化电压(10 mV)。
1.5.4 充放电测试
将LiFePO4、碳黑、PVDF按8∶1∶1的质量比混合,溶解于NMP中,通过涂布、干燥、切片得到LiFePO4正极片。组装LiFePO4/SPE/Li扣式电池,采用蓝电CT3001测试仪,在40 ℃下进行电池循环性能(0.2 C,2.5~4 V)测试。
2 结果与讨论
2.1 结构表征
IL的1H NMR如图1所示,与文献对比可得,谱图中化学位移δH=7.13、3.76、2.57、1.70~1.77、1.30~1.36、1.19和0.90的峰,分别对应—N—CH=C、—N—CH2—C—、—N=C—CH2—C、—C—CH2—C—、—C—CH2—C、—N=C—C—CH3和—C—CH3,分峰数及氢个数与文献基本一致,同时,从核磁氢谱中可知,阴离子交换后化学位移整体右移,表明阴离子TFSI-对咪唑阳离子产生了影响,证明阴离子交换成功。
PEO/PIL/IL SPE-20%和纯PEO的ATR谱图如图2所示,与纯PEO红外谱图相比,在PEO/PIL/IL SPE-20%谱图中出现了TFSI-阴离子的峰(1179 cm-1,569 cm-1)[17-18],而单体VIM和PEGMA的C=C双键特征峰(1 650 cm-1)没有在红外中出现,表明聚离子液体的聚合反应较为彻底。此外,在600~800 cm-1范围内出现了属于烷基链伸缩振动所引起的新峰,证明了存在C(1)、C(2)、C(3)位被烷基取代的咪唑离子液体。因此,通过红外证实了此实验成功制备了PEO/PIL/IL三者共混的固态聚合物电解质。
2.2 膜材料表征
通过XRD研究了PEO基固态聚合物电解质添加PIL/IL前后的结晶变化,结果如图3a所示,纯PEO在2θ=19.1°和23.3°处有两个尖锐的衍射峰,表明PEO具有半结晶性[19]。初步分析加入锂盐虽然一定程度上可以降低PEO的结晶度,但随着锂盐量的增加,成膜困难,机械强度显著降低,所以PEO SPE结晶度降低程度有限。与PEO SPE相比,添加PIL/IL后的衍射峰明显下降,其中,2θ=23.3°的衍射峰几乎消失,表明PEO/PIL/IL SPE-2的结晶度大幅降低。这是由于相似相溶原理,PIL与IL能与PEO混合的更为均匀,便于它们穿插在PEO链段中,进一步打破了PEO链段的规则排序,导致电解质中非晶态区显著增多[20-21],随之有更多的聚合物链可以参与Li+离子传输,使得固态电解质获得更高的离子电导率。
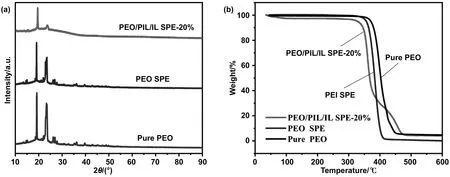
图3 PEO/PIL/IL SPE-20%、PEO SPE和纯PEO的XRD谱图(a)和TG曲线(b)
图3b是纯PEO,PEO SPE和PEO/PIL/IL SPE-20%的热失重图,初始分解温度即为热稳定值。由图可知,纯PEO在380 ℃左右开始分解,添加LiTFSI后,PEO SPE的分解温度降至350 ℃,这是由于LiTFSI的高解离和低晶格能造成了电解质的稳定性降低[22]。然而,随着PIL和IL的加入,初始分解温度又有下降(320 ℃),同时出现了不同于前两者的两步分解过程,这是因为IL具有相对较低的热分解温度,造成了热分解温度的进一步下降。不过,改性后的电解质材料在300 ℃前无显著分解,仍然具有较高的安全性,完全满足电池的使用需求。
2.3 电化学性能测试
2.3.1 离子电导率测试
离子电导率是衡量固态聚合物电解质是否能应用于电池的重要标准之一,因此我们通过电化学阻抗技术来评价改性PEO基固态聚合物电解质的电化学性能,结果如图4所示。4a~4d为4种SPE膜在不同温度下阻抗图,4e为离子电导率随温度的变化曲线。由图4可知,4种电解质膜的离子电导率随着温度的升高而升高,且经PIL/IL改性后的固态聚合物电解质离子电导率都有明显地提升。以IL添加量20%为例,与PEO SPE相比,在30 ℃下,离子电导率由3.93×10-6S·cm-1提高至7.41×10-5S·cm-1;40 ℃下,离子电导率由7.43×10-6S·cm-1提高至2.27×10-4S·cm-1,离子电导率得到如此显著地提升是由于PIL/IL的共混,有效打破了PEO链段排序,加速了Li+在链段间的迁移。此外通过实验发现,当IL含量高于20%时,离子电导率并不会有很明显地提升,同时还会造成电解质成膜困难,因此,接下来的研究我们选取IL含量为20%的固态聚合物电解质进行对比实验。

图4 SPEs的阻抗图:PEO SPE(a)、PEO/PIL/IL SPE-10%(b)、PEO/PIL/IL SPE-20%(c)、PEO/PIL/IL SPE-30%(d)和离子电导率随温度变化曲线图(e)
2.3.2 电化学窗口测试
作为一种性能优异的固态电解质,除了具备高的离子电导率外,还需要具备宽的电化学窗口,以适配不同充放电压下的正极材料,因此,我们采用线性扫描方法研究了SPE的电化学窗口,结果如图5所示,相比于PEO SPE的电化学窗口(4.3 V),改性后的PEO/PIL/IL SPE-20%的窗口提高至4.8 V,说明改性后的SPE能在更高的电压范围下应用。这与咪唑离子液体C(2)位上活泼氢质子被烷基取代有关,同时由于PIL/IL的共同作用,增加了TFSI-阴离子的浓度,促进了电极界面上稳定的钝化层形成,提高了固态聚合物电解质的稳定性。

图5 PEO SPE和PEO/PIL/IL SPE-20%在40 ℃下的LSV曲线
2.3.3 锂离子迁移数测试
在锂电池充放电过程中,锂离子会通过电解质在正负极之间往复迁移,而当锂离子在正极或负极表面沉积或嵌入时,锂离子会被快速消耗,从而形成一定程度的浓差极化,造成不均匀的空间电场,加剧锂枝晶的生成;而当电解质内部的离子迁移数能够达到某种特定的程度,这种浓差极化便会得到一定的缓解,因此,固态聚合物电解质需要具备更高的锂离子迁移数。本文通过计时电流法结合电化学阻抗法研究了40 ℃下PEO SPE和PEO/PIL/IL SPE-20%的锂离子迁移数,测试结果如图6所示,计算结果如表2所以。相比于PEO SPE(0.08),PEO/PIL/IL SPE-20%表现出较高的锂离子迁移数(0.30),进而有效地抑制锂枝晶的生成,提高Li+在固态锂电池中的迁移速率。

图6 PEO SPE(a)和PEO/PIL/IL SPE-20%(b)在40 ℃,10 mV直流电压下的电流-时间曲线,插图显示了极化前后电池的EIS曲线

表2 SPEs的锂离子迁移数
2.3.4 充放电测试
为了了解改性后电解质实际应用于固态电池中的性能,组装了LiFePO4|SPE|Li全固态电池,并测试了其在40 ℃,0.2 C倍率下的充放电性能。从图7a可以看出,LiFePO4|PEO/PIL/IL SPE-20%|Li全电池初始充电容量125.7 mAh·g-1,放电容量125.0 mAh·g-1,远远高于PEO SPE(57.4 mAh·g-1/56.1 mAh·g-1),经过20次循环后,LiFePO4|PEO/PIL/IL SPE-20%|Li全电池放电容量达到稳定状态(150.0 mAh·g-1以上),100次循环后,放电容量依然维持在150.0 mAh·g-1以上,且库伦效率始终保持在99%以上。实验证实,采用PIL/IL共混改性PEO制备出的新型固态锂电池,展现出较高的容量和优秀的循环性能,说明这种改性的方法相比于单一采用离子液体或聚离子液体改性有更好的效果,这将为以锂金属为负极的固态电池的研究提供一种新思路。

图7 LiFePO4|PEO SPE|Li和LiFePO4|PEO/PIL/IL SPE-20%|Li电池在0.2 C,40 ℃下的循环性能和库伦效率(a)以及LiFePO4|PEO/PIL/IL SPE-20%|Li电池对应的充放电曲线(b)
3 结 论
(1)通过合成PIL/IL,并将其与PEO共混制备出一种新型PEO基固态聚合物电解质。
(2)通过XRD及TG分析,表明经PIL/IL改性后的固态聚合物电解质结晶度显著降低,同时表现出较好的热稳定性(320 ℃)。
(3)通过对离子液体添加量为20%的电解质膜进行电化学性能测试,发现该电解质膜在40 ℃下表现出高的离子电导率(2.27×10-4S·cm-1),宽的电化学窗口(4.8 V)和较高的锂离子迁移数(0.3)。
(4)组装LiFePO4/Li全电池进行充放电测试,发现其稳定放电容量高达150.0 mAh·g-1,库伦效率保持在99%以上,展现出较高的容量和循环稳定性。
