催化氧化除氨氮/锰滤料活性恢复方式优化研究
2022-06-02张永志郑佳慧李宇洋黄廷林
程 亚,张永志,郑佳慧,李宇洋,黄廷林
催化氧化除氨氮/锰滤料活性恢复方式优化研究
程 亚,张永志,郑佳慧,李宇洋,黄廷林*
(西安建筑科技大学环境与市政工程学院,陕西省环境工程重点实验室,西北水资源与环境生态教育部重点实验室,陕西 西安 710055)
以催化氧化除氨氮/锰失活滤料为研究对象,考察了3种不同恢复方式(自然恢复,投加碱度,再次挂膜)对滤料催化氧化氨氮、锰效能的影响.结果表明,自然恢复(1#)滤柱,投加碱度(2#)滤柱,再次挂膜(3#)滤柱分别于4,2,3d后氨氮去除率达到90%以上;逐渐提高氨氮浓度,3#再次挂膜滤柱出水氨氮浓度波动最大,1#自然恢复滤柱恢复期间出水亚硝氮积累时间最长且峰值最高.3根滤柱催化氧化去除锰活性恢复速度均较快.1#自然恢复滤柱和2#碱度恢复滤柱均能在2d内将锰完全去除.3#挂膜滤柱是在停止投加高锰酸钾后5d内实现将进水锰完全去除.氨氮和锰的相互影响实验结果表明,3根滤柱中投加碱度(2#)滤柱表现最优.尽管氨氮抑制锰的去除,但是投加碱度滤柱随着进水氨氮浓度的升高出水锰浓度始终低于0.1mg/L;锰对氨氮的去除影响不显著.XRD分析结果表明,受其表面负载新生成氧化膜的影响,高锰酸钾重新挂膜滤柱的滤料样品的结晶度较差.综合考虑氨氮和锰的活性恢复效率以及挂膜过程中药品的投加,提出采用自然恢复方式最适.
活性恢复;失活滤料;除氨氮/锰;催化氧化;地下水处理
当前我国地下水的氨氮、锰污染问题日益突出[1-3].由于地下水流动缓慢,更新周期长,一旦受到污染,仅仅依靠其自身完成全部净化修复几乎不可能[4-5].且由氨氮、锰造成的地下水污染危害严重[6–8].为满足国家饮用水水质标准和供水保证率不断提高的要求,防范并应对地下水水质污染的风险,去除氨氮和锰已成为我国水处理行业迫在眉睫的问题[9].
目前,传统饮用水处理技术难以经济有效地解决氨氮、锰污染问题[9–11].尤其是当地下水受到氨氮和锰等多重污染时,常规的地下水处理工艺很难将受到多重污染的地下水源水处理达标.当前国内外给水厂常用的除锰方法有化学氧化法[12-13]和生物法[14],常用的去除氨氮的方法有物理化学法[15-16]和微生物法[17].微生物法去除氨氮和锰对环境适应能力差,出水污染物易超标[18].化学氧化去除氨氮和锰的药剂投加量难以掌握,易生成有毒副产物.而利用沸石的吸附法也存在吸附容量有限的问题.
铁锰复合氧化物滤料催化氧化除氨氮和锰作为一种新兴且卓有成效的新型滤料,可用作自来水厂多种滤池的过滤材料,实现饮用水中氨氮、锰的同步高效去除.铁锰复合氧化物滤料经氧化还原沉淀法生产完成后,在石英砂滤料表面沉积形成了一种主要成分为O、C、Mn、Fe、Ca、Si的铁锰复合氧化物,能够持续、高效的去除水中的氨氮和锰[19-20].但在大规模推广应用过程中发现,不同储存方式的铁锰复合氧化物滤料经过长时间储存运输后,滤料的初期催化性能及催化活性恢复会受到不同程度的影响.干式储存和湿式储存是目前常用的两种储存方法.前期研究了不同储存条件与不同储存时间下对氨氮和锰去除性能的影响,结果表明湿式存储下的滤料较干式存储方式更易恢复催化活性[21].
前期实验缺乏对铁锰复合氧化物滤料催化氧化去除氨氮、锰活性恢复方法系统性研究,也缺少在实际应用过程中可操作条件下的滤料活性恢复研究.因此,本研究针对湿式存放的失活滤料,采用3种恢复方式(自然恢复,投加碱度,再次挂膜)开展了活性恢复方式的优化研究,重点比较了3种恢复方式下滤料催化氧化氨氮、锰效能的变化,以及滤料微观结构特征的差异,从而确定最佳的恢复方式,为后续工程实践提供理论依据.
1 材料与方法
1.1 滤料来源
采用氧化还原沉淀法生产的成熟铁锰复合氧化物滤料[22],生产完成后采用湿式储存法储存,即不进行干燥,直接将湿滤料密封保存.本研究中3根滤柱所使用的滤料均是使用该种方法保存40d的滤料.
1.2 实验装置
中试系统中滤柱材质为有机玻璃,内径为 100mm,滤料填充高度为1.2m,由粒径为 0.75~ 1.2mm 的石英砂填充.如图1所示.滤柱沿程有6个取样口,分别位于滤料上表面由上到下 0, 10, 20, 40, 70, 100cm处.
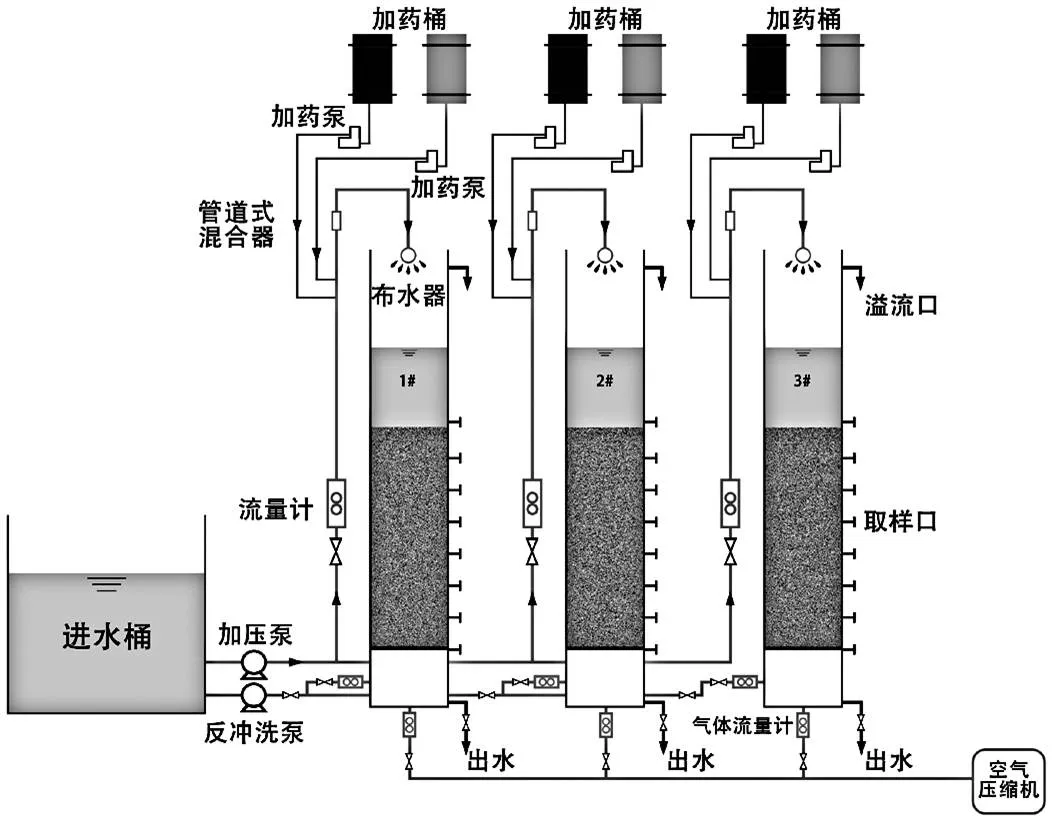
图1 中试系统流程
1.3 实验水质
本实验采用西安市某地下水厂进水,其水质参数见表1.

表1 水厂地下水水质参数
1.4 实验方法
实验过程中采用3组完全相同滤柱系统,分别为滤柱1#、2#、3#,具体运行方式如下:1#为自然恢复滤柱,持续投加氨氮以及锰进行运行恢复;2#滤柱为投加碱度恢复滤柱,除投加氨氮和锰外,还持续投加碳酸氢钠,将碱度提高100mg/L(以CaCO3计)进行恢复;3#滤柱为再次挂膜滤柱,投加氨氮、氯化锰(0.3mg/L Mn2+)和高锰酸钾(按与氯化锰完全反应的90%投加),反应生成氧化物随原水进入滤柱,经过滤后,被截留从而沉积在滤料的表面,从而实现再次挂膜,运行21d停止挂膜.在运行的前10d,保持3根滤柱进水氨氮浓度均为0.5mg/L,1#、2#锰浓度均为0.3mg/L,3#滤柱在投加高锰酸钾挂膜阶段,进水均检测不到锰.后期依据去除效果,逐渐提高滤柱进水氨氮(0.5~2.5mg/L)、锰浓度(0.3~2.5mg/L),滤柱采取下向流方式运行,滤速为4m/h,空床接触时间为15min.
1.5 分析项目及方法
滤柱运行期间,对滤柱进出水三氮(氨氮、硝氮、亚硝氮)和锰进行检测.检测不同挂膜时间滤柱沿程氨氮、锰浓度的变化,通过SEM、XRD等微观表征方法表征不同恢复方式下氧化膜表面形态及晶体结构.
2 结果与讨论
2.1 三种恢复方式下滤料去除氨氮和锰效果比较
不同恢复方式下,滤柱进出水三氮(氨氮、硝氮、亚硝氮)随运行时间的变化规律如图2(a),(b),(c)所示.由图2(a)可知,在0~10d,氨氮进水为0.5mg/L, 1#自然恢复滤柱氨氮去除率在4d内由35.5%升高至90%;2#碱度恢复滤柱去除率在2d内由50%升高至90%;3#重新挂膜滤柱去除率在3d内由49%升高至90%,恢复速度呈现:2#碱度恢复>3#重新挂膜>1#自然恢复.
而后,在逐渐提高氨氮浓度的过程中发现,3#重新挂膜滤柱的出水氨氮浓度波动最大,意味着该恢复方式滤柱活性较差.通过对硝氮(图2(b))、亚硝氮(图2(c))的检测结果发现,在10~20d期间3根滤柱均出现了出水亚硝氮升高现象,且1#自然恢复滤柱亚硝氮的积累时间最长以及峰值均最明显,但是在10~20d期间3根滤柱亚硝氮浓度迅速降低,硝氮浓度迅速升高,氨氮大部分转化为了硝氮.这与铁锰复合氧化物催化氧化氨氮的机理(①NH4+吸附;②铁锰复合氧化物催化氧化NH4+;③生成产物,如NO3-)相一致[22].
进一步比较不同运行时间(5,10,20d) 3根滤柱沿程去除氨氮的效果变化,结果如图2(d)所示.由尽管在运行第5d时, 3根滤柱的去除率均达到了100%,但3根滤柱沿程的氨氮去除能力却呈现出一定的差异,滤柱沿程去除能力呈现:1#自然恢复>2#碱度恢复>3#重新挂膜.
运行到第10d,滤柱进水氨氮浓度提高至1mg/L, 3根滤柱沿程去除氨氮能力出现显著差异,1#自然恢复滤柱性能最优,且该滤柱在此阶段活性得到明显的提升;到第20d氨氮浓度提高至1.5mg/L,此时3根滤柱沿程除氨氮能力基本一致,意味着2#碱度滤柱和3#重新挂膜滤柱在此期间去除氨氮能力得到了明显提高.滤柱沿程去除效率越高,说明滤柱去除氨氮活性恢复越好.因此,总体上看滤柱氨氮去除能力恢复速率:1#自然恢复滤柱>2#碱度滤柱>3#重新挂膜.


图3 滤柱进出水锰随运行时间变化
不同恢复方式下,滤柱进出水锰随运行时间的变化规律如图3所示.由图3可知,在0~10d,锰进水浓度为0.3mg/L,1#自然恢复滤柱和2#碱度恢复滤柱均能在2d内将锰完全去除.后续运行过程中,进水锰浓度逐渐提高至1.5mg/L后,1#自然恢复滤柱和2#滤柱在5d内出水锰浓度就能稳定在0.1mg/L以下.在第21d, 3根滤柱进水锰浓度提升至2.0mg/L,2#滤柱出水锰仍能保持<0.1mg/L,而1#滤柱出水锰浓度却显著波动,直至第27d出水锰浓度才稳定.因此除锰活性恢复速率2#滤柱>1#滤柱.
3#挂膜滤柱由于需要挂膜21d,是在停止投加高锰酸钾后5d后才实现将进水锰完全去除,因此3#挂膜滤柱除锰的活性恢复速度最慢. 3种不同恢复方式下,1#和2#滤柱除锰能力恢复速度均较快,3#挂膜滤柱除锰恢复速度最慢.
2.2 氨氮和锰的相互影响实验
保持进水锰浓度为1mg/L,改变氨氮的进水浓度分别为0, 1.0和2.0mg/L,比较3根滤柱沿程去除锰的效能变化,结果如图4(a)所示.由实验结果可知,随着进水氨氮浓度的提高, 3根滤柱沿程去除锰的能力均出现了显著的下降,表明氨氮的存在抑制了活性滤料对锰的去除能力.但是,仔细比较发现, 3根滤柱中投加碱度恢复滤柱表现最优,说明碱度的提高显著促进了铁锰复合氧化物滤料的活性,这与前期实验的研究结果相一致[23].尽管2#滤柱沿程去除能力出现一定能力下降,但是滤柱出水锰浓度始终低于0.1mg/L,而其他滤柱当进水氨氮浓度提高时,出水锰均出现了超标现象,表明此时自然恢复滤柱和重新挂膜滤柱的去除锰活性较差.当进水氨氮浓度为1mg/L时,随着锰浓度的提高,滤柱沿程去除氨氮的效能不变.结合锰催化氧化去除的机理推测,Mn2+与铁锰复合氧化物上的活性位点结合后被催化氧化生成新的锰氧化物[24],其上有新的活性位点供氨氮反应,因此锰对氨氮的去除没有影响.而氨氮与铁锰复合氧化物上的活性位点结合后,不能提供新的活性位点,因此氨氮的存在抑制了活性滤料对锰的去除能力.

2.3 元素组成与形态分析

图5 恢复运行10d后滤料表面锰氧化物Mn2p的XPS光谱

表2 滤料表面氧化物中各价态锰元素含量
采用XPS对原始滤料、自然恢复滤料、碱度恢复滤料以及重新挂膜滤料表面的锰元素价态及含量进行分析.图5为原始滤料及3根滤柱中样品的Mn2p光谱,光谱在大约642.3和653.9eV处存在2个主峰,分别对应Mn 2p3/2和Mn 2p1/2峰.4种样品的Mn 2p3/2峰可以拟合为3个特征峰,分别对应于Mn4+、Mn3+和Mn2+[25-26].表2列出了各价态锰相应的原子比.值得注意的是,1#滤柱样品中各价态锰的比例与原始滤料相似.2#滤柱样品的Mn3+含量较高(43.7%),说明碱度恢复有利于Mn3+的生成,这可能证明Mn3+在铁锰复合氧化物滤料催化氧化氨氮的过程中发挥了关键的作用,这与先前的研究结果相一致[24,27].3#滤柱样品中Mn2+的比例(19.5%)比原始滤料(17.3%)略高,Mn3+和Mn4+比例也相对低,可能是由于3#滤柱重新挂膜后新生成的氧化物中Mn2+较多.
通过滤料表面元素组成可知(表3), 3种不同恢复方式恢复后的滤料表面组成较原始滤料无明显的变化.表明滤料活性的恢复与元素的组成无显著关联.
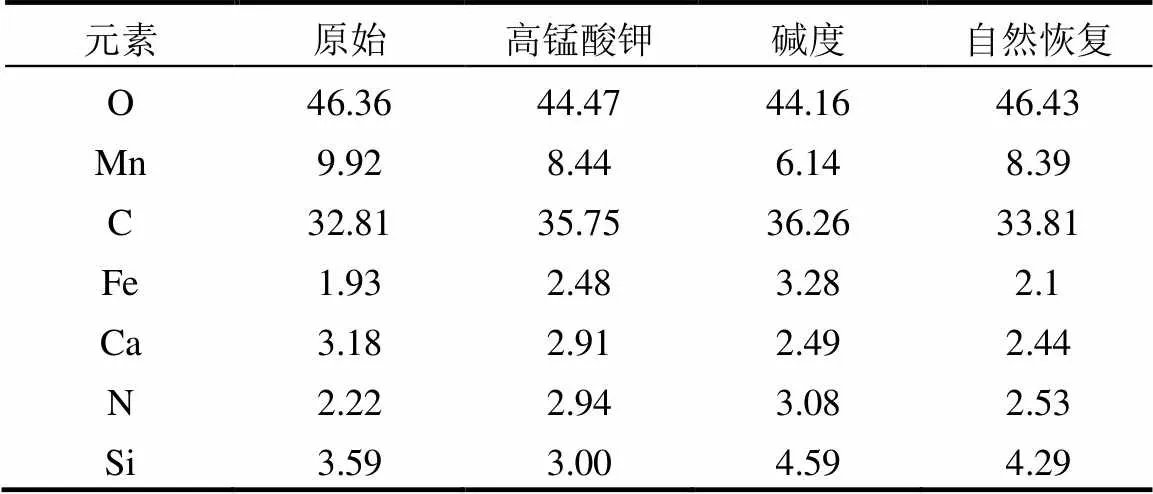
表3 滤料表面元素组成(%)

图6 滤料表面形态比较
采用SEM对滤料的表面形态进行分析,结果如图5所示,原始滤料表面粗糙,由不规则且大小不均匀的颗粒堆积而成(图6(a));重新挂膜后滤料表面形态未发生明显变化(图6(b)),意味着高锰酸盐重新挂膜生成的氧化物与原始氧化膜无显著差异;而经碱度恢复滤料表面形态出现了变化,尽管该滤料表面仍粗糙不平,但是颗粒状较初始滤料不明显(图6(c)),这可能是由于投加的碱度与表面氧化膜相互作用影响;经自然恢复滤料表面趋于光滑(图6(d)).上述研究结果表明,不同恢复条件下运行滤料表面复合锰氧化物形态呈现不同的变化特征.
2.4 XRD分析
为了表征滤料的晶体结构,对3根滤柱不同运行时间的样品进行了XRD检测,结果如图7所示.图7(a)为恢复10d的3滤柱(R1,R2,R3)中氧化物样品的XRD谱图比较,这些XRD谱图与水钠锰矿的谱图较为一致,且表现为低强度的扩散峰[28].但是本文发现,经高锰酸钾重新挂膜滤柱样品的谱图明显比其他2根滤柱样品及原始滤料的结晶度更差,这主要是由于高锰酸钾挂膜新生成了结晶性差的氧化膜负载在滤料表面,而非晶态的结构有利于锰氧化物对污染物的去除[29].此外,还比较了不同运行时间(10,20和35d) 3根滤柱滤料样品氧化膜晶体结构的特征,结果如图7(b)、(c)、(d)所示.结果表明,自然恢复滤柱以及碱度恢复滤柱随运行时间,结晶度基本保持不变,而高锰酸钾重新挂膜滤柱的滤料样品的结晶度也没有发生显著增强,主要是由于本研究中该滤柱运行至24d停止挂膜,其低结晶度主要受其表面负载新生成氧化膜的影响.由于新生成的氧化膜催化活性有限,因此,采取重新挂膜恢复滤料催化活性的方式在3种滤料恢复方式中表现一般.

结合XPS的分析结果,3#重新挂膜滤柱结晶度更差的原因可能与Mn3+比例的降低,Mn2+的含量较高有关.Mn3+比例的降低也不利于氨氮的催化氧化.而1#和2#滤柱样品结晶度与原始滤料相差不大的原因可能是1#和2#滤柱样品中Mn4+、Mn3+和Mn2+的比例相似,Mn3+的比例也相对较高,晶体结构保持较好.综合比较发现,滤料表面氧化物中Mn3+和Mn2+的比例可能与氧化物的结晶度有所关联.活性锰氧化物中Mn3+比例越高,Mn2+的比例越低,活性锰氧化物结晶度就越高,有利于催化氧化活性保持;反之,活性锰氧化物中Mn3+比例越低,Mn2+的比例越高,活性锰氧化物结晶度就越差,不利于活性锰氧化物催化氧化活性的保持.
3 结论
3.1 三种不同恢复方式下,滤柱催化氧化去除氨氮活性恢复速度呈现2#碱度恢复>3#重新挂膜>1#自然恢复的滤柱,其中3#重新挂膜滤柱应对高负荷污染出水浓度波动最大,1#自然恢复滤柱恢复期间出水亚硝氮积累时间最长且峰值最高.
3.2 三种不同恢复方式下,1#自然恢复的滤柱和2#碱度恢复滤柱催化氧化去除锰活性恢复速度均较快. 3#挂膜滤柱由于重新挂膜除锰活性恢复速度最慢.
3.3 氨氮和锰的相互影响结果表明,进水氨氮抑制锰的去除, 3根滤柱中投加碱度恢复滤柱表现最优.随着进水氨氮浓度的升高出水锰浓度始终低于0.1mg/L;锰对氨氮的去除影响不显著.
3.4 XPS和XRD分析结果表明碱度恢复有利于Mn3+的生成,Mn3+在铁锰复合氧化物滤料催化氧化氨氮的过程中发挥了关键的作用,这有助于氨氮的去除.重新挂膜恢复不利于Mn3+的生成,且Mn2+比例会升高,氧化物的结晶度也会降低,不利于氨氮的去除.
3.5 SEM和XRD分析结果表明,不同恢复条件下运行滤料表面复合锰氧化物形态呈现不同的变化特征.自然恢复滤柱以及碱度恢复滤柱随运行时间,结晶度基本保持不变,而高锰酸钾重新挂膜滤柱的滤料样品的结晶度较差.
[1] 李圣品,李文鹏,殷秀兰,等.全国地下水质分布及变化特征 [J]. 水文地质工程地质, 2019,46(6):1–8.
Li S P, Li W P, Yin X L, et al. Distribution and evolution characteristics of national groundwater quality from 2013 to 2017 [J]. Hydrogeology & Engineering Geology, 2019,46(6):1–8.
[2] 余 东,周金龙,陈劲松,等.新疆喀什地区高铁锰地下水空间分布特征及成因分析 [J]. 环境化学, 2020,39(11):3235–3245.
Yu D, Zhou J L, Chen J S, et al. Spatial distribution characteristics and genesis of groundwater with high iron and manganese content in Kashi Prefecture, Xinjiang [J]. Environmental Chemistry, 2020,39(11):3235– 3245.
[3] Wang H, Yang Q, Ma H, et al. Chemical compositions evolution of groundwater and its pollution characterization due to agricultural activities in Yinchuan Plain, northwest China [J]. Environmental Research, 2021,200:111449.
[4] 董姝娟.北京城近郊地下水三氮数值模拟及其自净能力评价 [D]. 中国地质大学(北京), 2010.
Dong S J. Nitrogen numerical simulation in Beijing urban groundwater and monitored naturalattenuation about groundwater [D]. China University of Geosciences (Beijing), 2010.
[5] 危润初,肖长来,梁秀娟.吉林市城区地下水污染时空演化 [J]. 中国环境科学, 2014,34(2):417–423.
Wei R C, Xiao C L, Liang X J. Spatio-temporal evolution of groundwater pollution in the urban areas of Jilin City [J]. China Environmental Science, 2014,34(2):417–423.
[6] Hoaghia M-A, Andrei M L, Cadar O, et al. Health risk assessment associated with nitrogen compounds contaminated drinking water in Medias Region [J]. Studia Universitatis Babes-Bolyai Chemia, Cluj-Napoca: Univ Babes-Bolyai, 2016,61(3):451–460.
[7] Grandjean P, Landrigan P J. Neurobehavioural effects of developmental toxicity [J]. Lancet Neurology, 2014,13(3):330–338.
[8] Farina M, Avila D S, da Rocha J B T, et al. Metals, oxidative stress and neurodegeneration: a focus on iron, manganese and mercury [J]. Neurochemistry International, 2013,62(5):575–594.
[9] Abu Hasan H, Abdullah S R S, Kamarudin S K, et al. Simultaneous NH4+-N and Mn2+removal from drinking water using a biological aerated filter system: Effects of different aeration rates [J]. Separation and Purification Technology, Amsterdam: Elsevier, 2013,118:547– 556.
[10] Qin W, Li W G, Zhang D Y, et al. Ammonium removal of drinking water at low temperature by activated carbon filter biologically enhanced with heterotrophic nitrifying bacteria [J]. Environmental Science and Pollution Research, Heidelberg: Springer Heidelberg, 2016,23(5):4650–4659.
[11] Tobiason J E, Bazilio A, Goodwill J, et al. Manganese Removal from Drinking Water Sources [J]. Current Pollution Reports, Heidelberg: Springer Heidelberg, 2016,2(3):168–177.
[12] 张晓健,林朋飞,陈 超,等.自来水厂应急除锰净水技术研究 [J]. 给水排水, 2013,49(12):27–31.
Zhang X J, Lin P F, Chen C, et al. Study on emergency manganese removal technologies for water treatment plant [J]. Water & Wastewater Engineering, 2013,49(12):27–31.
[13] 徐满天,唐玉朝.源水化学氧化与排泥水生物氧化除锰技术研究 [D]. 合肥:安徽建筑大学, 2017.
Xu M T, Tang Y C. Study on manganese removal technology of chemical oxidation in row water and bacteria oxidation in sludge water [D]. Hefei: Anhui Jianzhu University, 2017.
[14] Diaz-Alarcón J A, Alfonso-Pérez M P, Vergara-Gómez I, et al. Removal of iron and manganese in groundwater through magnetotactic bacteria [J]. Journal of Environmental Management, 2019,249:109381.
[15] 刘文龙,钱仁渊,包宗宏.吹脱法处理高浓度氨氮废水 [J]. 南京工业大学学报(自然科学版), 2008,(4):56–59.
Liu W L, Qian R Y, Bao Z H. Treatment of high concentration ammonia-nitrogen wastewater by air stripping [J]. Journal of Nanjing Tech University (Natural Science Edition), 2008,(4):56–59.
[16] 何彩庆,陈云嫩,殷若愚,等.离子交换/吸附法净化氨氮废水的研究进展 [J]. 应用化工, 2021,50(2):481–485.
He C Q, Chen Y N, Yin R Y, et al. Removal of ammonium from water and wastewater using the adsorption and ion exchange method: a review [J]. Applied Chemical Industry, 2021,50(2):481–485.
[17] 王刘煜,李 冬,曾辉平,等.生物滤池同步净化低温高铁锰氨氮地下水[J]. 中国环境科学, 2019,39(8):3300-3307.
Wang L Y, Li D, Zeng H P, et al. Simultaneous purification of high-iron, manganese and ammonia nitrogen from low temperature groundwater in biological filter [J]. China Environmental Science, 2019,39(8):3300-3307.
[18] Sathishkumar K, Murugan K, Benelli G, et al. Bioreduction of hexavalent chromium by Pseudomonas stutzeri L1and Acinetobacter baumannii L2 [J]. Annals of Microbiology, 2017,67(1):91–98.
[19] 曹 昕.铁锰复合氧化物催化氧化去除地下水中氨氮研究 [D]. 西安建筑科技大学, 2015.
Cao X. The study on catalytic oxidation of ammonia in groundwater by co-oxides of iron and manganese [D]. Xi'an University of Architecture & Technology, 2015.
[20] 白筱莉,黄廷林,张瑞峰,等.铁锰复合氧化膜同步去除地表水中氨氮和锰 [J]. 中国环境科学, 2017,37(12):4534–4540.
Bai X L, Huang T L, Zhang R F, et al. The simultaneous removal of ammonium and manganese from surface water by iron-manganese co-oxides film [J]. China Environmental Science, 2017,37(12):4534– 4540.
[21] Cheng Y, Xiong W Y, Huang T L. Mechanistic insights into effect of storage conditions of Fe-Mn co-oxide filter media on their catalytic properties in ammonium-nitrogen and manganese oxidative removal [J]. Separation and Purification Technology, Amsterdam: Elsevier, 2021,259:118102.
[22] Cheng Y, Huang T L, Sun Y, et al. Catalytic oxidation removal of ammonium from groundwater by manganese oxides filter: Performance and mechanisms [J]. Chemical Engineering Journal, 2017, 322:82–89.
[23] Cheng Y, Zhang S S, Huang T L, et al. Effect of alkalinity on catalytic activity of iron–manganese co-oxide in removing ammonium and manganese: Performance and mechanism [J]. International Journal of Environmental Research and Public Health, 2020:14.
[24] Cheng Y, Xiong W Y, Huang T L. Catalytic oxidation removal of manganese from groundwater by iron–manganese co-oxide filter films under anaerobic conditions [J]. Science of The Total Environment, 2020,737:139525.
[25] Liang X, Hart C, Pang Q, et al. A highly efficient polysulfide mediator for lithium–sulfur batteries [J]. Nature Communications, 2015,6(1): 5682.
[26] Ilton E S, Post J E, Heaney P J, et al. XPS determination of Mn oxidation states in Mn (hydr)oxides [J]. Applied Surface Science, 2016,366:475–485.
[27] Madison A S, Tebo B M, Mucci A, et al. Abundant porewater Mn(III) is a major component of the sedimentary redox system [J]. Science, American Association for the Advancement of Science, 2013.
[28] Bruins J H, Petrusevski B, Slokar Y M, et al. Biological and physico-chemical formation of Birnessite during the ripening of manganese removal filters [J]. Water Research, 2015,69:154–161.
[29] Yang H, Yan Z, Du X, et al. Removal of manganese from groundwater in the ripened sand filtration: Biological oxidation versus chemical auto-catalytic oxidation [J]. Chemical Engineering Journal, 2020,382: 123033.
Optimization of recovery method for catalytic ammonium/manganese oxidation by active filter media.
CHENG Ya, ZHANG Yong-zhi, ZHENG Jia-hui, LI Yu-yang, HUANG Ting-lin*
(Shaanxi Key Laboratory of Environmental Engineering, Key Laboratory of Northwest Water Resource, Ministry of Education, School of Environmental and Municipal Engineering, Xi’an University of Architecture and Technology, Xi’an 710055, China)., 2022,42(5):2112~2119
Taking deactivated filter media as the research object, the effects of three different recovery methods (natural recovery, adding basicity, and re-hanging film) on the catalytic oxidation efficiency of the filter media for ammonium (NH4+-N) and manganese (Mn2+) removal were investigated. The experimental results showed that the NH4+-N removal rate of natural recovery (1#) filter column, adding basicity (2#) filter column and re-hanging film (3#) filter column was above 90% after running for 4d, 2d and 3d, respectively. When the influent NH4+-N concentration increased gradually, the effluent NH4+-N concentration of 3# filter column fluctuated the most, while the effluent nitrite accumulation time of 1# filter column was the longest and the peak value was the highest. The recovery rate of Mn2+removal activity of all three filter columns was fast. Both 1# and 2# filter columns could completely remove Mn2+in 2 days and 3# filter column could completely remove the influent Mn2+within 5days after stopping adding potassium permanganate. The experimental results of the interaction between NH4+-N and Mn2+showed that 2# filter column performed the best among the three filter columns. Although NH4+-N inhibited the removal of Mn2+, with the increase of influent NH4+-N concentration, the effluent Mn2+concentration of the 2# filter column was always lower than 0.1mg/L. Mn2+had no significant effect on NH4+-N removal. The results of XRD analysis showed that the crystallinity of the filter media samples in 3# filter column was poor due to the influence of the new formed oxide film on its surface. Considering the recovery efficiency of NH4+-N and Mn2+as well as the addition of chemical agents, the natural recovery method is the most suitable recovery method.
activity recovery;deactivated filter media;ammonium/manganese removal;catalytic oxidation;groundwater treatment
X523
A
1000-6923(2022)05-2112-08
程 亚(1990-),女,山东济宁人,副教授,博士,主要研究方向为微污染水源水处理.发表论文10余篇.
2021-09-22
国家自然科学基金资助项目(52000145,51778521);国家重点研发计划项目(2019YFD1100101)
* 责任作者, 教授, huangtinglin@xauat.edu.cn
