基于Nrf2信号通路探讨艾迪注射液联合GP化疗干预Lewis肺癌小鼠的作用研究
2022-06-01陈函王柯胡志强马康汪静
陈函 王柯 胡志强 马康 汪静
〔摘要〕 目的 探討艾迪注射液联合吉西他滨+顺铂化疗干预Nrf2信号通路对Lewis肺癌小鼠的作用。方法 建立Lewis肺癌小鼠模型40只,随机分为5组,模型组每天给予生理盐水0.1 mL/10 g;GP化疗组给予顺铂5 mg/kg+吉西他滨50 mg/kg;低、中、高剂量组在GP化疗组的基础上分别给与艾迪注射液0.05 mL/10 g、0.1 mL/10 g、0.2 mL/10 g。顺铂每5 天给予一次,吉西他滨每7天给予一次,给药共14 d。实验期间观察小鼠的一般活动状况,监测小鼠体质量。实验结束后检测小鼠瘤体积;ELISA法检测IL-6表达水平;免疫组化法检测Nrf2信号通路关键蛋白的表达;HE染色分析小鼠各主要脏器及肿瘤组织的病理变化。结果 (1)治疗14 d后,与模型组比较,0~5 d各治疗组小鼠体质量均出现不同程度下降,而随着实验时间的延长,低、中和高剂量组小鼠体质量开始增长,而GP化疗组小鼠后期体质量呈下降趋势。与模型组比较,各治疗组小鼠瘤体积显著降低(P<0.01),并且各组瘤重显著下降(P<0.001),其中中剂量组的抑瘤率最高,高剂量组及低剂量组次之,GP化疗组抑瘤率最低。(2)与模型组比较,GP化疗组脾与胸腺指数显著降低(P<0.05),而与GP化疗组比较,低、中和高剂量组脾与胸腺指数显著增加。(3)与模型组比较,各组IL-6表达均明显下降(P<0.05);与GP化疗组相比,中剂量组IL-6表达明显下降(P<0.05)。(4)与模型组比较,GP化疗导致的肝、肾脏器损伤可被艾迪注射液改善,并能协同GP化疗杀伤肿瘤细胞。(5)与模型组相比,GP化疗组Nrf2、NQO1、GSTA1和HO-1蛋白表达量均上升(P<0.05);与GP化疗组相比,低、中和高剂量组Nrf2、NQO1、GSTA1和HO-1蛋白表达量均降低(P<0.05)。结论 艾迪注射液联合GP化疗可干预Nrf2信号通路发挥抗小鼠Lewis肺癌作用,且艾迪注射液可对GP化疗起到减毒增效作用。
〔关键词〕 艾迪注射液;GP化疗;Lewis肺癌;IL-6;Nrf2信号通路
〔中图分类号〕285.5 〔文献标志码〕A 〔文章编号〕doi:10.3969/j.issn.1674-070X.2022.05.011
The effect of Aidi injection combined with GP chemotherapy on Lewis lung cancer
mice based on Nrf2 signaling pathway
CHEN Han WANG Ke HU Zhiqiang MA Kang WANG Jing
(1. College of Pharmacy, Ningxia Medical University, Yinchuan, Ningxia 750004, China; 2. Key Laboratory of Ningxia Ethnomedicine Modernization, Ministry of Education, Ningxia Medical University, Yinchuan, Ningxia 750004, China;
3. Oncology Hospital, General Hospital of Ningxia Medical University, Yinchuan, Ningxia 750004, China)
〔Abstract〕 Objective To investigate the effect of Aidi injection combined with gemcitabine and cisplatin chemotherapy on Nrf2 signaling pathway in Lewis lung cancer mice. Methods Forty Lewis lung cancer model in mice were established, which were randomly divided into five groups: model group was given normal saline (0.1 mL/10 g) every day. GP chemotherapy group was given cisplatin 5 mg/kg+gemcitabine 50 mg/kg. On the basis of GP chemotherapy group, the low-dose, medium-dose and high-dose groups were given 0.05 mL/10 g, 0.1 mL/10 g, 0.2 mL/10 g Aidi injection respectively. Cisplatin was given every 5 days, and gemcitabine was given every 7 days for 14 days. The general activity of the mice was observed and the weight and the change of the tumors volume in mice were recorded. The expression level of IL-6 was detected by ELISA, and expression of key proteins in Nrf2 signaling pathway were detected by immunohistochemical staining, the pathological changes of the major organs and the tumors in mice were tested by HE staining. Results (1) After 14 days of treatment, the body weight of mice in each treatment group was decreased in different degrees compared with model group in 0-5 days. With the extension of experimental time, the body weight of mice in low-dose, medium-dose and high-dose groups began to increase, while the body weight of mice in GP chemotherapy group showed a downward trend in the later stage. Compared with the model group, tumor volume of each treatment group was significantly reduced (P<0.01), and tumor weight of each treatment group was significantly reduced (P<0.001), the medium-dose group had the highest tumor inhibition rate, followed by the high-dose and low-dose groups, and the GP chemotherapy group showed the lowest tumor inhibition rate. (2) Compared with the model group, the index of spleen and thymus in GP chemotherapy group decreased significantly (P<0.05), compared with GP chemotherapy group, the index of spleen and thymus in low-dose, medium-dose and high-dose groups increased significantly (P<0.05). (3) Compared with model group, the expression of IL-6 in each group decreased significantly (P<0.05). Compared with GP chemotherapy group, the expression of IL-6 in the medium-dose group decreased significantly (P<0.05). (4) Compared with model group, the damage of liver and kidney organs caused by GP chemotherapy could be improved by Aidi injection, and tumor cells could be killed with GP chemotherapy. (5) Compared with model group, the expression levels of Nrf2,NQO1, GSTA1 and HO-1 protein in GP chemotherapy group were higher than those in model group (P<0.05). Compared with GP chemotherapy group, the expression levels of Nrf2, NQO1, GSTA1 and HO-1 protein in low-dose, medium-dose and high-dose groups decreased (P<0.05). Conclusion Aidi injection combined GP chemotherapy could play the role on reducing toxicity and increasing efficacy through intervening Nrf2 signaling in anti-Lewis lung cancer.17F5C7C4-E5BB-40FE-9927-32BC637A3486
〔Keywords〕 Aidi injection; GP chemotherapy; Lewis lung cancer; IL-6; Nrf2 signaling pathway
我国肺癌的发病率呈上升趋势,且死亡率位居其他癌症之首[1-3]。化疗是中晚期肺癌患者治疗的主要手段,但化疗药的不良反应严重影响患者的生存质量,因此,如何降低化疗带来的不良反应而提高疗效已经成为肿瘤研究的热点之一。近年来,研究证实,中医药可以联合化疗药物通过调节免疫、抗氧化应激等发挥减毒增效的作用[4-5]。Nrf2信号通路是细胞存活的重要防御机制之一[6]。研究发现,肿瘤细胞中Nrf2的累积可抵抗放化疗所产生的氧化应激损伤,导致癌症治疗效果下降[7-8]。艾迪注射液由斑螯、人参、黄芪、刺五加等经提取精制而成,用于多种癌症的辅助治疗及术后的巩固治疗[9-10]。本研究将艾迪注射液联合GP化疗(吉西他滨+顺铂)用于治疗小鼠Lewis肺癌,旨在探究其疗效及艾迪注射液对GP化疗的减毒增效作用。
1 材料和方法
1.1 实验动物
40只SPF级雌性C57BL/6N小鼠购于北京维通利华实验动物技术有限公司[SCXK9(京)2016-0006],分笼饲养于宁夏医科大学实验动物中心[宁夏医科大学伦理第2018-50号],鼠龄(28~34) d,体质量(14±2) g。均自由饮水及饮食,环境温度(20±2) ℃,相对湿度45%~70%。本研究符合3R原则[11]并经宁夏医科大学实验动物伦理委员会批准同意,动物使用伦理审批号IACUC-NYLAC-2019-104。
1.2 实验细胞系
小鼠Lewis肺癌细胞株(LLC)(批号:191012,中国科学院典型培养物保藏委员会细胞库)于宁夏医科大学宁夏特色中医药协同创新中心保存并进行实验。
1.3 主要试剂
艾迪注射液(批号:20180912,贵州益佰制药股份有限公司);顺铂(批号:15663-27-1,上海源叶生物科技有限公司);吉西他滨(批号:95058-81-4,上海源叶生物科技有限公司);小鼠IL-6 ELISA试剂盒(批号:EK0411,武汉博士德生物工程有限公司);Nrf2、NQO1、GSTA1和HO-1抗体(批号:AF0639、DF6437、DF6514、AF5393,江苏亲科生物研究中心有限公司)。
1.4 主要仪器
CO2培养箱(型号:3111,赛默飞世尔科技有限公司);酶标仪(型号:SIM-F124,美国热电公司);涡旋机(型号:MX-S,上海珂淮仪器有限公司);组织切片机(型号:cm1950,德国徕卡公司);正置荧光显微镜(型号:BX53F,日本奥林巴斯有限公司)。
1.5 动物模型制备及分组
复苏培养LLC细胞,当细胞生长状态良好并处于对数生长期时收集细胞。稀释细胞至5×106个/mL,吸取细胞悬液后,于C57BL/6N小鼠右侧背部皮下进行注射(0.2 mL/只)。肿瘤体积大于50 mm3时将40只小鼠随机分为5组。(1)模型组:给予生理盐水腹腔注射,不做其他处理。(2)GP化疗组:给予顺铂(5 mg/kg,0.2 mL/只,每5天腹腔注射给药)和吉西他滨(50 mg/kg,0.2 mL/只,每7天腹腔注射给药)。(3)低剂量组:艾迪注射液0.05 mL/10 g腹腔注射,每天1次,连续2周;顺铂和吉西他滨用量用法同GP化疗组。(4)中剂量组:艾迪注射液0.1 mL/10 g腹腔注射,每天1次,连续2周;顺铂和吉西他滨用量用法同GP化疗组。(5)高剂量组:艾迪注射液0.2 mL/10 g腹腔注射,每天1次,连续2周;顺铂和吉西他滨用量用法同GP化疗组。
1.6 观察指标
1.6.1 小鼠一般状况及体质量、肿瘤体积变化 每天定时观察记录小鼠饮食饮水、毛发亮度及精神状态等情况。在实验期间每2天测体质量并采用游标卡尺測量各组小鼠肿瘤体积,根据公式,瘤体积(V)=1/2ab2(a代表肿瘤长径,b代表肿瘤短径)[12],单位为mm3;实验结束后,处死小鼠,剥取心、肝、脾、肺、肾、胸腺以及肿瘤并测脏器质量,分别计算脏器指数与抑瘤率。根据公式,脏器指数(脏器指数=脏器质量/动物质量×100%);抑瘤率=(模型组肿瘤体积-治疗组肿瘤体积)/模型组肿瘤体积×100%[13]。
1.6.2 小鼠血清IL-6水平检测 小鼠处死前眼球取血,12 000 r/min离心5 min(离心半径8 cm),取血清放置-80 ℃冰箱中备用。根据ELISA试剂盒说明书进行IL-6检测。
1.6.3 小鼠各器官及肿瘤组织HE染色 心、肝、脾、肺、肾与肿瘤组织均经甲醛固定、系列脱水和透明后,石蜡包埋、切片、复水、染色。染色结束后,将石蜡切片进行脱水及透明。最后滴加中性树胶,加盖玻片封片,随后在正置荧光显微镜下观察,拍照记录。
1.6.4 小鼠肿瘤组织免疫组化检测 肿瘤组织经甲醛固定后,石蜡包埋,切片,厚度约5 μm。常规脱蜡、水化,高温修复抗原,免疫组化画圈笔圈住组织,滴加内源性过氧化物酶阻断剂,孵育后,分别滴加Nrf2、NQO1、GSTA1和HO-1抗体(1∶200),4 ℃冰箱孵育过夜。PBS冲洗,滴加反应增强液,PBS冲洗,滴加增强酶标山羊抗兔IgG聚合物,PBS冲洗,DAB显色,苏木精复染,脱水,二甲苯透明,中性树胶封片,光学显微镜下观察,拍照,ImageJ统计阳性表达量(n≥3)。
1.7 统计学方法17F5C7C4-E5BB-40FE-9927-32BC637A3486
数据分析采用SPSS 24.0软件进行。对于计量资料,数据采用“x±s”表示,多组样本间均数比较采用One-way ANOVA,方差不齊采用秩和检验。检验水准α=0.05,P<0.05表示差异有统计学意义。
2 结果
2.1 艾迪注射液联合GP化疗对Lewis肺癌小鼠一般情况的影响
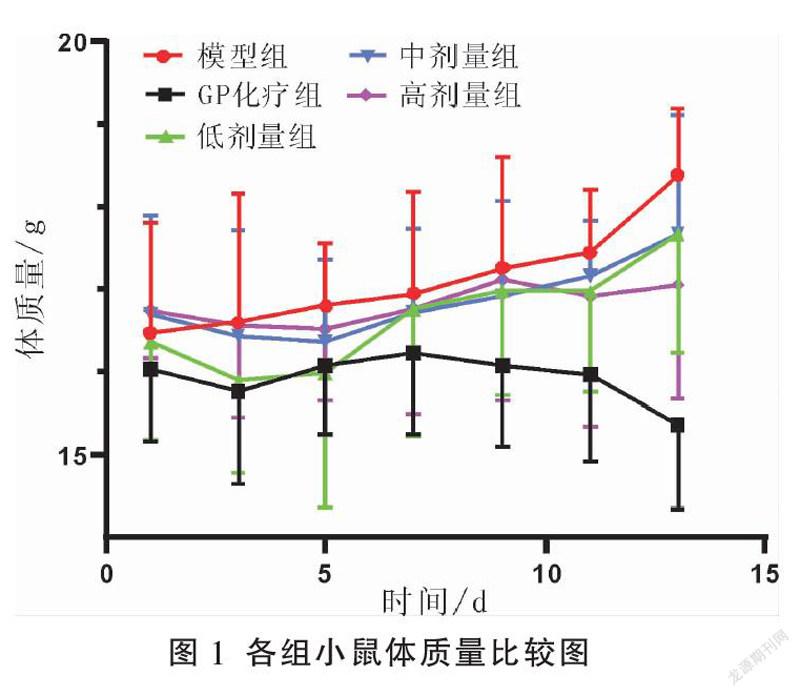
接种Lewis肺癌细胞约3 d后,小鼠后背皮下肿瘤体积大于50 mm3,此时各组给予相应药物治疗。治疗期间,模型组小鼠体质量稳步增长,毛发亮丽,进食饮水正常,反应灵敏。GP化疗组小鼠体质量增长缓慢,后期体质量呈下降趋势,随着给药次数增多及治疗时间延长,小鼠毛发杂乱,倦卧懒动,进食及饮水量减少,反应迟钝,而低、中和高剂量组小鼠体质量增幅、毛发杂乱程度、进食饮水及对外界刺激的反应均优于GP化疗组。
2.2 艾迪注射液联合GP化疗对Lewis肺癌小鼠体质量及抑瘤率的影响
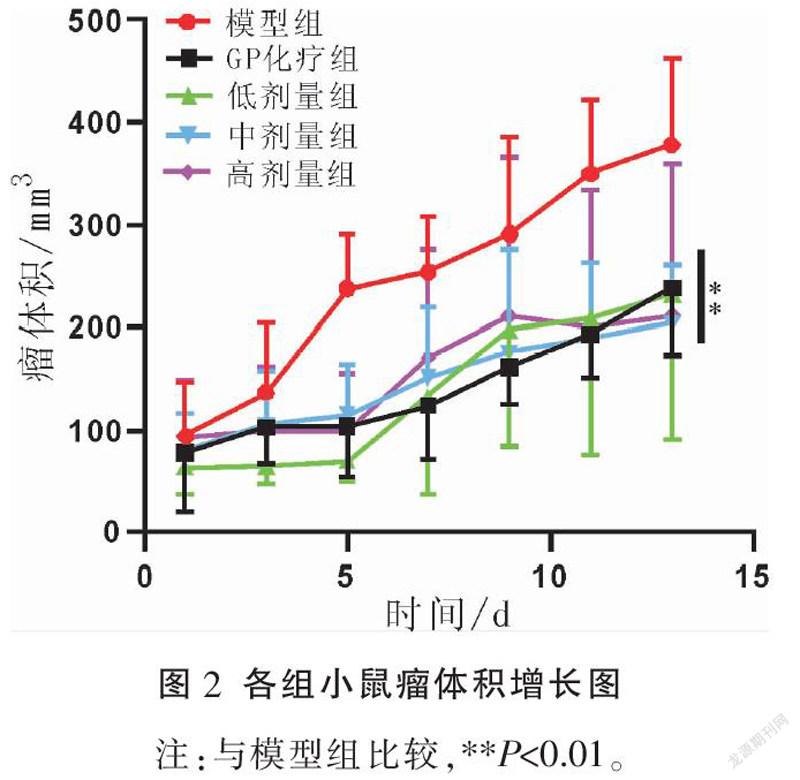
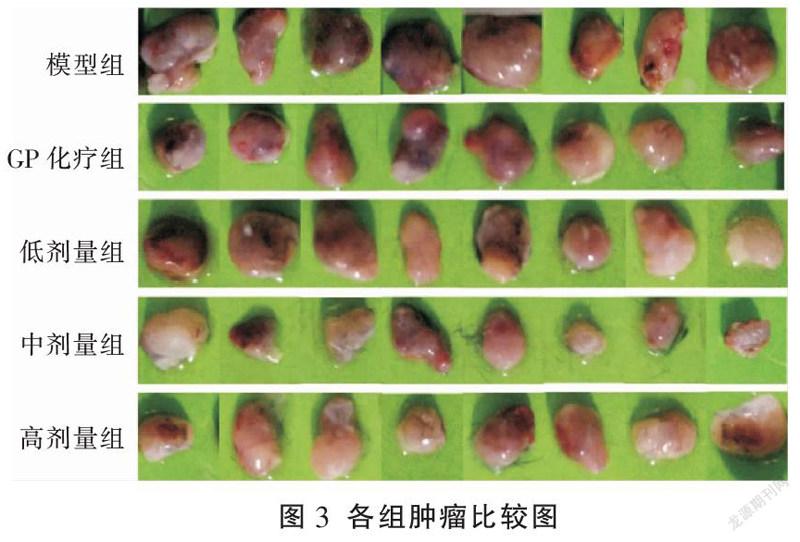
各组小鼠造模前体质量差异无统计学意义(P>0.05)。与模型组比较,前期0~5 d各治疗组小鼠体质量出现不同程度下降,而随着实验时间的延长,低、中和高剂量组小鼠体质量开始增长,而GP化疗组小鼠后期体质量呈下降趋势。与模型组比较,各组肿瘤体积显著降低(P<0.01),并且各组瘤重显著下降(P<0.001);与GP化疗组比较,低、中和高剂量组瘤重均下降,其中中、高剂量组差异具有统计学意义(P<0.05)。与GP化疗组比较,低、中和高剂量组抑瘤率均上升,其中中、高剂量组差异具有统计学意义(P<0.05)。详见图1-3、表1。
2.3 艾迪注射液联合GP化疗对Lewis肺癌小鼠脏器指数的影响
各组小鼠心、肝和肺脏器指数差异无统计学意义(P>0.05)。肾脏方面,与模型组比较,GP化疗组和低剂量组质量降低(P<0.05);与GP化疗组比较,高剂量组质量增加(P<0.05);低、中、高剂量组差异无统计学意义(P>0.05)。脾与胸腺方面,与模型组比较,GP化疗组质量降低(P<0.01),与GP化疗组比较,低、中、高剂量组质量均增加(P<0.05);低、中、高剂量组差异无统计学意义(P>0.05)。详见表2。
2.4 艾迪注射液联合GP化疗对Lewis肺癌小鼠血清中IL-6表达水平的影响
与模型组比较,各组小鼠血清中IL-6水平均明显下降(P<0.05);与GP化疗组相比,中剂量组IL-6水平明显下降(P<0.05);低、中、高剂量组间差异无统计学意义(P>0.05)。详见图4。
2.5 艾迪注射液联合GP化疗对Lewis肺癌小鼠脏器组织病理的影响
模型组心脏和肺脏组织结构完整,未有病变产生;在肝脏与肾脏组织中,肝细胞结构完整、排列整齐,肾脏组织中有偶见炎症细胞浸润,肾小管上皮细胞伴有轻微水肿;脾脏组织中红髓和白髓界限清晰。GP化疗组心脏与肺脏组织中,心肌结构稍紊乱,部分纤维间隙增大;在肝脏与肾脏组织中,肝细胞中度水肿并伴有炎症浸润,细胞核出现边缘化,核固缩溶解消失,且肾小球出现严重核固缩现象,并且基底膜增厚,炎症细胞浸润,出现“玻璃样”病变,表明GP化疗对小鼠肝肾损伤严重;在脾脏组织中,红髓和白髓界限紊乱,淋巴细胞数量减少,细胞排列散乱,红髓里有大量红细胞。经低、中、高剂量组治疗后,可见肝组织内胞质丰富,细胞核膜完整,偶有细胞质空洞样变,轮廓清晰;肾组织内肾小球结构较完整,固缩较改善,紊乱程度减轻;脾组织内红髓和白髓交界明显,胞排列相对整齐,红髓里红细胞数量减少,淋巴细胞增多。以上研究表明,艾迪注射液与GP联用后,可明显改善GP化疗对主要脏器的损伤程度。肿瘤组织HE染色结果显示,模型组肿瘤细胞核大而圆,呈条索状排列整齐;GP化疗组肿瘤细胞较多出现核固缩、边缘化;艾迪注射液与之联合后可见肿瘤细胞大部分出现核固缩现象,空泡化明显,细胞间排列紊乱,病理性核分裂明显减少,表明艾迪注射液联合GP化疗显著促进肿瘤细胞的凋亡。详见图5。
2.6 艾迪注射液联合GP化疗对Lewis肺癌小鼠肿瘤组织中Nrf2信号通路的影响
与模型组相比,GP化疗组Nrf2、NQO1、GSTA1和HO-1蛋白表达量均上升(P<0.01),而低、中和高剂量组Nrf2、NQO1、GSTA1和HO-1蛋白表达量均降低(除低剂量组的NQO1表达)(P<0.05)。与GP化疗组相比,低、中和高剂量组Nrf2、NQO1、GSTA1和HO-1蛋白表达量均降低(P<0.001)。高剂量组Nrf2、NQO1及GSTA1蛋白表达量较低、中剂量组低(P<0.01);低、中剂量组HO-1蛋白表达差异无统计学意义(P>0.05),但均较高剂量组低(P<0.01)。详见图6。
3 讨论
肺癌的发生、发展与多种因素有关。肺癌早期难以被发现,确诊时多已是中晚期[14-15]。很多中晚期患者需要接受放化疗来延长总生存期,因此,放化疗带来的不良反应贯穿整个癌症治疗的始终[16-17]。张晓春[18]研究发现,艾迪注射液联合GP方案在非小细胞肺癌的治疗中,抗癌效应增加,患者的生存质量改善,化疗的不良反应减少。库丽加那提·帕提汗等[19]研究发现,对肺腺癌小鼠采用多西紫杉醇化疗中应用艾迪注射液,可以提升抑瘤效果。
本研究结果显示,艾迪注射液与GP化疗联合后,可改善小鼠的食欲状况,并发挥抑瘤作用(P<0.05)。更为重要的是,与GP化疗组相比,艾迪注射液与GP化疗联合可提升主要免疫器官的脏器指数,对主要脏器脾脏和胸腺等免疫器官起到保护作用(P<0.05);并能显著改善GP化疗对主要脏器(肾)的损伤情况。IL-6属于多效细胞因子,具有促进肿瘤生长、增殖和复发的作用[20-21],艾迪注射液联合GP化疗可以显著降低小鼠血清中IL-6水平(P<0.05)。Nrf2作为调控抗氧化的主要因子,在肿瘤细胞中的稳定或异常表达创造了有利于肿瘤细胞生存的环境[22-23]。当肿瘤细胞给予顺铂后,会触发细胞内的氧化应激,诱导肿瘤细胞凋亡[24]。与此同时,胞内活性氧升高,Nrf2会被激活进入细胞核并激活相关的Ⅱ相解毒酶,如NQO1、GSTA1和HO-1,从而削弱化疗药的“杀”细胞作用,保护细胞生存[25]。本研究中艾迪注射液联合GP化疗可显著降低肿瘤组织中Nrf2、NQO1、GSTA1与HO-1蛋白表达水平(P<0.05)。而在本研究,低、中和高剂量组在不同方面有着较好的抗肿瘤及减毒增效作用,而具体某种剂量下结果最优仍需后期深入研究。17F5C7C4-E5BB-40FE-9927-32BC637A3486
总之,艾迪注射液联合GP化疗可通过干预Nrf2信号通路对Lewis肺癌小鼠起到减毒增效的作用。本研究结果将为优化肺癌病人的治疗方案和弘扬我国中药制剂(艾迪注射液)提供有力的实验证据。
参考文献
[1] 辛雯艳,黄 磊,闫贻忠.2005-2013年中国肿瘤登记地区肺癌流行和疾病负担时间趋势分析[J].中华肿瘤防治杂志,2019,26(15): 1059-1065.
[2] SATO K, MIMAKI S, YAMASHITA R, et al. Association between the mutational smoking signature and the immune microenvironment in lung adenocarcinoma[J]. Lung Cancer, 2020, 147: 12-20.
[3] KUDO K, OHASHI K, MAKIMOTO G, et al. Triplet therapy with afatinib, cetuximab, and bevacizumab induces deep remission in lung cancer cells harboring EGFR T790M in vivo[J]. Molecular Oncology, 2017,11(6): 670-681.
[4] 周 辉,刘 畅,刘杨霖,等.猴头菌多糖对Lewis肺癌荷瘤小鼠抑瘤作用及其机制研究[J].湖南中医药大学学报,2017,37(12):1320-1322.
[5] 邱 晓,李学涛,居瑞军,等.中药“扶正固本”与化疗药联合抗肿瘤的研究进展[J].世界中西医结合杂志,2018,13(11):1615-1619.
[6] 杨开锋,李 兰,周 虹,等.氧化应激与细胞自噬凋亡对卵巢早衰调控的研究进展[J].湖南中医药大学学报,2021,41(5):809-814.
[7] KITAMURA H, MOTOHASHI H. NRF2 addiction in cancer cells[J]. Cancer Science, 2018, 109(4): 900-911.
[8] JUNG B J, YOO H S, SHIN S, et al. Dysregulation of NRF2 in cancer: from molecular mechanisms to therapeutic opportunities[J]. Biomolecules & Therapeutics, 2018, 26(1): 57-68.
[9] XIAO Z, JIANG Y, WANG C Q, et al. Clinical efficacy and safety of aidi injection combination with vinorelbine and cisplatin for advanced non-small-cell lung carcinoma: A systematic review and meta-analysis of 54 randomized controlled trials[J]. Pharmacological Research, 2020, 153: 104637.
[10] 张 红,张向业.艾迪注射液配合化疗治疗晚期非小细胞肺癌临床观察[J].湖南中医药大学学报,2009,29(4):65-66.
[11] 马雪曼,于明薇,张甘霖,等.小鼠Lewis肺癌不同部位皮下移植瘤模型的比较[J].中国实验动物学报,2017,25(4):386-390.
[12] 周 婷,荣风年,赵 珊,等.丙戊酸对卵巢癌SKOV3裸鼠移植瘤生长抑制作用的研究[J].中国老年学杂志,2008(9):851-853.
[13] 周 婷.丙戊酸对卵巢癌SKOV3裸鼠移植瘤生长抑制作用的研究[D].济南:山东大学,2008.
[14] 赵炳芬.吉西他滨或长春瑞滨联合顺铂治疗国人非小细胞肺癌近期疗效与骨髓抑制的Meta分析[J].重庆医学,2016,45(29):4092-4094.
[15] 苏 雷,魏秀芹.从我国肺癌防控发展看早期肺癌的诊疗策略[J]. 医学研究杂志,2020,49(9):1-5.
[16] 白红松,寿建忠,毕新刚,等.87例肌层浸润性膀胱癌新辅助化疗的临床疗效分析[J].临床泌尿外科杂志,2021,36(9):704-708.
[17] KATHAWALA R J, GUPTA P, ASHBY C R, et al. The modulation of ABC transporter-mediated multidrug resistance in cancer: a review of the past decade[J]. Drug Resistance Updates, 2015, 18: 1-17.
[18] 张晓春.艾迪注射液联合GP方案治疗非小细胞肺癌临床观察[J]. 辽宁中医药大学学报,2016,18(2):173-175.
[19] 库丽加那提·帕提汗,艾力扎提·艾则孜,侯梅华.艾迪注射液对肺腺癌小鼠多西紫杉醇化疗敏感性的影响探讨[J].临床和实验医学杂志,2018,17(14):1465-1469.
[20] TANAKA T, KISHIMOTO T. Targeting interleukin-6: all the way to treat autoimmune and inflammatory diseases.[J]. International Journal of Biological Sciences, 2012, 8(9): 1227-1236.
[21] 王永清,韩媛媛,韩德兰,等.黄芪多糖联合顺铂对Lewis肺癌小鼠的抑瘤作用及其机制[J].山东医药,2017,57(44):39-41.
[22] 张昆鹏,张晓愉,李少一,等.圣草酚通过调节Nrf2通路促进氧化应激诱导的肝癌细胞的凋亡[J].中国免疫学杂志,2021,37(12):1449-1453.
[23] MENEGON S, COLUMBANO A, GIORDANO S. The dual roles of NRF2 in cancer[J]. Trends in Molecular Medicine, 2016, 22(7): 578-593.
[24] 孙朝跃.野黄芩苷增敏顺铂抗非小细胞肺癌以及对顺铂肾毒性保护作用研究[D].广州:广州中医药大学,2019:1-117.
[25] JEDDI F, SOOZANGAR N, SADEGHI M R, et al. Contradictory roles of Nrf2/Keap1 signaling pathway in cancer prevention/promotion and chemoresistance[J]. DNA Repair, 2017, 54: 13-21.
(本文編辑 周 旦)17F5C7C4-E5BB-40FE-9927-32BC637A3486
