基于真实情境的工艺流程复习课项目式教学研究
2022-05-30钟素琴李根薰邹标
钟素琴 李根薰 邹标


摘 要:以“磷酸铁锂电池正极金属材料回收”为研究课题,通过“磷酸铁锂电池正极材料分离探讨”“设计分离磷酸铁锂电池中锂、铁元素的实验方案”“对磷酸铁锂电池中锂铁元素分离工艺的评价及改进”,开展磷酸铁锂电池的回收工艺设计探讨,结合科学思维方法,设计实验方案,培养学生运用科学方法进行方案设计的能力。
关键词:磷酸铁锂电池;深度学习;真实情境;项目式
化学工艺流程是高考化学难点内容。工艺流程题是涉及化学实验基础知识、化学理论、概念,工业生产知识等。需要学生全面综合判断,灵活运用所学理论进行深度问题解决。工艺流程的教学也是教师教学的难点问题,教师既要着重于基础又要关注学生现场学习、归纳总结、迁移运用等能力培养。本文将介绍基于真实情境的工艺流程复习课项目式学习教学案例,学生通过自主设计工艺流程,并在流程的逐步完善中实现真实问题的深度解决。
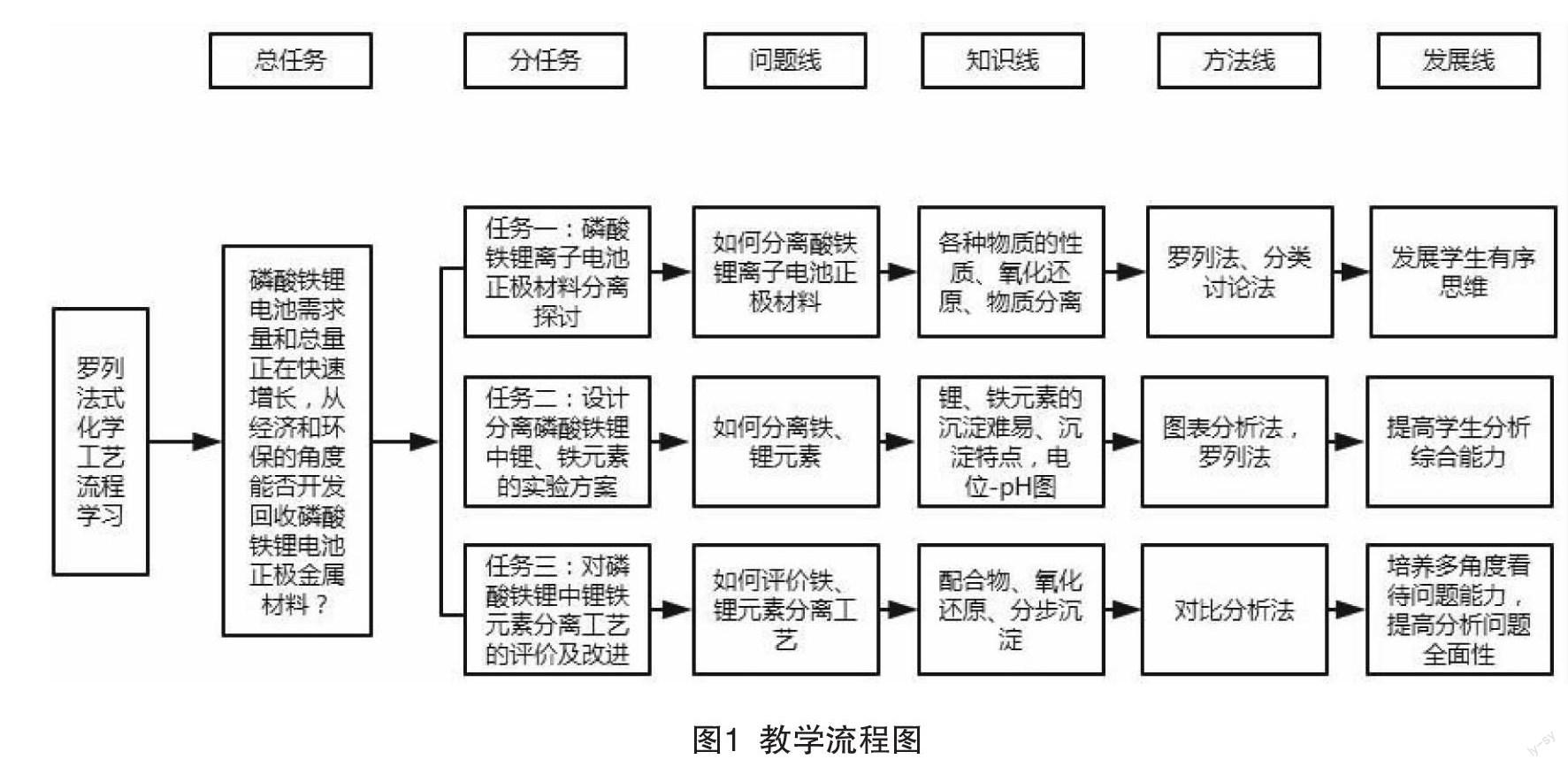
1 教学目标和教学流程
本节课结合深度学习的理念将学生置于真实情景的学习氛围中,通过3个任务的解决实现磷酸铁锂电池中有价金属元素的工艺流程设计。本节课教学目标为:(1)能根据物质的性质,结合沉淀溶解平衡和氧化还原反应等原理,分析从磷酸铁锂电池中分离有价金属的方法;(2)能灵活运用罗列法完成磷酸铁锂正极材料回收工艺的初步设计及完善;(3)能从科学角度对工艺流程的设计进行初步评价。项目具体学习流程图如图1所示。
2 教学过程
2.1 磷酸铁锂电池正极材料分离探讨
【情境】 2021年磷酸铁锂电池随着新能源汽车、5G基站、电化学储能、二轮车等其他领域的需求呈现快速增长态势,开发一套磷酸铁锂电池的回收工艺,实现锂资源的重复利用,不仅具有经济价值,更是保护环境的需要。
【问题】 磷酸铁锂离子电池正极材料主要包含磷酸铁锂、有机粘结剂、乙炔黑、铝箔等,请同学们讨论并提出实现这些物质分离的方法[ 1 ]。
【学生活动1】 学生通过小组活动讨论各组成物质的特点,厘清每一种物质的分离方法,接着制定混合物的分离方法。
主要结论:有机物沸点低、可溶于有机溶剂且可燃;炭黑难溶,可以燃烧除去或者过滤除去;磷酸铁锂、铝箔为无机盐、金属单质可溶于酸碱溶液。
【学生活动2】 学生讨论各物质分离顺序,可依照排列组合法将所有顺序排列出来再逐一排除,选定最优分离顺序。
【备用方法】 (1)将正极片溶于适当有机溶剂,待粘接剂溶解后过滤得到磷酸铁锂、铝箔,乙炔黑。再采用适当酸碱溶液溶解铝箔,磷酸铁锂,从而分离炭黑。接着通过沉淀法分离出各种元素;(2)可以将正极材料置于高温下灼烧除去有机物及炭黑。再使用酸碱法将剩余物质溶解并逐步沉淀得到各种金属;(3)直接使用酸碱溶液将铝箔、活性物质全部溶解,过滤除去碳黑,并使用有机溶剂萃取除去有机杂质并使用沉淀法将铝、锂、铁等元素分离[ 2 ]。
【教师追问】 这么多种分离方法,选用哪一种最好?
【学生活动3】 结合实际,学生对每一种方法的可行性进行探討。
教师给予适当提示:①铝箔:适当的碱液可以将其与正极活性物质分离;②磷酸铁锂活性物质:在碱液中损失较少,但在酸溶液中可溶解。
【教师】 组织学生交流,互评,得出结论。
2.2 设计分离磷酸铁锂电池中锂、铁元素的实验方案
通过预处理得到正极活性物质以磷酸铁锂为主,但是该活性物质仍旧含有铁等杂质,因此需要进一步提纯。
【问题】 正极活性物质磷酸铁锂可溶于酸中,采用盐酸-双氧水浸出得到的浸出液主要成分有: Li+、Fe3+、H+、H2PO /HPO 和Cl- [ 3 ]。请按图2提示设计方案分离这些物质。
【学生活动1】 表1罗列了常见锂、铁元素沉淀的溶度积,小组根据表1讨论出锂、铁元素是如何以沉淀形式分离方案。
【备选方案】 方案1:利用氢氧化铁溶解度极低而氢氧化锂可溶的特点,实现分步沉淀;方案2:加入磷酸盐将铁、锂元素分别沉淀出来;方案3:将三价铁还原,并以草酸亚铁形式将铁元素分离,调节pH至碱性,加入磷酸盐,以磷酸锂形式沉淀锂;方案4:将三价铁还原,并以碳酸亚铁形式将铁元素分离,接着以磷酸锂形式沉淀锂[ 4 ]。
【教师追问】上述方案设计是基于Ksp数据设计的初步方案,并没有考虑到各种沉淀的实际属性,请同学们阅读表2,根据锂、铁元素沉淀的化学特点分析初步方案的可行性。
【学生活动2】 学生对4种备选方案的可行性进行探讨,分析得出结论:方案1不可行,三价铁易形成胶体而难以分离,且需要考虑原溶液中含有PO,加入碱液以后可能会形成磷酸铁沉淀。方案4亦不可行,因为碳酸亚铁在有水、氧气的环境中易被氧化。方案2、方案3有可能可行。
【教师】 上述2个理论上可行的方案,还需要在实践中进一步修改完善。
【学生活动3】 方案3中,在二价铁、磷酸根,锂离子共存体系如何控制pH,实现二价铁分离?分离磷酸锂时,又如何控制pH?请同学们根据图3,图4铁、锂元素的电位-pH图进行分离实验设计[ 5 ]。
【教师指导】 电位-pH图呈现了不同pH条件下,锂、铁、磷元素的结合形式。电位大小表示物质氧化还原性强弱,电位值越正,表示物质氧化态的氧化性越强,电位值为越负,表示物质还原态的还原性越强。
【学生】 通过图3可以分析得出:pH<0时,锂、铁、磷元素分别以亚铁离子、铁离子、锂离子,磷酸根离子存在。因此,在二价铁、磷酸根,锂离子共存体系中,需控制pH<0,并添加草酸将二价铁以草酸亚铁的形式沉淀出来,而且要注意防止二价铁被氧化成三价铁。要得到较为纯净的磷酸锂需先将体系中的铁元素彻底清除,并且调节pH到12以上,再添加磷酸钠。
【教师】 请同学们根据以上讨论画出从磷酸锂铁电池正极片分离出铁、锂元素的实验流程图。
【学生活动4】 小组讨论画出分离磷酸铁锂电池的实验流程如图5。
2.3 对磷酸铁锂电池中锂铁元素分离工艺的评价及改进
【问题】请同学们根据本次讨论的分离磷酸铁锂电池的实验流程图中,加入草酸将二价铁完全沉淀,过滤后的母液中调节pH至碱性,加入磷酸钠分离得到磷酸锂的方法进行评价。
【教师】 要对一套分离方案进行评价,首先要找到评价的视角。本部分内容中我们将学习从方法的科学性、方案可操作性(简易、安全、环保)二个方面对分离工艺进行评价。
【学生活动1】 学生通过小组讨论,从科学性角度分析上述方案:在加入草酸时,由于草酸亚铁的溶解度(Ksp=2.1×10-7)小于草酸锂(稍可溶),采用该方法理论上可以将大部分铁元素以草酸亚铁形式除去。但使用该方法在锂回收液中会残留一定量的铁元素,由于二价铁在溶液中不稳定,整套工艺在有氧条件下进行,因此会有部分二价铁氧化为三价铁[ 1 ]。而三价铁可以与草酸形成Fe(CO),Fe(CO)等多种可溶性配合物。从而导致铁元素残留在母液中。
【学生活动2】 有哪些方法可以克服二价铁氧化造成分离困难的问题?
学生通过讨论得出方案如下:
【改进方案】 方案1:在加入草酸過程中,通入惰性气体保护,防止二价铁氧化,从而减少母液中残留铁元素。方案2:加入草酸同时加入适当还原剂如铁粉,从而减少二价铁氧化。
【学生活动3】 学生从可操作性对原方案进行分析,并和改进方案进行对比。
从操作简易性方面,原方案中只需要沉淀,过滤等基本操作,但改进方案1中需要无氧环境,对操作,设备要求高,改进方案2操作简单。
从安全性方面,原方案使用的药品为草酸盐及磷酸盐,为常见酸碱,但改进方案1无需增加额外药品,改进方案2铁粉的使用安全可控。
从环保方面,原方案和改进方案1中碱液使用给后续处理带来一定困难,但改进方案2中的铁粉可考虑回收利用。
【教师评价】 同学们的改进方案从理论上都可以实现铁元素完全分离。但是方案1需要在惰气环境下进行,对设备要求高,方案2可操作性较强,总体优于方案1。
【教师总结】 一套工艺是否有价值还要考虑其是否能够用于工业推广,上述方案中使用较大量碱液,铁粉等物质,这些物质能否符合工业生产要求,需要在实际生产中进一步优化方案,以便获取最大回收价值。
3 总结
本节课以真实的“磷酸铁锂离子电池正极材料的有价金属回收”问题为项目,引导学生从正极活性材料富集,锂铁元素分离,分离方案的评价三个角度展开分析。学生在问题解决中逐步绘制出工艺流程图,并对流程图中关键问题:开发简易高效的工艺,实现正极活性物质富集、开发锂铁元素完全分离工艺进行了深度解决。通过方案评价讨论,让学生认识到工业生产工艺与实验室工艺的差异,培养学生工程思维。
参考文献
[1] 李欢.废旧磷酸铁锂电池中有价金属的回收技术研究[D].福州:福州大学,2016.
[2] 林丽.废弃磷酸铁锂回收利用方法研究[J].资源与环境,2017(2):161-162.
[3] 周有池,文小强,刘雯雯,等.废旧磷酸铁锂正极粉回收制备电池级碳酸锂工艺研究[J].有色金属世界,2018(12):176-179.
[4] 张英杰,许斌,梁风,等.废旧磷酸铁锂电池正极材料的回收研究现状[J].人工晶体学报,2019,48(5) : 800-808.
[5] 赵中伟,刘旭恒.Li-Fe-P-H2O系热力学分析[J].中国有机金属学报,2006,16(7):1257-1263.
