覆盆子茎中1个新的半日花烷型二萜苷
2022-05-24陈丽楠付辉政王兰欣杨甲玺肖小武罗跃华
陈丽楠,付辉政,王兰欣,钟 兰,杨甲玺,肖小武,任 琦,罗跃华*
覆盆子茎中1个新的半日花烷型二萜苷
陈丽楠1, 2,付辉政2*,王兰欣1, 2,钟 兰1, 2,杨甲玺1, 2,肖小武2,任 琦2,罗跃华1, 2*
1.南昌大学药学院,江西 南昌 330006 2.江西省药品检验检测研究院,国家药监局中成药质量评价重点实验室,江西省药品与医疗器械质量工程技术研究中心,江西 南昌 330029
研究华东覆盆子茎的化学成分。利用硅胶、ODS柱色谱、Sephadex LH-20葡聚糖凝胶柱色谱、高效制备液相色谱等色谱方法进行分离纯化,根据理化性质及波谱数据分析鉴定化合物结构。从覆盆子茎中分离得到17个化合物,分别鉴定为松脂素(1)、黑麦草内酯(2)、催吐萝芙木醇(3)、(−)-丁香脂素(4)、13-对映-半日花烷-8(17),13-二烯-3β,15,18-三醇(5)、3β,18-di-hydroxy-manool(6)、(+)-儿茶素(7)、(−)-儿茶素(8)、邻苯二甲酸二丁酯(9)、goshonoside-F1(10)、3β-hydroxy-manool-18--β--glucoside(11)、goshonoside-F2(12)、goshonoside-F5(13)、goshonoside-F4(14)、goshonoside-F3(15)、goshonoside-F7(16)、异槲皮素(17)。化合物11为新化合物,命名为覆盆子苷B;化合物6为新的天然产物,化合物1~4为首次从该植物中分离得到,化合物1~17为覆盆子茎中首次分离。
华东覆盆子;二萜苷;覆盆子苷B;松脂素;黑麦草内酯;催吐萝芙木醇;(−)-丁香脂素
悬钩子属植物种类多样分布广泛,目前世界范围内有700多种。据统计,我国有悬钩子属植物194种及88变种[1]。实际上中国境内已经发现的种类有201种98变种[2]。覆盆子是蔷薇科悬钩子属植物华东覆盆子Hu的干燥未成熟果实,具有益肾固精缩尿、养肝明目之功效,临床常用于治疗遗精滑精、遗尿、尿频、阳痿早泄、目暗昏花等症[3]。且覆盆子为江西重要药材,在江西德兴进行了规模化栽培,德兴覆盆子是国家地理标志产品,具有药食同源特性。目前对覆盆子果实已经进行了大量的研究,结果表明覆盆子富含黄酮类、萜类、酚酸类等成分,具有抗氧化、抗炎、抗肿瘤、抗真菌、抗血栓、抗骨质疏松、降血糖和调节中枢神经系统作用[4-5],其中萜类成分抗肿瘤作用较为显著[5]。为了进一步开发利用该药用资源并寻找有效的抗肿瘤成分,阐明药效物质基础,在本课题组前期对覆盆子研究的基础上[6],继续对覆盆子茎进行化学成分研究。利用各种色谱技术从覆盆子茎水煎液中分离出17个化合物,分别为松脂素(pinoresinol,1)、黑麦草内酯(loliolide,2)、催吐萝芙木醇(vomifoliol,3)、(−)-丁香脂素 [(−)- syringaresinol,4]、13-对映-半日花烷-8(17),13-二烯-3β,15,18-三醇 [13-ent-labda-8(17),13-diene-3β, 15,18-triol,5]、3β,18-di-hydroxy-manool(6)、(+)-儿茶素 [(+)-catechin,7]、(−)-儿茶素 [(−)-catechin,8]、邻苯二甲酸二丁酯(dibutylphthalate,9)、goshonoside-F1(10)、3β-hydroxy-manool-18--β--glucoside(11)、goshonoside-F2(12)、goshonoside-F5(13)、goshonoside-F4(14)、goshonoside-F3(15)、goshonoside-F7(16)、异槲皮苷(isoquercetin,17)。化合物11为新化合物,命名为覆盆子苷B,化合物6为新的天然产物,化合物1~4为首次从该植物中分离得到,化合物1~17为覆盆子茎中首次分离。
1 仪器与材料
岛津LC-2030C 3D Plus型液相色谱仪(日本岛津公司);Agilent 8890型气相色谱仪(安捷伦公司);岛津20-AD型制备高效液相色谱仪(日本岛津公司);Buchi中压液相制备色谱仪(瑞士步琪公司);Sartorius BP211D型电子天平(德国赛托利斯集团);Autopol IV-T/V型旋光仪(美国DKSH公司);Varian UNITY INOVA 600型超导核磁共振仪(美国Varian公司);Micromass ZabSpec质谱仪(美国Micromass公司);Waters ACQUITY UPLC/Xevo G2 Q TOF高分辨质谱仪(美国Waters公司);电热恒温水浴锅(上海跃进医疗器械厂);EYELA SB-1000型旋转蒸发仪,EYELA A-1000 S型循环水真空泵(日本EYELA公司)。Sephadex LH-20(瑞典Amersham Biosciences公司);C18反相填料为日本YMC产品;制备色谱柱为YMC(250 mm×20 mm,10 μm);柱色谱硅胶、薄层色谱硅胶为青岛海洋化工厂生产;水为Milli-Q一级水;色谱所用试剂为色谱级试剂;-无水葡萄糖(批号11833-201908)对照品购自中国食品药品检定研究院;其他所用试剂均为分析纯。
华东覆盆子茎采自江西省抚州市崇仁县,经江西省药品检测研究院付辉政副研究员鉴定为悬钩子属华东覆盆子Hu的茎,标本(20200526)保留在江西省药品检测研究院标本室。
2 提取与分离
取干燥覆盆子茎去叶(5.5 kg),室温下经粉粹、水煎煮提取2次,每次2 h、减压浓缩等步骤得覆盆子茎浓缩液(3 L)。将浓缩液用适量水稀释,依次用二氯甲烷、醋酸乙酯和水饱和正丁醇各萃取3次,减压浓缩得二氯甲烷部位(8.4 g)、醋酸乙酯部位(42.1 g)、正丁醇部位(205.0 g)。
二氯甲烷部位经正相硅胶柱色谱,石油醚-醋酸乙酯(5∶1→1∶1)梯度洗脱,经TLC检测合并相似流分,浓缩得到16个组分A1~A16。其中A12经Sephadex LH 20柱色谱分离,甲醇洗脱后,经TLC检测得主斑点,经反相制备高效液相色谱,流动相为甲醇-水(36∶64,10 mL/min),得到化合物1(5.4 mg,R=36.4 min)。A13经Sephadex LH-20柱色谱分离,甲醇洗脱后,经TLC检测得主斑点,经反相制备高效液相色谱,流动相为甲醇-水(20∶80,10 mL/min),得到化合物2(2.5 mg,R=41.0 min)。A14经Sephadex LH-20柱色谱分离,甲醇洗脱后,经TLC检测合并得3个流分Fr.1~3。Fr.1经反相制备高效液相色谱,流动相为甲醇-水(22∶78,10 mL/min),得到化合物3(3.5 mg,R=27.1 min);Fr.2经反相制备高效液相色谱,流动相为甲醇-水(38∶62,10 mL/min),得到化合物4(5.0 mg,R=21.8 min)。A15经Sephadex LH-20柱色谱分离,甲醇洗脱后,经TLC检测得主斑点,经反相制备高效液相色谱,流动相为甲醇-水(30∶70,10 mL/min),得到化合物5(11.1 mg,R=33.7 min)和6(5.1 mg,R=35.4 min)。
醋酸乙酯部位经正相硅胶柱色谱,二氯甲烷-甲醇(体积比12∶1→4∶1)梯度洗脱,经TLC检测合并相似流分,得到8个部分B1~B7。B2经正相硅胶柱色谱,二氯甲烷-甲醇(体积比12∶1→4∶1)梯度洗脱,得到8个部分Fr.1~8。其中Fr.4经Sephadex LH-20柱色谱分离,甲醇洗脱后,经TLC检测得主斑点,经反相制备高效液相色谱,流动相为甲醇-水(20∶80,10 mL/min),得到化合物7(8.7 mg,R=14.1 min)和8(40.1 mg,R=10.9 min);其中Fr.2经Sephadex LH-20柱色谱分离,甲醇洗脱后,经反相制备高效液相色谱,流动相为甲醇-水(66∶34,10 mL/min),得到化合物9(4.5 mg,R=24.5 min)。B4经过反相ODS柱色谱分离,甲醇-水(10∶100→100∶0)梯度洗脱,经高效液相色谱检测后,合并相同组分,体积分数100%甲醇洗脱的流分,经Sephadex LH-20柱色谱分离,甲醇洗脱后,经TLC检测得主斑点,经过反相制备高效液相色谱,流动相为乙腈-水(24∶76,10 mL/min),得到化合物10(96.7 mg,R=43.3 min)、11(8.7 mg,R=53.2 min)、12(84.5 mg,R=79.6 min)。B6经过反相ODS柱色谱分离,甲醇-水(10∶100→100∶0)梯度洗脱,经高效液相色谱检测后,合并相同组分,体积分数100%甲醇洗脱的流分,经Sephadex LH-20柱色谱分离,甲醇洗脱后,经TLC检测得主斑点,经反相制备高效液相色谱,流动相为乙腈-水(27∶73,10 mL/min),得到化合物13(140.0 mg,R=9.8 min)、14(47.4 mg,R=44.5 min)、15(27.4 mg,R=25.3 min)、16(27.4 mg,R=25.3 min)。B7经过反向ODS柱色谱分离,甲醇-水(10∶100→100∶0)梯度洗脱,经高效液相色谱检测后,合并相同组分,体积分数50%甲醇洗脱的流分,经Sephadex LH-20柱色谱分离,甲醇洗脱后,经TLC检测得主斑点,经反相制备高效液相色谱,流动相为甲醇-水(30∶70,10 mL/min),得到化合物17(27.4 mg,R=45.7 min)。
3 结构鉴定
化合物6:白色无定形粉末,溶于吡啶、甲醇,[α]25 D−10° (0.025, CH3OH),(nm): 201。超高效液相色谱-四极杆-飞行时间串联质谱给出准分子离子峰/345.239 2 [M+Na]+(计算值345.240 6,C20H34O3Na),结合1H-NMR和13C-NMR谱确定其分子式为C20H34O3。
1H-NMR谱低场区显示2组双键质子信号H6.23 (1H, m, H-14),5.62 (1H, dd,= 10.8, 2.0 Hz, H-15a), 5.21 (1H, dd,= 10.8, 2.0 Hz, H-15b);4.98 (1H, s, H-17a), 4.83 (1H, s, H-17b);此外,1H-NMR谱还给出3组甲基信号H0.84 (3H, s), 1.04 (3H, s), 1.52 (3H, s)。13C-NMR谱显示20个碳信号,其中2对双键信号C149.6, 117.7;147.8, 107.4。将化合物6的核磁数据与已知化合物(−)-3β-hydroxymanool[7]进行比较,两者核磁数据相似,且旋光度都为左旋,但化合物6的18号位的碳谱数据往低场移动。18号氢是在3.69 (1H, d,= 10.7 Hz, H-18a) 和4.18 (1H, d,= 10.7 Hz, H-18b),表明化合物6在已知化合物(−)-3β-hydroxymanool的基础上18号位多1个羟基。并且在HMBC中,氢信号(H3.69,H4.18) 和二萜苷元C-18 (C67.8) 相关,进一步表明羟基连接在18号位置。所以化合物6的平面结构为3,18-dihydroxy-manool。
NOESY谱中观察到H-5与H-9、H-18相关,表明C-18为β型,H-9为β型,则C-19为α型。H-3与H-19相关,H-3为α型,OH-3为β型。综上化合物6鉴定为3β,18-dihydroxy-manool,结构如图1所示。具体核磁数据见表1。

图1 化合物6的结构主要的HMBC相关图
化合物11:白色无定形粉末,溶于吡啶、甲醇,[α]25 D−56° (0.03, CH3OH),(nm): 201。超高效液相色谱-四极杆-飞行时间串联质谱给出准分子离子峰/507.293 3 [M+Na]+(计算值507.303 6,C26H44O8Na),结合1H-NMR和13C-NMR谱确定其分子式为C26H44O8。酸水解和衍生化气相分析检出-葡萄糖,与对照品-无水葡萄糖出峰时间一致。且水解后的母核[α]25 D−13° (0.01, CH3OH),与化合物6的比旋度基本一致,且都为左旋,所以连接的糖为型葡萄糖。
酸水解过程:取化合物11 2 mg,加入2 mol/L HCl 2 mL,封口,80摄氏度水浴中反应4 h,用等体积氯仿萃取2次,将水层减压浓缩至干,即得皂苷样品的完全酸水解物。
1H-NMR谱低场区显示2组双键质子信号H6.21 (1H, dd,= 17.2, 10.8 Hz, H-14), 5.61 (1H, dd,= 10.8, 2.0 Hz, H-15a), 5.19 (1H, dd,= 10.8, 2.0 Hz, H-15b); 4.95 (1H, s, H-17a), 4.79 (1H, s, H-17b);1个糖的端基质子信号H4.89 (1H, d,= 7.8 Hz)。并且根据端基氢相对较大的3H-1, H-2偶合常数值也表明糖的端基碳构型为β-型。此外,1H-NMR谱还给出3组甲基信号H0.79 (3H, s), 0.94 (3H, s), 1.49 (3H, s)。13C-NMR谱显示26个碳信号,其中2对双键信号C150.4, 112.3; 148.5, 108.0;1个糖分子碳信号C106.9 (C-1′), 75.7 (C-2′), 79.7 (C-3′), 73.0 (C-4′), 79.9 (C-5′), 64.1 (C-6′)。对比化合物11与化合物6碳氢谱数据,化合物11比6多了1个葡萄糖单元。
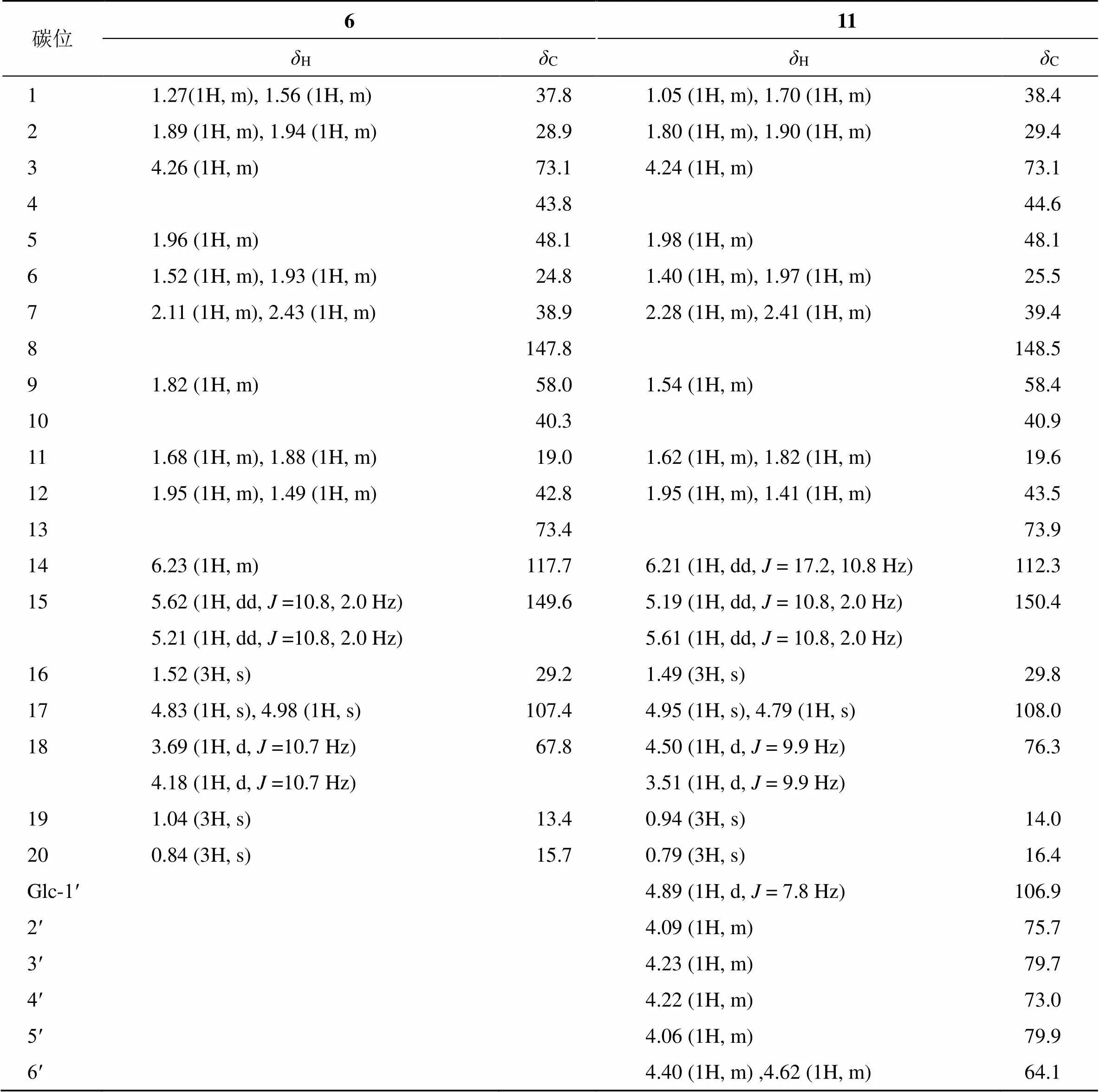
表1 化合物6、11的1H-NMR和13C-NMR波谱数据(600/150 MHz, C5D5N)
在HMBC(图2)中,葡萄糖的端基氢信号H-1′ (H4.89) 和二萜苷元碳信号C-18 (C76.3) 相关,表明葡萄糖单元连接在苷元的C-18位。

图2 化合物11的结构和主要的HMBC相关图
NOESY谱中观察到H-5与H-9、H-18相关,表明C-18为β型,H-9为β型,则C-19为α型。H-3与H-19相关,H-3为α型,OH-3为β型。H-19与H-20相关,表明C-20为α型。H-9(H1.54)、H-17(H4.98)、H-17(H4.83)与H-16相关,则C-16为α型,OH-13为β型。
综上所述,化合物11结构鉴定为3β-hydroxy- manool-18--β--glucoside,为1个新化合物,命名为覆盆子苷B。结构见图2。具体核磁数据见表1。
化合物1:白色粉末。ESI-MS/: 381.4 [M+Na]+, 357.4 [M-H]−。1H-NMR (600 MHz, CDCl3): 6.92 (4H, m, H-2, 2′, 6, 6′), 6.82 (2H, dd,= 8.2, 2.1 Hz, H-5, 5′), 5.64 (2H, s, 6, 6′-OH), 4.74 (2H, d,= 4.4 Hz, H-7, 7′), 4.29~4.20 (2H, m, H-9b, 9′b), 3.90 (8H, m, 3, 3′-OCH3, H-9a, 9′a), 3.11 (2H, m, H-8, 8′);13C-NMR (150 MHz, CDCl3): 132.9 (C-1, 1′), 108.5 (C-2, 2′), 146.6 (C-3, 3′), 145.2 (C-4, 4′), 114.2 (C-5, 5′), 118.9 (C-6, 6′), 85.8 (C-7, 7′), 54.1 (C-8, 8′), 71.6 (C-9, 9′), 55.9 (3, 3′-OCH3)。以上数据与文献报道基本一致[8],故鉴定化合物1为松脂素。
化合物2:无色晶体(甲醇)。ESI-MS/: 197.2 [M+H]+。1H-NMR (600 MHz, CDCl3): 5.69 (1H, s, H-7), 4.33 (1H, s, H-3), 2.46 (1H, d,= 14.5 Hz, H-4a), 1.97 (1H, d,14.5 Hz, H-2a), 1.74 (1H, d,14.4 Hz, H-4b), 1.76 (3H, s, H-11), 1.51 (1H, dd,14.5, 3.5 Hz, H-2b), 1.47 (3H, s, H-9), 1.27 (3H, s, H-10);13C-NMR (150 MHz, CDCl3): 35.9 (C-1), 47.3 (C-2), 66.8 (C-3), 45.6 (C-4), 86.6 (C-5), 182.3 (C-6), 112.9 (C-7), 171.8 (C-8), 26.4 (C-9), 30.6 (C-10), 27.0 (C-11)。以上数据与文献报道基本一致[9],故鉴定化合物2为黑麦草内酯。
化合物3:无色晶体(甲醇)。ESI-MS/: 225.3 [M+H]+。1H-NMR (600 MHz, CDCl3): 5.90 (1H, s, H-2), 5.85 (1H, dd,= 15.6, 5.4 Hz, H-2′), 5.79 (1H, d,= 15.6 Hz, H-1′), 4.41 (1H, m, H-3′), 2.44 (1H, d,= 17.0 Hz, H-6a), 2.24 (1H, d,= 17.0 Hz, H-6b), 1.89 (3H, s, H-3), 1.30 (3H, d,= 6.4 Hz, H-3′), 1.08 (3H, s, H-5a), 1.01 (3H, s, H-5b);13C-NMR (150 MHz, CDCl3): 197.9 (C-1), 126.9 (C-2), 162.6 (C-3), 79.0 (C-4), 41.1 (C-5), 49.7 (C-6), 18.8 (C-7), 22.9 (C-8), 23.7 (C-9), 135.7 (C-1′), 128.9 (C-2′), 68.0 (C-3′), 24.0 (C-4′)。以上数据与文献报道基本一致[10],故鉴定化合物3为催吐萝芙木醇。
化合物4:无色油状液体。ESI-MS/: 441.4 [M+Na]+。1H-NMR (600 MHz, CDCl3): 6.67 (4H, s, H-2, 2′, 6, 6′), 4.66 (2H, d,= 3.0 Hz, H-7, 7′), 4.22 (2H, m, H-9a, 9′a), 3.83 (12H, s, 3, 3′, 5, 5′-OCH3), 3.82 (2H, m, H-9b, 9′b), 3.08 (2H, m, H-8, 8′);13C-NMR (150 MHz, CDCl3): 131.9 (C-1, 1′), 104.4 (C-2, 2′), 148.6 (C-3, 3′), 133.2 (C-4, 4′), 148.6 (C-5, 5′), 104.4 (C-6, 6′), 86.8 (C-7, 7′), 55.3 (C-8, 8′), 72.3 (C-9, 9′), 56.6 (3, 3′, 5, 5′-OCH3)。以上数据与文献报道基本一致[11],故鉴定化合物4为(−)-丁香脂素。
化合物5:白色粉末。ESI-MS/: 322.2 [M+H]+。1H-NMR (600 MHz, C5D5N): 5.80 (1H, t,= 6.7 Hz, H-14), 4.96 (1H, s, H-17a), 4.67 (1H, s, H-17b), 4.51 (2H, d,= 6.6 Hz, H-15), 4.24 (1H, m, H-3), 4.16 (1H, d,= 10.5 Hz, H-18a), 3.68 (1H, d,= 10.5 Hz, H-18b), 1.74 (3H, s, H-16), 1.24 (1H, m, H-1), 1.04 (3H, s, H-19), 0.84 (3H, s, H-20);13C-NMR (150 MHz, C5D5N): 38.6 (C-1), 28.6 (C-2), 73.1 (C-3), 43.5 (C-4), 47.8 (C-5), 24.5 (C-6), 37.5 (C-7), 149.0 (C-8), 56.7 (C-9), 39.8 (C-10), 22.6 (C-11), 39.0 (C-12), 137.7 (C-13), 126.1 (C-14), 59.2 (C-15), 16.6 (C-16), 106.8 (C-17), 67.5 (C-18), 13.1 (C-19), 15.4 (C-20)。以上数据与文献报道基本一致[12],故鉴定化合物5为13-对映-半日花烷-8(17),13-二烯- 3β,15,18-三醇。
化合物6:白色无定形粉末。核磁数据见表1。以上数据与文献报道的数据类似[7],故鉴定化合物6为3β,18-di-hydroxy-manool。经系统查阅文献,该化合物仅由人工合成得到,未从植物分离得到。
化合物7:黄色无定形粉末。ESI-MS/: 291.2 [M+H]+。1H-NMR (600 MHz, CH3OD): 6.73 (1H, d,= 2.0 Hz, H-2′), 6.66 (1H, d,= 8.1 Hz, H-5), 6.61 (1H, dd,= 8.1, 2.0 Hz, H-6′), 5.82 (1H, d,= 2.2 Hz, H-8), 5.75 (1H, d,= 2.2 Hz, H-6), 4.46 (1H, d,= 7.5 Hz, H-2), 3.87 (1H, td,= 7.9, 5.4 Hz, H-3), 2.74 (1H, dd,= 16.1, 5.4 Hz, H-4a), 2.40 (1H, dd,= 16.1, 8.2 Hz, H-4b);13C-NMR (150 MHz, CH3OD): 81.1 (C-2), 67.0 (C-3), 26.7 (C-4), 155.8 (C-5), 93.7 (C-6), 156.0 (C-7) 94.4 (C-8), 155.1 (C-9), 99.0 (C-10), 130.4 (C-1′), 114.2 (C-2′), 144.48 (C-3′), 144.50 (C-4′), 113.4 (C-5′), 118.2 (C-6′)。以上数据与文献报道基本一致[13],故鉴定化合物7为(+)-儿茶素。
化合物8:棕黄色无定形粉末。ESI-MS/: 291.2 [M+H]+。1H-NMR (600 MHz, DMSO-6): 6.72 (1H, s, H-2′), 6.68 (1H, d,8.0 Hz, H-5′), 6.60 (1H, d,= 7.9 Hz, H-6′), 5.89 (1H, s, H-6), 5.69 (1H, s, H-8), 4.88 (1H, brs, OH), 4.48 (1H, d,= 7.4 Hz, H-2), 3.83 (1H, q,= 7.1 Hz, H-3), 2.66 (1H, dd,= 16.0, 5.3 Hz, H-4eq), 2.35 (1H, dd,= 16.0, 8.0 Hz, H-4ax);13C-NMR (150 MHz, DMSO-6): 81.0 (C-2), 66.3 (C-3), 27.9 (C-4), 156.2 (C-5), 93.8 (C-6), 156.4 (C-7), 95.1 (C-8), 155.3 (C-9), 99.1 (C-10), 130.6 (C-1′), 115.1 (C-2′), 144.8 (C-3′), 144.8 (C-4′), 114.5 (C-5′), 118.4 (C-6′)。以上数据与文献报道基本一致[14],鉴定化合物8为(−)-儿茶素。
化合物9:淡黄色油状物。ESI-MS/: 301.3 [M+Na]+。1H-NMR (600 MHz, DMSO-6): 7.67 (2H, dd,= 5.8, 3.3 Hz, H-2, 5), 7.72 (2H, dd,= 5.8, 3.3 Hz, H-3, 6), 4.24 (4H, t,= 6.6 Hz, H-8, 8′), 1.63 (4H, m, H-9, 9′), 1.35 (4H, m, H-10, 10′), 0.93 (6H, m, H-11, 11′);13C-NMR (150 MHz, DMSO-6): 131.7 (C-1, 2), 131.5 (C-4, 5), 128.6 (C-3, 6), 167.2 (C-7, 7′), 65.0 (C-8, 8′), 30.0 (C-9, 9′), 18.6 (C-10, 10′), 13.5 (C-11, 11′)。以上数据与文献报道一致[15-16],故鉴定化合物9为邻苯二甲酸二丁酯。
化合物10:白色粉末。ESI-MS/: 507.2 [M+Na]+, 483.2 [M-H]−。1H-NMR (600 MHz, C5D5N): 5.61 (1H, t,= 6.1 Hz, H-14), 4.98 (1H, d,= 7.8 Hz, 15--Glc-H-1), 4.94 (1H, s, H-17a), 4.62 (1H, s, H-17b), 3.70 (1H, dd,= 10.5, 3.4 Hz, H-18a), 4.19 (1H, dd,= 10.5, 4.2 Hz, H-18b), 1.66 (3H, s, 16-CH3), 1.05 (3H, s, 19-CH3), 0.83 (3H, s, 20-CH3);13C-NMR (150 MHz, C5D5N): 39.6 (C-1), 29.7 (C-2), 73.9 (C-3), 44.6 (C-4), 48.6 (C-5), 25.5 (C-6), 38.5 (C-7), 115.0 (C-8), 57.4 (C-9), 40.8 (C-10), 23.3 (C-11), 39.8 (C-12), 141.8 (C-13), 122.5 (C-14), 66.9 (C-15), 17.7 (C-16), 107.8 (C-17), 68.3 (C-18), 14.2 (C-19), 16.4 (C-20), 104.6 (C-1 of 15--Glc), 76.4 (C-2 of 15--Glc), 79.8 (C-3 of 15--Glc), 72.9 (C-4 of 15--Glc), 79.8 (C-5 of 15--Glc), 64.0 (C-6 of 15--Glc)。以上数据与文献报道基本一致[12],故鉴定化合物10为goshonoside-F1。
化合物12:白色粉末。ESI-MS/: 507.2 [M+Na]+, 483.2 [M-H]−。1H-NMR (600 MHz, C5D5N): 5.79 (1H, t,= 5.9 Hz, H-14), 4.92 (1H, s, H-17a), 4.89 (1H, d,= 7.8 Hz, 18--Glc-H-1), 4.62 (1H, s, H-17b), 4.48 (1H, d,= 5.9 Hz, H-15), 3.51 (1H, d,= 9.9 Hz, H-18), 1.70 (3H, s, 16-CH3), 0.95 (3H, s, 19-CH3), 0.77 (3H, s, 20-CH3);13C-NMR (150 MHz, C5D5N): 39.3 (C-1), 29.4 (C-2), 73.1 (C-3), 44.6 (C-4), 48.1 (C-5), 25.5 (C-6), 38.3 (C-7), 150.1 (C-8), 57.6 (C-9), 40.7 (C-10), 23.7 (C-11), 40.1 (C-12), 138.8 (C-13), 126.9 (C-14), 60.2 (C-15), 17.6 (C-16), 107.7 (C-17), 75.8 (C-18), 14.1 (C-19), 16.4 (C-20), 107.0 (C-1 of 18--Glc), 76.3 (C-2 of 18--Glc), 79.7 (C-3 of 18--Glc), 73.1 (C-4 of 18--Glc), 79.8 (C-5 of 18--Glc), 64.1 (C-6 of 18--Glc)。以上数据与文献报道基本一致[12],故鉴定化合物12为goshonoside-F2。
化合物13:白色粉末。ESI-MS/: 669.3 [M+Na]+, 645.3 [M-H]−。1H-NMR (600 MHz, C5D5N): 5.57 (1H, d,7.6 Hz, H-14), 4.93 (1H, d,7.8 Hz, H-1 of 15--Glc), 4.88 (1H, s, H-17a), 4.86 (1H, d,7.8 Hz, H-1 of 18--Glc), 4.58 (1H, s, H-17b), 4.46 (1H, d,10.0 Hz, H-18a), 3.50 (1H, d,10.0 Hz, H-18b), 1.64 (3H, s, H-16), 0.92 (3H, s, H-19), 0.73 (3H, s, H-20);13C-NMR (150 MHz, C5D5N): 36.8 (C-1), 26.9 (C-2), 70.4 (C-3), 42.1 (C-4), 45.6 (C-5), 23.1 (C-6), 35.8 (C-7), 148.2 (C-8), 55.1 (C-9), 38.2 (C-10), 21.0 (C-11), 37.5 (C-12), 139.2 (C-13), 119.8 (C-14), 64.7 (C-15), 15.3 (C-16), 105.2 (C-17), 73.4 (C-18), 11.6 (C-19), 14.0 (C-20), 102.4 (C-1 of 15--Glc), 73.8 (C-2 of 15--Glc), 77.2 (C-3 of 15--Glc), 70.6 (C-4 of 15--Glc), 77.3 (C-5 of 15--Glc), 61.5 (C-6 of 15--Glc), 104.5 (C-1 of 18--Glc), 73.8 (C-2 of 18--Glc), 77.3 (C-3 of 18--Glc), 70.7 (C-4 of 18--Glc), 77.4 (C-5 of 18--Glc), 61.6 (C-6 of 18--Glc)。以上数据与文献报道基本一致[12],故鉴定化合物13为goshonoside-F5。
化合物14:白色无定形粉末。ESI-MS/: 653.3 [M+Na]+, 629.3 [M-H]−。1H-NMR (600 MHz, C5D5N): 5.60 (1H, t,= 6.7 Hz, H-14), 4.96 (1H, d,= 7.7 Hz, 15--Glc-H-1), 4.90 (1H, s, H-17a), 4.82 (1H, d,= 7.7 Hz, 18--Glc-H-1), 4.57 (1H, s, H-17b), 3.74 (1H, d,= 9.6 Hz, H-18a), 3.44 (1H, d,= 9.6 Hz, H-18b), 1.63 (3H, s, H-16), 0.77 (3H, s, H-19), 0.71 (3H s, H-20);13C-NMR (150 MHz, C5D5N): 39.2 (C-1), 19.5 (C-2), 37.0 (C-3), 38.4 (C-4), 48.7 (C-5), 25.1 (C-6), 38.7 (C-7), 149.5 (C-8), 56.9 (C-9), 40.2 (C-10), 22.6 (C-11), 39.1 (C-12), 141.1 (C-13), 121.5 (C-14), 66.3 (C-15), 17.1 (C-16), 106.9 (C-17), 79.9 (C-18), 18.5 (C-19), 15.6 (C-20), 104.0 (C-1 of 15--Glc), 75.7 (C-2 of 15--Glc), 79.0 (C-3 of 15--Glc), 72.2 (C-4 of 15--Glc), 79.1 (C-5 of 15--Glc), 63.3 (C-6 of 15--Glc), 106.2 (C-1 of 18--Glc), 75.6 (C-2 of 18--Glc), 79.0 (C-3 of 18--Glc), 72.2 (C-4 of 18--Glc), 79.1 (C-5 of 18--Glc), 63.3 (C-6 of 18--Glc)。以上数据与文献报道基本一致[12],故鉴定化合物14为goshonoside-F4。
化合物15:白色无定形粉末。ESI-MS/: 644.7 [M+Na]+。1H-NMR (600 MHz, C5D5N): 5.58 (1H, t,= 7.0 Hz, H-14), 4.97 (1H, d,= 7.8 Hz, H-1 of 15--Glc), 4.85 (1H, s, H-17a), 6.35 (1H, d,= 7.2 Hz, 18--Glc-H-1), 4.56 (1H, s, H-17b), 4.45 (2H, m, H-15), 1.65 (3H, s, 16-CH3), 1.26 (3H, s, 19-CH3), 0.69 (3H, s, 20-CH3);13C-NMR (150 MHz, C5D5N): 38.6 (C-1), 18.9 (C-2), 37.1 (C-3), 48.3 (C-4), 49.9 (C-5), 27.3 (C-6), 38.3 (C-7), 148.6 (C-8), 56.9 (C-9), 39.4 (C-10), 22.3 (C-11), 38.9 (C-12), 141.1 (C-13), 121.3 (C-14), 66.2 (C-15), 17.0 (C-16), 107.4 (C-17), 177.8 (C-18), 17.3 (C-19), 15.6 (C-20), 103.9 (C-1 of 15--Glc), 75.4 (C-2 of 15--Glc), 79.0 (C-3 of 15--Glc), 72.9 (C-4 of 15--Glc), 79.9 (C-5 of 15--Glc), 63.6 (C-6 of 15--Glc), 96.5 (C-1 of 18--Glc), 74.5 (C-2 of 18--Glc), 78.8 (C-3 of 18--Glc), 71.2 (C-4 of 18--Glc), 79.1 (C-5 of 18--Glc), 62.3 (C-6 of 18--Glc)。以上数据与文献报道基本一致[17],故鉴定化合物15为goshonoside-F3。
化合物16:白色无定形粉末。ESI-MS/: 653.7 [M+Na]+。1H-NMR (600 MHz, C5D5N): 5.62 (1H, t,= 6.5 Hz, H-14), 4.97 (1H, d,= 7.8 Hz, 15--Glc-H-1), 4.92 (1H, s, H-17a), 5.00 (1H, d,= 7.8 Hz, 3--Glc-H-1), 4.59 (1H, s, H-17b), 3.70 (1H, dd,= 11.6, 4.1 Hz, H-3), 4.52~4.61 (2H, m, H2-15), 1.72 (3H, s, 16-CH3), 1.26 (3H, s, 18-CH3), 0.91 (3H, s, 19-CH3), 0.69 (3H, s, 20-CH3);13C-NMR (150 MHz, C5D5N): 38.2 (C-1), 24.7 (C-2), 85.0 (C-3), 39.1 (C-4), 55.8 (C-5), 24.6 (C-6), 37.3 (C-7), 148.8 (C-8), 55.2 (C-9), 39.7 (C-10), 22.1 (C-11), 38.0 (C-12), 141.2 (C-13), 121.7 (C-14), 65.6 (C-15), 16.7 (C-16), 107.1 (C-17), 28.9 (C-18), 17.2 (C-19), 15.0 (C-20), 102.7 (C-1 of 3--Glc), 75.5 (C-2 of 3--Glc), 78.6 (C-3 of 3--Glc), 72.4 (C-4 of 3--Glc), 79.1 (C-5 of 3--Glc), 63.1 (C-6 of 3--Glc), 103.1 (C-1 of 15--Glc), 75.4 (C-2 of 15--Glc), 78.3 (C-3 of 15--Glc), 72.0 (C-4 of 15--Glc), 78.8 (C-5 of 15--Glc), 63.0 (C-6 of 15--Glc)。以上数据与文献报道基本一致[17],故鉴定化合物16为goshonoside-F7。
化合物17:黄色粉末。ESI-MS/: 463.1 [M-H]−。1H-NMR (600 MHz, DMSO-6): 6.22 (1H, d,= 2.2 Hz, H-6), 6.43 (1H, d,= 2.2 Hz, H-8), 7.59 (2H, m, H-6′, 2′), 6.86 (1H, d,= 8.8 Hz, H-5′), 5.48 (1H, d,= 7.0 Hz, Glc-H-1′);13C-NMR (150 MHz, DMSO-6): 156.5 (C-2), 133.1 (C-3), 177.5 (C-4), 161.2 (C-5), 98.7 (C-6), 164.5 (C-7), 93.5 (C-8), 156.2 (C-9), 104.0 (C-10), 121.2 (C-1′), 116.2 (C-2′), 144.8 (C-3′), 148.5 (C-4′), 115.2 (C-5′), 121.6 (C-6′), 100.9 (C-1′′), 74.1 (C-2′′), 76.5 (C-3′′), 69.9 (C-4′′), 77.6 (C-5′′), 61.0 (C-6′′)。以上数据与文献报道基本一致[18],故鉴定化合物17为异槲皮苷。
利益冲突 所有作者均声明不存在利益冲突
[1] 中国科学院中国植物志编辑委员会.中国植物志 (第三十七卷) [M].北京: 科学出版社, 1985: 118.
[2] 顾姻.悬钩子属植物资源及其利用 [J].植物资源与环境, 1992, 1(2): 50-60.
[3] 中国药典 [S].一部.2020: 399-400.
[4] 程丹, 李洁, 周斌, 等.覆盆子化学成分与药理作用研究进展 [J].中药材, 2012, 35(11): 1873-1876.
[5] Yu G H, Luo Z Q, Wang W B,.Hu: A review of the phytochemistry and pharmacology [J]., 2019, 10: 799.
[6] Zhong R J, Guo Q, Zhou G P,.Three new labdane-type diterpene glycosides from fruits ofand their cytotoxic activities against five humor cell lines [J]., 2015, 102: 23-26.
[7] Tiansheng Lu, Vargas D, Franzblau S G,.Diterpenes from[J]., 1995, 38(2): 451-456.
[8] 刘志华, 王金兰, 赵明, 等.工业大麻地上部分化学成分研究 [J].中草药, 2021, 52(15): 4463-4472.
[9] 查显进, 石强, 邵峰, 等.泽漆化学成分研究 [J].中草药, 2021, 52(2): 341-348.
[10] 毛华丽, 占扎君, 钱捷.黑面神化学成分的研究 [J].中草药, 2009, 40(S1): 100-102.
[11] 齐曼, 郑晓珂, 曹彦刚, 等.皂角刺醋酸乙酯部位化学成分研究 [J].中草药, 2018, 49(23): 5510-5515.
[12] Tanaka T, Kawamura K, Kitahara T,.Ent-labdane-type diterpene glucosides from leaves of[J]., 1984, 23(3): 615-621.
[13] Moyo F, Gashe B A, Majinda R R T.A new flavan from[J]., 1999, 70(4): 412-416.
[14] Nechepurenko I V, Polovinka M P, Komarova N I,.Low-molecular-weight phenolic compounds fromroots [J]., 2008, 44(1): 31-34.
[15] 李小辉, 袁名睿, 陆雪萍, 等.麦冬的化学成分研究 [J].中草药, 2021, 52(13): 3804-3809.
[16] 万仲贤, 吴建国, 吴飞, 等.白花鬼针草化学成分研究[J].世界中医药, 2020, 15(10): 1391-1394.
[17] Ohtani K, Yang C R, Miyajima C,.Labdane-type diterpene glycosides from fruits of[J]., 1991, 39(9): 2443-2445.
[18] 谢朋飞, 邹录惠, 邱莉, 等.华山矾地上部分的化学成分研究 [J].中草药, 2014, 45(20): 2895-2899.
A new labdane diterpene glycoside from stems of
CHEN Li-nan1, 2, FU Hui-zheng2, WANG Lan-xin1, 2, ZHONG Lan1, 2, YANG Jia-xi1, 2, XIAO Xiao-wu2, REN Qi2, LUO Yue-hua1,2
1.School of Pharmacy, Nanchang University, Nanchang 330006, China 2.Jiangxi Institute for Drug Control, NMPA Key Laboratory of Quality Evaluation of Traditional Chinese Patent Medicine, Jiangxi Engineering Research Center for Drug and Medical Device Quality, Nanchang 330029, China
To study the chemical constituents of the stems of.The chemical constituents were isolated and purified by column chromatography on silica gel, ODS, Sephadex LH-20 and MPLC.Their structures were elucidated on basis of physicochemical properties and spectroscopic analysis.Seventeen compounds were isolated from the stems of,and identified as pinoresinol (1), loliolide (2), vomifoliol (3), (−)-syringaresinol (4), 13--labda-8(17),13-diene-3β,15,18-triol (5), 3β,18-di-hydroxy-manool (6), (+)-catechin (7), (−)-catechin (8), dibutylphthalate (9), goshonoside-F1 (10), 3β-hydroxy-manool-18--β--glucoside (11), goshonoside-F2 (12), goshonoside-F5 (13), goshonoside-F4 (14), goshonoside-F3 (15), goshonoside-F7 (16), isoquercetin (17).Compound 11 is a new compound named as goshonoside B and compound 6 is a new natural product, compounds 1—4 were isolated from the plant for the first time, compounds 1—17 were isolated from the stems offor the first time.
Hu; diterpene glycoside; goshonoside B; pinoresinol; loliolide; vomifoliol; (−)-syringaresinol
R284.1
A
0253 - 2670(2022)10 - 2941 - 08
10.7501/j.issn.0253-2670.2022.10.002
2021-09-26
江西省自然科学基金资助项目(20192BAB205115);江西省中医药标准化项目(2021A05);江西省卫生健康委科技计划项目(SKJP_220219796)
陈丽楠(1994—),女,在读硕士,主要从事中药活性成分研究。
通信作者:付辉政,研究员。Tel: (0791)88158716 E-mail: fhzfhz620@sohu.com
罗跃华,主任中药师。Tel: (0791)88158689 E-mail: emailluo@sohu.com
[责任编辑 王文倩]
