工业大麻地上部分化学成分研究(Ⅱ)
2022-05-24王金兰刘志华赵英楠时志春梁欣蕊孙立秋张树军
王金兰,刘志华,赵英楠,赵 明,李 军,时志春,王 丹,梁欣蕊,孙立秋,张树军
工业大麻地上部分化学成分研究(Ⅱ)
王金兰1, 2,刘志华1,赵英楠1, 2,赵 明1, 2,李 军1, 2,时志春1, 2,王 丹1, 2,梁欣蕊1,孙立秋1, 2,张树军1, 2
1.齐齐哈尔大学化学与化学工程学院,黑龙江 齐齐哈尔 161006 2.黑龙江省工业大麻加工技术创新中心,黑龙江 齐齐哈尔 161006
研究工业大麻地上部分的化学成分。采用硅胶柱色谱及HPLC等色谱技术进行分离纯化,通过理化性质与波谱数据分析鉴定结构。从工业大麻地上部分的醋酸乙酯萃取物中分离得到20个单体化合物,分别鉴定为大麻色原烯(1)、次大麻色原烯(2)、次大麻酚(3)、(2, 6)-2,6-壬二烯酸(4)、大麻艾尔松酚(5)、acetyl cannabispirol(6)、对羟基苯甲醛(7)、8-羟基乙酸芳樟酯(8)、羟基二氢博伏内酯(9)、次大麻艾尔松酚(10)、6-hydroxy-∆(7,8)-cannabichromene(11)、cannabispiran(12)、cannabispiradienone(13)、13-羟基-9,11,15-十八碳三烯酸(14)、(±)-2,3,3a,5-tetrahydro- 1-benzo[]pyrrolo[2,1-b][1,3]oxazin-1-one(15)、次大麻艾尔松酸B(16)、亚麻酸甲酯(17)、棕榈酸甲酯(18)、2,5-二叔丁基苯(19)、-[2-()-hydroxy-2-(4-hydroxy-phenyl)-ethyl]-3-(4-hydroxy-3-methoxy- phenyl)-acrylamide(20)。化合物15为新天然产物,命名为大麻内酰胺A;化合物4、8、9、14、19、20为首次从该属植物中分离得到,且补充了化合物10、16的核磁共振碳谱数据。
工业大麻;大麻素;螺环;大麻内酰胺A;(2, 6)-2,6-壬二烯酸;8-羟基乙酸芳樟酯;次大麻艾尔松酚
工业大麻L.是植株中四氢大麻酚(tetrahydrocannabinol,THC)含量低于0.3%,不具备提取毒性成分THC或直接作为毒品吸食价值的汉麻,又叫火麻、黄麻、汉麻等,为桑科大麻属一年生草本植物,多雌雄异株,在我国各地均有分布[1],但仅黑龙江、云南2省允许规模化种植。近年来人们对工业大麻进行了广泛的研究,结果表明其提取物具有抗肿瘤、抗氧化、抗菌、抗炎、抗惊厥和神经保护等作用[2]。为进一步开发利用工业大麻资源,本研究在前期研究[3]的基础上,从工业大麻甲醇提取液醋酸乙酯萃取物中分离得到20个化合物,分别鉴定为大麻色原烯(cannabichromene,1)、次大麻色原烯(cannabivarichromene,2)、次大麻酚(cannabivarin,3)、(2,6)-2,6-壬二烯酸 [(2,6)-2,6-nonadienoic acid,4]、大麻艾尔松酚(cannabielsoin,5)、acetyl cannabispirol(6)、对羟基苯甲醛(-hydroxybenzaldehyde,7)、8-羟基乙酸芳樟酯(8-hydroxylinalyl acetate,8)、羟基二氢博伏内酯(hydroxydihydrobovolide,9)、次大麻艾尔松酚(cannabielsoin-C3,10)、6-hydroxy-(7,8)- cannabichromene(11)、cannabispiran(12)、cannabispiradienone(13)、13-羟基-9,11,15-十八碳三烯酸(13-hydroxy-9,11,15-octadecatrienoic acid,14)、2,3,3a,5-tetrahydro-1-benzo[]pyrrolo [2,1-b][1,3]oxazin-1-one(15)、次大麻艾尔松酸 B(cannabielsoic acid B-C3,16)、亚麻酸甲酯(methyl linolenate,17)、棕榈酸甲酯(methyl hexadecanoate,18)、2,5-二叔丁基苯酚(2,5-di-tert-butylphenol,19)、-[2-()-hydroxy-2-(4-hydroxy-phenyl)-ethyl]-3-(4- hydroxy-3-methoxy- phenyl)-acrylamide(20)。其中化合物15为新天然产物,化合物4、8、9、14、19、20为首次从该属植物中分离得到。
1 材料与仪器
X-6 显微熔点测定仪(北京泰克仪器有限公司);Bruker AV-600型核磁共振波谱仪(瑞士Bruker公司,TMS为内标);AUTOPOL V型旋光仪(美国鲁道夫公司);圆二色谱仪(J-1500 CD光谱仪,日本分光株式会社);半制备高压液相色谱仪(日本日立公司,LC-6AD泵,Shodex RI SE-61视差折光检测器);PREP-SIL(250 mm×10 mm,5 μm)不锈钢色谱柱;PREP-ODS(250 mm×10 mm,5 μm)不锈钢色谱柱;柱色谱用硅胶(200~300目)为青岛海洋化工厂产品;薄层色谱硅胶板为烟台化工厂生产。有机溶剂为国药集团上海试剂厂产品,其他试剂为分析纯。
工业大麻于2018年7月采自于黑龙江省大兴安岭地区,经大兴安岭金亿顺汉麻种植专业合作社刘祥忠高级农艺师鉴定为工业大麻L.。标本(CSL-201807)收藏于齐齐哈尔大学天然产物研究室。
2 提取与分离
干燥的工业大麻地上部分5.5 kg,用甲醇室温浸泡3 d后过滤,重复3次,合并甲醇浸提液浓缩至小体积加水混悬,依次用正己烷和醋酸乙酯萃取5次,合并醋酸乙酯萃取液并减压浓缩至恒定质量,得到醋酸乙酯萃取物87.7 g。
取醋酸乙酯萃取物32.0 g,用硅胶柱色谱分离,依次用正己烷-醋酸乙酯(6∶4)8.5 L、(3∶7)7.0 L,醋酸乙酯-甲醇(8∶2)4.0 L、(5∶5)4.0 L,甲醇(3.0 L)洗脱,经TLC检测合并相同流分,浓缩得到12个组分(F1~F12)。F3(7.37 g)用硅胶柱色谱分离,依次用正己烷-醋酸乙酯(9∶1)6.0 L、(7∶3)5.0 L,醋酸乙酯(2.0 L),醋酸乙酯-甲醇(5∶5)2.0 L洗脱,经TLC检测合并相同流分,浓缩得到13个组分(F3-1~F3-13)。F3-7(1.31 g)用正相高效液相色谱(正己烷-醋酸乙酯97∶3,体积流量4 mL/min)分离得化合物1(1.8 mg,R=17.56 min)、2(2.9 mg,R=31.04 min)、3(1.6 mg,R=57.46 min)。F4(4.0 g)经硅胶柱色谱分离,依次用正己烷-醋酸乙酯(8∶2)4.0 L、(6∶4)1.5 L、(3∶7)3.0 L,醋酸乙酯-甲醇(5∶5)1.0 L洗脱,经TLC检测合并相同流分,浓缩得到9个组分(F4-1~F4-9)。F4-4(232.0 mg)用正相高效液相色谱(正己烷-醋酸乙酯8∶2,体积流量4 mL/min)分离得到8个组分(F4-4-1~F4-4-8)。F4-4-2(74.8 mg)用反相高效液相色谱(甲醇-水8∶2,体积流量4 mL/min)分离得化合物4(3.0 mg,R=5.21 min)。F4-5-2(402.2 mg)用正相高效液相色谱(正己烷-醋酸乙酯9∶1,体积流量4 mL/min)分离得化合物5(4.6 mg,R=27.09 min)。F4-5-3(304.8 mg)用正相高效液相色谱(正己烷-醋酸乙酯8∶2,体积流量4 mL/min)分离得到8个组分(F4-5-3-1~F4-5-3-8)。F4-5-3-4(60.7 mg)用反相高效液相色谱(甲醇-水8∶2,体积流量4 mL/min)分离得化合物6(1.6 mg,R=6.48 min)。F4-5-3-5(46.5 mg)用反相高效液相色谱(甲醇-水8∶2,体积流量4 mL/min)分离得化合物7(1.9 mg,R=3.92 min)、8(1.1 mg,R=6.79 min)、9(1.7 mg,R=4.63 min)、10(4.0 mg,R=7.13 min)、11(2.8 mg,R=8.86 min)。F4-5-3-7(32.7 mg)用反相高效液相色谱(甲醇-水8∶2,体积流量4 mL/min)分离得化合物12(2.0 mg,R=6.88 min)。F4-6(501.2 mg)用正相高效液相色谱(正己烷-醋酸乙酯75∶25,体积流量4 mL/min)分离得化合物13(2.4 mg,R=27.34 min)。F5(2.3 g)经硅胶柱色谱分离,依次用正己烷-醋酸乙酯(7∶3)2.0 L、(5∶5)1.5 L、(1∶9)1.0 L,醋酸乙酯-甲醇(5∶5)1.0 L洗脱,经TLC检测合并相同流分,浓缩得到10个组分(F5-1~F5-10)。F5-5(37.7 mg)用正相高效液相色谱(正己烷-醋酸乙酯7∶3,体积流量4 mL/min)分离得化合物14(1.0 mg,R=9.38 min)。F5-6(678.3 mg)用正相高效液相色谱(正己烷-醋酸乙酯7∶3,体积流量4 mL/min)分离得到10个组分(F5-6-1~F5-6-10)。F5-6-6(94.6 mg)用正相高效液相色谱(正己烷-醋酸乙酯8∶2,体积流量4 mL/min)分离得化合物15(1.5 mg,R=21.3 min)。F6(2.01 g)经硅胶柱色谱分离,依次用正己烷-醋酸乙酯(65∶35)2 L、(6∶4)1.5 L、(1∶9)1.0 L洗脱,经TLC检测合并相同流分,浓缩得到15个组分(F6-1~F6-15)。F6-9(93.0 mg)用正相高效液相色谱(正己烷-醋酸乙酯4∶6,体积流量4 mL/min)分离得到6个组分(F6-9-1~F6-9-6)。F6-9-1(42.6 mg)用正相高效液相色谱(正己烷-醋酸乙酯6∶4,体积流量4 mL/min)分离得化合物16(3.3 mg,R=9.26 min)。F8(8.6 g)经硅胶柱色谱分离,依次用正己烷-醋酸乙酯(2∶8)3.0 L、(0∶1)2.0 L、醋酸乙酯-甲醇(9∶1)3.0 L、(6∶4)3.0 L洗脱,经TLC检测合并相同流分,浓缩得到11个组分(F8-1~F8-11)。F8-2(98.7 mg)用反相高效液相色谱(甲醇-水95∶5,体积流量4 mL/min)分离得化合物17(3.1 mg,R=7.58 min)、18(1.3 mg,R=10.91 min)、19(1.5 mg,R=16.73 min)。F8-6(542.5 mg)用反相高效液相色谱(甲醇-乙腈-水23∶7∶70,体积流量4 mL/min)分离得化合物20(3.5 mg,R=29.98 min)。
3 结构鉴定
化合物1:淡黄色脂状物,[α]25 D−53.2° (0.4, CH3OH);1H-NMR (600 MHz, CDCl3)6.61 (1H, d,= 10.0 Hz, H-1), 6.25 (1H, s, H-5′), 6.11 (1H, s, H-3′), 5.49 (1H, d,= 10.0 Hz, H-2), 5.09 (1H, m, H-6), 2.42 (2H, t,= 7.4 Hz, H-1″), 1.66 (3H, s, H-8), 1.58 (3H, s, H-9), 1.57 (2H, m, H-2″), 1.38 (3H, s, H-10), 1.30 (4H, m, H-3″, 4″), 0.88 (3H, t,= 6.8 Hz, H-5′′);13C-NMR (150 MHz, CDCl3): 154.1 (C-2′), 150.9 (C-6′), 144.8 (C-4′), 131.6 (C-7), 127.3 (C-6), 124.2 (C-1), 116.7 (C-2), 109.2 (C-5′), 107.6 (C-1′), 107.0 (C-3′), 78.2 (C-2), 41.3 (C-5), 35.9 (C-1′′), 31.4 (C-3′′), 30.2 (C-2′′), 26.5 (C-9), 25.9 (C-8), 22.7 (C-4), 22.5 (C-34′′), 17.8 (C-10), 14.2 (C-5′′)。以上数据与文献报道基本一致[4],故鉴定化合物1为大麻色原烯。
化合物2:淡黄色脂状物,[α]25 D−20.5° (0.2, CH3OH);1H-NMR (600 MHz, CDCl3): 6.61 (1H, d,= 10.0 Hz, H-1), 6.25 (1H, s, H-5′), 6.11 (1H, s, H-3′), 5.49 (1H, d,= 10.0 Hz, H-2), 5.09 (1H, m, H-6), 2.42 (2H, t,= 7.4 Hz, H-1′′), 2.10 (2H, m, H-5), 1.76 (1H, m, H-4a), 1.66 (3H, s, H-8), 1.65 (1H, m, H-4b), 1.58 (2H, m, H-2′′), 1.57 (3H, s, H-9), 1.38 (3H, s, H-10), 0.92 (3H, t,= 7.4 Hz, H-3′′);13C-NMR (150 MHz, CDCl3): 154.1 (C-2′), 150.9 (C-6′), 144.8 (C-4′), 131.6 (C-7), 127.3 (C-6), 124.2 (C-1), 116.7 (C-2), 109.2 (C-5′), 107.6 (C-1′), 107.0 (C-3′), 78.2 (C-2), 41.3 (C-5), 38.0 (C-1′′), 26.5 (C-9), 25.9 (C-8), 24.0 (C-2′′), 22.7 (C-4), 17.8 (C-10), 13.8 (C-3′′)。以上数据与文献报道基本一致[4],故鉴定化合物2为次大麻色原烯。
化合物3:浅黄色脂状物;1H-NMR (600 MHz, CDCl3): 8.15 (1H, s, H-2), 7.14 (1H, d,= 7.8 Hz, H-5), 7.07 (1H, d,= 7.8 Hz, H-4), 6.43 (1H, s, H-5′), 6.29 (1H, s, H-3′), 2.48 (2H, t,= 7.4 Hz, H-1′′), 2.38 (3H, s, H-7), 1.63 (2H, m, H-2′′), 1.60 (6H, s, H-9, 10), 0.89 (3H, t,= 6.6 Hz, H-3′′);13C-NMR (150 MHz, CDCl3): 154.7 (C-2′), 153.0 (C-6′), 144.3 (C-4′), 136.9 (C-6), 136.9 (C-3), 127.6 (C-4), 127.5 (C-5′), 126.4 (C-2), 122.7 (C-5), 110.8 (C-1′), 109.9 (C-3′), 108.7 (C-1), 77.3 (C-8), 37.2 (C-1′′), 27.2 (C-9, 10), 23.9 (C-2′′), 21.5 (C-7), 13.8 (C-3′′)。以上数据与文献报道基本一致[4],故鉴定化合物3为次大麻酚。
化合物4:淡黄色粉末,mp 136~138 ℃;1H-NMR (600 MHz, CDCl3): 7.07 (1H, dt,= 15.6, 6.6 Hz, H-3), 5.84 (1H, d,= 15.6 Hz, H-2), 5.43 (1H, dt,= 10.2, 8.4 Hz, H-6), 5.31 (1H, dt,= 10.2, 7.8 Hz, H-7), 2.29 (2H, m, H-4), 2.22 (2H, m, H-5), 2.04 (2H, m, H-8), 0.96 (3H, t,= 7.2 Hz, H-18);13C-NMR (150 MHz, CDCl3): 171.1 (C-1), 151.5 (C-3), 133.1 (C-6), 127.0 (C-7), 120.9 (C-2), 32.4 (C-4), 25.5 (C-5), 20.6 (C-8), 14.2 (C-9)。以上数据与文献报道基本一致[5],故鉴定化合物4为 (2,6)- 2,6-壬二烯酸。
化合物5:淡黄色脂状物,[α]25 D−36.9° (0.17, CHCl3);1H-NMR (600 MHz, CDCl3): 6.30 (1H, s, H-2′), 6.28 (1H, s, H-4′), 5.38 (1H, brs, 5′-OH), 5.07 (1H, s, H-9a), 5.04 (1H, s, H-9b), 4.11 (1H, d,= 6.0 Hz, H-2), 3.33 (1H, dd,= 11.4, 6.0 Hz, H-3), 2.49 (2H, t,= 7.8 Hz, H-1′′), 1.88 (1H, m, H-4), 1.83 (3H, s, H-10), 1.72 (3H, m, H-5a, 6), 1.57 (3H, m, H-5b, 2′′), 1.48 (3H, s, H-7), 1.30 (4H, m, H-3′′, 4′′), 0.88 (3H, t,= 6.6 Hz, H-5′′);13C-NMR (150 MHz, CDCl3): 159.9 (C-1′), 153.3 (C-8), 152.0 (C-5′), 144.8 (C-3′), 116.8 (C-6′), 111.4 (C-9), 109.7 (C-4′), 103.2 (C-2′), 89.3 (C-2), 69.2 (C-1), 48.3 (C-4), 42.0 (C-3), 36.0 (C-1′′), 34.6 (C-6), 31.5 (C-3′′), 30.9 (C-2′′), 28.2 (C-7), 25.8 (C-5), 22.6 (C-4′′), 22.6 (C-10), 14.0 (C-5′′)。以上数据与文献报道基本一致[6],故鉴定化合物5为大麻艾尔松酚。
化合物6:浅黄色粉末,mp 184~185 ℃,[α]25 D21.5° (1.0, CHCl3);1H-NMR (600 MHz, CDCl3)6.36 (1H, s, H-7), 6.14 (1H, s, H-5), 5.07 (1H, s, OH-8), 4.66 (1H, s, H-4′), 3.75 (3H, s, -OCH3), 2.85 (2H, t,= 7.2 Hz, H-3), 2.42 (2H, m, H-2′a, 6′a), 2.10 (3H, s, H-2′′), 2.03 (2H, m, H-2), 1.90 (2H, m, H-5′), 1.70 (2H, m, H-2′b, 6′b), 1.38 (2H, m, H-3′);13C-NMR (150 MHz, CDCl3)170.8 (C-1′′), 160.0 (C-6), 153.0 (C-8), 146.5 (C-4), 128.5 (C-9), 102.2 (C-5), 100.9 (C-7), 69.0 (C-4′), 55.4 (-OCH3), 47.9 (C-1), 34.9 (C-2), 31.0 (C-3), 29.1 (C-3′, 5′), 27.1 (2′, 6′), 21.5 (C-2′′)。以上数据与文献报道基本一致[7],故鉴定化合物6为acetyl cannabispirone。
化合物7:无色针状结晶(氯仿),mp 110~114 ℃;1H-NMR (600 MHz, CDCl3): 9.88 (1H, s, H-7), 7.82 (2H, d,= 8.4 Hz, H-2, 6), 6.95 (2H, d,= 8.4 Hz, H-3, 5), 5.51 (1H, s, 4-OH);13C-NMR (150 MHz, CDCl3): 190.8 (C-7), 161.1 (C-4), 132.4 (C-2, 6), 130.2 (C-1), 115.9 (C-3, 5)。以上数据与文献报道基本一致[8],故鉴定化合物7为对羟基苯甲醛。
化合物8:淡黄色脂状物;1H-NMR (600 MHz, CDCl3): 5.91 (1H, dd,= 17.4, 10.8 Hz, H-2), 5.47 (1H, t,= 7.2 Hz, H-6), 5.22 (1H, brd,= 17.4 Hz, H-1a), 5.08 (1H, brd,= 10.8 Hz, H-1b), 4.44 (2H, brs, H-8), 2.10 (2H, m, H-5), 2.07 (3H, s, H-2′), 1.65 (3H, m, H-9), 1.63 (2H, m, H-4), 1.30 (3H, s, H-10);13C-NMR (150 MHz, CDCl3): 171.2 (C-1′), 144.8 (C-7), 130.3 (C-2), 129.4 (C-6), 111.9 (C-1), 73.3 (C-3), 70.2 (C-8), 41.5 (C-5), 28.0 (C-4), 22.5 (C-2′), 21.0 (C-9), 14.0 (C-10)。以上数据与文献基本一致[9],故鉴定化合物8为 8-羟基乙酸芳樟酯。
化合物9:浅黄色粉末,mp 131~135 ℃,[α]25 D6.5° (0.5, CHCl3);1H-NMR (600 MHz, CDCl3): 3.02 (1H, s, 4-OH), 2.02 (1H, m, H-5a), 1.95 (3H, s, H-10), 1.82 (3H, s, H-11), 1.75 (1H, m, H-5b), 1.25 (6H, m, H-6~8), 0.88 (3H, t,= 6.6 Hz, H-9);13C-NMR (150 MHz, CDCl3): 172.0 (C-1), 157.7 (C-3), 125.4 (C-2), 106.9 (C-4), 36.0 (C-6), 31.5 (C-8), 22.6 (C-5), 22.4 (C-7), 13.9 (C-9), 10.7 (C-10), 8.5 (C-11)。以上数据与文献报道基本一致[10],故鉴定化合物9为羟基二氢博伏内酯。
化合物10:淡黄色脂状物,[α]25 D−30.9° (0.1, CHCl3);1H-NMR (600 MHz, CDCl3)6.30 (1H, s, H-2′), 6.27 (1H, s, H-4′), 5.37 (1H, br s, OH-5′), 5.07 (1H, s, H-9a), 5.04 (1H, s, H-9b), 4.11 (1H, d,= 6.0 Hz, H-2), 3.33 (1H, dd,= 11.4, 6.0 Hz, H-3), 2.48 (2H, t,= 7.8 Hz, H-1′′), 1.88 (1H, m, H-4), 1.82 (3H, s, H-10), 1.72 (3H, m, H-5a, 6), 1.59 (3H, m, H-5b, 2′′), 1.48 (3H, s, H-7), 0.92 (3H, t,= 6.6 Hz, H-3′′);13C-NMR (150 MHz, CDCl3)159.9 (C-1′), 153.4 (C-8), 152.0 (C-5′), 144.6 (C-3′), 116.8 (C-6′), 111.4 (C-9), 109.8 (C-4′), 103.2 (C-2′), 89.3 (C-2), 69.2 (C-1), 48.3 (C-4), 42.0 (C-3), 38.1 (C-1′′), 34.7 (C-6), 28.3 (C-7), 25.8 (C-5), 24.3 (C-2′′), 22.6 (C-10), 13.9 (C-5′′)。该化合物的NMR数据与大麻艾尔松酚(5)对照,仅在高场相差2个亚甲基,其余数据基本一致,根据文献报道[11],确定为大麻艾尔松酚(5)的丙基同系物,鉴定化合物10为次大麻艾尔松酚。
化合物11:淡黄色脂状物;1H-NMR (600 MHz, CDCl3): 6.62 (1H, d,= 10.2 Hz, H-1), 6.24 (1H, s, H-5′), 6.12 (1H, s, H-3′), 5.47 (1H, d,= 10.2 Hz, H-2), 4.93 (1H, brs, H-8a), 4.83 (1H, brs, H-8b), 4.68 (1H, m, 2′-OH), 4.06 (1H, t,= 6.6 Hz, H-6), 2.44 (2H, t,= 7.2 Hz, H-1′′), 1.70 (3H, s, H-9), 1.38 (3H, s, H-10), 0.88 (3H, t,= 6.6 Hz, H-5′′);13C-NMR (150 MHz, CDCl3): 153.9 (C-2′), 151.0 (C-6′), 147.2 (C-4′), 144.9 (C-7), 126.9 (C-8), 117.0 (C-1), 111.1 (C-2), 109.1 (C-5′), 107.7 (C-1′), 106.8 (C-3′), 77.9 (C-3), 75.9 (C-6), 37.0 (C-1′′), 35.9 (C-3′′), 31.5 (C-2′′), 30.6 (C-9), 29.3 (C-5), 26.4 (C-4), 22.5 (C-4′′), 17.6 (C-10), 14.0 (C-5′′)。以上数据与文献报道基本一致[12],故鉴定化合物11为6-hydroxy-∆(7,8)- cannabichromene。
化合物12:浅黄色粉末,mp 179~180 ℃;1H-NMR (600 MHz, CDCl3): 6.38 (1H, s, H-7), 6.11 (1H, s, H-5), 4.92 (1H, s, 8-OH), 3.75 (3H, s, -OCH3), 2.95 (2H, t,= 7.2 Hz, H-3), 2.52 (2H, m, H-6′), 2.51 (2H, m, H-3′), 2.49 (2H, m, H-5′), 2.23 (2H, m, H-2), 2.82 (2H, m, H-2′);13C-NMR (150 MHz, CDCl3): 212.9 (C-4′), 160.3 (C-6), 152.9 (C-8), 146.5 (C-4), 126.7 (C-9), 102.1 (C-5), 100.9 (C-7), 55.4 (-OCH3), 47.7 (C-1), 39.0 (C-3, 5), 35.3 (C-2), 34.4 (2, 6), 31.0 (C-3)。以上数据与文献报道基本一致[13],故鉴定化合物12为cannabispiran。
化合物13:浅黄色粉末,mp 158~161 ℃;1H-NMR (600 MHz, CDCl3):6.99 (2H, d,= 10.2 Hz, H-2′, 6′), 6.46 (1H, s, H-7), 6.38 (2H, d,= 10.2 Hz, H-3′, 5′), 6.22 (1H, s, H-5), 4.84 (1H, s, OH-8), 3.77 (3H, s, -OCH3), 3.11 (2H, t,= 7.2 Hz, H-3), 2.32 (2H, t,= 7.2 Hz, H-2);13C-NMR (150 MHz, CDCl3): 193.4 (C-4′), 160.2 (C-6), 154.0 (C-8), 152.5 (C-2′, 6′), 147.1 (C-4), 128.8 (C-9), 128.3 (C-3′, 5′), 103.8 (C-5), 101.0 (C-7), 55.6 (-OCH3), 55.3 (C-1), 38.3 (C-2), 31.0 (C-3)。以上数据与文献报道基本一致[14],故鉴定化合物13为cannabispiradienone。
化合物14:淡黄色脂状物,[α]25 D+6.9° (0.1, CHCl3);1H-NMR (600 MHz, CDCl3): 6.53 (1H, dd,= 15.0, 10.8 Hz, H-11), 5.98 (1H, t,= 11.4 Hz, H-10), 5.69 (1H, dd,= 15.0, 6.0 Hz, H-12), 5.58 (1H, m, H-16), 5.44 (1H, m, H-9), 5.36 (1H, m, H-15), 4.24 (1H, m, H-13), 2.34 (4H, m, H-2, 14), 2.18 (2H, m, H-8), 2.07 (2H, m, H-17), 1.62 (2H, m, H-3), 1.40~1.25 (8H, m, H-4~7), 0.97 (3H, t,= 7.6 Hz, H-18);13C-NMR (150 MHz, CDCl3): 178.2 (C-1), 135.1 (C-16), 135.0 (C-9), 132.8 (C-12), 127.8 (C-11), 125.8 (C-10), 123.7 (C-15), 72.1 (C-13), 35.3 (C-14), 34.1 (C-2), 29.4 (C-4), 29.0 (C-5), 29.0 (C-6), 28.9 (C-7), 27.6 (C-8), 24.8 (C-3), 20.8 (C-17), 14.2 (C-18)。以上数据与文献报道基本一致[15],故鉴定化合物14为13-羟基-9,11,15-十八碳三烯酸。
化合物15:浅黄色粉末,mp 88~90 ℃;HR-ESI-MS/: 190.086 0 [M+H]+(计算值 190.086 8),推得分子式为C11H11NO2。1H-NMR谱(表1)中,在8.31 (1H, d,= 8.4 Hz, H-2), 7.28 (1H, t,= 8.4 Hz, H-3), 7.12 (1H, td,= 8.4, 7.8 Hz, H-4), 7.04 (2H, d,= 7.8 Hz, H-5) 各给出1个芳香质子信号,根据其偶合常数推测其为邻二取代苯,5.28 (1H, dd,= 7.2, 5.4 Hz, H-4′) 给出1个连氧次甲基信号,5.06 (1H, d,= 15.0 Hz, H-7a) 和4.92 (1H, d,= 15.0 Hz, H-7b) 给出1个连氧苄基信号,2.61 (2H, m, H-2′), 2.50 (1H, m, H-3′a), 2.07 (1H, m, H-3′b) 给出2个饱和亚甲基信号。13C-NMR谱(表1)中,给出了11个碳的信号,其中171.9给出1个酮羰基信号,134.1, 127.6, 124.3, 124.3, 123.8, 119.6给出6个烯碳信号,推测含有1个苯环,87.2, 68.0给出2个连氧碳,剩余2个为饱和碳。
由HMBC谱(图1)可知,H-7 (5.02, 4.96) 与C-4′ (87.2), C-1 (134.1), C-5 (124.3), C-6 (123.8) 相关,由此证明存在苄基结构单元。H-4′ (5.28) 与C-7 (68.0), C-1′ (171.9), C-2′ (30.0), C-3′ (24.7) 相关。H-5 (7.02) 与C-7 (68.0), C-1 (134.1), C-3 (127.6) 相关。H-2 (8.31) 与C-4 (124.3), C-6 (123.8) 相关。H-3 (7.28) 与C-1 (134.1), C-2 (119.6), C-4 (124.3), C-5 (124.3) 相关。H-4 (7.12) 与C-2 (119.6), C-3 (127.6), C-5 (124.3), C-6 (123.8) 相关。H-2′ (2.61) 与C-1′ (171.9), C-3′ (24.7), C-4′ (87.2) 相关。H-3′ (2.50, 2.07) 与C-1′ (171.9), C-2′ (30.0), C-4′ (87.2) 相关。由1H-1H COSY谱可知,H-3′ (2.50, 2.07) 与H-4′ (5.28) 相关。H-3′ (2.50, 2.07) 与H-2′ (2.61) 相关。H-5 (7.02) 与H-4 (7.12) 相关。H-3 (7.28) 与H-4 (7.12) 相关。H-3 (7.28) 与H-2 (8.31) 相关。根据对该分子进行旋光测试其比旋光度接近0,并且该分子的实测CD图谱在200~400 nm的Cotton效应几乎为零,因此推测化合物15是1对外消旋体。由此可以推测化合物15的结构为(±)-2,3,3a,5-tetrahydro-1-benzo[] pyrrolo [2,1-b][1,3]oxazin-1-one。经与文献对照[16],该化合物系由人工合成得到,未见其作为植物的次级代谢产物相关报道,并根据波谱数据综合分析结合苯并四氢异吡喃结构单元的文献报道[17],纠正了文献所报道该分子C-7的数据错误[16]。

表1 化合物15的核磁共振波谱数据(600/150 MHz, CDCl3)
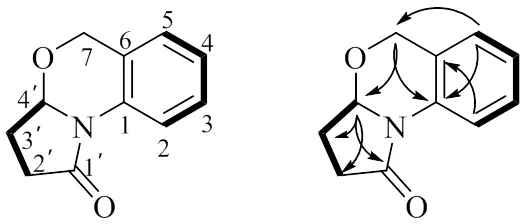
图1 化合物15主要的HMBC (H→C) 和1H-1H COSY (―) 相关
化合物16:白色粉末,mp 215~217 ℃,[α]25 D+21.1° (0.1, CHCl3);1H-NMR (600 MHz, CDCl3): 6.42 (1H, s, H-5′), 5.08 (2H, d,= 7.0 Hz, H-9), 4.35 (1H, d,= 5.8 Hz, H-2), 3.44 (1H, dd,= 11.1, 5.8 Hz, H-3), 2.97 (2H, m, H-1′′), 1.84 (3H, s, H-10), 1.53 (3H, s, H-7), 0.96 (3H, t,= 7.8 Hz, H-3′′);13C-NMR (150 MHz, CDCl3): 164.6 (C-7′), 160.1 (C-2′), 155.2 (C-1′), 152.5 (C-8), 149.2 (C-3′), 116.9 (C-6′), 114.0 (C-5′), 111.8 (C-9), 105.5 (C-4′), 91.2 (C-3), 68.7 (C-1), 48.0 (C-4), 41.5 (C-3), 36.7 (C-1′′), 34.6 (C-6), 28.1 (C-7), 25.6 (C-5), 24.4 (C-2′′), 22.6 (C-10), 14.2 (C-3′′)。该化合物的NMR数据与大麻艾尔松酸 B 对照,仅在高场相差2个亚甲基,其余数据基本一致,根据文献报道[11],判断其为大麻艾尔松酸B的丙基同系物,故鉴定化合物16为次大麻艾尔松酸B。
化合物17:浅黄色油状物;1H-NMR (600 MHz, CDCl3): 5.35 (6H, m, H-9, 10, 12, 13, 15, 16), 3.67 (3H, s, H-1′), 2.81 (4H, m, H-11, 14), 2.30 (2H, t,= 7.8 Hz, H-2), 2.06 (4H, m, H-8, 17), 1.61 (2H, m, H-3), 1.34~1.28 (8H, m, H-4~7), 0.98 (3H, t,= 7.5 Hz, H-18);13C-NMR (150 MHz, CDCl3): 174.3 (C-1), 132.0 (C-9), 130.3 (C-16), 128.3 (C-12), 128.3 (C-13), 127.7 (C-15), 127.1 (C-10), 51.5 (C-1′), 34.1 (C-2), 29.6 (C-7), 29.2 (C-6), 29.2 (C-5), 29.1 (C-4), 27.2 (C-3), 25.6 (C-8), 25.5 (C-11), 24.9 (C-14), 20.6 (C-17), 14.3 (C-18)。以上数据与文献报道基本一致[18],故鉴定化合物17为亚麻酸甲酯。
化合物18:白色粉末,mp 28~29 ℃;1H-NMR (600 MHz, CDCl3): 3.37 (3H, s, H-1′), 2.30 (1H, d,= 7.8 Hz, H-2), 1.61 (2H, m, H-3), 1.29 (28H, m, H-4~17), 0.88 (3H, t,= 6.6 Hz, H-18)。以上数据与文献报道基本一致[19],故鉴定化合物18为棕榈酸甲酯。
化合物19:白色粉末,mp 140~142 ℃;1H-NMR (600 MHz, CDCl3): 7.54 (1H, d,= 8.4 Hz, H-3), 7.35 (1H, brs, H-6), 7.13 (1H, brd,= 8.4 Hz, H-4), 1.33 (9H, s, H-9~11), 1.28 (9H, s, H-12~14);13C-NMR (150 MHz, CDCl3): 147.7 (C-1), 147.6 (C-5), 138.5 (C-2), 124.5 (C-3), 124.0 (C-4), 119.1 (C-6), 34.9 (C-8), 34.5 (C-7), 31.4 (C-9~11), 30.2 (C-12~14)。以上数据与文献报道基本一致[20],故鉴定化合物19为2,5-二叔丁基苯酚。
化合物20:淡黄色脂状物,[α]25 D−34.5° (1.4, CH3OH);1H-NMR (600 MHz, DMSO-6): 9.32 (2H, brs, 7, 6′-OH), 7.93 (1H, t,= 5.4 Hz, N-H), 7.30 (1H, d,= 15.6 Hz, H-3), 7.14 (2H, d,= 8.4 Hz, H-4′, 8′), 7.11 (1H, s, H-5), 6.98 (1H, d,= 7.8 Hz, H-9), 6.78 (1H, d,= 7.8 Hz, H-8), 6.71 (2H, d,= 8.4 Hz, H-5′, 7′), 6.53 (1H, d,= 15.6 Hz, H-2), 4.53 (1H, t,= 6.6 Hz, H-2′), 3.80 (3H, s, -OCH3), 3.38 (1H, m, H-1′a), 3.19 (1H, m, H-1′b);13C-NMR (150 MHz, DMSO-6): 166.0 (C-1), 156.9 (C-6′), 148.7 (C-7), 148.3 (C-6), 139.4 (C-3), 134.5 (C-3′), 127.6 (C-4′, 8′), 126.9 (C-4), 122.0 (C-9), 119.6 (C-2), 116.1 (C-8), 115.2 (C-5′, 7′), 111.2 (C-5), 71.7 (C-2′), 56.0 (-OCH3), 47.5 (C-1′)。以上数据与文献报道基本一致[21],故鉴定化合物20为-[2-()-hydroxy-2-(4-hydroxy-phenyl)- ethyl]-3-(4-hydroxy-3-methoxyphenyl)-acrylamide。
4 讨论
工业大麻在抗肿瘤、抗氧化、抗菌、抗炎、抗惊厥和神经保护等方面具有广阔的应用前景和极高的药理研究价值,其中以大麻素类成分最受人们关注。为进一步探讨工业大麻药效基础物质,本研究继续对工业大麻醇提液醋酸乙酯萃取物化学成分进行研究,得到了20个单体化合物。这些次生代谢产物除大麻素类以外,其他类成分大多具有较强的生物活性,如羟基二氢博伏内酯(9)对HIV病毒具有抑制作用[10],这提示工业大麻的抗HIV作用可能与该类成分有关;亚麻酸甲酯(17)、-[2-(S)- hydroxy-2-(4-hydroxy-phenyl)-ethyl]-3-(4-hydroxy-3-methoxy-phenyl)-acrylamide(20)等具有一定的抗氧化作用[21-22]等。这些活性成分从工业大麻醋酸乙酯萃取物中分离得到,预示工业大麻具有较好的药物开发前景。本研究通过进一步研究工业大麻的物质基础,并推测成分与生物活性的相关性,可为综合利用工业大麻资源、研究开发新型药物等提供理论依据。此外,一些稀有大麻素类成分波谱数据不全面,本研究补充了2个大麻素丙基同系物次大麻艾尔松酚(10)和次大麻艾尔松酸B(16)的核磁共振碳谱数据,为后续开发工业大麻应用提供支撑。
利益冲突 所有作者均声明不存在利益冲突
[1] 李俊, 朱雪雯, 万会花, 等.大麻中大麻素类化学成分及其分析方法研究进展 [J].中草药, 2020, 51(24): 6414-6425.
[2] 王秋月, 卢芳, 刘树民.大麻及大麻素药用价值的现代研究进展 [J].中药药理与临床, 2020, 36(4): 222-227.
[3] 刘志华, 王金兰, 赵明, 等.工业大麻地上部分化学成分研究 [J].中草药, 2021, 52(15): 4463-4472.
[4] Wang G, Zhu L J, Zhao Y Q,.A natural product fromsubsp.inhibits homeodomain- interacting protein kinase 2 (HIPK2), attenuating MPP+-induced apoptosis in human neuroblastoma SH-SY5Y cells [J]., 2017, 72: 64-73.
[5] Snider B B, Allentoff A J, Kulkarni Y S.Type III intramolecular[2 + 2]cycloadditions of vinylketenes [J]., 1988, 53(22): 5320-5328.
[6] Monroe A Z, Gordon W H, Wood J S,.Structural revision of a Wnt/β-catenin modulator and confirmation of cannabielsoin constitution and configuration [J].(), 2021, 57(46): 5658-5661.
[7] Shoyama Y, Nishioka I..XIII.two new spiro-compounds, cannabispirol and acetyl cannabispirol [J]., 1978, 26(12): 3641-3646.
[8] 李小辉, 袁名睿, 陆雪萍, 等.麦冬的化学成分研究 [J].中草药, 2021, 52(13): 3804-3809.
[9] Masaki Y, Hashimoto K, Kaji K J.Facile functionalization of the isopropylidene terminus of acyclic monoterpenes by way of benzenesulfenyl chloride addition [J]., 1984, 40(18): 3481-3490.
[10] Zhang H J, Nguyen V H, Nguyen M C,.Sesquiterpenes and butenolides, natural anti-HIV constituents from[J]., 2005, 71(5): 452-457.
[11] Radwan M M, Chandra S, Gul S,.Cannabinoids, phenolics, terpenes and alkaloids of[J]., 2021, 26(9): 2774.
[12] Radwan M M, Elsohly M A, Slade D,.Biologically active cannabinoids from high-potency[J]., 2009, 72(5): 906-911.
[13] El-Feraly F S, Chan Y M.Total synthesis of cannabispiran and (±)-dehydrocannabispiran [J]., 1981, 44(5): 557-561.
[14] Cromble L, Mary W, Crombie L,.Isolation of cannabispiradienone and cannabidihydrophenanthrene.biosynthetic relationships between the spirans and dihydrostilbenes of Thailand[J]., 1979, 20(7): 661-664.
[15] Bang M H, Han J T, Kim H Y,.13-Hydroxy-9,11, 15-octadecatrienoic acid from the leaves of[J]., 2002, 25(4): 438-440.
[16] Taylor R, Cayley A, Gallagher K,.Preparation of novel polycyclic heterocycles using a tin(II) chloride dihydrate-mediated deacetalisation-bicyclisation sequence [J]., 2008, 2008(23): 3846-3856.
[17] Sakai N, Moriya T, Konakahara T.An efficient one-pot synthesis of unsymmetrical ethers: A directly reductive deoxygenation of esters using an InBr3/Et3SiH catalytic system [J]., 2007, 72(15): 5920-5922.
[18] 彭芳, 熊亮, 何育霖, 等.益母草化学成分及其抗氧化活性研究 [J].中国药学杂志, 2020, 55(21): 1775-1779.
[19] 王星星, 王重娟, 李仲昆.鸡矢藤的化学成分及药理活性研究进展[J].世界中医药, 2021, 16(5): 826-830.
[20] 夏少立, 曹悦, 李庆林, 等.新疆一枝蒿的化学成分研究 [J].中草药, 2020, 51(13): 3393-3398.
[21] Li X, Li X M, Xu G M,.Antioxidant metabolites from marine alga-derived fungusEN-48 [J]., 2014, 7: 120-123.
[22] 乔璐, 栗磊, 宋梦娇, 等.石胆草脂溶性成分GC-MS分析及其抗氧化活性研究 [J].中国医药科学, 2020, 10(17): 78-81.
Chemical constituents from acrial part of
WANG Jin-lan1, 2, LIU Zhi-hua1, ZHAO Ying-nan1, 2, ZHAO Ming1, 2, LI Jun1, 2, SHI Zhi-chun1, 2, WANG Dan1, 2, LIANG Xin-rui1, SUN Li-qiu1, 2, ZHANG Shu-jun1, 2
1.College of Chemistry and Chemical Engineering, Qiqihar University, Qiqihar 161006, China 2.Heilongjiang Industrial Hemp Processing Technology Innovation Center, Qiqihar 161006, China
To study the chemical constituents from aerial part of.The chemical constituents were isolated by silica gel column chromatography and HPLC, and the structures were identified by their spectral data and physicochemical properties analysis.Twenty compounds were isolated from, and identified as cannabichromene (1), cannabivarichromene (2), cannabivarin (3), (2,6)-2,6-nonadienoic acid (4), cannabielsoin (5), acetyl cannabispirol (6),-hydroxybenzaldehyde (7), 8-hydroxylinalyl acetate (8), hydroxydihydrobovolide (9), cannabielsoin-C3(10), 6-hydroxy- ∆(7,8)-cannabichromene (11), cannabispiran (12), cannabispiradienone (13), 13-hydroxy-9,11,15-octadecatrienoic acid (14), 2,3,3a,5-tetrahydro-1-benzo[]pyrrolo[2,1-b][1,3]oxazin-1-one (15), cannabielsoic acid B-C3(16), methyl linolenate (17), methyl hexadecanoate (18), 2,5-di-tert-butylphenol (19),-[2-()-hydroxy-2-(4-hydroxy-phenyl)-ethyl]-3-(4-hydroxy-3-methoxy-phenyl)- acrylamide (20).Compound 15 is new natural product, named cannabinolactam A.Compounds 4, 8, 9, 14, 19, 20 are isolated fromgenus for the first time.Furthermore, the assignments of13C-NMR data of compounds 10 and 16 are reported for the first time.
L.; cannabinoids; spiro ring; cannabinolactam A; (2,6)-2,6-nonadienoic acid; 8-hydroxylinalyl acetate; cannabielsoin-C3
R284.1
A
0253 - 2670(2022)10 - 2949 - 07
10.7501/j.issn.0253-2670.2022.10.003
2021-09-14
黑龙江省省属高等学校基本科研业务费科研项目(145109513);齐齐哈尔大学研究生创新科研项目(YJSCX2019030)
王金兰,女,副教授,硕士生导师,主要从事天然产物化学研究。E-mail: jinlwang@163.com
[责任编辑 王文倩]
