“黄芪-太子参”对慢性心力衰竭作用机制的网络药理学分析
2022-05-21陈美慧韩宇博隋艳波
陈美慧,韩宇博,隋艳波,刘 莉
(1.黑龙江中医药大学,黑龙江 哈尔滨 150040;2.黑龙江中医药大学附属第一医院,黑龙江 哈尔滨 150040)
慢性心力衰竭(chronic heart failure,CHF)是由心脏结构和(或)功能异常引起静息或负荷时心输出量减少和(或)心内压力增高的一组复杂临床综合征,可表现为呼吸困难、心悸、乏力、下肢水肿等症状,是各种心脏疾病的终末阶段。因其高患病率、住院率、死亡率给社会和个人带来沉重负担。全球患有心力衰竭的人数超过2 600 万,随着我国人口老龄化趋势加剧,心力衰竭流行病学调查的最新结果显示我国约有1 370 万心衰患者,而年龄阶段在35 岁以上的患病率为1.3%[1]。一项多中心随机对照实验表明标准基础治疗联合口服中药芪苈强心胶囊,可显著改善CHF 主要结局指标N 末端脑钠肽前体水平[2]。《中国心力衰竭诊断和治疗指南2018》也明确指出了中医中药的干预作用,越来越多的中医药治疗被广泛用于临床,且中医药治疗心衰具有稳定病情、改善心功能、提高生存质量等优势[3]。中 医 学 者 认 为CHF 属“喘 证”、“虚 劳”、“水肿”等范畴,病机可概括“虚”、“瘀”、“水”,其虚实消长的动态决定了心衰的发展演变[4]。
刘莉教授治疗CHF 以补虚扶正为指导思想,结合中医经典与多年的临床经验,以“益气温阳、活血利水”为治疗大法,总结运用“参芪益心方”为治疗CHF 的经验方,取得了较好疗效[5-7]。方中“黄芪-太子参”共为君药,两者均为益气之品,共奏补益脏腑之功。黄芪、太子参药性平和,同归脾、肺经。黄芪有补气固表、利尿之功效,具有保护心肌细胞和血管内皮细胞,抑制心肌肥厚、心肌纤维化的作用[8,9]。太子参有益气健脾、生津润肺之功效,可以保护心肌、改善氧化应激状态、降血脂等[10,11]。目前,“黄芪-太子参”治疗CHF 的机制尚不明确。网络药理学作为一种中药新药的研究方法,可以通过建立网络模型,对中药成分与疾病的靶点、通路进行分析,揭示药物与疾病的作用关系。因此,本研究借网络药理学优势,对“黄芪-太子参”治疗CHF 的潜在机制进行分析,为临床应用提供一定的理论依据,从而进一步指导用药。
1 材料与方法
1.1 “黄芪-太子参”药对活性成分的收集与筛选
利用TCMSP 数据库(https://tcmspw.com/tcmsp.php)分别检索“黄芪”、“太子参”,得到中药化学成分信息,将相关参数设置为:口服生物利用度(OB)>30%且类药性(DL)>0.18,筛选后获取黄芪、太子参的活性成分及药物靶点。
1.2 药物-疾病-靶点网络的构建
以“Chronic Heart Failure”为关键词,通过在线人类孟德尔遗传数据库OMIM(http://www.omim.org/)与 人 类 基 因 数 据 库GeneCards(http://genecards.org/)进行检索,收集CHF 的相关靶点。应用Interactivenn 平 台(http://www.interactivenn.net/)获取药物与疾病的靶点交集。将交集靶点(Drug-Disease)导入Cytoscope3.7.1 软件,构建药物-疾病-靶点(drug-disease-target,DDT)的可视化网络。
1.3 蛋白互作网络的建立
使用String 数据库,将Drug-Disease 结果上传,设定物种为“Homo sapiens”,最低互动分数为0.400,导出靶蛋白互作网络(protein-protein interaction network,PPI),再使用Cytoscope3.7.1 软件对节点分析排序。
1.4 GO 功能和KEGG 通路富集分析
在DAVID 数据库中导入Drug-Disease 结果,进行基因本体(Gene Ontology,GO)分析和基于京都基因与基因百科全书(Kyoto Encyclopedia of Genes and Genomes,KEGG)信号通路富集分析,再根据Pvalue 数值排序,筛选10 项GO 功能和KEGG 通路12 条进行可视化分析。
2 结果
2.1 黄芪-太子参药对化学成分信息
通过TCMSP 数据库检索“黄芪”、“太子参”得到所有化学成分,经过筛选(符合OB>30%且DL>0.18 条件),最终共获得28 个有效化学成分,黄芪20 个,太子参8 个。根据OB 值,将各药物排名前5的有效成分基本信息列出,见表1。

表1 黄芪-太子参的化学成分基本信息Tab 1 Basic information on chemical compositions of Radix Astragali-Radix Pseudostellariae
2.2 DDT 网络的构建
运用TCMSP 数据库获得黄芪-太子参药对作用靶点共106 个,在OMIM 与Gene Cards 数据库搜索得到CHF 相关基因靶点10 352 个,将所得药物与疾病靶点进行交集化处理,共得到104 个药物-疾病靶点,见图1。运用Cytoscape3.7.1 软件对中药调控网络进行可视化处理发现,该网络具有104 个节点、389 条边,见图2。

图1 药物-疾病-靶点(DDT)韦恩图Fig 1 Drug-disease-target(DDT)Wayne diagram

图2 药物-疾病-化学成分-靶点网络Fig 2 Drug-disease-chemical composition-target network
2.3 PPI 网络的构建及可视化分析结果
进入String 互联网界面,将Drug-Disease 的交集靶点全部导入数据库,物种选择“Homo sapiens”,最低互动分数为0.400,利用Cytoscape 软件,根据Degree 值对104 个节点进行有序排列,前5 个靶点依 次 为IL-6、VEGFA、CASP3、MAPK8、EGFR。见图3。
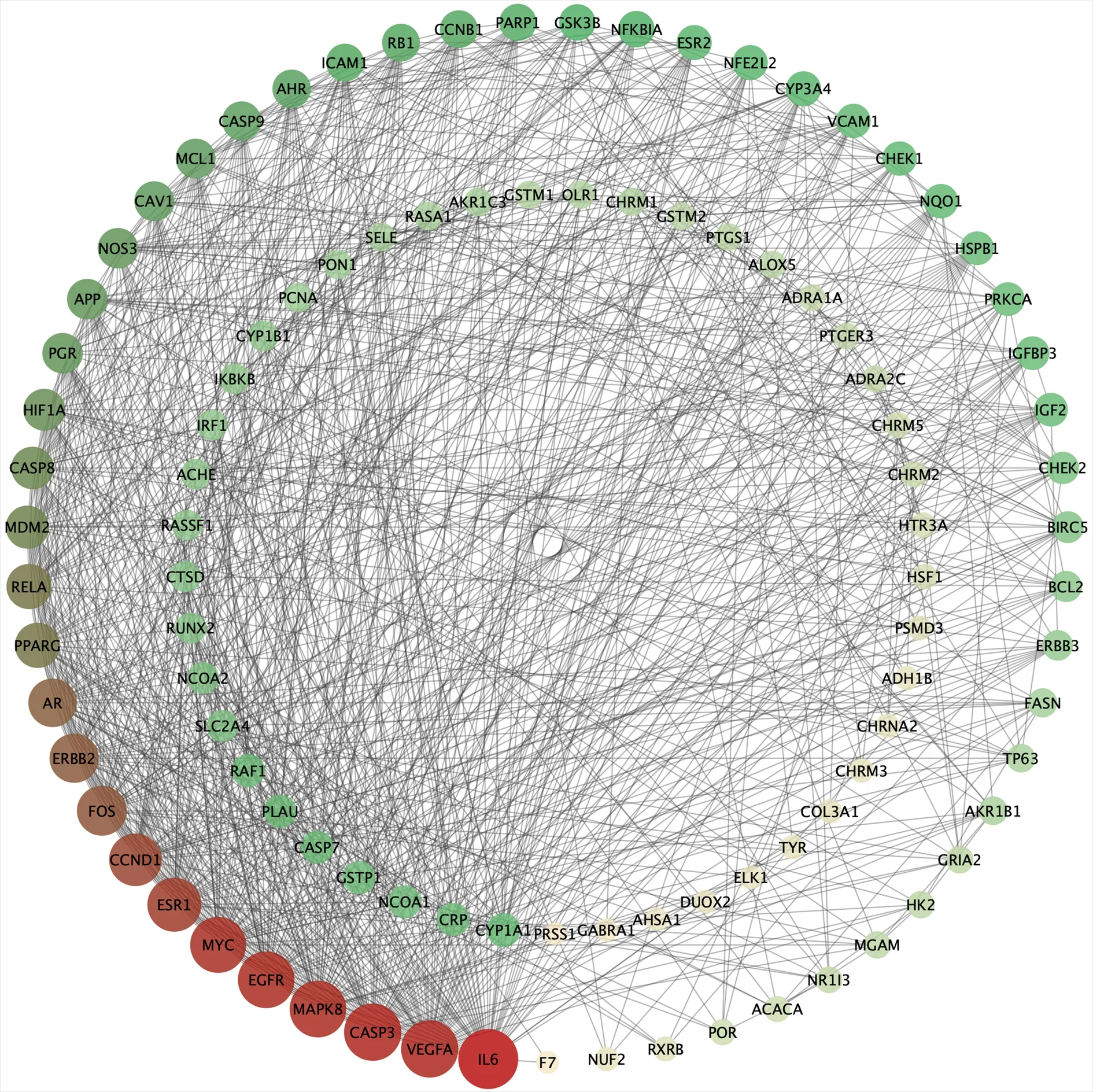
图3 关键靶点排序结果Fig 3 Sequencing results of key targets
2.4 GO 功能分析
应用DAVID 数据库对所得到的104 个“药物-疾病”靶点进行GO 功能分析,共得出49 条功能注释。利用OmicShare 平台对细胞成分(cell component,CC)、分子功能(molecular function,MF)和生物过程(biological process,BP)类别分析,并依据P值和富集靶点数,将靠前的GO 富集分析结果进行排序。见图4~7。
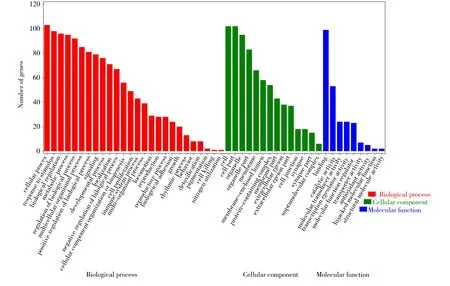
图4 GO 功能分析图-GO 柱状图Fig 4 GO function analysis diagram-GO histogram
2.5 KEGG 富集分析
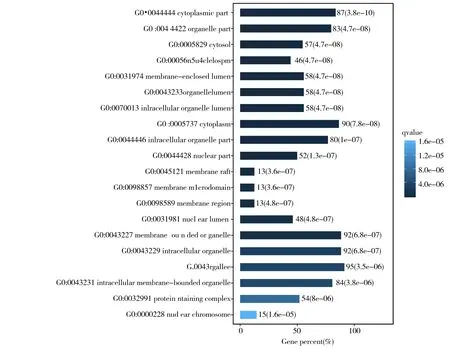
图5 细胞成分的GO 功能分析图Fig 5 GO function analysis diagram of cell component

图6 分子功能的GO 功能分析图Fig 6 GO function analysis diagram of molecular function
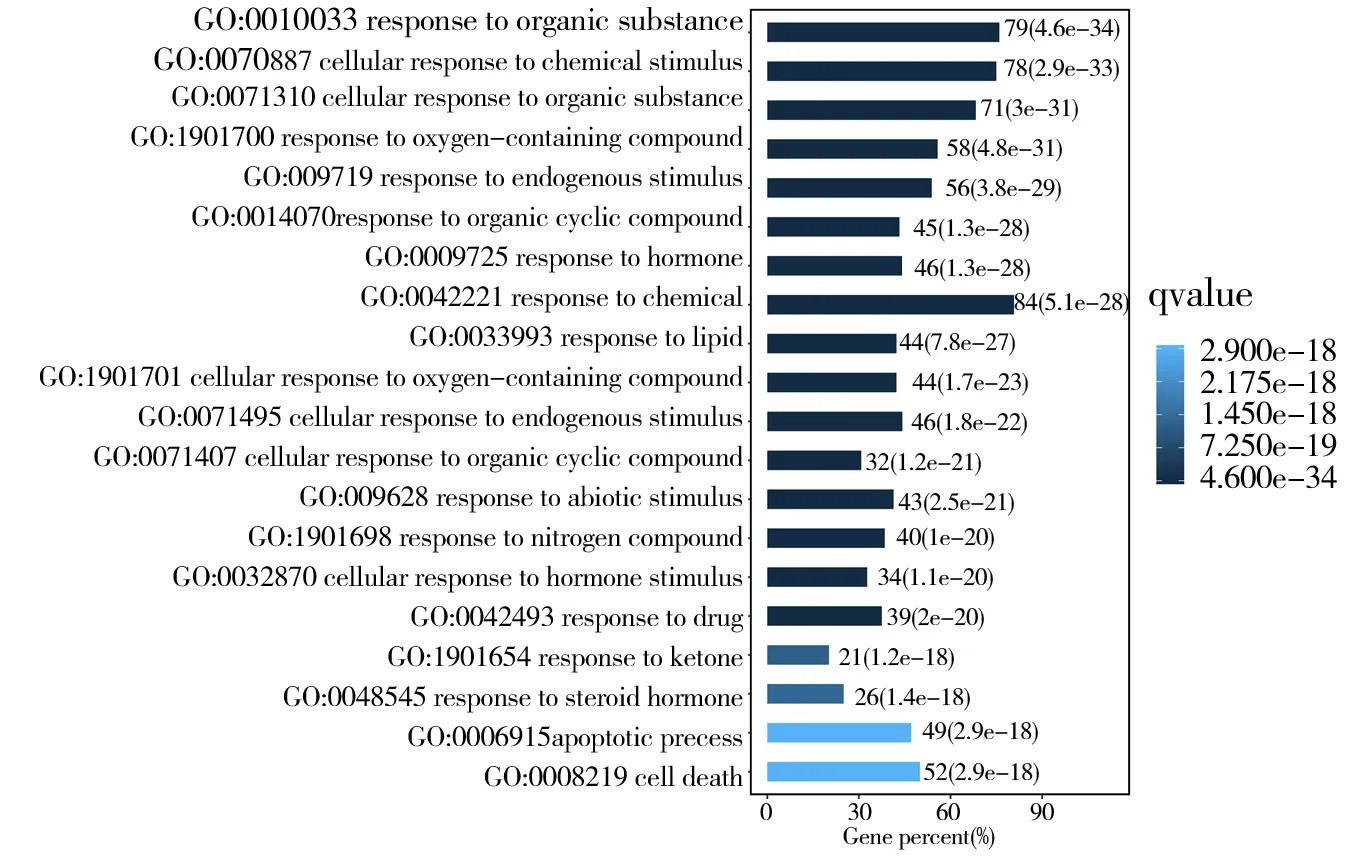
图7 生物过程的GO 功能分析图Fig 7 GO function analysis diagram of biological process
通 过DAVID 平 台,对104 个DDT 进 行KEGG富集分析,共得到86 条富集通路,结果表明“黄芪-太子参”治疗CHF 与多种信号通路相关,根据KEGG 气泡图显示其中排名靠前的通路主要有PI3K-Akt、MAPK、TNF 等,见图8。通过Cytoscape软件对DDT 与富集通路进行可视化网络展示,该网络具有140 个节点,510 条边,见图9。
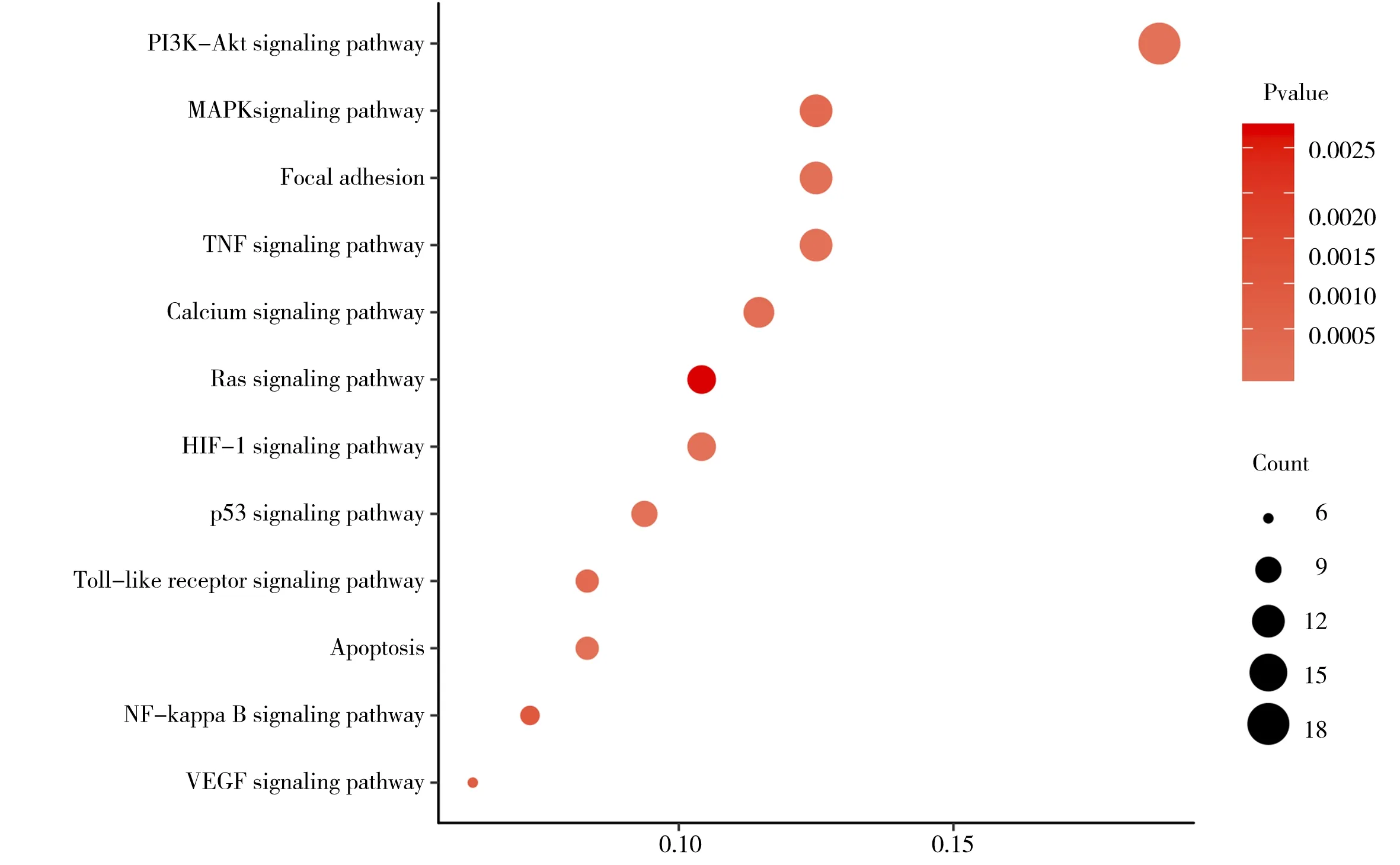
图8 KEGG 富集分析气泡图Fig 8 Bubble diagram of KEGG enrichment analysis
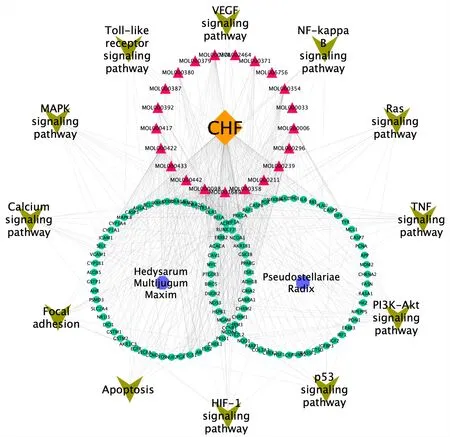
图9 药物-疾病-靶点-通路网络Fig 9 Drug-disease-target-pathway network
3 讨论
CHF 是一种缓慢进展性病变,指在原有慢性心脏病的基础上逐渐出现心衰的症状和体征。CHF与炎症反应、氧化应激、血管内皮功能调节等有关,其最关键的病理、生理机制为心室重构,然而心肌细胞凋亡、心肌肥大及心肌纤维化等是心室重构的基本特征。CHF 以老年患者居多,且病情迁延不愈,耗伤人体正气,则心气亏虚。黄芪为补气之要药,具有益气温阳之功,大量研究证实黄芪及其有效成分具有明显的强心作用,可改善心衰[12]。太子参为气血双补之品,补气滋阴而不助热,可改善急性心肌梗死所致的CHF,具有保护心肌的作用[10]。基于网络药理学研究发现,黄芪、太子参两味中药内含有多种有效成分,可作用于多靶点、多通路,共同调节生物功能影响CHF。
本研究经过筛选统计,共获得28 个化学成分,其中芒柄花素、山奈酚、槲皮素、β-谷甾醇等为主要化合物。在CHF 的发展过程中,氧化应激、炎症因子、血管紧张素Ⅱ(AngⅡ)可等诱导心肌细胞发生凋亡,启动代偿性结构重构,而进一步发展则会引发心肌肥厚、心脏顺应性下降等病理性重构,最终发展成为心力衰竭。活性氧的大量堆积可促发病人体内氧化应激功能紊乱,引起心肌细胞损伤和死亡,与心力衰竭心室重构病理过程密切相关。于雪等[13]建立H9C2 心肌细胞缺氧复氧模型,发现芒柄花素能够降低心肌细胞内活性氧水平,改善细胞贴壁的状态,增加细胞存活率,对心肌细胞有一定的保 护 作 用。 Toll 样 受 体4(Toll-like receptor 4,TLR4)是心肌细胞中表达量最高的TLR 的亚型,通过与配体结合,激活下游NF-κB,诱导炎症因子的产生,在炎症反应中发挥重要作用[14]。相关研究表明[15]山奈酚能明显改善H9c2 细胞活性,这种情况可能与抑制TLR4/NF-κB 信号通路相关,通过抗心肌细胞炎症的发生而减少细胞凋亡,从而发挥保护心血管的作用。槲皮素作为黄酮类化合物,具有抗氧化应激、抑制炎症反应,抑制纤维化等多种生物作用,对心、肝、肾等器官具有明显保护作用[16],可明显降低AngⅡ诱导的心肌肥大细胞中Akt 磷酸化水平,从而抑制其活性[17]。此外,槲皮素还可通过抑制NADPH 氧化酶介导eNOS 磷酸化以增加内皮细胞生物利用度,改善血管内皮细胞功能,对心脏具有保护作用[18]。Choi 等[19]研究发现β-谷甾醇能抑制IL-6 活性,减少肿瘤坏死因子-α(tumor necrosis factor-α,TNF-α)和白介素(IL)-1β(IL-1β)等炎性因子的释放,改善炎症反应,且通过上调SOD、下调ERK1/2 水平,参与到缓解氧化应激和抑制细胞凋亡过程中[20]。可见黄芪、太子参中相关化学成分对CHF 的治疗有一定的积极作用。
根据PPI 网络图显示,“黄芪-太子参”药对通过多靶点对CHF 发挥作用,分析后得出相互作用最多的靶点有IL-6、血管内皮生长因子(vascular endothelial growth factor,VEGF)A、CASP3、MAPK8、表皮生长因子受体(epidermal growth factor receptor,EGFR)等。IL-1、IL-6、TNF-α 等炎症因子对CHF 的发展可产生直接作用,其中IL-6 是一种重要的炎症介质。相关实验证实IL-6 刺激转化生长因子(TGF-β)的表达,使心肌细胞外基质胶原合成增加,降解减少,引起心肌纤维化,导致或加重心室重构,促进CHF 的发生[21,22]。VEGFA 是VEGF 家族主要的成员因子,在调节血管生成过程中具有重要作用,心肌组织内VEGFA 与VEGF-R1、VEGF-R2特异性受体结合后,通过多条生物途径,诱导内皮细胞增殖、分化、迁移,参与CHF 的血管重构和心肌血管生成[23],另一方面,VEGFA 由心肌细胞受炎症、机械作用和细胞因子刺激产生,其心肌能量代谢 变 化 影 响 着CHF 的 发 展[24,25]。心 肌 细 胞 凋 亡 是代偿性心肌重构转向心力衰竭的关键,受多种因子调控,其中CASP3、MAPK8 为比较重要的蛋白。CASP3 能够引发Caspase 级联反应,诱导细胞凋亡。Wang 等[26]的研究发现通过调控心衰大鼠心肌组织中Bcl-2 的表达,降低Bax 和Caspase 3 表达水平,从而抑制心肌细胞凋亡,达到改善大鼠心功能的作用。当激活MAPK8 时,上皮细胞中存在一种促凋亡蛋白BMF 发生磷酸化,进入线粒体,产生生物作用,启动细胞凋亡程序,从而导致心脏结构发生改变[27]。Ang Ⅱ引起的血管平滑肌细胞肥大与表皮生长因子受体EGFR 反式激活有关,EGFR 为一种跨膜糖蛋白,通过诱导内质网应激发挥作用,为血管重构的关键成分[28]。此外,EGFR 的激活会促使受体酪氨酸激酶发生磷酸化,导致一系列信号通路的启动,进而调控心肌细胞增殖、分化等[29]。综合上述,潜在靶点经多种途径参与CHF 病理、生理过程。
对“黄芪-太子参”药对治疗CHF 进行GO 分析发现,黄芪-太子参通过多种形式参与其生物学进程,主要涉及细胞凋亡、血管内皮细胞迁移、氧化应激反应、炎症反应等。经KEGG 富集分析得到多条信号通路,主要的通路有PI3K-AKT、MAPK、TNF等。PI3K-AKT 是体内一条重要的信号转导通路,PI3K 为上游信号,能激活并促使其下游的AKT 发生磷酸化,参与信号转导过程,通过调控下游多种蛋白,对血管再生、心肌细胞凋亡自噬、能量代谢、Ca2+循环蛋白及炎症反应等活动产生影响,与CHF的 发 生 与 发 展 关 系 紧 密[30,31]。PI3K 表 达 水 平 和AKT 磷酸化水平下降,对心脏功能的改善与恢复有着积极的作用。相关实验[32]表明黄芪中活性成分能通过上调SIKE 抑制TBK1/PI3K/AKT 活性,预防心肌肥厚。MAPK 是将信号从细胞外传导到细胞核内的重要传递者,广泛存在于各种细胞中,参与细胞生长、增殖、分化、凋亡以及应激、炎症和自噬等多种生理病理过程,当MAPK 信号通路激活,细胞外调节蛋白激酶(ERKs)、c-Jun 氨基末端激酶(JNK)和p38 丝裂原活化蛋白激酶(p38MAPK)磷酸化,调控基因表达,造成心肌细胞肥大、凋亡等,从而导致心肌肥厚、心肌纤维化[33,34]。抑制ERKs、JNK、p38MAPK 通路,能减轻心肌细胞凋亡,降低心肌自噬水平,减少心肌损伤,使心肌细胞因子水平正常化,改善心室收缩功能[35-37]。TNF 信号传导通路的激活,可促进细胞生长、分化,同时诱发细胞凋亡、炎症反应,多种途径参与心室重构。心肌细胞本身不能产生TNF-α,当CHF 出现时,TNF-α 能够在细胞中表达,激活NF-κB 转录到细胞核,诱导IL-6、环氧化酶(COX)等炎症因子,刺激心肌细胞肥大和凋亡,导致组织重构[38-40],加重CHF 的病情。因此,本研究认为“黄芪-太子参”可能通过多靶点、多途径、多信号通路等协调发挥生物学效应,从抑制细胞凋亡、减轻炎症反应、对抗心室重构等多方面达到延缓心衰的发展的目的。
黄芪、太子参为补益之品,药物性质稳定。本研究基于网络药理学,构建可视化网络图,发现“黄芪-太子参”药对中含28 个有效化学成分、104 个靶点、86 条通路与CHF 存在潜在相关性,其作用机制可能通过抑制细胞凋亡、抗炎、抗氧化应激等途径协同治疗CHF,为今后挖掘治疗基因及深入研究“黄芪-太子参”或中药治疗CHF 的机制提供基本参考依据。
作者贡献度说明:
陈美慧:研究设计,实施研究,采集及统计分析数据,文章撰写等。韩宇博:工作指导、文章内容审阅。隋艳波:工作指导、技术支持等。刘莉:研究设计,工作指导、文章审阅等。
