红薯生物质碳气凝胶的制备及其吸附性能
2022-05-20施逸帆
施逸帆,孙 京
(辽宁石油化工大学 石油化工学院,辽宁 抚顺 113001)
碳气凝胶作为气凝胶的一个分支,是一种新兴的碳基功能性材料,因其具有较高的比表面积与丰富的孔隙结构,故成为学者研究的热点[1-4]。在过去的研究中,通常以工业原料如酚醛树脂等作为碳源,在限氧的条件下进行高温热解碳化,得到具有特殊结构的碳气凝胶[5-8]。因为,此类碳气凝胶的原材料在生产过程中会产生大量污染,所以越来越多的科研人员选择自然界中最广泛存在的生物质材料作为碳气凝胶新的碳源[9-17]。生物质碳气凝胶因其原料的环保性、制备工艺的便捷性以及低廉的成本而具备独特的优势。目前,对生物质的研究大多集中在木材、植物表皮、植物果实等以木质素或纤维素为主要成分的材料上,对植物其他部分的研究较少[18-21]。
本文以典型的植物块根红薯为原料,通过冷冻干燥与一步活化法制备了对染料具有较高吸附能力的生物质碳气凝胶,通过考察制备过程中的碳化温度与活化步骤对碳气凝胶形貌的影响,碳气凝胶针对不同染料的吸附性能与离子强度对吸附作用的影响,评估红薯生物质碳气凝胶在污染物吸附方面的应用前景,为水体环境的净化探索新的可行路径。
1 实验部分
1.1 实验原料、试剂与仪器
原料及试剂:红薯,产地为福建省漳州市漳浦县六鳌镇;氢氧化钾(KOH)、盐酸(HCl)、氯化钠(NaCl),分析纯,国药集团化学试剂有限公司;甲基蓝(MB)、甲基橙(MO)、茜素红(ARS)、罗丹明B(Rd B)、柠檬黄(LY),纯度为98%,阿拉丁试剂公司;去离子水为实验室自制。
仪器:CXG1100-60管式反应炉、FD-1B-80冷冻干燥机,上海诚献仪器设备有限公司;JSM-7800F扫描电子显微镜,日本电子株式会社;Rigaku Ultimate IV粉末X射线衍射仪,日本理学株式会社;DXR2xi拉曼光谱仪、Evolution 220 UV-VIS分光光度仪,赛默飞世尔科技公司;ASAP 2460比表面积及孔径分析仪,麦克默瑞提克(上海)仪器有限公司。
1.2 SPCA生物质气凝胶的制备
将红薯去皮,切成小块(1 cm×1 cm×1 cm)。用去离子水冲洗后放入-16℃冰箱保存3 h,使其结构稳定。将冷冻后的红薯置于冷冻干燥机干燥24 h后,放入刚玉坩埚中,在氮气氛围的管式炉中进行碳化。氮气流速设置为250 mL/min,管式炉以5℃/min的速度升温至300℃,停留1 h以去除细胞内残留的水,然后升高温度至预定值,热解3 h。热解完成后,用去离子水洗净产物,最终产物记为SPCA-X,X为最终碳化温度。
1.3 ASPCA生物质气凝胶的制备
将红薯去皮,切成小块(1 cm×1 cm×1 cm)。用去离子水冲洗后放入-16℃冰箱保存3 h,使其结构稳定。将冷冻后的红薯置于冷冻干燥机干燥24 h后,浸泡在质量分数为5%的氢氧化钾溶液中9 h。用去离子水冲洗干净后再置于冰箱冷冻3 h,冷冻干燥机中干燥24 h。干燥后的产物置于镍坩埚中,在氮气氛围的管式炉中进行碳化。氮气流速设置为250 mL/min,管式炉以5℃/min的速度升温至300℃,停留1 h后升高温度至预定值,热解3 h。热解完成后,以质量分数为2%的盐酸洗涤,并用去离子水冲洗至pH为7.0左右。最终产物记为ASPCA-X,X为最终碳化温度。
1.4 生物质气凝胶的表征
1.4.1 扫描电镜(SEM) 采用扫描电镜对碳气凝胶的微观结构进行分析。实验条件:加速电压为5 000 V,探测电流为3.2 nA。
1.4.2 X射线衍射(XRD) 采用粉末X射线衍射仪对样品进行分析。实验条件:以Cu-Ka靶(0.154 nm)为辐射源,管电压为40 kV,管电流为40 mA,扫描角度为10°~80°,扫描速度为5(°)/min。
1.4.3 拉曼光谱(Raman) 采用拉曼光谱仪进行分析。实验条件:激发波长为532 nm,记录波长为40~4 000 cm-1。
1.4.4 BET比表面积测试(BET) 采用比表面积分析仪对样品进行分析。在77.3 K环境中通过氮气吸附-脱附测试对样品进行表征。
1.4.5 紫外吸光度(UV) 采用UV-VIS分光光度仪测定上清液中的染料吸光度,并以此为基准标定染料浓度。
1.5 吸附性能表征
将10~300 mg染料溶解于1 L去离子水中,得到染料预溶液(质量浓度为10~300 mg/L),并测定各染料的标准吸光曲线。将10 mg生物质碳气凝胶和10 mL去离子水加入透明玻璃瓶中混合,密封,以100 r/min的转速预平衡10 min后,加入一定量的预平衡液,得到混合溶液。
生物质碳气凝胶的吸附量Q(mg/g)计算公式:

式中,C0和Ce分别为初始溶液中染料的质量浓度和吸附平衡后溶液中染料的质量浓度,mg/L;V为溶液体积,L;m为生物质碳气凝胶吸附剂的质量,g。
在动力学实验中,染料的初始质量浓度为100 mg/L,混合溶液的p H为6.5~8.5,混合时环境温度为(25±1)℃,转速为100 r/min。在一定时间内,通过上清液的紫外吸收峰测定其分时吸附量,并通过准二级动力学模型对吸附动力学进行描述,具体模型如下:
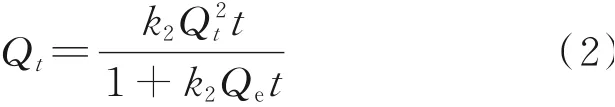
式中,Qe为吸附平衡时单位质量生物质碳气凝胶上的吸附量,mg/g;Qt为吸附时间t时单位质量生物质碳气凝胶上的吸附量,mg/g;t为吸附时间,min;k2为准二级动力学速率常数,g/(mg·min)。为了保证精度,所有实验重复3次。
2 结果与讨论
2.1 生物质碳气凝的表征
图1为生物质碳气凝胶的拉曼光谱。从图1可以看出,生物质碳气凝胶样品在1 355 cm-1和1 585 cm-1处出现了两个特征峰,分别为碳材料的D峰和G峰。D峰是材料中的无序碳造成的,表明晶格的缺陷,而G峰是sp2有序碳的结构反映[22-24]。根据ID/IG对比分析可知,未添加活化剂时的ID/IG比添加时的ID/IG略高,但数值差异较小,这说明活化剂的添加有助于形成石墨型结构,但并不会对其结构造成太大影响。
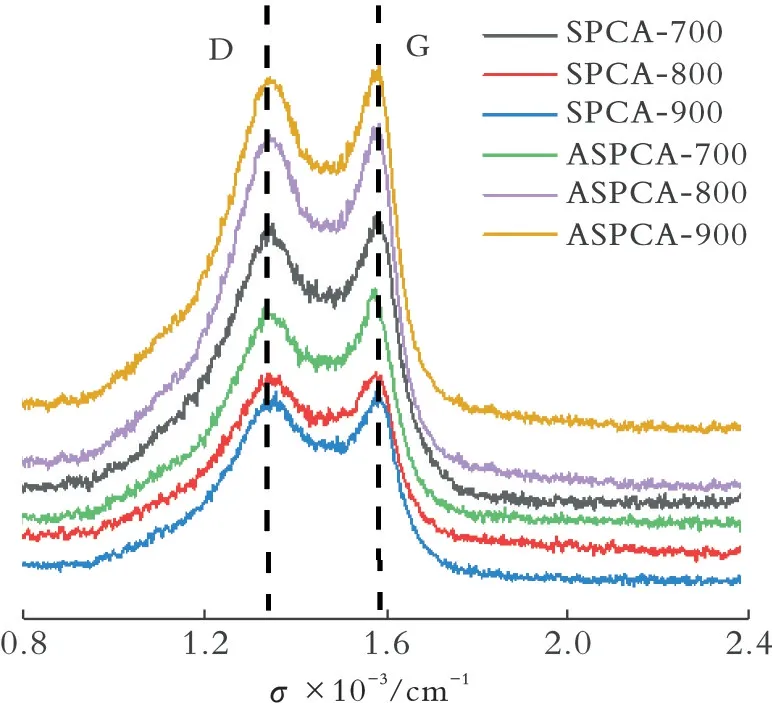
图1 生物质碳气凝胶的拉曼光谱
通过低温氮气吸附-脱附法分析SPCA和ASPCA的孔隙结构,结果见图2。从图2可以看出,根据IUPAC对吸附等温线的分类,SPCA的等温线可归为III型,而ASPCA的等温线可归为IV型[25];图2(b)、(d)、(f)中ASPCA的等温线均出现了在较低的相对压力(p/p0)下迅速升高的曲线,这表明已形成微孔结构,而吸附-脱附曲线之间的回滞环也表明微孔的大量存在[26];当吸附过程继续时,在p/p0为1.0附近没有出现斜率趋近于0的平台,这表明在碳气凝胶的结构中存在部分大孔。相比之下,SPCA的吸附-脱附曲线在p/p0从0到接近1.0时,始终呈现出近乎水平的吸附-脱附曲线,这表明碳气凝胶基本无微孔生成。
表1为BET低温氮气吸附-脱附数据。由表1可知,ASPCA-900的比表面积为591.47 m2/g,而未经活化的SPCA-900仅有0.27 m2/g;ASPCA-900的微孔面积为448.91 m2/g,占总比表面积75.8%。随着碳化温度的升高,ASPCA的比表面积快速增加,这得益于KOH在高温下对碳气凝胶的活化再造孔的作用[27-30]。对SPCA而言,高温或低温下样品的比表面积均较低,微孔面积几乎可忽略不计,这可能是由于植物细胞的细胞壁存在一定的刚性,在碳化过程中刚性结构坍塌,引起生物质结构被破坏,导致形成的孔隙坍缩,无法形成有效的多孔结构[31]。采用一步活化方式利用KOH碱溶液浸润红薯气凝胶,使碱溶液深入红薯的细胞结构中,刻蚀细胞壁结构,并且在碳化过程中参与碱活化,形成了大量的孔隙结构,使ASPCA测出的比表面积和微孔面积大大增加,这与图2中ASPCA的吸附-脱附等温线类型非常吻合。
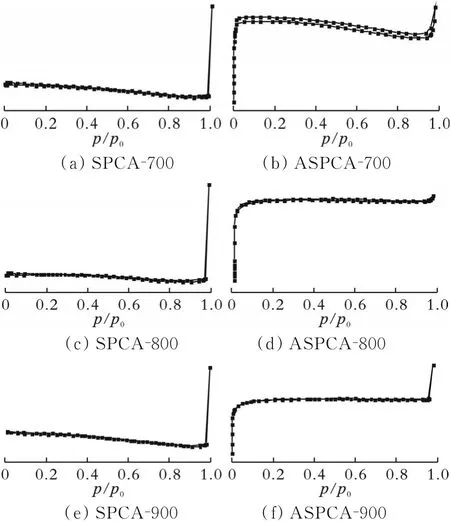
图2 生物质碳气凝胶的吸附-脱附等温曲线
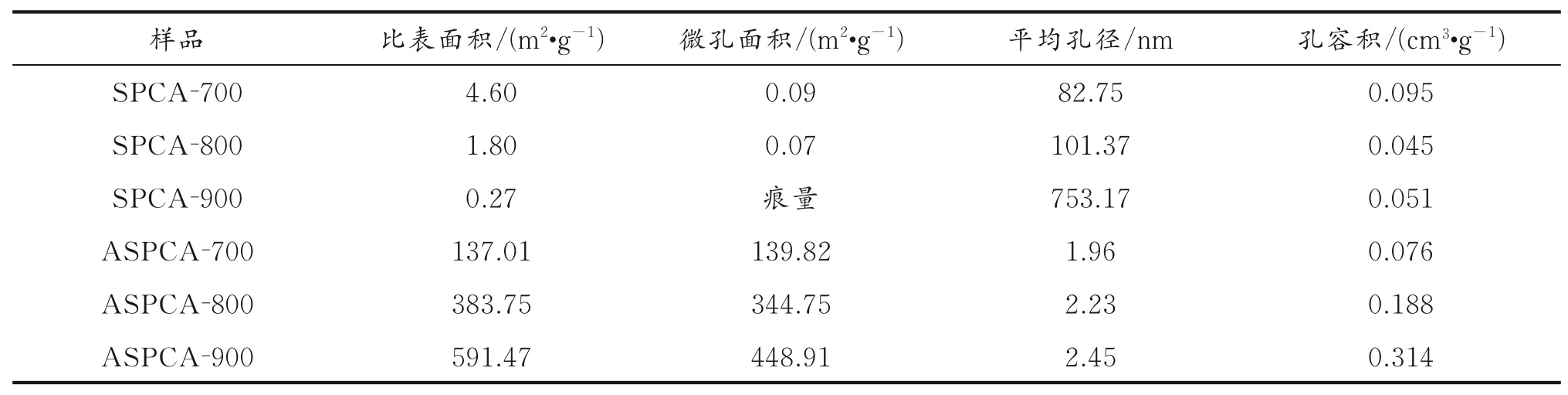
表1 BET低温氮气吸附-脱附数据
针对最具代表性的SPCA-900与ASPCA-900,通过XRD分析了其晶型的区别,结果见图3。从图3可以看出,SPCA-900和ASPCA-900均在24°和44°处出现衍射峰,分别对应(002)和(100)面,这表明碳气凝胶是由石墨型碳和无定型碳组成的[32-33]。然而,两者曲线很类似,这证明活化步骤对碳的主体结构和类型的影响有限,该结果与拉曼光谱得出的结论相吻合。
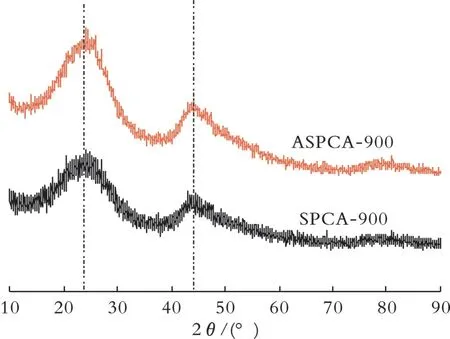
图3 生物质碳气凝胶的XRD谱图
2.2 碳化温度与活化程序对形貌的影响
图4为生物质碳气凝胶的SEM图。从图4(a)-(c)可以看出,SPCA主要为片状结构,表面较为光滑,这可能是刚性的细胞壁结构所形成的微观形貌;图4(a)、(b)中基本不存在可见的孔隙结构,图4(c)中存在少量的圆形小孔,该小孔的直径约为1μm,这与表1中SPCA-900的平均孔径为753.17 nm的数据相吻合。从图4(d)-(f)可以看出,ASPCA存在丰富的孔隙结构,无SPCA形貌中的大量平整的片状结构;随着碳化温度的升高,ASPCA的孔隙大量增加;ASPCA的多孔结构均匀分布在连续的碳网络上,具有三维网状结构和连通的微孔。值得注意的是,具有连续碳骨架的互联三维结构会促进小颗粒的传导,增加最大吸附容量[34]。

图4 生物质碳气凝胶的SEM图
2.3 吸附性能研究
针对碳气凝胶的吸附性能,选取罗丹明B(Rd B)、甲基橙(MO)、甲基蓝(MB)、柠檬黄(LY)和茜素红(ARS)进行研究。为了对生物质碳气凝胶的吸附性能做出初步筛选,以RdB为预选原料,吸附时间为24 h,对ASPCA的吸附性能进行初步评测,结果见表2。

表2 ASPCA对RdB的24 h吸附量
由表2可知,ASPCA-700吸附量最小,仅为40.0 mg/g,而ASPCA-900吸附量则达到了140.2 mg/g。这是由于ASPCA-900具有较高的比表面积和孔容积,可以更多地吸附水体中的有机污染物。
设定吸附时间为48 h,评价多种染料的吸附性能,结果见表3。由表3可知,ASPCA-900吸附剂对阳离子型染料Rd B的吸附性能较好,吸附量超过200.0 mg/g;而ASPCA-900吸附剂对同为阴离子型染料,且分子结构均为磺酸钠盐的MO、MB、LY和ARS表现差距较大。这是因为:从分子结构出发,生物质碳气凝胶表面主要依靠静电引力使染料吸附在其表面,同时生物质碳气凝胶表面仍存在一定量的-OH与-COOH等官能团,使其表面电荷偏向负电性,增加了对阳离子型染料的吸附能力,故对RdB的吸附效果较强。由表3还可以看出,ASPCA对相对分子质量较小、分子结构较小的阴离子型染料MO与ARS具有良好的吸附效果,而对相对分子质量大、分子结构大的阴离子型染料MB与LY的吸附效果明显降低。该现象和吸附剂中的孔径分布相对应,ASPCA-900中以微孔为主要结构,其微观尺度小于1 nm,对分子结构较大的染料的吸附能力小于分子结构较小的染料。

表3 ASPCA-900对不同染料的吸附性能
在吸附过程中,溶液的离子强度对吸附性能存在双向影响:一方面,水中的离子会与吸附物竞争吸附位点,从而使对污染物的吸附量降低;另一方面,离子强度的增加会提高吸附质与吸附剂之间的吸引力,增加吸附质与吸附剂的有效碰撞率,从而提高吸附量[35-36]。在吸附时间为24 h的条件下,考察NaCl质量分数对吸附性能的影响,结果见表4。由表4可知,当溶液中NaCl质量分数为3%时,ASPCA-900对RdB或ARS的吸附量均达到最大值,并且对ARS和RdB的吸附量均大于在去离子水中24 h吸附量。随着NaCl质量分数的增加,染料的盐析作用增加了其在固相与液相间的分隔,但是过多的Na+会与同为阳离子型的Rd B竞争吸附点位;而离子质量分数升高在一定程度上降低阴离子型的ARS与生物质气凝胶之间的静电斥力,最终导致了对ARS的吸附增量大于对Rd B的吸附增量[37]。值得注意的是,海水的盐质量分数同样在3%左右,这可以充分发挥生物质气凝胶的最大吸附能力。

表4 离子强度对不同染料的吸附性能
考察吸附时间对红薯生物质碳气凝胶吸附染料ARS和RdB的影响,结果见图5。从图5可以看出,ASPCA-900对染料的吸附可以分为两个阶段,即60 min之前的快速吸附阶段和60 min之后的慢速吸附平衡阶段。在快速吸附阶段,吸附量随吸附时间的增加而快速增加,超过85%的染料在此阶段完成吸附。在慢速吸附阶段,随着吸附时间增加,吸附量增量减少,逐渐达到吸附平衡后不再增加。

图5 吸附时间对吸附量的影响
采用准二级动力学模型(PSO model)对吸附数据进行拟合,结果见表5。由表5可知,ASPCA-900对污染物的吸附复合准二级动力学模型,相关系数R2>0.990 0。这说明化学吸附是红薯生物质碳气凝胶的控速步骤[38-39]。

表5 ASPCA-900准二级动力学拟合参数
表6为不同生物质碳气凝胶的对比结果。由表6可知,本文所制备的生物质碳气凝胶吸附剂具有一定的竞争力。

表6 不同生物质碳气凝胶的对比结果
3 结 论
以典型的植物块根红薯为碳源,通过一步活化法制备了具有高比表面积的活化生物质碳气凝胶ASPCA。研究发现,提高碳化温度与碱活化可以显著增加ASPCA的比表面积,900℃下碳化的ASPCA比表面积较未活化前提升了约2 000倍;ASPCA对分子量较小的染料或阳离子型染料有良好的吸附性能;在去离子水中,对阳离子型染料罗丹明B的吸附量可达到202.2 mg/g,对阴离子型染料茜素红的吸附量可达160.2 mg/g。当水中NaCl质量分数为3%时,可一定程度增加红薯生物质碳气凝胶的吸附量。对吸附数据进行拟合发现,吸附过程符合准二级动力学模型。本实验为污染水体净化提供了新的环保吸附材料选择,为水处理提供了一种可行的方案。
