猫眼草黄素对破骨细胞分化及自噬作用的研究*
2022-05-17苏珮茹罗香雅曾春平
苏珮茹,罗香雅,曾春平,周 琳
(广州医科大学附属第五医院/广州市加速康复腹部外科重点实验室/广州医科大学第五临床医学院,广东 广州 510700)
骨质疏松症是一种系统性代谢性骨病,其特征是骨量降低、骨组织微结构损坏,进而导致骨脆性增加、骨折风险增高。随着人口老龄化的加剧,骨质疏松症发生率逐年升高,因骨质疏松产生的并发症如骨折,严重影响患者日常生活,并给患者及家属带来了严重的心理和经济负担,因此寻求有效防治骨质疏松的方法成为目前亟待解决的问题[1]。
猫眼草黄素是一种多甲氧基黄酮,存在于多种植物中,如泽漆(俗称猫眼草)、黄花蒿、细花线纹香茶菜、岩筋菜等植物中[2]。黄酮类化合物是一种常见植物多酚,这类化合物与雌激素结构类似,具有抗炎、抗氧化、抗肿瘤、抗感染等作用[3]。部分黄酮类化合物能通过调控成骨细胞或破骨细胞功能,从而保护骨组织[4]。近期研究发现,猫眼草黄素能通过Wnt/β-catenin通路促进成骨细胞分化,改善雌激素缺乏诱导的骨丢失,从而对骨细胞起保护作用[5]。此外,猫眼草黄素是青蒿素代谢相关的CYP450酶亚型的抑制剂,能显著提高青蒿素的抗疟性[6]。研究发现,双氢青蒿素能显著抑制破骨细胞的分化[7]。因此,推测猫眼草黄素除了能促进成骨细胞增殖,还能抑制破骨细胞分化。越来越多的研究表明,自噬参与破骨细胞的形成、分化及骨吸收作用等多个阶段[8-10]。自噬与破骨细胞的关系是目前破骨细胞与骨质疏松症相关研究的新方向。因此,本文主要探讨了猫眼草黄素对破骨细胞分化的影响及自噬在其中的作用,从而为骨质疏松症提供潜在的临床治疗方法。
1 材料与方法
1.1材料与试剂 猫眼草黄素(C19H18O8,分子量:374.34,纯度98%,CAS号:603-56-5)购自云南西力生物技术股份有限公司,采用二甲基亚砜配置成10 μmol/L溶液备用,按各目标浓度进行稀释。小鼠单核巨噬细胞RAW264.7购自美国ATCC公司;α-MEN培养基和胎牛血清购自美国Gibco公司,核转录因子-κB受体活化因子(RANK)配体(RANKL)购自美国R&D公司,抗LC3B抗体、抗ATG5抗体、辣根过氧化物酶(HRP)标记羊抗兔IgG抗体购自成都正能生物科技公司。
1.2方法
1.2.1细胞培养与分组 将小鼠单核巨噬细胞RAW264.7用含10%小牛血清的α-MEM完全培养基培养于37 ℃、5% CO2培养箱中。空白组给予完全培养基,模型组给予含50.0 ng/mL RANKL的培养基,A~F组给予不同水平猫眼草黄素(0.5、1.0、2.5、5.0、10.0、20.0 μmol/L)+含50.0 ng/mL RANKL的培养基。
1.2.2抗酒石酸酸性磷酸酶染料(TRAP)染色 当细胞汇合度达到80%以上时,将小鼠单核巨噬细胞RAW264.7按每孔1.0×103的密度接种于96孔板中,用含10%小牛血清的α-MEM完全培养基培养,贴壁后按分组处理,每2天换1次培养液,总共培养5 d。4%多聚甲醛室温固定细胞20 min,加入TRAP染色20 min,光镜下观察破骨细胞并计数,具有3个或更多个核的TRAP阳性多核细胞被认为是破骨细胞样细胞。
1.2.3采用猫眼草黄素干预破骨细胞 (1)不同水平的干预。细胞接种贴壁后,加入含0、1.0、5.0、10.0 μmol/L猫眼草黄素的完全培养基及50.0 ng/mL RANKL刺激24 h,提取细胞裂解液,采用免疫印迹法(Western blot)检测自噬相关蛋白表达情况:取细胞蛋白提取液,蛋白定量后加入蛋白上样缓冲液,100 ℃煮沸5 min;以12%十二烷基硫酸钠聚丙烯酰胺凝胶电泳并转移至聚偏氟乙烯膜,5%脱脂奶粉室温封闭2 h后孵一抗,4 ℃孵育过夜,用磷酸盐缓冲液(PBST)洗涤;再加入相应的HPR标记二抗孵育1 h,PBST洗涤后显影。(2)不同时间的干预。将RAW264.7细胞株按每孔5.0×104的密度接种于6孔板,加入含10.0 μmol/L猫眼草黄素的完全培养基及50.0 ng/mL RANKL,分别持续诱导1、3、5 d,收集细胞提取细胞裂解液,采用Western blot检测自噬相关蛋白表达情况。
1.3统计学处理 采用SPSS23.0统计学软件进行数据分析,计量资料多组间比较采用方差分析,P<0.05为差异有统计学意义。
2 结 果
2.1猫眼草黄素对破骨细胞分化的影响 C~F组破骨细胞数量与模型组比较,差异有统计学意义(P<0.05)。见图1、2。

A.空白组;B.模型组;C.A组;D.B组;E.C组;F.D组;G.E组;H.F组。
2.2不同水平干预对自噬相关蛋白表达的影响 与空白组比较,模型组及B、D、E组中自噬相关蛋白ATG5表达未见明显变化(P>0.05)。与空白组比较,模型组自噬相关蛋白LC3Ⅱ表达及LC3Ⅱ/LC3Ⅰ比值增加(P<0.05)。与模型组比较,B、D、E组自噬相关蛋白LC3Ⅱ表达及LC3Ⅱ/LC3Ⅰ比值降低(P<0.05)。见图3。
2.3不同时间干预对自噬相关蛋白表达的影响 与模型组比较,猫眼草黄素干预1、3、5 d时,自噬相关蛋白ATG5表达无明显变化(P>0.05)。在干预3、5 d时,自噬相关蛋白LC3的表达较模型组明显下降(P<0.05)。作用时效越长,猫眼草黄素抑制自噬的作用越明显。见图4。
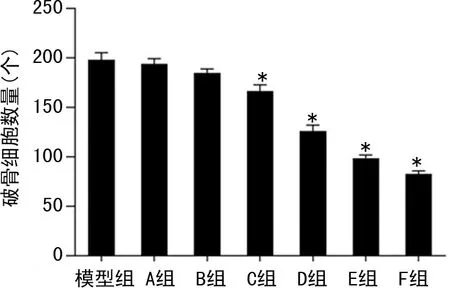
与模型组比较,*P<0.05。

图3 不同水平猫眼草黄素干预的Western blot检测结果

图4 不同时间干预的Western blot检测结果
3 讨 论
骨质疏松是一种全身性代谢性骨病,在临床上按病因主要分为原发性和继发性。原发性骨质疏松症为临床上常见类型,其可分为两型:Ⅰ型为绝经后骨质疏松症,发生于绝经后女性,主要由于雌激素缺乏导致骨量的流失;Ⅱ型为老年性骨质疏松症,多见于老年人,主要是年龄相关的生理性退行病变。继发性骨质疏松症病因明确,是由某些药物或疾病等引起的骨质量低下、骨微结构破坏和骨折风险增加的代谢性疾病,如糖皮质激素性骨质疏松、甲状腺功能亢进性骨质疏松症、糖尿病性骨质疏松症、风湿类疾病引起的继发性骨质疏松等。
破骨细胞是高度分化的多核巨细胞,起源于造血干细胞,并受RANK和巨噬细胞集落刺激因子的调控,其主要功能是骨吸收[11]。在正常生理情况下,破骨与成骨的动态平衡使骨代谢保持稳定状态,当这种平衡被打破时,就可能导致骨稳态失衡,最终发生骨质疏松[12]。目前治疗骨质疏松的药物很多,如雌激素、双膦酸盐、降钙素、RANKL抑制剂等[13],但部分具有费用昂贵、不良反应多等缺点。如双磷酸盐长期使用会引起胃肠道反应和肾功能损害;长时间使用雌激素替代治疗会提高乳腺癌及子宫癌等肿瘤疾病的发生风险[14]。天然化合物具有疗效显著、作用靶点广泛、不良反应少等特点,有可能成为骨质疏松治疗的最佳策略。
骨保护素(OPG)-RANKL-RANK系统是调节骨形成和骨吸收的关键信号通路[15]。研究发现,在去卵巢优势的大鼠模型中,骨髓细胞中的RANKL表达明显升高,促使OPG与RANKL比值下降,导致破骨细胞活性增强、骨吸收增强,提示绝经后患者雌激素缺乏会激活OPG-RANKL-RANK轴而导致骨质量下降,进而导致骨质疏松[16]。目前多项研究发现,对于继发性骨质疏松症,部分药物或疾病可以通过OPG-RANKL-RANK信号通路促进破骨细胞的形成及骨吸收,从而导致骨量丢失。如糖皮质激素能促进RANKL分泌,促使RANKL与RANK结合并激活下游信号通路,从而提高破骨细胞活性,促进破骨细胞分化成熟。因此,长期使用糖皮质激素易引起骨量丢失。炎性因子、生长因子等能激活RANK/RANKL通路,进而促进破骨细胞分化成熟及骨吸收功能,导致骨质疏松[17]。因此,抑制OPG-RANKL-RANK信号通路,有利于治疗骨质疏松症[18]。
猫眼草黄素是一种多甲氧基黄酮。研究表明,猫眼草黄素能抑制肠道病毒71型[19]和显著提高青蒿素的抗疟性[6],其通过Wnt/β-catenin通路促进成骨细胞分化,改善雌激素缺乏诱导的骨丢失,从而对骨细胞起保护作用[5]。目前,关于猫眼草黄素对破骨细胞作用的研究较少见。本研究组前期研究证实,低剂量的猫眼草黄素可高效抑制RANKL诱导的信号通路,对破骨细胞的分化和活性产生影响,并最终调节骨代谢失衡。本研究结果显示,通过不同水平猫眼草黄素干预后,TRAP染色阳性的破骨细胞数目逐渐减少,提示猫眼草黄素对破骨细胞的分化有抑制作用,且呈剂量依赖性,与前期研究结果相符。猫眼草黄素能抑制破骨细胞分化,其作用可能是通过抑制RANKL诱导的各种信号通路实现的。而多项研究发现,原发性及继发性骨质疏松症主要通过调节OPG-RANKL-RANK信号通路来促进破骨细胞分化、成熟及骨吸收。猫眼草黄素属于黄酮类化合物,与雌激素结构类似,具有抗炎、抗氧化等作用,其自身的生物活性与其抗骨质疏松的特性密切相关,可能具有抑制类风湿关节炎、氧化应激、雌激素缺乏等病因引起的骨质疏松症的作用。上述研究提示,猫眼草黄素有可能成为靶向RANKL信号通路的新型药物,其对各种类型骨质疏松症的作用及分子调控机制还有待进一步研究。
自噬是细胞在外界环境因素的影响下,利用溶酶体降解自身衰老、变性或受损的大分子物质及细胞器的过程,在真核细胞内调节细胞的代谢中起重要作用[20-21]。研究表明,自噬功能紊乱会导致肿瘤[22]、心脏病[23]、神经退行性疾病及免疫失调等重大疾病[24]。目前越来越多文献表明,自噬参与调控骨髓间充质干细胞、成骨细胞的增殖及破骨细胞的分化与活性的变化等,对于维持骨稳态至关重要[25]。提示自噬有可能是骨代谢疾病的发病机制之一。研究发现,部分黄酮类化合物能通过调控自噬来调控细胞分化与功能,如山柰酚通过降解p62/SQSTM1抑制破骨细胞分化[26];葛根素能抑制破骨细胞的自噬和增殖,自噬相关基因ATG5、ATG7和Beclin1的过度表达能逆转葛根素抑制破骨细胞的自噬和增殖[27]。自噬在破骨细胞分化、成熟及骨吸收的过程中扮演重要角色,与自噬相关的蛋白(如ATG5、ATG7、ATG4B、ATG12和LC3等)[28]在破骨细胞形成与骨吸收过程中发挥重要的作用,其中LC3Ⅱ是LC3Ⅰ的脂化形式,其依赖泛素蛋白酶复合体定位于吞噬泡膜上,参与自噬溶酶体形成,常被用作自噬形成的标志物[29]。本研究结果显示,猫眼草黄素在干预破骨细胞过程中对自噬相关蛋白ATG5表达的影响不明显,但能抑制破骨细胞内的自噬相关蛋白LC3表达,且破骨细胞分化时间越长,其抑制自噬的能力越明显。提示猫眼草黄素可能通过自噬途径抑制破骨细胞分化。
综上所述,猫眼草黄素对破骨细胞的分化有抑制作用,且呈剂量依赖性,其可能通过自噬途径发挥抑制作用。本研究为猫眼草黄素对骨质疏松的治疗提供了研究基础及新方向,但具体的作用机制还有待进一步研究。