黄芩苷镁盐对CCl4诱导SD大鼠急性肝损伤保护机制
2022-05-13王朔李卫白冰黄群薛润国邢恩鸿郭亚春宋鸿儒
王朔 李卫 白冰 黄群 薛润国 邢恩鸿 郭亚春 宋鸿儒
(1承德医学院,河北 承德 067000;2承德监狱医院;3承德市第一中心医院;4承德医学院附属医院;5河北北方学院)
急性肝损伤极有可能最终发展为肝衰竭。急性肝衰竭病势急、并发症多、难治愈、预后差。目前针对急性肝损伤的有效治疗方法十分有限,寻找开发新的治疗药物及治疗措施,深入研究和探讨急性肝损伤的发病机制意义重大。本实验采用四氯化碳(CCl4)制备大鼠急性肝损伤模型。CCl4 有肝脏毒性且导致急性肝损伤的机制复杂,研究表明与氧化应激有关〔1〕。氧化应激是由于机体受到活性氧(ROS)等其他有害刺激后体内活性氧自由基异常,引起机体过氧化损伤,进而激活了抗氧化损伤防御机制,来维系机体氧化还原的平衡。生理自稳状态下核转录因子(NF)-E2相关因子(Nrf)2 表达水平较低;当机体受到氧刺激后,Nrf2活化入核与抗氧化反应元件(ARE)结合并启动下游由ARE调控的一系列蛋白基因的表达,进而引发抗氧化应激损伤的作用〔2〕。黄芩苷能抗氧化,在一定程度上能保护大鼠免受CCl4造成急性肝损伤〔3〕,但其水溶性差,黄芩苷镁盐吸收更好,且前期实验已证明黄芩苷镁盐对CCl4诱导的SD大鼠急性肝损伤有保护作用〔4〕。本研究继续采用CCl4诱导的急性肝损伤大鼠为研究对象,通过检测Nrf2/ARE信号通路中相关蛋白的变化来探讨黄芩苷镁盐对CCl4诱导急性肝损伤大鼠保护作用机制。
1 材料和方法
1.1实验动物 50只SPF级雄性SD大鼠,150~170 g,购于北京维通利华实验动物技术有限公司,许可证号:SCXK(京)2016-0011。先将所有大鼠在SPF级屏障动物室适应性饲养1 w,自由饮水,室内温度18~22℃,保持室内湿度50%~60%,每日光照12 h。
1.2实验仪器与试剂 -80℃低温冰箱(美国Thermo公司);磁力搅拌器(中国江苏波西瓦尔公司);MyCycler Thermal Cycler(美国BIO-RAD公司);低温高速离心机(丹麦Labogene公司);LightCycler® 96(瑞士Roche公司);GelDoc凝胶成像仪(美国BIO-RAD公司);化学发光图像分析系统(中国上海Tanon 公司)。冻存样本核蛋白提取试剂盒(河北贝博实验用品有限公司);CCl4(国药集团化学试剂有限公司);异甘草酸镁注射液(正大天晴药业集团股份有限公司);注射用还原型谷胱甘肽(上海复旦复华药业有限公司);二喹啉甲酸(BCA)蛋白浓度测定试剂盒(美国Thermo公司);醌氧化还原酶(NQO)1 antibody(美国CST公司);LaminB1 antibody、BeyoECL Star(中国碧云天公司);anti-Nrf2 antibody、anti-Heme Oxygenase 1 antibody(英国Abcam公司);PrimeScript RT reagent kit with gDNA Eraser 试剂盒、引物、SYBY Premix Ex Taq TM Ⅱ试剂盒(中国大连宝生物公司);黄芩苷镁盐(我校刘翠哲教授课题组提供,其纯度为93.1%。)。
1.3方法
1.3.1实验动物分组与造模 雄性SD大鼠50只,体重150~170 g,随机分为5组:空白对照组、模型组、异甘草酸镁组、还原型谷胱甘肽组及黄芩苷镁盐组,每组10只。空白对照组与模型组每天尾静脉注射等体积的无菌生理盐水;异甘草酸镁组每天尾静脉注射异甘草酸镁18 mg/kg;还原型谷胱甘肽组每天尾静脉注射还原型谷胱甘肽150 mg/kg;黄芩苷镁盐组按照100 mg/kg尾静脉注射黄芩苷镁盐,每日1次,连续给药1 w。末次给药2 h后,各药物组按1 ml/kg腹腔注射50%的CCl4溶液,空白对照组腹腔注射等体积的橄榄油溶液。禁食,自由饮水,24 h后用4%水合氯醛麻醉解剖大鼠,腹主动脉取血后迅速摘除肝脏,用预冷的生理盐水清洁后于-80℃保存,用于后续的Western印迹和实时荧光定量-聚合酶链反应(PCR),以检测各组Nrf2、NQO1 和血红素氧合酶(HO)-1的蛋白和mRNA 表达水平。
1.3.2Western印迹 -80℃冰箱取出肝组织样本,眼科剪碎于研钵,随后加入蛋白裂解液冰上研磨,裂解反应45 min,收集匀浆液至EP管中,置于4℃离心机进行离心(12 000 r/min离心15 min),转移上清至另一EP管,再次离心(12 000 r/min,15 min,4℃),收集上清液并分装,置于-80℃冰箱保存。随后加入100 ml提前预冷的缓冲液在离心沉淀物中,涡旋振荡15 s冰上静置10 min,反复4次(冰上反应共40 min);静置结束后离心(16 000 r/min,10 min,4℃),再将上清液移至另一预冷的无菌EP管中,最终得到的上清即为核蛋白。严格按照BCA定量试剂盒说明书进行蛋白定量,蛋白样品与上样缓冲液混匀后于100℃水浴锅中变性5 min,配制10%分离胶和5%浓缩胶,上样量为30 μg,80 V/30 min,120 V/1.5 h进行电泳。按照2 mA/cm2膜,恒流转膜2 h。完成转膜后将聚偏氟乙烯(PVDF)膜在含5% 脱脂奶粉的封闭液中封闭1 h,洗膜,加入稀释好的一抗溶液(量根据膜面积以0.1 ml/cm2计算),于摇床上室温孵育1~2 h或4℃过夜。TBST洗膜4次,每次7 min。加二抗,摇床上室温孵育1~2 h。ECL试剂盒显影,图像用Quantity one软件分析,LaminB进行数据校正。
1.3.3实时荧光定量PCR 常规提取肝组织中的总RNA,按照试剂盒要求逆转录为cDNA,Nrf2、HO-1、NQO1及内参 GAPDH的引物分别为Nrf2:上游引物:5′-GACCTAAAGCACAGCCAACACAT-3′,下游引物:5′-CTCAATCGGCTTGAATGTTTGTC-3′;HO-1:上游引物:5′-TGTCCCAGGATTTGTCCGAG-3′,下游引物:5′-ACTGGGTTCTGCTTGTTTCGCT-3′;NQO1:上游引物:5′-GGGGACATGAACGTCATTC-TCT-3′,下游引物:5′-AGTGGTGACTCCTCCCAGACAG-3′;GAPDH:上游引物:5′-GCACCGTCAAGGCTGAGAAC-3′,下游引物:5′-TGGTGAAGACGCCAGTGGA-3′。按照试剂盒说明书进行PCR,利用 2-ΔΔCt法对基因表达进行相对定量分析。
1.4统计学方法 采用SPSS22.0软件进行单因素方差分析、t检验。
2 结 果
2.1Western印迹检测Nrf2、NQO1和HO-1蛋白表达 与空白对照组比较,其余各组Nrf2蛋白水平均显著升高,异甘草酸镁组、还原型谷胱甘肽组、黄岑甘镁盐组HO-1、NQO1蛋白水平均显著升高(均P<0.05);与模型组比较,异甘草酸镁组、还原型谷胱甘肽组、黄岑甘镁盐组Nrf2、HO-1、NQO1蛋白水平均显著升高(均P<0.05)。见图1、表1。
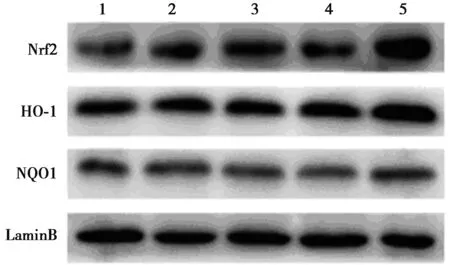
1~5:空白对照组,模型组,异苷草酸镁组,还原型谷胱甘肽组,黄芩苷镁盐组图1 Western印迹检测各组Nrf2、HO-1、NQO1表达

表1 各组Nrf2、HO-1、NQO1蛋白水平比较
2.2各组Nrf2、HO-1、NQO1 mRNA水平比较 与空白对照组比较,其余各组Nrf2 mRNA水平均显著升高,异甘草酸镁组、还原型谷胱甘肽组、黄岑甘镁盐组HO-1、NQO1 mRNA水平均显著升高(均P<0.05);与模型组比较,异甘草酸镁组、还原型谷胱甘肽组、黄岑甘镁盐组Nrf2、HO-1、NQO1 mRNA水平均显著升高(均P<0.05)。见表2。

表2 各组Nrf2、HO-1、NQO1 mRNA水平比较
3 讨 论
研究发现,梨头草提取物、青蒿琥酯、鬼针草水提物、雷公藤总苷、青藤碱等能通过缓解氧化应激和炎症反应对CCl4诱导的急性肝损伤起到保护作用〔5~8〕。机体受到氧化应激刺激后,体内多种信号通路被激活,通过多种途径介导肝细胞损伤。Nrf2/ARE信号通路可以通过调控Ⅱ相解毒酶及抗氧化物基因的表达来调控肝脏新陈代谢促进毒物外排起到抗氧化作用,同时还可以促进肝细胞再生,从而保护肝脏〔9~11〕。
在肝、肾等解毒器官中高表达的Nrf2是调控抗氧化重要转录因子〔12〕。胞质内Kelch 样环氧氯丙烷相关蛋白(Keap)1是Nrf2的特异性受体。生理自稳状态下,Nrf2位于细胞质中与Keap1耦联,其活性被抑制,同时通过Keap1 介导的泛素化对Nrf2进行持续降解以维持与转录形成的Nrf2之间的平衡〔13〕。当机体受到氧化应激刺激后,Keap1介导的泛素化被阻止,同时Keap1 的构像发生改变,使Nrf2 与Keapl 发生解耦联,Nrf2 从胞质转位至细胞核并与下游的目的基因ARE 结合,从而启动下游多个抗炎、抗氧化蛋白及解毒酶等基因的表达,进而激活Nrf2 信号通路,发挥抗氧化作用,促进机体毒物的外排〔14〕。有研究表明敲除Nrf2基因的小鼠,肝脏中丙二醛(MDA)水平会显著升高,小鼠会表现出严重的肝损伤。相反激活Nrf2及其下游基因HO-1表达,可降低体内MDA和ROS水平,减轻过氧化反应所引起的肝损伤〔15〕。
传统医学用黄芩治疗湿热黄疸等肝胆病,黄芩苷镁盐是其有效成分黄芩苷在药材中的存在形式,研究证明黄芩苷能抗氧化,对CCl4致大鼠肝损伤有保护作用〔3〕,且黄芩苷镁盐水溶性好,比黄芩苷更容易被吸收。本研究结果表明黄芩苷镁盐能够显著促进Nrf2蛋白的活化及核内基因的表达,Nrf2活化后入核与ARE结合,激活Nrf2/ARE信号通路,启动下游HO-1和NQO1基因表达,促进HO-1和NQO1蛋白合成。本研究结果说明黄芩苷镁盐在CCl4诱导大鼠的急性肝损伤模型体内,能够调控Nrf2/ARE信号通路。还原型谷胱甘肽具有较强清除自由基、抑制胞膜脂质过氧化作用,本研究结果说明GSH能够通过调节氧化系统和抗氧化系统平衡,对CCl4诱导的肝细胞损伤起到保护作用。黄芩苷镁盐对CCl4诱导的急性肝损伤保护作用机制可能与Nrf2/ARE信号通路被激活有关,通过上调下游HO-1和NQO1 mRNA及蛋白的表达水平,进而发挥抗氧化作用,降低肝组织中MDA水平,促进机体毒物外排,从而减轻CCl4对肝脏的损伤程度。
此外,本研究还发现单独给予CCl4造模也可提高Nrf2的核内表达,这可能是由于外界刺激,肝细胞防御性应激反应所导致的。但急性肝损伤的发生发展是一个及其复杂的过程,多种机制参与,黄芩苷镁盐对急性肝损伤的保护作用,可能还会通过其他的途径进行调控,有待日后进一步研究。
