高铁酸钠合成工艺及其在印染废水处理应用研究*
2022-05-11徐婉莹张文雅赵业军
张 颖,何 雪,徐婉莹,张文雅,赵业军
(武汉东湖学院 生命科学与化学学院,湖北 武汉 430212)
具有最高价态+6价铁的含氧酸盐,即高铁酸盐是一种集氧化、絮凝、杀菌、吸附、助凝、除臭为一体的新型高效多功能水处理剂[1-3],其还原产物对环境也不存在二次污染;作为处理剂和净水剂,高铁酸盐表现出优异的氧化、吸附和絮凝去除污染的协同功能,以及比氯系氧化剂更强的杀菌消毒能力[4,5]。本文采用钛白副产FeSO4精制后的溶液直接合成Na2FeO4,与普通的FeSO4净化工艺相比,减少了FeSO4结晶的步骤,不仅简化工艺流程,而且提高原料的利用率。研究采用钛白副产FeSO4精制后的溶液直接合成Na2FeO4的优化条件,探讨Na2FeO4对于模拟碱性印染废水甲基橙溶液处理的效果。
1 实验部分
1.1 仪器与试剂
I3型紫外-可见分光光度计(济南淘能仪器);TDZ5-WS型高速离心机(湖南湘仪)。
FeSO4(工业级武汉方圆钛白,其中FeSO4·7H2O含量84.0%~87.0%,Ti含量0.3%~0.4%);H2SO4(开封东大),聚丙烯酰胺、甲基橙(国药集团);还原铁粉(上海展云),NaClO(武汉欣申),H2O2、NaOH(天津市凯通),以上试剂均为分析纯。
1.2 FeSO4的提纯
称取适量的工业FeSO4加入H2SO4调节溶液的pH值为2.8,加入适量还原铁粉,恒温70~90℃反应1h,趁热抽滤。滤液中加入5mL BaCl2溶液,微沸0.5h,趁热抽滤后加入少量聚丙烯酰胺,缓慢搅拌10min。趁热抽滤,滤液为提纯后的FeSO4溶液。
1.3 Na2FeO4的制备
移取60mL NaClO溶液与NaOH固体混合均匀,冷却至室温。取上一步精制的FeSO4溶液加入H2O2,混合均匀后加入NaClO和NaOH混合溶液,搅拌反应一定时间后离心,取上层紫红色清液,即为Na2FeO4溶液。
1.4 Na2FeO4处理印染废水
实验水样标准曲线由甲基橙稀释不同倍数制得。分别移取定量实验最佳条件制备的Na2FeO4液体,置于50mL的容量瓶中,处理时间为最适时间,选用最适pH值处理,测定经Na2FeO4处理后模拟印染废水甲基橙溶液的降解率。
2 结果与讨论
2.1 FeSO4溶液精制工艺的对比
称取适量的工业FeSO4加入H2SO4调节溶液的pH值为2.8,加入适量还原铁粉,恒温70~90℃反应1h,趁热抽滤。滤液采用以下4种不同工艺进行净化处理:(1)同时加入BaSO4、BaCl2和聚丙烯酰胺;(2)加入聚丙烯酰胺絮凝,H2O2氧化;(3)加入BaSO4、BaCl2同时处理FeSO4;(4)同时加入BaCl2和聚丙烯酰胺;微沸0.5h。趁热抽滤,滤液为提纯后的FeSO4溶液。结果见表1。
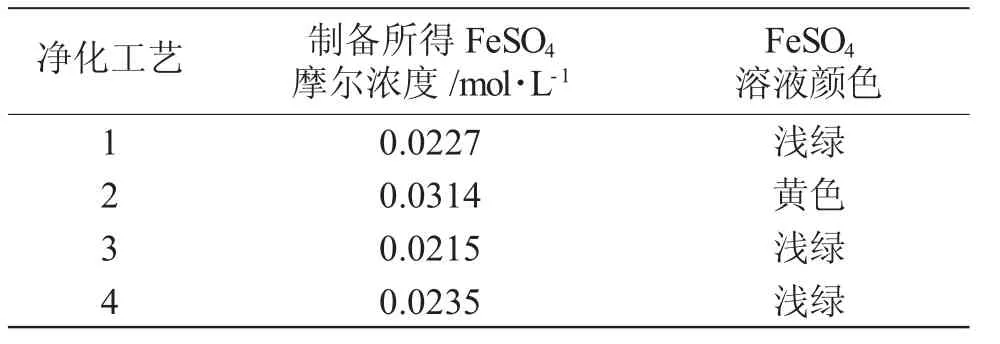
表1 FeSO4溶液制备方案对比Tab.1 Comparison of schemes for preparing ferrous sulfate solution
工艺(2)虽然FeSO4浓度最高,但其颜色为黄色,说明溶液中Fe3+含量高,不符合FeSO4精制的目标;其余3种工艺颜色符合要求,第4种工艺浓度相对较高,故选用第4种工艺。
2.2 Na2FeO4的制备
2.2.1 FeSO4用量对Na2FeO4吸光度的影响 在400~600nm波长范围内对Na2FeO4进行光谱扫描,测得Na2FeO4最大吸收波长为505nm。反应温度45℃、反应时间60min,在一定量的NaClO溶液中加入NaOH 30g、改变FeSO4溶液的加入量。将不同条件下制备的Na2FeO4使用紫外-可见分光光度计于505nm处测定其吸光度值,结果见图1。
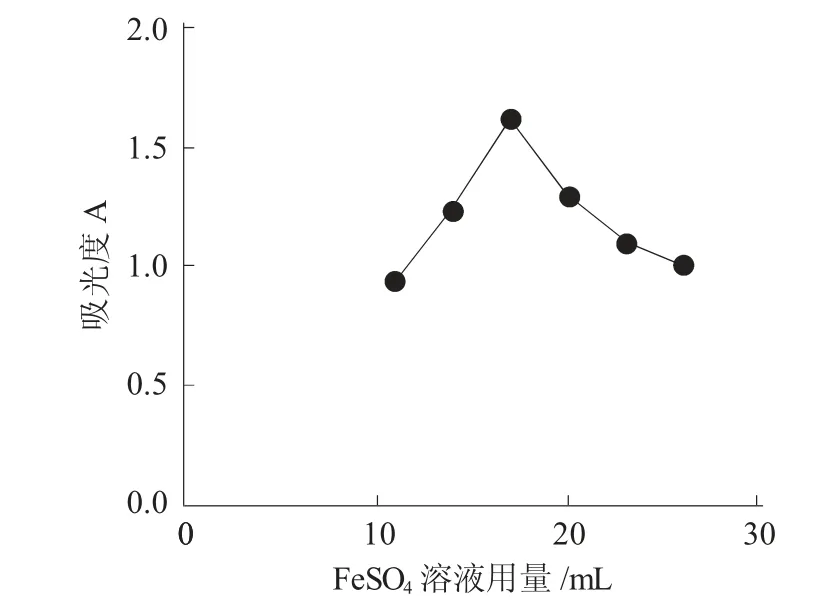
图1 FeSO4用量的影响Fig.1 Influence of dosage of ferrous sulfate
由图1可知,FeSO4的最佳用量为17mL。
2.2.2 NaOH用量对Na2FeO4吸光度的影响 反应温度45℃、反应时间60min,在一定量的NaClO溶液中加入17mL FeSO4溶液,改变NaOH的加入量。实验结果见图2。
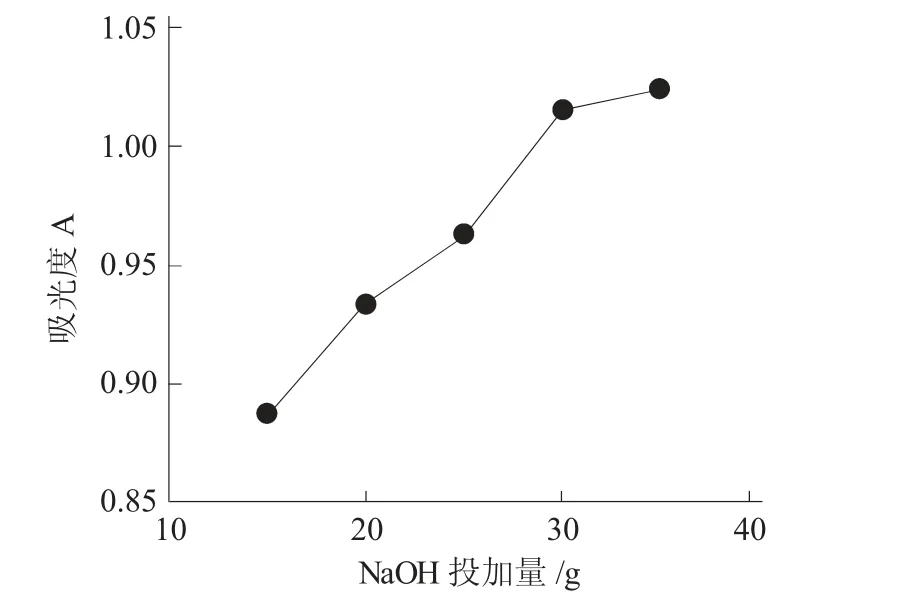
图2 NaOH用量的影响Fig.2 Influence of dosage of sodium hydroxide
由图2可知,当NaOH用量较少时,Na2FeO4的吸光度随着NaOH投加量的增加而升高,但其变化较小;随着NaOH用量继续增加,Na2FeO4的吸光度开始有明显变化;但当NaOH投加量超过30g后,Na2FeO4的吸光度波动不大,并且过多的NaOH会放热致使Na2FeO4分解。综合以上因素,NaOH用量以30g为宜。
2.3 反应时间对Na2FeO4吸光度的影响
在FeSO4溶液为17mL时,NaOH 30g、反应温度45℃条件下,分别测定反应20、40、60、80、100min后的Na2FeO4吸光度。结果见图3,反应最适时间为60min。
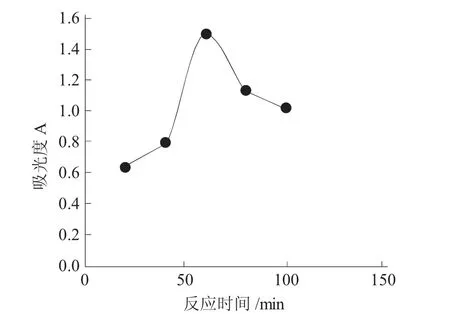
图3 反应时间的影响Fig.3 Effect of reaction time
综上所述,制备Na2FeO4的最佳条件为:在NaClO体积为60mL时,FeSO4溶液为17mL,NaOH 30g,45℃反应60min,Na2FeO4溶液含量最高。
2.4 Na2FeO4处理碱性印染废水的探讨
2.4.1 Na2FeO4用量的影响 取一定量碱性的甲基橙溶液,加入上一步制备的Na2FeO4溶液进行混合,反应3h,离心,取上清液测定吸光度得出去除率。图4为Na2FeO4溶液的用量影响。

图4 Na2FeO4溶液的用量影响Fig.4 Influence of dosage of sodium
由图4可知,Na2FeO4最适用量为10mL。
2.4.2 pH值的影响 取一定量的甲基橙溶液配置成pH值分别为7、8、9、10、11、12、13的溶液,加入上一步制备的Na2FeO4溶液进行混合,反应3h,离心,取上清液测定吸光度得出去除率。图5为甲基橙溶液pH值的影响。
由图5可知,适宜的印染废水pH值为12。
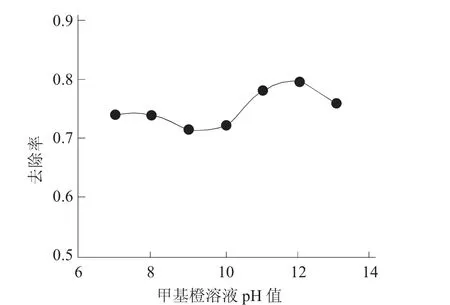
图5 甲基橙溶液pH值的影响Fig.5 Effect of pH of methyl orange solution
2.4.3 反应时间的影响 取一定量的甲基橙溶液,加入上一步制备的Na2FeO4溶液,反应不同时间,离心。取上清液测定吸光度得出降解率。图6为反应时间的影响。

图6 反应时间的影响Fig.6 Effect of reaction time
由图6可知,综合考虑最适的处理时间为3h。
综上所述,能达到最佳处理模拟印染废水甲基橙溶液的条件为:Na2FeO4用量10mL、甲基橙溶液pH值为12、反应时间3h,甲基橙去除率达到72.5%。
3 结论
本文采用钛白副产FeSO4精制后的溶液直接合成Na2FeO4,与普通的FeSO4净化工艺相比,减少了FeSO4结晶的步骤,不仅简化工艺流程,而且提高原料的利用率。
FeSO4净化后制备Na2FeO4的优化条件为:在NaClO体积为60mL时,FeSO4溶液为17mL,NaOH 30g,45℃反应60min,Na2FeO4溶液含量最高。加入制备的Na2FeO410mL,在pH值为12时,处理时间3h为最佳处理时间,经过处理后的模拟印染废水甲基橙溶液去除率达到72.5%。