不同频率电针对AD模型大鼠干预及对NMDAR亚基基因表达的影响
2022-05-11王飞高珊汪伯毅胡剑明沈峰
王飞 高珊 汪伯毅 胡剑明 沈峰
(1武汉市第一医院针灸科,湖北 武汉 430022;2湖北中医药大学针灸骨伤学院;3武汉市第一医院中医部)
阿尔茨海默病(AD)导致患者认知、行为异常,在老年患者中发病率较高,患者主要临床表现为记忆力减退,认知困难,患者时间、空间定向能力部分丧失,性格寡僻冷漠,精神行为异常〔1〕。针灸治疗AD效果显著,作用机制是降低脑β-淀粉样蛋白(Aβ)表达,抑制神经元、突触细胞凋亡,有助于脑源性神经营养因子分泌,对神经元、突触损伤有一定的修复作用〔2,3〕。N-甲基-D-天冬氨酸受体(NMDAR)属于一种兴奋性氨基酸受体,有研究证实,NMDAR在学习、记忆过程中发挥着重要作用〔4〕。本文旨在研究不同频率电针对AD模型大鼠的干预效果及对NMDAR亚基基因表达的影响。
1 材料与方法
1.1实验动物 选取雄性Wistar大鼠40只,4~5月龄,平均体重350~400 g,均由湖北省实验动物研究中心提供,许可证号:SCXK(鄂)2008-0005。所有大鼠在温度(22±2)℃,湿度55%环境中喂养1 w。
1.2方法
1.2.1模型建立 40只大鼠称重后使用10%水合氯醛注射,对大鼠给予腹腔麻醉,大鼠脑立体定位仪固定后,根据《大鼠脑立体定位图谱》确定大鼠海马区齿状回,原点为前囟,向后移动距离3.2 mm,中线旁开距离2.5 mm,向下深度3.5 mm,在大鼠颅骨上使用牙科钻进行钻孔〔5〕。使用磷酸盐缓冲液配置Aβ1~42溶液,浓度为1 μg/μl,在37℃中孵育1 w形成寡聚肽,使用5 μl微量注射器将Aβ1~42溶液注射至大鼠海马齿状回,分别在双侧注射5 μl溶液,速度为1 μl/min,在5 min内注射完成,留针5 min促进药物充分吸收,使用牙托粉将颅骨钻孔封闭,皮肤缝合后,使用碘酒消毒。假手术组10只大鼠,在大鼠双侧齿状回区注入5 μl 0.9%无菌生理盐水,其他与上述模型建立一致。所有建模成功的大鼠腹腔注射4×104U青霉素,连续注射3 d,避免感染发生。
1.2.2电针干预 模型组、2 Hz组、50 Hz组、假手术组,各10只。建模成功15 d后,对大鼠进行干预,选择大鼠百会穴、肾俞穴进行针刺:使用鼠套将大鼠固定,百会穴进针方式为针尖向前平刺,针刺角度保持15°,距离5 mm;肾俞穴进针方式为稍向内斜刺,针刺角度保持45°,距离5 mm。采用韩式电针仪(设置参数:连续波型,电流为1 mA)导线连接大鼠百会穴、肾俞穴,左右侧肾俞穴需要每天交替使用〔6〕。1次/d,7 d为1个疗程,连续治疗2个疗程。2 Hz组电针频率为2 Hz,50 Hz组电针频率为50 Hz。模型组和假手术组不做处理。
1.2.3行为学相关指标 采用WMT-100S水迷宫视频分析系统,进行定位航行实验:平台确定在第3象限中间,离水面距离1 cm,大鼠面向池壁从四个象限分别各放入水1次,统计大鼠隐藏到水面以下平台时间,时间在120 s内,即为逃避潜伏期。空间探索实验:将平台去除后,从原平台象限对侧象限将大鼠放入水中,观察大鼠游泳轨迹,时间在120 s内,记录大鼠在平台象限中逗留时间、跨越平台象限次数。
1.2.4海马区突触数目检测 大鼠断头处死后将颅骨快速剥离后,取出大鼠海马组织大小为1 mm3,放在2.5%的戊二醛固定液中固定保存,制作切片,环氧树脂包埋,染色后,透射电子显微镜下(日立HT7700)统计突触计数。
1.2.5Western印迹 将采集到的标本10 000 r/min离心10 min,取出上清液,采用二喹啉甲酸(BCA)蛋白浓度测定试剂盒检测蛋白定量,将50 μg蛋白加入到2×十二烷基硫酸钠(SDS)凝胶加样缓冲液中,100℃加热处理5 min促使蛋白变性。SDS-聚丙烯酰胺凝胶电泳(PAGE)完成后进行转膜,结束后取下硝酸纤维素膜,在5%脱脂牛奶中4℃下封闭1 h,封闭结束后,加一抗使用0.05%~0.10% TBST给予稀释〔突触素(SYN)、突触后致密蛋白(PSD)-95、β淀粉样前体蛋白(APP)、Aβ1~40、Aβ25~35一抗为1∶1 000〕,4℃孵育过夜保存,之后使用0.05%~0.10% TBST洗膜,3次,每次为5 min,加二抗使用0.05%~0.10% TBST给予稀释(1∶10 000),室温摇动孵育1 h,最后使用0.05%~0.10% TBST洗膜,3次,每次5 min。采用二氨基联苯胺(DAB)染色试剂盒显色,光密度扫描后进行定量分析。以GAPDH为内参。
1.2.6NR1、NR2A、NR2B mRNA表达检测 采用荧光定量检测NR1、NR2A、NR2B基因表达,将采集到的标本,置于一次性真空无抗凝剂的采血管中,使用聚蔗糖(Ficoll)液分离单个核细胞。Trizol提取细胞RNA,经过电泳检测RNA并定量,经过逆转录合成cDNA。之后进行实时荧光定量聚合酶链反应(PCR),探针或SYBR 反应25 μl,反应条件:94℃ 5 min,94℃ 45 s,60℃ 1 min,40个循环,设置标准组和空白对照。将PCR实验前3~15个循环荧光信号作为荧光本底信号,调节基线,采用2-△△Ct分析NR1、NR2A、NR2B mRNA基因表达。
1.3统计学处理 采用SPSS20.0软件进行方差分析、t检验。
2 结 果
2.1不同频率电针对大鼠行为学相关指标的影响 与模型组相比,其余3组平均逃避潜伏期、首次跨越平台时间显著减少,跨越平台次数显著增加(P<0.05)。与假手术组相比,2 Hz组、50 Hz组平均逃避潜伏期、首次跨越平台时间显著增加,跨越平台次数显著减少(P<0.05)。50 Hz组平均逃避潜伏期、首次跨越平台时间显著低于2 Hz组,跨越平台次数显著高于2 Hz组(P<0.05)。见表1。
2.2不同频率电针对大鼠海马区突触数目的影响 与模型组相比,其余3组海马区突触数目均显著增加(P<0.05)。与假手术组相比,2 Hz组、50 Hz组海马区突触数目均显著降低(P<0.05)。50 Hz组海马区突触数目显著高于2 Hz组(P<0.05)。见表1。
2.3不同频率电针对大鼠海马区SYN、PSD-95表达的影响 与模型组相比,其余3组SYN、PSD-95表达均显著增加(P<0.05)。与假手术组相比,2 Hz组、50 Hz组SYN、PSD-95表达均显著降低(P<0.05)。50 Hz组SYN、PSD-95表达显著高于2 Hz组(P<0.05)。见表1、图1。

表1 各组行为学相关指标、海马区突触数目、SYN、PSD-95水平比较
2.4不同频率电针对大鼠海马区NR1、NR2A、NR2B mRNA的影响 与模型组相比,其余3组NR1、NR2A、NR2B基因表达显著升高(P<0.05)。与假手术组相比,2 Hz组、50 Hz组NR1、NR2A、NR2B基因表达显著降低(P<0.05)。50 Hz组NR1、NR2A、NR2B基因表达显著高于2 Hz组(P<0.05)。见表2。
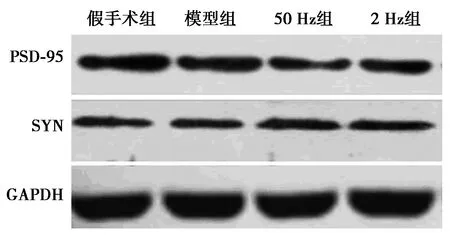
图1 Western印迹检测SYN、PSD-95水平

表2 各组NR1、NR2A、NR2B mRNA影响
2.5不同频率电针对大鼠海马区APP、Aβ1~40、Aβ25~35蛋白的影响 与模型组相比,其余3组APP、Aβ1~40、Aβ25~35蛋白显著降低(P<0.05)。与假手术组相比,2 Hz组、50 Hz组APP、Aβ1~40、Aβ25~35蛋白显著升高(P<0.05)。50 Hz组APP、Aβ1~40、Aβ25~35蛋白显著低于2 Hz组(P<0.05)。见图2、表3。
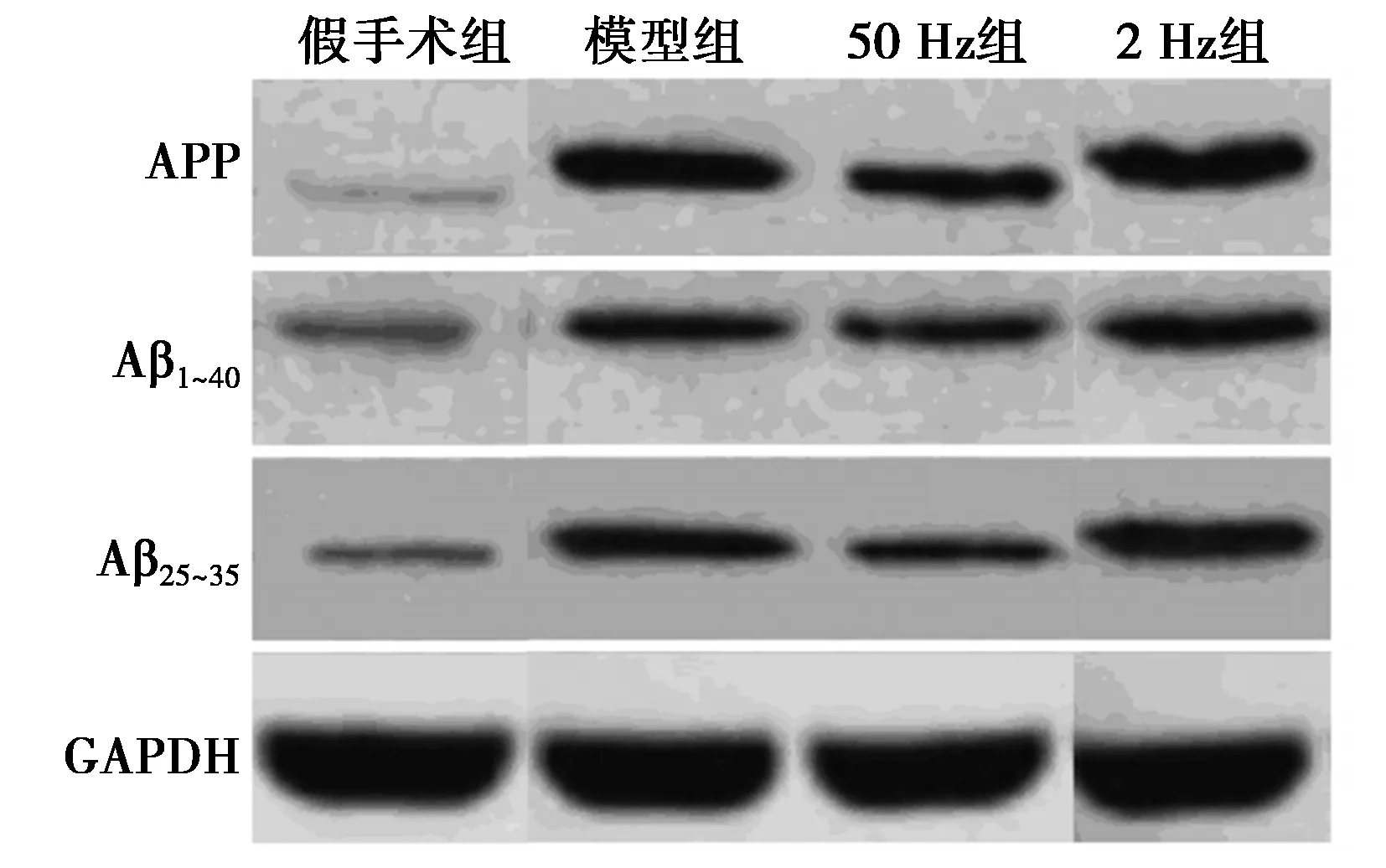
图2 Western印迹检测APP、Aβ1~40、Aβ25~35蛋白表达

表3 各组APP、Aβ1~40、Aβ25~35蛋白表达比较
3 讨 论
AD主要的病理变化是由于Aβ累积引起老年斑发生,细胞内的Tau蛋白因为过度磷酸化导致神经纤维缠结,弥漫性神经元发生变性、缺失,严重会造成全脑萎缩〔7,8〕。我国人口老龄化现象越来越明显,并且随着患者年龄增加,AD发病率也随之升高〔9〕。
本研究结果说明50 Hz电针能有效改善大鼠学习记忆障碍,提高大鼠学习记忆能力。与沈晓艳等〔10〕研究结果保持一致。研究指出,AD发病及发展受突触丢失的影响,突触损伤是AD最早出现的病理变化,当AD发病时,突触退行性变快速恶化,主要分布在海马以及所有的皮质中〔11,12〕。本研究结果说明50 Hz电针对AD大鼠突触影响效果最明显。
SYN是一种与突触可塑性密切相关的蛋白,也是电针治疗脑病的重要标志物〔13〕。PSD-95与突触后可塑性具有相关作用〔14〕。本研究结果提示电针能提高大鼠学习记忆能力,其中50 Hz电针作用效果最强,调控SYN、PSD-95水平上调,有助于突触结构和功能重塑,起到改善AD学习障碍。NMDAR参与中枢神经系统发育及发展过程,NMDAR主要包括NR1、NR2亚基等类型,对钙离子具有较高的通透性,其中NR1作为基本亚基是构成离子通道的重要组成,NR2能有效提高NR1对兴奋性氨基酸作用〔15,16〕。NMDAR主要存在于海马区、大脑皮层、下丘脑等,参与中枢神经系统可塑性发育过程。Wang等〔17〕研究指出,NMDAR激动剂在维持、增加学习记忆发挥着重要作用。
APP来源于淀粉样前体蛋白,正常情况下对细胞无影响,在多种组织中均有表达,尤其是在脑、肾、心肌等组织中表达水平相对较高。Kumar等〔18〕研究指出,APP对神经元可塑性具有一定抗炎作用,在蛋白质裂解酶作用下形成Aβ,从而破坏细胞。APP通过γ酶异常切割,形成Aβ1~40、Aβ25~35蛋白,是淀粉样斑主要有效成分,会提高毒性,损伤神经元,Aβ沉积是AD发病的主要原因〔19〕。本研究结果提示50 Hz频率电针对AD模型大鼠干预效果最为显著,避免Aβ过度累积,降低神经毒性作用。与刘若兰等〔20〕研究结果保持一致。
