基于镍基碱式碳酸盐修饰电极的无酶葡萄糖电化学传感器构建
2022-05-09张智锋王松磊李海峰李恳恳魏培媛武康宁
刘 丽,张智锋,王松磊,*,李海峰,李恳恳,马 亮,魏培媛,张 也,武康宁
(1.宁夏大学食品与葡萄酒学院,宁夏 银川 750021;2.华中农业大学食品科学技术学院,湖北 武汉 430000;3.宁夏华信达健康科技有限公司,宁夏 灵武 751400)
目前,葡萄糖含量已经成为饮料产品的一项重要指标,然而不同人群对葡萄糖的摄入量要求不同[1-2]。当人体出现低血糖时,可以适量摄入葡萄糖含量较高的饮品,以满足机体的需求,但当人体处于正常生理状态时,如果在短时间内摄入过多的葡萄糖,可能会对人体产生一些不良的后果,特别是患有糖尿病或肥胖症的病人,后果则会非常的严重。因此,为了满足不同人群对葡萄糖的需求,对饮料中葡萄糖含量的监测评估十分必要。
目前,许多技术已用于食品中葡萄糖含量的检测,如比色法[3]、荧光法[4-5]、色谱分析法[6-7]、质谱法[8]、毛细管电泳法[9]和电化学方法[10-12]等,前几种方法有其自身的优点,但也有设备昂贵、操作复杂等不足,使其在实际应用中受到一定程度的限制。电化学方法因高灵敏度、低成本、高选择性而广泛的用于电催化氧化葡萄糖,电化学葡萄糖传感器根据有无酶的参与可分为酶基传感器和无酶传感器[13-15],酶基传感器由于制备工艺复杂、成本高和稳定性差而阻碍了其进一步的发展[16]。相比之下,稳定、低成本且高灵敏度的无酶葡萄糖传感器引起了广大研究人员的关注[17]。近年来,过渡金属氧化物和氢氧化物被认为是构建无酶葡萄糖传感器的有效材料[18-20],特别是极具前景的金属镍,由于其具有数量多、低毒性和高的电催化氧化葡萄糖活性的优点,被广泛用于构建无酶葡萄糖传感器[21-23]。此外,利用碳基材料作为过渡金属纳米颗粒的基底可以有效改善电子传导速率并增加活性位点的暴露数量。
本实验通过一步水热法制备了Ni2(CO3)(OH)2纳米材料并将其原位生长于碳纸上,构建无酶葡萄糖传感器。以期成功用于2 款市售饮料中葡萄糖的检测,为饮料中葡萄糖的检测提供新思路。
1 材料与方法
1.1 材料与试剂
凉茶、功能饮料 市购。
碳纸 苏州晟尔诺科技有限公司;硝酸镍(Ni(NO3)2g6H2O)、葡萄糖、无水乙醇、乙二醇、丙酮 国药集团化学试剂有限公司;果糖、柠檬酸、乳糖、蔗糖、尿素、氢氧化钠、抗坏血酸 上海瑞安有限公司;实验中所用试剂均为分析纯,实验用水均为去离子水。
1.2 仪器与设备
CHI-660E电化学工作站 上海辰华仪器有限公司;SQP分析天平 赛多列斯科学仪器有限公司;FCH-202数显加热磁力搅拌器 上海弗鲁克有限公司;TGL-16M高速离心机 上海卢湘仪离心机仪器有限公司;DHG-9036A电热恒温鼓风干燥箱、DZF-6020真空干燥箱上海精宏有限公司;JP-040ST超声波清洗器 深圳市浩盟牌清洗设备有限公司;FYF01水热反应釜 艾析五金专营店;Smart Lab X射线衍射仪、SU4800场发射扫描电子显微镜 日本日立公司。
1.3 方法
1.3.1 工作电极的制备
碳纸预处理:将整张一页纸大小的碳纸裁剪成2 cmh3 cm,分别用丙酮、无水乙醇和去离子水对碳纸进行超声清洗20 min,然后在60 ℃真空干燥箱中烘干,备用。
用分析天平准确称取1.163 2 g硝酸镍,0.900 9 g尿素,加入15 mL溶剂(乙二醇-水,5∶5,V/V),磁力搅拌20 min,将溶液转移至50 mL的聚四氟乙烯内衬高温反应釜中,将预处理的碳纸移入反应釜,密闭后放入烘箱,160 ℃高温下连续反应6 h。待反应釜自然冷却至室温后,将碳纸取出用无水乙醇和去离子水清洗,冲洗掉附着于碳纸表面的没有完全生长的材料,反应釜中的溶液经离心干燥后用于后续实验材料的表征。将碳纸放入真空干燥箱中60 ℃条件下6 h,得到Ni-CHs/CP电极(图1)。

图1 Ni-CHs/CP电极制备流程示意图Fig.1 Schematic diagram of Ni-CHs/CP electrode preparation process
1.3.2 电化学测试
电化学测试使用三电极系统,Ni-CHs/CP为工作电极,铂丝为对电极,甘汞电极为参比电极。设置电位窗口为0~0.7 V,扫描速率为0.1 V/s,在 0.1 mol/L的NaOH电解液中,对Ni-CHs/CP电极进行电化学测试。
1.4 数据处理
实验数据采集自CHI660E电化学工作站,由Origin 2018绘图,由Office制表。
2 结果与分析
2.1 Ni-CHs/CP电极材料的表征
由图2a可知,裸碳纸表面比较光滑,呈三维交织结构。由图2b、c可知,Ni-CHs纳米颗粒将碳纸完全包裹使碳纸表面比较粗糙,增大了与电解液的接触面积,其结构是由大量小颗粒组成,具有许多纳米级孔隙,增加了活性位点暴露的数量,从而提升了工作电极的电化学性能。由图2d可知,Ni-CHs为颗粒状,颗粒尺寸相对均一,约为100~150 nm。

图2 裸碳纸(a)和不同放大倍数下的Ni-CHs/CP电极(b~d)扫描电镜图Fig.2 SEM images of bare carbon paper (a) and Ni-CHs/CP at different magnifications (b-d)
由于碳纸自身的衍射峰强度过高,而无法明显观察到Ni-CHs的衍射峰,因此为了消除碳纸基体对测试结果的影响,对Ni-CHs粉末进行X射线衍射分析,如图3所示,在14.7°、17.5°、24.2°和34.7°处可观察到4个强衍射峰,与镍的碱式碳酸盐Ni2(CO3)(OH)2的(020)、(120)、(130)、(-201)晶面(JCPDS No.35-0501)相对应。表明所合成的材料为Ni-CHs。
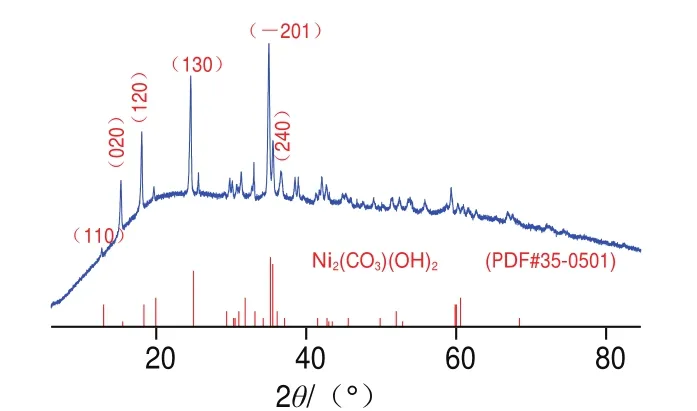
图3 Ni-CHs粉末的X射线衍射谱图Fig.3 XRD spectrum of Ni-CHs powder
Ni-CHs是通过一步水热法合成的,根据文献[24]推断其合成机理如下:

首先,尿素在加热条件下水解,形成NH3·H2O和CO2(反应1),随后二者转化为OH-和(反应2和3),OH-、和Ni2+又形成Ni2(CO3)(OH)2(反应4),这与所测的X射线衍射图谱一致。
2.2 无酶葡萄糖传感器的电化学表征
2.2.1 循环伏安曲线
在电化学工作站中,采用三电极体系考察所制备电极的电化学行为。分别在0.1 mol/L NaOH电解液和含有5 mmol/L葡萄糖的0.1 mol/L NaOH电解液中进行Ni-CHs/CP电极的循环伏安扫描。
由图4可知,裸碳纸在葡萄糖加入前后循环伏安曲线并无明显的变化,而当负载了Ni-CHs纳米粒子后,可观察到一对明显的氧化还原峰。这是由于Ni-CHs在碱性溶液中二价镍离子与溶液中OH-结合生成三价镍离子,即:Ni2(CO3)(OH)2被氧化为NiOOH[25](反应5),此过程中有电子的转移,所以会产生峰电流。在加入5 mmol/L葡萄糖时氧化峰电流响应有明显提高,电流强度为9.56 mA/cm2,是没加葡萄糖时的1.9 倍。这是因为在碱性介质中,葡萄糖的氧化通常伴随着一个多步骤的过程,高价态的NiOOH参与葡萄糖的氧化,将葡萄糖转化为葡萄糖酸内酯,同时自身又被还原为Ni2+(反应6),这部分Ni2+在通电条件下在此又被氧化为Ni3+,产生一定的响应电流,从而导致Ni2+/Ni3+氧化峰响应电流强度的增加。

图4 裸碳纸(a)和Ni-CHs/CP(b)在有/无葡萄糖存在下的循环伏安曲线Fig.4 CV curves of bare carbon paper (a) and Ni-CHs/CP (b) in the presence or absence of glucose

2.2.2 反应类型的判断
为考察Ni-CHs/CP的表面动力学过程,在0.1 mol/L NaOH电解液中,设置扫描速率为10 ~100 mV/s,由图5可知,随着扫描速率的增加,阳极峰电流(Ipa)和阴极峰电流(Ipc)的绝对值均持续增加。同时,阳极峰电位有一定的正移,阴极峰电位有一定的负移。这是因为葡萄糖及其氧化的中间产物会被Ni-CHs/CP的活性位点吸附,从而占据了工作电极的活性位点使电解质溶液中的葡萄糖不能及时的扩散到工作电极表面,导致电极表面极化,使得峰电位有一定的偏移。为了进一步研究Ni-CHs/CP电极检测葡萄糖时的电子转移过程,对氧化峰和还原峰电流值进行数据处理可得二者与扫描速率平方根呈现良好的线性关系(R2=0.998)。表明Ni-CHs/CP在电解质溶液中催化氧化葡萄糖的过程受扩散控制。

图5 不同扫描速率下5 mmol/L葡萄糖在Ni-CHs/CP的循环伏安图(A)和峰电流与扫描速率平方根的线性拟合图(B)Fig.5 CV curves of 5 mmol/L glucose in Ni-CHs/CP at different scanning speeds (A) and linear fitting between peak current and square root of scanning rate (B)
2.2.3 传感器对葡萄糖的时间-电流曲线
采用时间-电流曲线研究Ni-CHs/CP电极对葡萄糖的检测性能。对工作电位进行优化,由图4b可知,葡萄糖发生氧化的电位区间在0.48~0.53 V之间,因此选择0.48、0.5、0.53 V为工作电压。在NaOH电解液中从400~1 200 s,每隔100 s加入0.1 mmol/L的葡萄糖溶液,所得不同电位下的时间-电流曲线如图6所示。
由图6可知,当电位为0.48 V时,产生的电流比较稳定但电流阶梯型最小。电位为0.53 V时,有较好的电流响应,但与0.50 V下的时间-电流曲线相比其电流响应较低,且0.53 V的高电位下,电极表面会发生析氧反应,产生的氧气堵塞电子的传输通道,从而影响Ni-CHs/CP电极对葡萄糖的催化氧化性能[26]。所以最终选择0.50 V为该电极的最佳工作电位。

图6 不同电位下连续添加0.5 mmol/L葡萄糖的时间-电流曲线Fig.6 Time-current curves with successive addition of 0.5 mmol/L glucose under different potentials
在最佳的工作电位下,依次向匀速搅拌的电解液中加入一定浓度的葡萄糖溶液,得到的时间-电流曲线如图7所示。
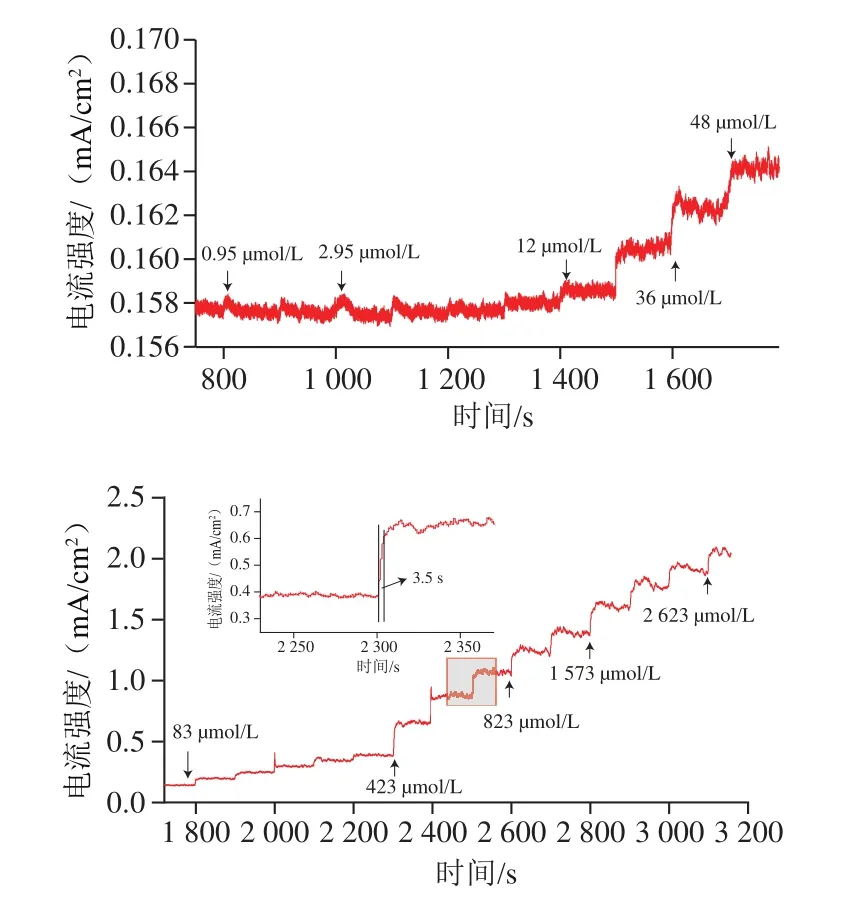
图7 Ni-CHs/CP电极的时间-电流曲线Fig.7 Time-current curve with Ni-CHs/CP electrode
由图7可知,当向体系中加入特定浓度的葡萄糖时,Ni-CHs/CP电极会产生相应的响应电流,葡萄糖浓度为0.95 µmol/L时,传感器对其产生响应。插图显示,加入葡萄糖时电流响应在3.5 s内就可达到稳定状态,表明Ni-CHs/CP电极对葡萄糖的响应速度较快。对葡萄糖浓度及对应的响应电流强度计算拟合后的线性如图8所示,拟合方程式为y=0.546 32x+0.720 8(R2=0.994)和y=1.252 8x+0.084 06(R2=0.983)。由此可知Ni-CHs/CP电极催化氧化葡萄糖的线性范围为0.950 μmol/L~1.023 mmol/L和1.223~2.623 mmol/L,检测的灵敏度为1 252 μAgmmol/(Lgcm),基于公式[27]:检出限(limit of detection,LOD)为3σ/S,其中σ为10 组空白样品度量值的标准偏差,S为线性回归的斜率。计算出检测限为0.31 μmol/L(信噪比为3∶1)。

图8 Ni-CHs/CP电极的电流强度与葡萄糖浓度的线性拟合图Fig.8 Linear fitting of current intensity of Ni-CHs/CP electrode versus glucose concentration
由表1可知,Ni-CHs/CP电极具有检测范围较宽、LOD低和灵敏度高的优点,对葡萄糖的检测具有较好的应用前景。

表1 Ni-CHs/CP传感器与其他已报道无酶传感器的性能对比Table 1 Performance comparison between Ni-CHs/CP sensor and other reported enzyme-free sensors
2.3 传感器的选择性及稳定性
对于葡萄糖传感器的进一步实际应用,抗干扰性能和稳定性非常的重要。饮料产品中除含有大量水之外,一般还含有乳糖、果糖、抗坏血酸、柠檬酸、蔗糖、食用香精及其他添加剂等。选择具有代表性的干扰物质对所制备传感器的选择性进行考察。在0.5 V的工作电位下,通过时间-电流法在电解液中边搅拌边连续添加乳糖、氯化钠、抗坏血酸、柠檬酸、蔗糖、果糖和葡萄糖。如图9a所示,加入葡萄糖时工作电极有明显的电流响应,加入稀释100 倍的干扰物质时,产生的电流响应很小,可以忽略不计。加入同等浓度的干扰物质时,乳糖、氯化钠、抗坏血酸、柠檬酸、蔗糖产生的电流响应非常微弱,果糖的产生的电流响应远小于葡萄糖的电流响应强度仅为葡萄糖的18%,且再次加入葡萄糖所产生的电流强度与第1次加入等量葡萄糖时产生的电流强度数值相近,表明干扰组分对自支撑Ni-CHs/CP电极的影响较小,由此可知Ni-CHs/CP电极对葡萄糖具有良好的选择性。

图9 Ni-CHs/CP电极的选择性(a)和稳定性(b)测试Fig.9 Selectivity (a) and stability (b) of Ni-CHs/CP electrode
在实际应用中,工作电极的稳定性也是评估传感器性能的一项重要指标,采用循环伏安法在含有5 mmol/L葡萄糖的0.1 mol/L NaOH电解质溶液中连续循环60次,取第1圈和第60圈作图,结果如图9b所示,Ni-CHs/CP电极循环第1圈与循环60圈相比峰值电流强度几乎保持不变,表明此工作电极对葡萄糖的检测具有良好的循环稳定性。
2.4 实际样品的检测
为了进一步验证Ni-CHs/CP电极的实用性,对市售的2 款饮料进行检测。利用加标回收率评估检测结果的准确性,采用时间-电流曲线进行加标后样品的电化学检测。取10 μL 0.12 mmol/L的样品1加入连续搅拌的0.1 mol/L NaOH电解液中,随后每隔100 s连续添加10 μL(0.05、0.10、0.15 mmol/L)的葡萄糖,记录到的电流-时间曲线如图10a所示,当待测液加入到电解液体系中时在极短的时间内响应电流就可达到稳定状态。图10b表明,工作电极表面产生的电流强度和所添加葡萄糖浓度之间呈现较好的线性关系,拟合方程式为y=0.590 92x+0.095 43,相关系数R2=0.990,以同样的方法对样品2进行加标回收。表2为根据图10b的线性曲线计算出的葡萄糖浓度,与GB 5009.8ü2016《食品中果糖、葡糖糖、蔗糖、麦芽糖、乳糖的测定》中高效液相色谱法检测食品中葡萄糖的测定结果一致,加标回收率为95.65%~105.56%,相对标准偏差为3.12%~5.86%,表明Ni-CHs/CP电极在实际样品葡萄糖检测中具有良好的应用前景,为葡萄糖的检测提供新的思路。
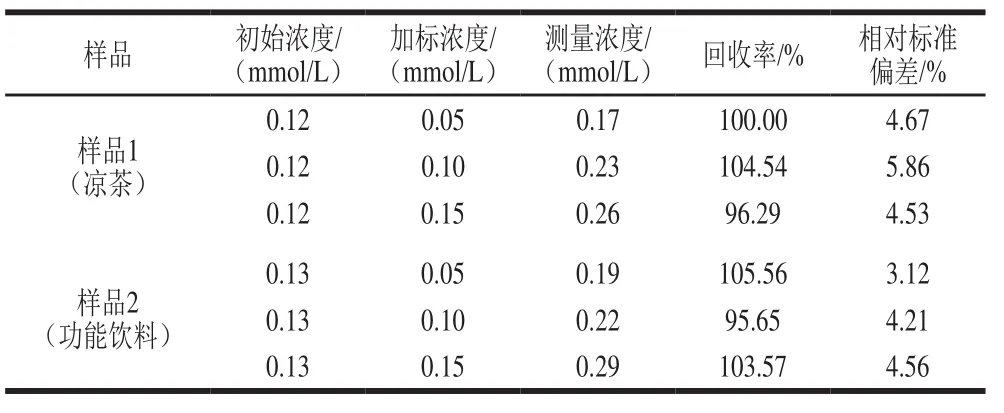
表2 饮料中葡萄糖的检测Table 2 Results of determination of glucose in beverage samples


图10 Ni-CHs/CP在实际样本中连续添加0.05 mmol/L葡萄糖时的电流-时间曲线(a)和电流强度-葡萄糖浓度的线性拟合图(b)Fig.10 Current-time curve of Ni-CHs/CP when 0.05 mmol/L glucose was continuously added to the actual sample (a) an linear fitting of current intensity versus glucose concentration (b)
3 结 论
基于镍基碱式碳酸盐对葡萄糖良好的电催化性能,本研究制备Ni2(CO3)(OH)2纳米粒子,通过水热法原位生长于碳纸基底上成功构建无酶葡萄糖传感器。在0.950 μmol/L~1.023 mmol/L和1.223~2.623 mmol/L范围内修饰电极峰电流强度与葡萄糖浓度存在良好的线性关系,LOD可达0.31 µmol/L。利用此法对市售2 款饮料进行检测,检测结果与GB 5009.8ü2016《食品中果糖、葡萄糖、蔗糖、麦芽糖、乳糖的测定》中高效液相色谱法检测食品中葡萄糖的测定结果一致。与已报道的其他葡萄糖检测方法相比较,该检测方法电极具有制备简单、快速、灵敏的特点,为饮料中葡萄糖的检测提供了新的思路。
