Real-time PCR和双向电泳联合鉴别婴幼儿配方羊乳粉的乳源成分
2022-05-09侯艳梅杨艳歌刘鸣畅王洪越王丹丹吴亚君
侯艳梅,杨艳歌,吴 桐,刘鸣畅,王洪越,王丹丹,吴亚君,*
(1.海普诺凯营养品有限公司,湖南 长沙 410000;2.中国检验检疫科学研究院,北京 100176)
羊乳作为特色小众乳品具有较好的营养特性,它的蛋白质构成、非蛋白氮含量、脂肪酸构成和寡糖种类与牛乳相比更接近于母乳[1-2],因此羊乳基婴幼儿配方奶粉具有特有的营养特性和健康益处,日益受到消费者欢迎,市场份额也在不断扩大,近些年全球销量增长率均保持10%以上[3]。然而奶羊的数量和日产量都远小于奶牛,导致羊乳粉的价格比牛乳粉高。因此羊乳制品中掺杂牛乳制品的经济利益欺诈现象时有发生。同时掺杂掺假也会引入牛源性过敏成分,增加致敏的风险,对消费者的健康构成威胁[4-5]。
我国《婴幼儿配方乳粉产品配方注册管理办法》规定了“产品名称中有动物性来源的,应当根据产品配方在配料表中如实标明使用的生乳、乳粉、乳清(蛋白)粉等乳制品原料的动物性来源。使用的乳制品原料有两种以上动物性来源时,应当标明各种动物性来源原料所占比例”[6]。为保证婴幼儿配方羊乳粉产品的质量,有必要开发一种灵敏度高和准确性好的原料检测方法。目前乳制品中乳源鉴定和检测的方法较多,有理化方法[7-10]、免疫技术[11-14]、基因方法[14-19]、蛋白方法[20-24]等。基因检测技术被公认是物种鉴定的金标准技术,其中实时聚合酶链式反应(real-time polymerase chain reaction,realtime PCR)技术操作简便、灵敏度高,被广泛用于食品物种检测标准中[25-26]。但real-time PCR法也存在一些限制,如灵敏度虽然高,且适用于各类基质样品,但由于核酸可存在于不同的组分中,包括全乳、脱脂乳、乳清等,因此对于核酸检测呈阳性的样品,还需要对组分来源进行确证。例如采用蛋白质电泳技术分析样品的蛋白组成,判定是否含有目标物种来源的蛋白质成分,才能对样品的真实性有准确的认识。蛋白质是乳品的主要营养成分,不同种源的乳品所包含的蛋白质组分有所不同,因此依据乳品的蛋白质或多肽指纹进行真伪检测也日益成为乳品质量评价的重要方法。其中双向电泳法是根据蛋白质等电点和分子质量两大特性,对蛋白进行高效分离,所得的图谱分辨率高、稳定性好,可以直观地展现不同种类、不同来源蛋白的差异[27]。笔者实验室已经发表了采用双向电泳技术进行乳源检测的研究[28-29]。但单独采用蛋白进行检测,操作流程复杂,检测耗时长,灵敏度不高,对实验人员要求高,不适合作为常规性检测方法。因此实验认为应该将DNA方法发展为一种快速初筛手段,将蛋白检测作为确证方法。
本研究首先建立婴幼儿配方乳粉DNA快速提取方法,采用具有远高于蛋白酶K降解能力的嗜热蛋白酶,通过温控设备一步式获取DNA,整个过程仅需17 min。优化建立乳粉中乳源成分快速real-time PCR筛查技术,不仅减少了检测时间,而且提高了扩增效率,包括哺乳动物,牛(家牛、水牛、牦牛)、羊(山羊和绵羊通用及单一乳源)以及山羊、绵羊单一物种检测方法,检测灵敏度好。采用快速、简便、灵敏的real-time PCR方法对样品的乳源进行初筛,然后对于检出牛基因成分的配方乳粉,再增加双向电泳乳源蛋白的检测,以αS1-酪蛋白、αS2-酪蛋白、κ-酪蛋白、β-乳球蛋白作为乳源判别的特征差异蛋白,并依据乳清蛋白和乳酪蛋白的特性,进一步判定样品中掺杂了牛乳还是牛乳清。通过以上两种技术联合,解决以往婴幼儿配方乳粉检测中因配料复杂,乳源判别困难的瓶颈问题。
1 材料与方法
1.1 材料与试剂
1.1.1 样品
婴幼儿配方羊乳粉、婴儿配方牛乳粉、全脂羊乳粉、脱脂羊乳粉、绵羊乳清粉、山羊乳清粉、山羊绵羊乳清粉、牛乳清粉、全脂牛乳粉、脱脂牛乳粉均由委托的乳品企业提供,水牛乳由广西水牛研究所提供;牛乳、绵羊乳、山羊乳、骆驼乳、马乳均从内蒙古的牧场收集;驴乳由青岛海关提供;牦牛乳由中国农业大学提供;市售婴幼儿配方羊乳粉均购自北京超市和网商平台;其他物种材料(猪、梅花鹿、马鹿、狗、兔、狐狸、水貂、大鼠、鸡、鸭、鱼),以及配方乳粉中常添加的植物源成分(葵花、大豆、椰子、玉米、菜籽),均为本实验室储存样品。
1.1.2 试剂
PDQeX prepGEM Universal DNA提取试剂盒英国MicroGEM公司;QuickGene DNA Tissue Kit L DNA提取试剂盒 日本Kurabo公司;NucleoSpin®Food德国Macherey-Nagel公司;DNeasy Mericon Food Kit德国Qiagen公司;Foodproof®GMO Sample Preparation Kit德国Biotecon Diagnostics公司;TaqMan Fast Advanced Master Mix 美国Applied Biosystems公司;BCA蛋白定量试剂盒 德国Merck公司;预染十二烷基硫酸钠-聚丙烯酰胺凝胶电泳(sodium dodecyl sulfate-polyacrylamide gel eletropheresis,SDS-PAGE)标准品(Prestained SDSPAGE Standards,Broad range)、两性电解质(Bio-Lyte 4/6 Ampholyte、Bio-Lyte 5/7 Ampholyte)、IPG预制胶条(7 cm、pH 4~7)、30%丙烯酰胺溶液、1.5 mol/L三羟甲基氨基甲烷(tris (hydroxymethyl) aminomethane,Tris)溶液(pH 8.8)、四甲基乙二胺(N,N,N’,N’-tetramethylethylenediamine,TEMED)、二硫苏糖醇(dithiothreitol,DTT)、3-[3-(胆酰胺丙基)二甲氨基]丙磺酸内盐(3-[(3-cholamidopropyl)dimethylammonio]-1-propanesulfate,CHAPS) 美国Bio-Rad公司。
1.1.3 引物探针
从GenBank数据库中提取哺乳动物、牛、家牛、水牛、牦牛、羊、山羊和绵羊以及其他乳源物种和近源物种的生长激素基因(GH)和cytb基因序列。利用Clustal X软件进行序列比对,利用Primer Premier 5.0软件分别在保守区域设计哺乳动物通用引物探针,在种间差异区域设计牛、羊、山羊和绵羊的特异性引物探针。其中牛为牛亚科牛族动物的统称,包括家牛(Bos taurus)、水牛(Bubalus bubalus)和牦牛(Bos grunniens),这3种乳在市场上的占有率较高,尤其是牛乳和水牛乳,占全世界乳产量的96%[30],通过设计一个牛族通用引物探针,可同时将牛乳、水牛乳、牦牛乳乳源成分扩出。同时由于婴幼儿配方羊乳粉的主要原料是羊乳,其常见的两个亚种是山羊和绵羊,因此实验首先设计了羊的通用引物,可同时实现对山羊和绵羊乳源成分的扩增。而市场上又有山羊乳和绵羊乳标识的乳粉,因此为了进一步满足标签查验的需求,实验又分别设计了山羊和绵羊引物探针,以进一步区分乳源。具体信息如表1所示,所有引物探针均在上海英潍捷基生物技术有限公司合成。
1.2 仪器与设备
7500 Fast实时荧光PCR仪 美国Applied Biosystems公司;Labsystems Multiskan Spectrum酶标仪、Pico17离心机(离心力≥12 000hg) 美国Thermo公司;Mini Protean 3 Cell垂直板电泳仪、PharosFX激光成像系统美国Bio-Rad公司;QuickGene Mini8L 日本Kurabo公司;Qubit 2.0核酸蛋白分析仪 美国Invitrogen公司;组织研磨机 德国Qiagen公司;涡旋仪 德国IKA公司;恒温混匀仪、微量移液器 德国Eppendorf公司;离心管、八连排PCR管 美国Axygen公司;电子天平德国Sartorius公司;qPCR仪 杭州安塔生物科技有限公司;恒温水浴锅 北京六一生物科技有限公司。
1.3 方法
1.3.1 快速real-time PCR
1.3.1.1 样品前处理
液态乳混匀后冷冻干燥,乳粉直接混匀分装;其他动植物样品统一用组织研磨仪粉碎,-80 ℃冻存。
1.3.1.2 DNA提取
分别称取50 mg婴幼儿配方牛乳粉和婴幼儿配方羊乳粉样品,用传统的CTAB法以及5种商业试剂盒进行DNA提取效果比较,部分步骤在说明书基础上进行了改良。其中采用PDQeX prepGEM通用DNA提取试剂盒改良后的步骤为:称取50 mg乳粉于1.5 mL离心管中,加入500 μL wash buffer,涡旋振荡1 min,12 000 r/min离心3 min,弃上清液,以洗去油脂,然后按照试剂盒配制100 μL提取反应体系(10 μL Histosolv,10 μL Orange Buffer,2 μL PrepGEM,78 μL H2O)重悬沉淀并移至PCR单管中,进行热循环反应:52 ℃细胞壁降解5 min,75 ℃细胞裂解10 min,95 ℃变性2 min,即可获取DNA。
改良的CTAB法在GB/T 19495.3ü2004《转基因产品检测 核酸提取纯化方法》[31]步骤的基础上,蛋白酶K量增加1 倍,氯仿去蛋白的步骤重复1次。NucleoSpin食品基因组DNA提取试剂盒、DNeasy Mericon食品基因组DNA提取试剂盒、QuickGene DNA多样本抽提试剂盒、Foodproof®GMO Sample Preparation核酸纯化试剂盒改良的步骤为:加入裂解液至样品自由悬浮于液体中,蛋白酶K量是说明书量的2 倍,所有样品于65 ℃、500 r/min舒适型恒温混匀仪中振荡孵育过夜,其他步骤按照各说明书操作,获取的DNA统一用100 μL无菌ddH2O溶解。用Qubit 2.0核酸蛋白定量仪测量DNA浓度,用哺乳动物引物探针作为内参照进行real-time PCR扩增效率评估,每份DNA重复扩增3次,-20 ℃保存DNA。
1.3.1.3 real-time PCR
real-time PCR检测采用25 μL反应体系:12.5 μLTaqMan Fast Advanced Master Mix,10 μmol/L上下游引物各0.5 μL,10 μmol/L探针0.5 μL,模板DNA 5 μL,用无菌水补至总体积25 μL。在7500 Fast real-time PCR仪进行PCR扩增,原始反应程序为:50 ℃去除RNA 2 min;95 ℃预变性10 min;95 ℃变性15 s,60 ℃退火1 min,35个循环。
1.3.1.4 通用性和特异性检测
real-time PCR检测分别以绵羊奶、山羊奶、牛乳、水牛乳、牦牛乳、骆驼乳、马奶、驴乳、马鹿、梅花鹿、猪、狗、兔、狐狸、水貂、大鼠、鸡、鸭、鱼、葵花、大豆、椰子、玉米、菜籽的DNA(5 ng/μL)为扩增对象进行扩增,以无菌水为空白对照,每个样品2个平行重复。
1.3.1.5 快速real-time PCR程序的建立
为缩短检测时间,建立快速real-time PCR检测流程,在上述典型传统扩增程序(设为①)的基础上进行优化,优化的程序设为②~⑧。分别采用羊和引物探针对羊乳和牛乳DNA进行扩增,分析扩增效果和检测时间,生成图像时阈值设为自动。在PCR同时,设置阳性对照、阴性对照和空白对照,每个反应设置2个平行,并重复实验1次。
②50 ℃去除RNA 2 min;95 ℃预变性10 min;95 ℃变性10 s,60 ℃退火1 min,35个循环。
③50 ℃去除RNA 2 min;95 ℃预变性7 min;95 ℃变性5 s,60 ℃退火30 s,35个循环。
④50 ℃去除RNA 2 min;95 ℃预变性5 min;95 ℃变性3 s,60 ℃退火15 s,35个循环。
⑤50 ℃去除RNA 2 min;95 ℃预变性2 min;95 ℃变性2 s,60 ℃退火10 s,35个循环。
⑥95 ℃预变性2 min;95 ℃变性2 s,60 ℃退火10 s,35个循环。
⑦95 ℃预变性2 min;95 ℃变性2 s,60 ℃退火8 s,35个循环。
⑧95 ℃预变性2 min;95 ℃变性2 s,60 ℃退火5 s,35个循环。
1.3.1.6 绝对灵敏度分析
将提取的山羊、绵羊、牛样品的DNA从100 ng/μL开始进行10 倍比稀释,使其质量浓度分别为100 ng/μL、10 ng/μL、1 ng/μL、100 pg/μL、10 pg/μL、1 pg/μL,共6个梯度,用筛选好的特异性引物探针进行real-time PCR扩增,每个反应设置3个平行。
1.3.1.7 实际灵敏度分析
分别按照质量分数为0.1%、1%、10%、50%、100%制备婴幼儿配方牛乳粉/婴幼儿配方羊乳粉、脱脂牛乳粉/脱脂羊乳粉、全脂牛乳粉/全脂羊乳粉、牛乳清粉/山羊绵羊乳清粉、牛乳清粉/全脂羊乳粉、牛乳清粉/脱脂羊乳粉模拟掺杂混合样品,混匀后提取DNA,进行realtime PCR扩增,每个反应设置3个平行。
1.3.2 双向电泳
前期双向电泳研究表明山羊乳和绵羊乳的蛋白无明显差异,牛乳和羊乳所含蛋白种类也基本相同,但在乳清蛋白区域及乳酪蛋白区域存在明显差异,即:牛αS1-酪蛋白和羊αS1-酪蛋白等电点基本相同,但牛αS1-酪蛋白分子质量比羊αS1-酪蛋白大;牛αS2-酪蛋白和羊αS2-酪蛋白,牛κ-酪蛋白和羊κ-酪蛋白分子质量均相同,但羊αS2-酪蛋白和牛κ-酪蛋白等电点更大。牛β-乳球蛋白和羊β-乳球蛋白分子质量相同,但羊β-乳球蛋白等电点大于牛β-乳球蛋白。从而选定牛αS1-酪蛋白、牛αS2-酪蛋白、牛κ-酪蛋白作为乳酪蛋白乳源判别的特征差异蛋白,以此判别婴幼儿配方羊乳粉中是否添加牛乳成分;并选定β-乳球蛋白作为判定婴幼儿配方羊乳粉中是添加牛乳清(蛋白)还是羊乳清(蛋白)成分的判别依据。本研究将联合该方法对本研究中的样品婴幼儿配方乳粉和常用配料以及市售配方乳粉的乳源成分进行判别。
1.3.2.1 样品预处理
称取1.5 g乳粉样品及配料置于15 mL离心管中,加10 mL去离子水,涡旋振荡,至充分溶解。使用BCA蛋白定量试剂盒对乳粉样品溶液的总蛋白进行测定,将蛋白质量浓度调整为20 mg/mL,存于4 ℃。
1.3.2.2 等电聚焦
预处理样品涡旋振荡混匀,吸取10 μL样品和150 μL水化液(8 mol/L尿素、4% CHAPS、40 mmol/L Tris、100 mmol/L DTT、0.5%两性电解质)混匀,使用IPG胶条进行等点聚焦。条件设定为50 V主动水化8 h;250 V线性30 min;500 V快速30 min;4 000 V线性3 h;4 000 V快速40 000 Vgh。
1.3.2.3 垂直电泳
SDS-PAGE参照文献[33]相关内容进行。其中分离胶为12%,电泳条件为10 mA恒流电泳。电泳结束,凝胶用考马斯亮蓝染液(50%甲醇、10%醋酸、0.25%考马斯亮蓝R250)染色1 h,用脱色液(25%甲醇、10%醋酸)脱色至凝胶背景消失,用蒸馏水浸泡1 h,随后用PharosFX激光成像系统拍照,获取双向电泳图谱。
1.3.3 市售样品乳源检测
市售样品各称取50 mg,采用PDQeX prepGEM通用DNA提取试剂盒按照1.3.1.2节改良步骤进行DNA提取,所有DNA质量浓度调制5 ng/μL,采用建立的快速realtime PCR程序进行乳源检测。牛基因检测呈阳性的样品再按照上述双向电泳步骤进行乳源蛋白分析。
1.4 数据统计及图表绘制
从仪器导出检测结果和数据,Excel软件计算并绘制图表。扩增图谱和标准曲线仪器自动生成,导出图谱进行组合。其中实际灵敏度的线性回归曲线的绘制是以目标样品含量的对数(ln值)为X轴,以相应的Ct均值为Y轴,绘制散点图,并添加趋势线(对数)。
2 结果与分析
2.1 6种DNA提取方法比较与一步法DNA快速提取方法的建立
基因检测限制快速应用的主要瓶颈在于传统DNA提取耗时长、操作复杂,因此建立一个简单、快速、高效的DNA提取方法是快速筛查需要解决的首要问题。实验选用6种提取方法:CTAB法、PDQeX prepGEM通用DNA提取试剂盒、NucleoSpin食品基因组DNA提取试剂盒、DNeasy Mericon食品基因组DNA提取试剂盒、QuickGene DNA多样本抽提试剂盒、Foodproof®GMO Sample Preparation核酸纯化试剂盒,并进行改良,以婴幼儿配方牛乳粉和婴幼儿配方羊乳粉为研究对象,比较DNA提取效果、提取时间、扩增效率,结果如图1所示。采用PDQeX的DNA提取质量浓度最高,婴幼儿配方牛乳粉为5.2 ng/μL、婴幼儿配方羊乳粉为63.20 ng/μL。采用4种柱层析试剂盒提取的DNA质量浓度差别不大,CTAB最低。从扩增效率看,CTAB扩增效果最低,PDQeX和4种柱层析试剂盒扩增效果差异不大,其中牛乳的Ct值在22.2~23.5之间,羊乳的Ct值在18.8~20.13之间。从提取时间看,CTAB耗时最长,约3 h,4种试剂盒耗时差别不大,约130~150 min,而PDQeX仅需温控反应一步式获取DNA,时间仅需17 min,大大缩短了提取时间。综上,PDQeX所用的时间最短,操作步骤最简便,提取效率高,可以满足检测需求,因此后续研究均采用此一步法进行DNA的快速提取。
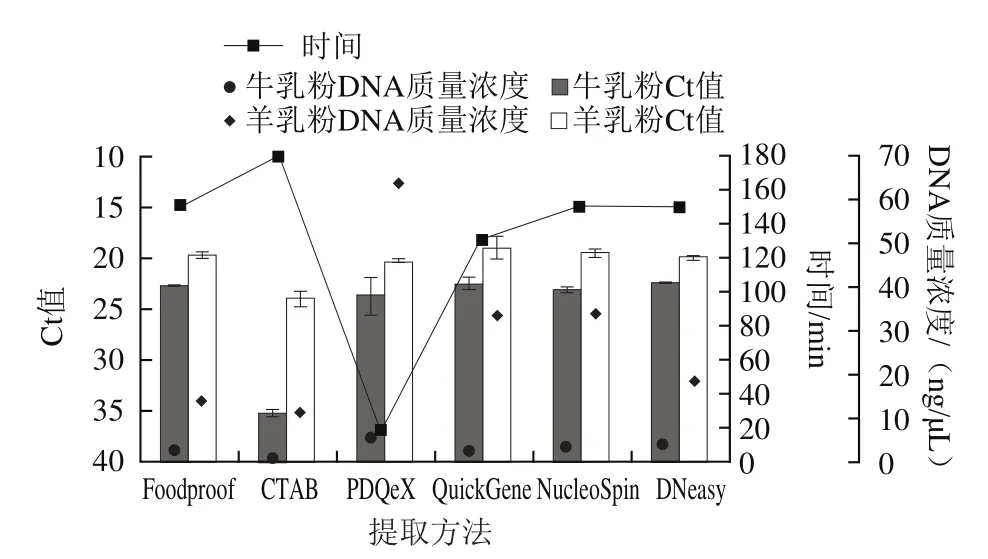
图1 6种提取方法对婴幼儿配方乳粉DNA效果分析Fig.1 Operational efficiencies of six DNA extraction methods for infant formula
2.2 real-time PCR方法检测乳源成分方法的建立
2.2.1 引物探针设计与特异性筛选
考虑到乳粉在生产过程中需要经过喷雾干燥、高温杀菌等加工处理,可能导致DNA断裂或者降解,为保证能从不同加工程度的乳制品中检测出目标动物成分,实验在设计引物探针的时候将扩增靶序列控制在150 bp以内,设计的哺乳动物内参照靶序列为82 bp左右,牛族靶序列为81 bp,羊靶序列为79 bp,山羊靶序列为139 bp,绵羊靶序列为136 bp。引物和探针序列见表1。
为对待测样品的DNA进行质量控制,根据常见的乳源(绵羊、山羊、家牛、水牛、牦牛等)均为哺乳动物的特性,设计了哺乳动物通用引物探针,real-time PCR通用性检测结果显示,设计的哺乳动物引物探针可以将所有哺乳动物源性成分扩出,扩增Ct值在24~30之间,表明通用性和覆盖性较好,其他非哺乳动物物种均无扩增结果,表明扩增的特异性较好,可以作为乳源成分DNA质控检测的内参照,PCR结果如图2A所示。设计的牛引物探针可将牛乳、牦牛乳、水牛乳扩出,平均Ct值分别为25.71f0.08、25.92f0.09、26.18f0.21。其他常见畜禽鱼物种(猪、梅花鹿、马鹿、狗、兔、狐狸、水貂、大鼠、鸡、鸭、鱼),以及配方乳粉中常添加的植物源成分(葵花、大豆、椰子、玉米、菜籽)未出现非特异扩增,表明牛引物探针覆盖性和特异性良好,结果如图2B所示。
羊通用引物探针可同时扩增绵羊乳和山羊乳,平均Ct值分别为24.14f0.07和24.41f0.08,对其他常见畜禽鱼以及婴幼儿配方乳粉中常添加的植物源成分无非特异扩增,表明羊的引物探针覆盖性和特异性良好,结果如图2C所示。山羊和绵羊这两对引物探针分别仅能特异性扩增山羊或绵羊成分,绵羊平均Ct值为20.15f0.09,山羊平均Ct值为26.34f0.17,特异性良好,结果分别如图2D和2E所示。
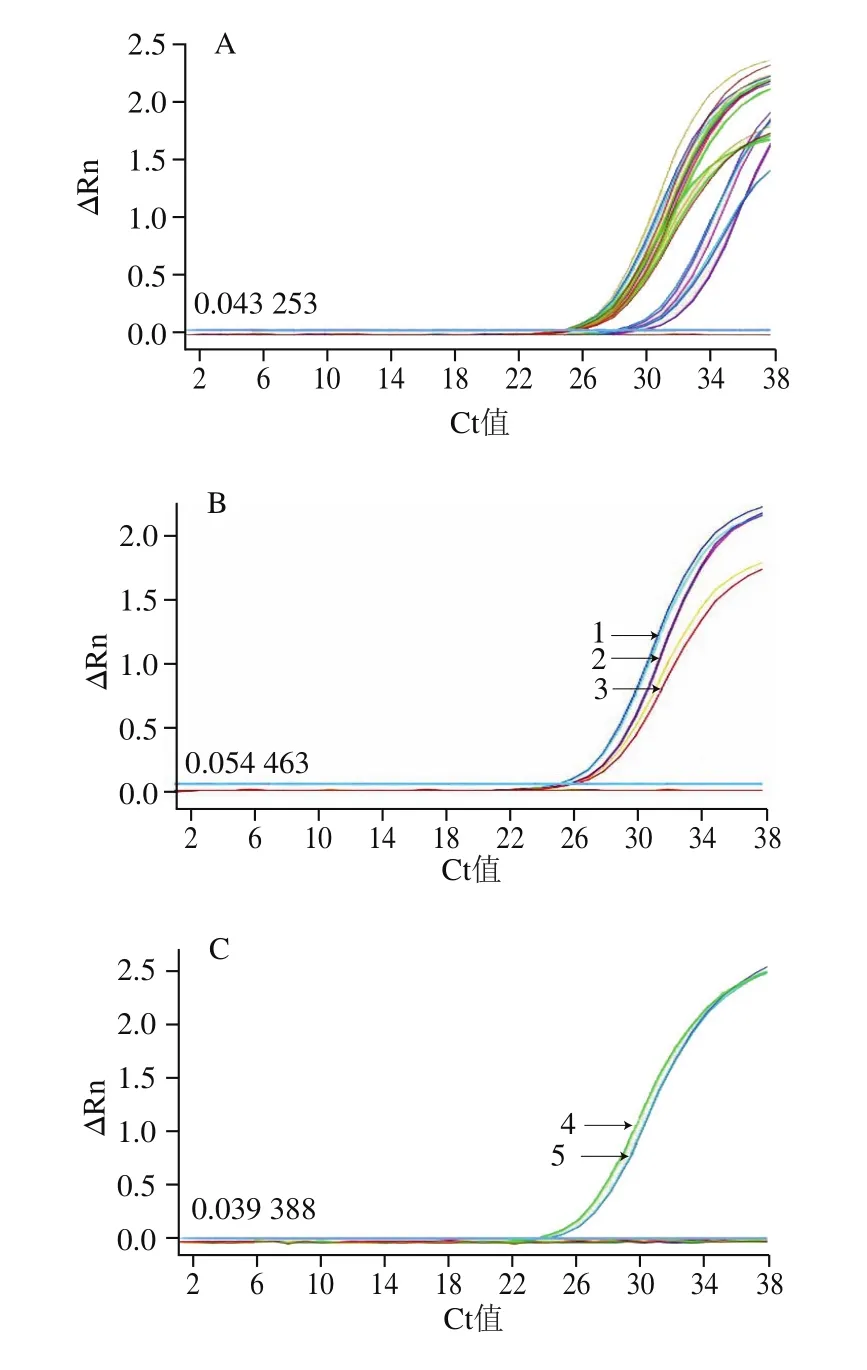
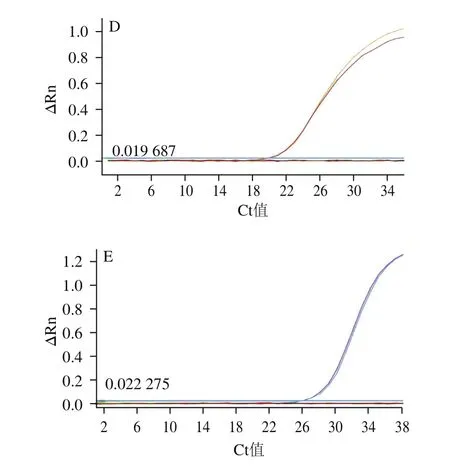
图2 real-time PCR引物探针特异性分析Fig.2 Specificity of primers and probes used for real-time PCR
2.2.2 快速real-time PCR检测体系的优化
为缩短检测时间,实验建立了快速real-time PCR检测流程,以婴幼儿配方牛乳粉和婴幼儿配方羊乳粉的DNA为模板,以牛和羊引物探针为代表对扩增效率进行分析。如图3所示,羊源性检测结果表明,从反应程序①~⑧,扩增的Ct值几乎保持不变,都在21左右,且扩增效率还稍有升高,Ct值从21.65提前到21.27。牛的扩增结果显示,从反应程序①~⑤,扩增时间逐渐缩短,扩增效率却逐渐提高,Ct值从26.16提前到25.50,之后再缩短检测时间扩增效率开始逐渐下降,到第⑧个反应程序时Ct值升至28.88。综合上述结果,以反应程序⑤作为快速real-time PCR检测的最优反应程序,此时不仅扩增时间缩减到28 min 26 s,比反应程序①的反应时间74 min 58 s缩减了47 min左右,且扩增效率还有所提高,Ct值可减少1左右,因此后续均采用该程序进行快速real-time PCR检测。
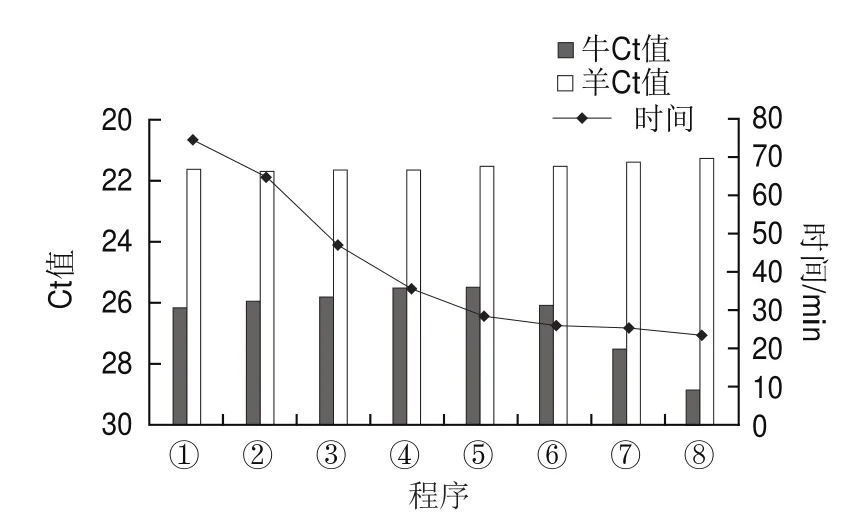
图3 快速real-time PCR检测体系优化结果Fig.3 Optimization of fast real-time PCR detection system
2.2.3 灵敏度分析
6个梯度浓度的DNA快速real-time PCR扩增检测结果显示:羊和绵羊的引物探针在DNA模板量为10 pg/μL时,尚有良好的扩增,此时平均Ct值分别为32.66f0.11和32.29f0.24;当低至1 pg/μL时,在特定的循环数内,不再有扩增,因此初步确定羊和绵羊的绝对灵敏度为10 pg/μL,结果如图4C、D所示。哺乳动物、牛和山羊引物探针检测结果显示,当DNA质量浓度达到100 pg/μL时,仍有良好的扩增,此时平均Ct值分别为32.16f0.12:33.07f0.04、30.73f0.09;但当DNA模板量低至10 pg/μL时,牛的Ct值超出35,哺乳动物和山羊虽然有扩增,平均Ct值分别为34.94f0.72和34.28f0.10,但荧光信号ΔRn值较低,已经接近阈值,因此初步确定哺乳、牛和山羊的绝对灵敏度为100 pg/μL,结果如图4A、B、E所示。根据仪器自动生成的标准曲线,哺乳动物、牛、羊、山羊和绵羊的线性相关系数R2分别为0.996、0.992、0.998、0.997、0.996(结果未提供),线性关系良好。因此确定本研究设计的哺乳动物、牛和山羊源性成分最低绝对灵敏度为100 pg/μL,羊和绵羊成分最低绝对灵敏度为10 pg/μL。
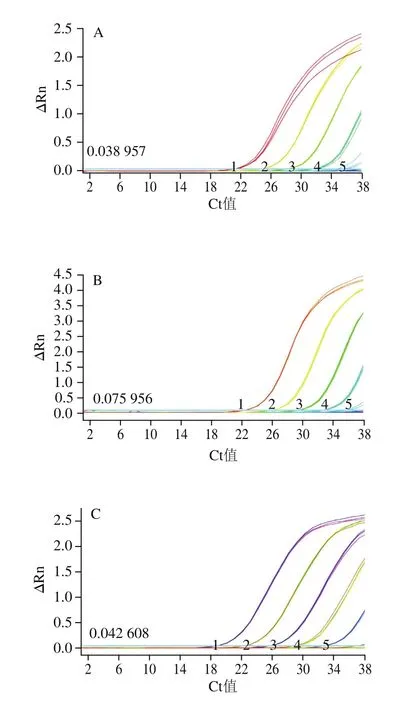
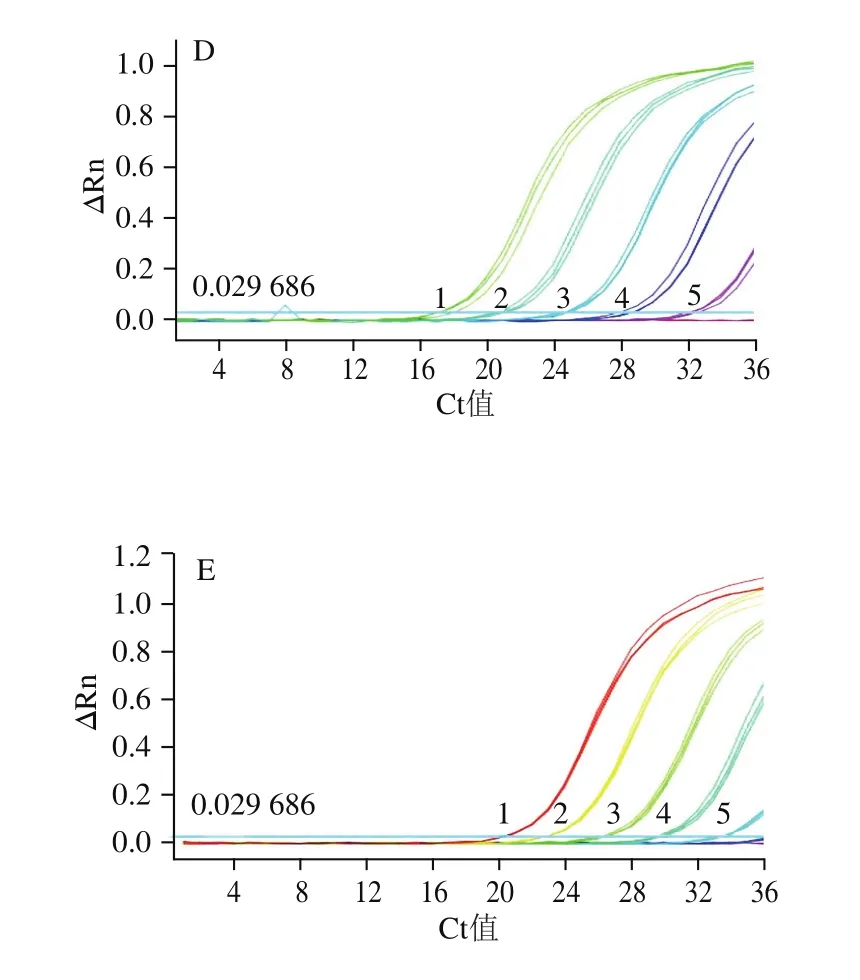
图4 乳源成分real-time PCR检测绝对灵敏度分析Fig.4 Sensitivity of detection of milk-derived ingredients by real-time PCR
2.2.4 常见婴幼儿配方粉及乳源配料模拟添加牛源性成分灵敏度分析
按照1.3.1.7节方法进行实际灵敏度检测。采用筛选的PDQeX prepGEM通用DNA提取试剂盒快速提取样品DNA,检测结果显示,乳清、脱脂乳粉、全脂乳粉以及婴幼儿配方中的牛源性成分检出限均可达1%,线性回归曲线R2均在0.9以上(图5),可满足适合用于实际样品的检测需求。
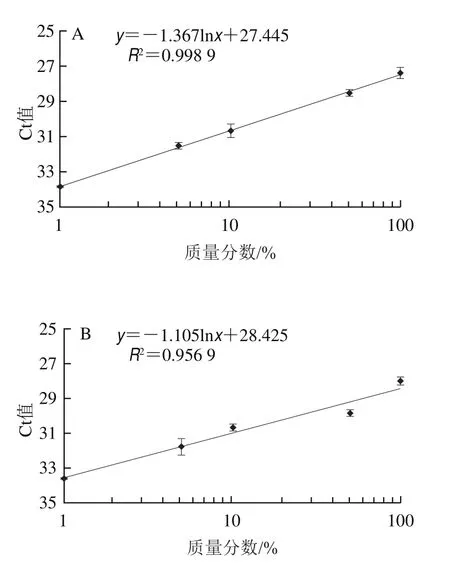
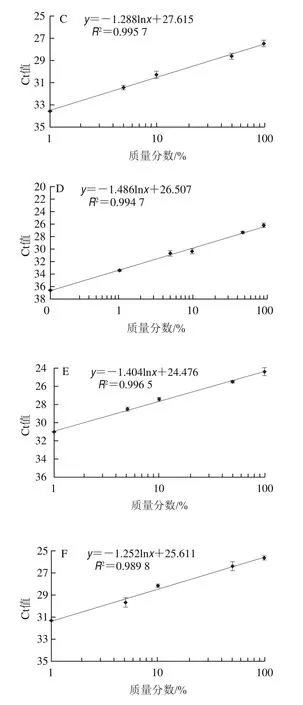
图5 婴幼儿配方羊乳粉及其常用配料中牛源性成分检测实际灵敏度分析Fig.5 Sensitivity of detection of bovine milk-derived ingredients in infant formula and common milk powder and whey products
2.3 方法联合检测婴幼儿配方乳粉及常用配料的乳源成分
联合前期研究已建立的乳源蛋白双向电泳蛋白检测方法[29],采用建立的real-time PCR基因检测方法对婴幼儿配方乳粉乳源检测的准确性进行评估。实验以收集的10 份婴儿配方粉及常用原料真实样品为研究对象,进行检测和结果对比分析。检测结果对比显示:1)牛乳清可检出牛基因成分,双向电泳可检出牛乳清蛋白,未检出牛乳酪蛋白成分。2)山羊乳清可检出羊和山羊基因成分,绵羊乳清可检出羊和绵羊基因成分,山羊绵羊乳清可检出羊、绵羊、山羊基因成分;3种乳清双向电泳检测均可检出羊乳清蛋白,均未检出乳酪蛋白成分。3)全脂牛奶粉和脱脂牛奶粉可检出牛基因成分,双向电泳可同时检出牛乳清蛋白和牛乳酪蛋白成分。4)全脂羊乳粉和脱脂羊乳粉可检出羊和山羊基因成分,双向电泳可同时检出羊乳清蛋白和羊乳酪蛋白成分。5)婴儿配方牛奶粉可检出牛基因成分,双向电泳可同时检出牛乳清蛋白和牛乳酪蛋白成分。6)婴儿配方羊奶粉可检出羊和山羊基因成分,双向电泳可同时检出羊乳清蛋白和羊乳酪蛋白成分;未检出牛乳清蛋白和牛乳酪蛋白成分。详细结果如表2所示,典型样品双向电泳特征图谱详见图6。通过两种方法对收集的真实样品的结果对比分析,双向电泳的结果和核酸结果完全一致;并且双向电泳的结果可以区分乳蛋白的来源,对核酸检测结果是一个重要的补充。
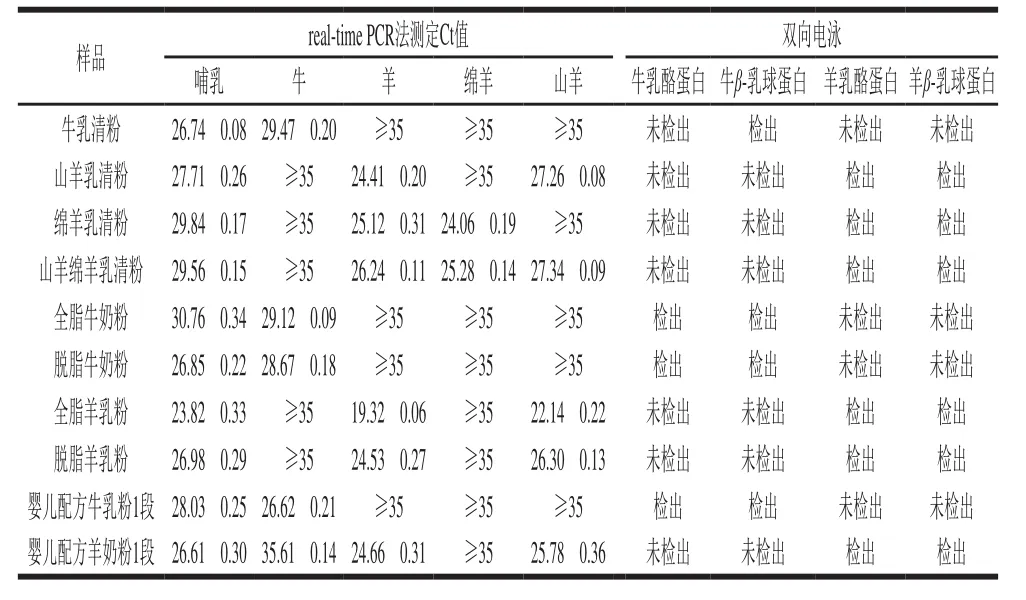
表2 婴幼儿配方乳粉及常用原料的乳源成分检测Table 2 Results of milk-derived ingredient detection in infant formula,whey powder and milk powder
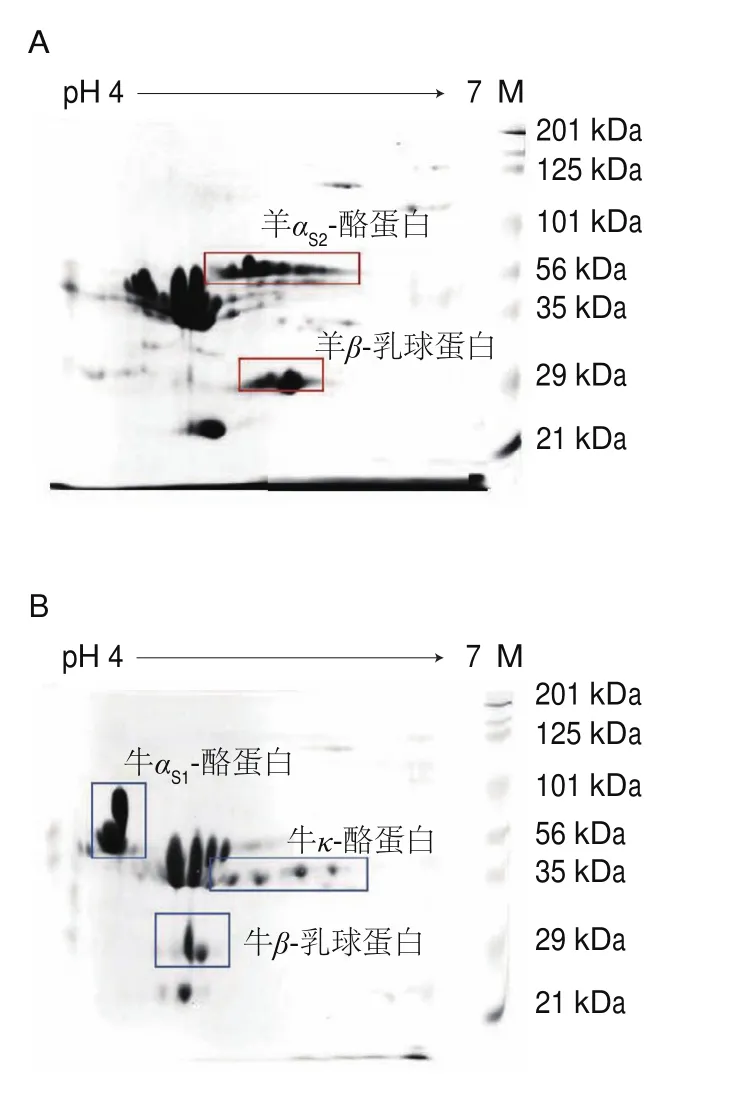
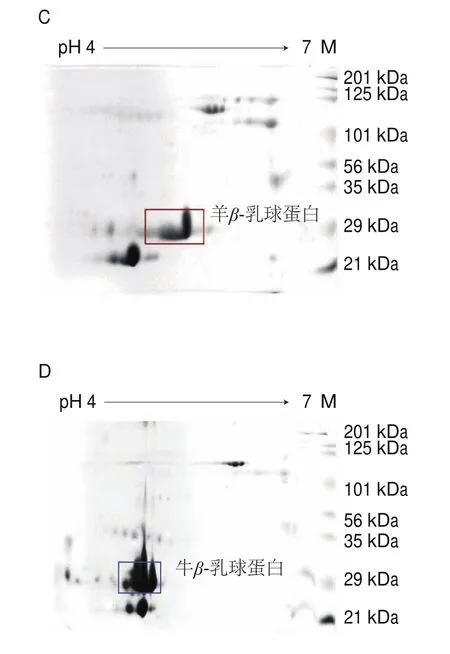
图6 典型样品双向电泳特征蛋白图谱Fig.6 Two-dimensional electrophoresis maps of typical milk powder samples
2.4 快速real-time PCR与双向电泳联合在市售婴幼儿配方粉样品乳源成分检测中的应用
抽检的20 份婴幼儿配方粉羊奶粉,其中8 份配料表标识乳清蛋白来源为羊源,5 份为牛源,3 份标识含乳清但未标识乳源来源,4 份配料表标识无乳清蛋白配料,联合检测结果见表3。采用建立的方法提取样品DNA,快速real-time PCR程序进行初筛,羊基因检测结果显示:所有样品均检出羊源性成分;有10 份检出山羊成分,未检出绵羊成分;有1 份检出绵羊成分,未检出山羊成分;其余9 份同时检出山羊和绵羊成分,但其中有2 份配料标识是纯山羊或纯绵羊,即10%的样品羊源性标识不一致。牛基因检测结果显示有11 份检出牛源性成分,对这11 份牛基因检测呈阳性的样品进一步采用双向电泳检测,以确证其蛋白来源,结果显示10%的样品同时检出牛乳酪蛋白和牛乳清蛋白,可能掺杂了牛乳;9 份检出牛乳清成分,去除5 份已标识乳清来源为牛源的样品,即20%的样品检出牛乳清掺杂成分。综合real-time PCR和双向电泳的检测结果,8 份婴幼儿配方粉羊奶粉检出与标签不符的乳源成分,占比40%。
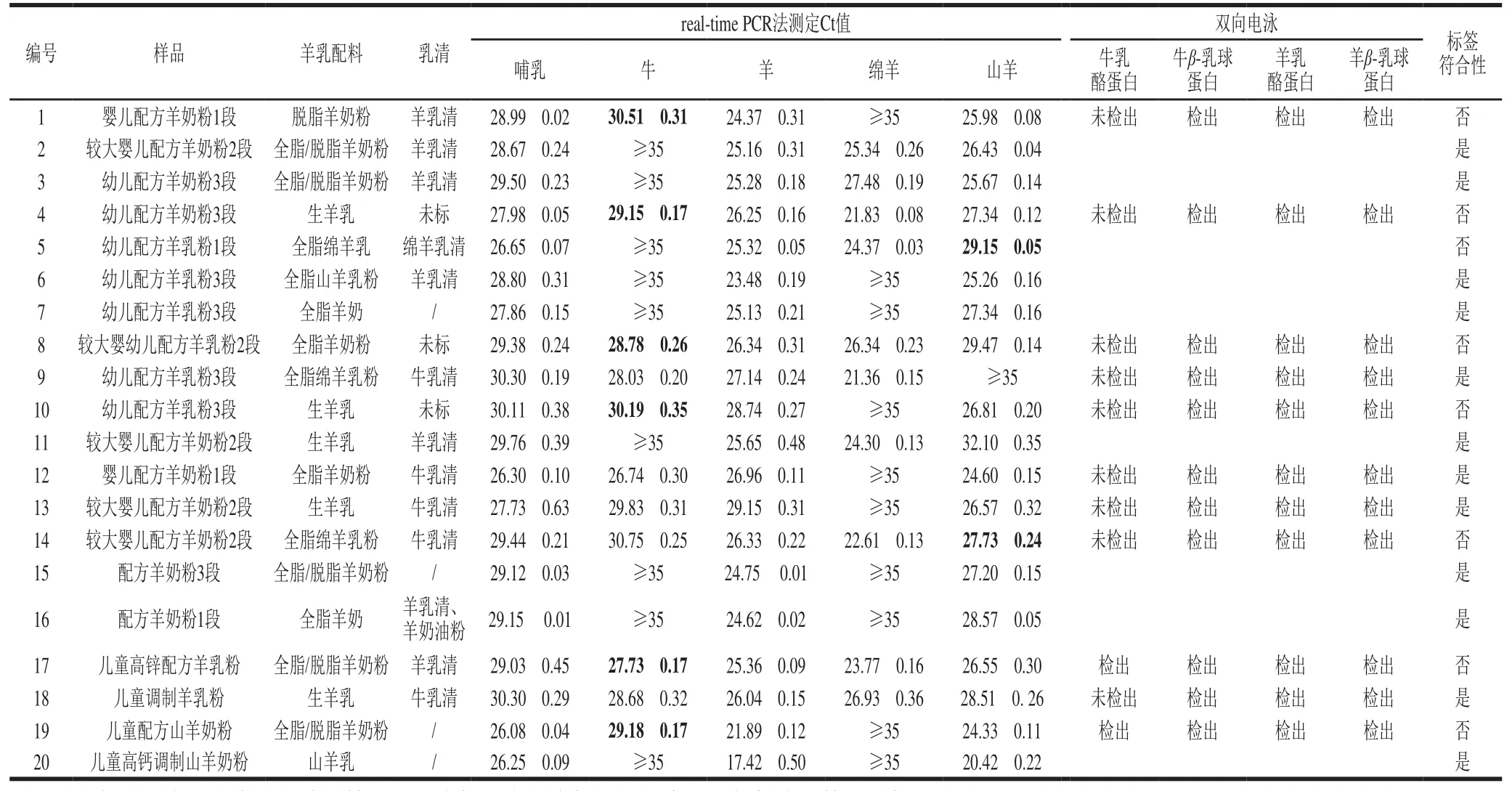
表3 市售婴幼儿配方羊奶粉中乳源成分检测Table 3 Results of detection of milk-derived ingredients in infant formula
3 讨 论
3.1 建立婴幼儿配方羊乳粉DNA快速提取方法的特点和优势
为实现婴幼儿配方羊乳粉样品DNA的快速提取,实验对提取方法进行筛选,通过CTAB法、一步法、吸附柱法的比较,最终选择PDQeX prepGEM通用DNA提取试剂盒。该技术采用具有远高于蛋白酶K降解能力的独特嗜热蛋白酶,其提取流程也不同于任何现有的核酸提取方法:不使用磁珠或吸附柱,也不使用SDS或CTAB,仅依靠温控反应即可实现一步式获取DNA。这样既去除了磁珠法/吸附柱法中吸附、洗脱、洗涤等需要反复移液操作而造成回收损失的环节,又在快速提取的同时,保证高回收率。样品前处理简便、快速,可在17 min内获取乳粉DNA,简化了提取步骤,提高了DNA提取效率,可满足现场快速筛查的需求。
3.2 联合real-time PCR和双向电泳进行婴幼儿配方羊乳粉乳源检测的必要性
本研究建立的婴幼儿配方羊乳粉中牛、羊、山羊、绵羊成分检测real-time PCR方法,可对婴幼儿配方羊乳粉的乳源成分进行快速初判,且方法的灵敏度较高(检出限1%),即便含有微量牛乳源也会被检出,说明该方法在检测的过程中不会造成假阴性和漏检的情况。由于婴儿配方乳粉是含有乳清、脱脂乳粉、全脂乳粉等复杂配料的混合制品,本研究推出联合双向电泳技术对乳源进行判别和确证的技术。采用该方法不仅可以区分牛乳和羊乳,还可依据乳清中不含酪蛋白的特性,进一步区分牛成分是来源于牛乳还是牛乳清。但相比于基因技术,双向电泳技术对手工操作依赖较大,并且操作步骤复杂、耗时较长、灵敏度稍低,且无法准确区分山羊和绵羊乳,因此需要联合基因的方法先对乳源进行快速初判,排除合格样品,再针对检出牛基因的样品采用双向电泳对乳源进行复核和确证。这样不仅提高了检测结果的准确性,也解决了以往配方乳粉中由于基质复杂导致乳源判别困难的问题,为配方乳产品乳源检测提供有利的技术支撑。
3.3 市售婴幼儿配方羊乳粉抽查结果显示存在乳源掺杂现象
线上线下市售婴幼儿配方羊乳粉的抽检结果表明,30%的产品掺杂了牛乳来源成分,其中10%的样品同时检出牛乳酪蛋白和乳清蛋白,20%检出牛乳清蛋白。同时检出牛乳酪蛋白和乳清蛋白的产品属于牛乳掺杂,违反了有关婴幼儿配方羊乳粉的要求。检出牛乳清蛋白的产品,20%未在配料表中进行乳源说明。依据国内外相关技术法规,例如国际食品法典委员会公布的标准Codex Stan 72-1981婴儿配方及特殊医用婴儿配方食品(2015修订版)[32]和国家食品药品监督管理总局第26号令[7],婴幼儿配方乳粉中动物源或植物源配料以及食品添加剂应当标出其种名,上述未在配料表中进行标注以及检出非标识乳源成分的产品不符合相关规定。
4 结 论
建立了一步法DNA快速提取流程和快速real-time PCR检测方法。从DNA提取到real-time PCR扩增,整个流程可在50 min内完成检测,可以区分牛、羊、绵羊、山羊乳源物种成分,实际灵敏度达1%。可以弥补双向电泳法操作复杂、耗时长、灵敏度不足、无法区分绵羊和山羊成分的不足。对牛基因检测呈阳性的样品进一步采用双向电泳法可对乳源成分进行复核和确证,并依据乳清蛋白和乳酪蛋白的特性,可判定样品掺杂成分是牛乳或牛乳清,能弥补real-time PCR法无法区分组分来源的不足。通过联合两种经典方法进行优势互补、弥补不足,解决了以往利用单一检测技术检测配方乳粉时存在的精准度和灵敏度限制的问题,以及出现的指标重叠,难以下结论,甚至误判的情况。为乳粉企业进行原料质控,政府实行监管和标签查验提供良好的技术支撑。
