负载型贵金属催化剂的臭氧分解性能
2022-04-28符启军邢德风王树东
王 婷 ,王 胜,符启军,邢德风,王树东
(1.洁净能源国家实验室,中国科学院大连化学物理研究所,辽宁 大连 116023;2.中国科学院大学,北京 100049)
近地面层的臭氧会严重危害人类健康和动植物的生长,特别是在光照充足的夏季,臭氧浓度明显上升[1-2]。长期暴露于高浓度臭氧中会诱发心血管疾病和危害呼吸系统,特别是严重危害幼儿、老年人及哮喘患者的健康[3-4]。因此,世界各国都制定了严格的标准来控制臭氧浓度。世界卫生组织颁布的《空气质量准则》中规定,日最高8 h内平均臭氧浓度不高于100 μg·m-3。2020年美国环保署(EPA)修订了臭氧及其他六种有害污染物的浓度标准,其中要求臭氧日最大8 h平均浓度不超过0.07×10-6。我国在2018年通过的国家环境质量标准《环境空气质量标准》(GB3095-2012)修订版中,规定日最大8 h内臭氧平均浓度不得高于100 μg·m-3(一级标准)和160 μg·m-3(二级标准)[5]。而在室内环境中,复印机、激光打印机、静电过滤器和静电除尘器等办公设备也会产生O3,特别是飞机在进入巡航高度,对流层臭氧会随着发动机引风系统进入机舱和油箱惰化系统,在机舱密闭环境中严重危害人体健康,同时会加速机载设备老化。因此,环境友好和经济高效的臭氧分解技术的开发具有重要意义[6-7]。
催化分解法因其高效的臭氧分解效率和技术经济性,是最具前景的臭氧脱除方法,但高活性和稳定性臭氧分解催化剂的开发是该技术的难点。常用的臭氧分解催化剂包括碳材料、贵金属、过渡金属氧化物、沸石和金属有机框架材料(MOFs)[8]。其中,贵金属催化剂具有优异的臭氧分解性能和良好的耐湿性。报道的贵金属臭氧分解催化剂如Pd[9-10]、Ag[11-12]、Au[13]、Pt和Ru等,Pd催化剂臭氧分解性能最优。Chang C L等[14]比较了Pd/Rh和Pt/Rh催化剂的臭氧分解性能,在臭氧浓度588×10-6和空速15 000 h-1时,Pd/Rh催化剂在25 ℃即可实现O3的完全转化,Pt/Rh催化剂则需100 ℃。Wu Mingcheng等[15]测试了催化剂Pt/Al2O3、Pd/Al2O3、Pd/Ni/Al2O3和Ni/Al2O3的臭氧分解性能,Pd/Al2O3催化剂不仅表现出最高的O3转化效率,而且在低温下,水蒸汽对O3分解反应的抑制作用也明显改善[16]。此外,Pd的臭氧分解和耐湿性能,还能通过Pd和MnOx之间的协同效应进一步提高[17]。Kameya T等[18]通过浸渍法在γ-MnO2上负载Pd,通过动力学研究,分析了活性降低速率和入口臭氧浓度、反应时间之间的函数关系,结果表明,Pd/MnO2催化剂具有最高的活性和稳定性。同样,Pd的掺杂对臭氧分解性能的提升在负载双组分过渡金属催化剂Pd-Co-MnOx/Al2O3[19]及分子筛负载催化剂PdO-CeO2/ZSM-5[20]被发现。而且Pd的促进作用或Pd与过渡金属之间的协同效应受Pd的负载量以及催化剂焙烧温度影响[21]。Yu Q等[22]研究表明,350 ℃焙烧得到的Pd-Mn/SiO2-Al2O3催化剂性能最优,在40 ℃、空速635 000 h-1、初始臭氧浓度0.6×10-6和相对湿度55%~65%条件下,反应80 h后仍能维持90%臭氧转化率。由上可见,Pd基催化剂臭氧分解性能的研究重点集中于Pd和过渡金属氧化物的协同效应。为了理清Pd活性位对于臭氧分解活性和耐水性的内在机制,本文采用等体积浸渍法和乙二醇还原法制得Pd/Al2O3催化剂,对催化剂在室温和不同湿度下的臭氧分解性能进行评价,研究其活性和稳定性,结合催化剂理化性能表征,阐明催化剂活性和稳定性与贵金属Pd的负载量、粒径之间的构效关系,揭示影响其分解活性的内在因素。
1 实验部分
1.1 试剂及材料
γ-Al2O3,工业级,直径(2~3) nm;硝酸钯[Pd(NO3)2]溶液,0.022 4 g·mL-1,上海久岭化工有限公司;乙二醇(EG),99.8%,阿拉丁;聚乙烯吡咯烷酮(PVP),Mw=40 000,默克。
采用γ-Al2O3粉末为载体,选用硝酸钯[Pd(NO3)2]溶液为活性组分前驱体,乙二醇为还原剂,聚乙烯吡咯烷酮为稳定剂。实验所用药品均为分析纯。
1.2 催化剂制备
采用等体积浸渍法制备Pd/Al2O3:将500 ℃焙烧4 h后的γ-Al2O3粉末压片成型,粉碎,筛分成(40~60)目颗粒,置于105 ℃烘箱中干燥12 h备用。采用浸渍法将Pd(NO3)2溶液负载于载体上,理论Pd负载质量分数分别为0.1%、0.5%、1.5%和2%,然后于105 ℃干燥2 h,500 ℃焙烧4 h,制得催化剂,分别命名为PdAl-0.1、PdAl-0.5、PdAl-1.5(PdAl-a)和PdAl-2。
乙二醇还原法[23]制备Pd/Al2O3:将γ-Al2O3粉末500 ℃焙烧4 h备用。然后,通过乙二醇还原法制备负载Pd催化剂。取1.34 mL的Pd(NO3)2溶液和一定量的PVP,10 mL的乙二醇加入到40 mL去离子水中,在圆底烧瓶中充分搅拌溶解后加入2 g备用的γ-Al2O3粉末。将圆底烧瓶在60 ℃下加热5 h,离心洗涤后干燥2 h,500 ℃焙烧4 h。然后,压片成型,粉碎,筛分,制得(40~60)目颗粒,105 ℃干燥12 h备用。负载Pd颗粒的尺寸通过调节PVP和Pd(NO3)2溶液的比例来控制,将n(Pd)∶n(PVP)=1∶20的样品命名为PdAl-b,n(Pd)∶n(PVP)=1∶1.25的样品命名为PdAl-c,无PVP添加的样品命名为PdAl-d。
1.3 催化剂表征
催化剂比表面积、孔容和孔径在Quantachrome NOVA 2200e上测得,并由BET和BJH理论计算得出。
样品在200 ℃脱气4 h除去表面吸附的气体和水后,在液氮温度(77 K)下测量样品的N2吸附-解吸等温线。
采用荷兰PANAlytical Empyrean X射线衍射仪分析样品的晶体结构,λ=0.154 2 nm,CuKa,工作电压40 kV,工作电流40mA,扫描速率5°·min-1,扫描范围5°~90°。
采用 TESCAN MIRA4 场发射扫描电镜观察催化剂表面形貌,能谱仪(EDS) 对催化剂表面各元素的含量和分布进行定性和定量分析,工作电压15 kV。
采用高分辨透射电子显微镜(TEM)JEM-2100检测 Pd 在催化剂上的分布和尺寸,工作电压200 kV。
元素价态通过Thermo Scientific K-Alpha X射线光电子能谱(XPS)来进行分析,AlKα,hv=1 486.6 eV,以C1s=284.80 eV结合能为能量标准进行荷电校正。
等离子发射光谱法 (ICP-OES) 用于在浸渍前测量Pd(NO3)2溶液中的Pd含量。
氧气程序升温脱附(O2-TPD)、水程序升温脱附(H2O-TPD)和一氧化碳脉冲(CO-Pulse)分析均在Quantachrome CHEMBET pulsar型化学吸附仪上进行。在TPD测试中,每次取约150 mg样品置于U型石英反应管中。首先在300 ℃的He气氛下处理1 h,然后降温冷却到室温,根据测试类型切换气体为3%O2/He,或H2O/Ar。吸附结束后,用He气吹扫30 min,待到基线稳定后,以5 ℃·min-1速率升温至900 ℃,用热导检测器(TCD)检测并记录信号的变化。CO-Pulse测试中,每次称取约50 mg样品置于U型石英反应管中,300 ℃对催化剂进行还原,然后在300 ℃的He气氛下处理1 h,降温冷却至30 °C,CO通过流动的He 注入样品。假设Pd颗粒为球形,平均粒径(dPd)由Pd的分散度计算得到,计算公式为:
式中,MPd为Pd原子质量,106.42 g·mol-1;ρPd为Pd密度,12 g·cm-3;SPd为Pd比表面积,47.78 m2·mol-1;DPd为样品表面Pd分散度。
CO原位红外测试(In-situCO DRIFTS)在配有MCT检测器的Nicolet 6700红外光谱仪上进行。每次称取约30 mg催化剂样品,放入反应池中,通入H2/Ar混合气,并升温至300 ℃处理1 h,然后降温至25 ℃,并用Ar吹扫表面,记录红外光谱扫描背景,分辨率 4 cm-1;然后切换成CO/Ar混合气保持60 min,最后再用Ar 吹扫30 min,并记录样品扫描图谱。
1.4 催化剂评价
将150 mg(40~60)目催化剂颗粒装入微型固定床石英反应器(i.d.=6 mm)中,测试所有上述催化剂在室温30 ℃下的O3催化分解性能。干气测试条件:总气量1.5 L·min-1,空速 600 L·(g·h)-1,入口臭氧浓度28.96 mg·m-3,空气和氩气作为平衡气,相对湿度RH<5%。耐水性能测试时,将流量1.4 L·min-1的空气通过恒温30 ℃水浴,使相对湿度RH>90%,其他条件同干气。臭氧由臭氧发生器(CFG,大连澳山环保科技有限公司)产生,进出口臭氧浓度由臭氧分析仪(Thermo Scientific,49i)监测。臭氧转化率通过下式计算:
式中,X为臭氧转化率;cin为反应器入口臭氧浓度,10-6;cout为反应器出口臭氧浓度,10-6。
2 结果与讨论
2.1 臭氧催化分解性能
在30 ℃、空速600 000 mL·(gcat·h)-1和相对湿度RH<5%条件下,比较了Pd质量分数分别为0.1%、0.5%、1.5%和2%的Pd/Al2O3催化剂的臭氧催化分解性能,结果如图1所示。
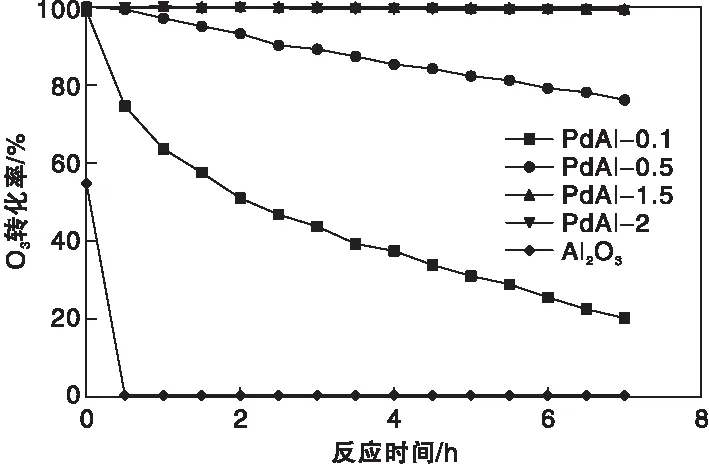
图1 不同Pd含量的Pd/Al2O3催化剂臭氧催化分解性能
由图1可以看出,随着Pd负载量的增加,臭氧催化分解活性增加,载体空白效应基本可以忽略。但是,当Pd质量分数从1.5%提高至2%时,性能基本保持不变,反应7 h后,PdAl-1.5和PdAl-2无明显差异。因此,考察Pd尺寸影响时,Pd质量分数保持1.5%。在相同反应条件下,考察Pd尺寸与臭氧分解性能的构效关系,如图2所示。

图2 1.5%Pd/Al2O3催化剂上Pd尺寸与臭氧分解性能的构效关系
由图2可以看出,采用等体积浸渍法制得的PdAl-a催化剂由于高Pd分散度和小尺寸,具有更高的臭氧分解性能。而且,臭氧催化分解反应属于结构敏感反应,Pd尺寸越小,活性越高。当其他条件不变,相对湿度提高到RH>90%时,新鲜催化剂转化率均有下降,反应30 min后催化剂活性随Pd尺寸的变化如图3所示,Pd尺寸越小,耐水性越高。

图3 1.5%Pd/Al2O3催化剂上Pd尺寸对催化剂耐水性的影响
2.2 织构参数和Pd分散度
实验测试了Pd/Al2O3催化剂的N2吸附-脱附等温线,如图4所示,并通过BET和BJH法计算其比表面积、孔容和孔径,结果如表1所示。

图4 不同Pd/Al2O3催化剂的N2吸附-脱附等温线

表1 不同催化剂的织构参数及Pd分散度
由图4和表1可以看出,所有催化剂都具有典型的Ⅳ型吸附等温线,存在明显的H1滞后环,具有介孔结构特征[24]。随着贵金属Pd负载量增加,催化剂比表面积略有降低。负载不同粒径Pd后,样品比表面积保持不变。因此,孔隙结构对Pd/Al2O3催化剂臭氧分解性能的影响可以忽略。Pd/Al2O3催化剂表面Pd纳米粒子的分散度,通过CO-Pulse测试确定。PdAl-a、PdAl-b、PdAl-c和PdAl-d催化剂的分散度逐渐变小,催化剂表面Pd尺寸越来越大,计算得出其粒径分别为4.34 nm、9.28 nm、11.61 nm和16.61 nm。聚集状态的PdO颗粒使得催化剂表面暴露的活性位点数量减少,O3分子吸附位点减少,因此,Pd尺寸越大的催化剂活性越低。
2.3 XRD
γ-Al2O3、PdAl-a、PdAl-b、PdAl-c和PdAl-d的XRD图如图5所示。

图5 1.5%Pd/Al2O3催化剂及Al2O3载体的XRD图
由图5可以看出,所有样品在2θ=45.81°、66.86°和84.93°均出现了γ-Al2O3(JCPDS 75-0921)衍射峰。同时,在PdAl-b、PdAl-c和PdAl-d样品的2θ=33.84°、54.71°和60.17°出现了PdO(JCPDS 75-0584)特征峰。而在样品PdAl-a上并未观察到Pd或是PdO的特征峰,表明该样品表面Pd高度分散,粒径较小。根据2θ=33.84°的PdO特征衍射峰的半峰宽(FWHM),并利用Scherrer公式计算得出PdAl-b、PdAl-c和PdAl-d样品表面PdO颗粒的尺寸分别为8.8 nm、11.7 nm和15.9 nm。推断Pd/Al2O3催化剂的臭氧分解活性依赖表面Pd及PdO尺寸[25]。
2.4 表面形貌
1.5%Pd/Al2O3催化剂的SEM照片如图6所示。由图6可以看出,所有Pd/Al2O3催化剂样品均呈现块状堆积结构,表面的堆积孔提供了反应物和产物吸附和扩散通道。为了进一步确定Pd元素的分布,对催化剂样品进行了SEM EDS测试,结果如图7所示。

图6 Pd/Al2O3催化剂的SEM照片

图7 Pd/Al2O3催化剂的Pd元素分布图
由图7可以看出,Pd元素均可以均匀分散在催化剂样品中,相比而言,PdAl-a样品表面的Pd元素分散度最高,该结果与CO-Pulse测试的结果一致。
Pd/Al2O3催化剂的TEM图如图8所示。由图8可以看出,γ-Al2O3载体具有短棒状结构,PdO呈颗粒状。通过对PdO颗粒进行粒径统计计算,得出PdAl-a、PdAl-b、PdAl-c和PdAl-d样品上PdO颗粒的平均粒径分别为(2.8±0.8) nm、(7.2±1.5) nm、(9.7±1.4) nm和(17.4±2.1) nm,该结果与CO-Pulse和XRD计算的结果基本吻合。

图8 Pd/Al2O3催化剂的TEM图
2.5 表面化学态
通过XPS分析不同1.5%Pd/Al2O3催化剂表面化学状态的差异,结果如图9和表2所示。

图9 Pd/Al2O3催化剂的XPS谱图

表2 不同Pd/Al2O3催化剂的XPS分析结果
由图9的Pd 3d XPS谱图可知,335.3 eV和340.7 eV分别归属于Pd03d5/2和Pd03d3/2的特征峰,而336.5 eV和341.5 eV分别归属于Pd2+3d5/2和Pd2+3d3/2的特征峰[26-28]。在PdAl-a、PdAl-b和PdAl-c样品的表面,同样存在Pd和PdO物种,但PdO含量明显高于Pd,这与XRD测试的结果一致。而在PdAl-d表面则仅存在PdO物种。此外,对催化剂表面Pd/(Pd+PdO)的比例进行分析,发现随着Pd粒径的增大,样品表面Pd/(Pd+PdO)的比值逐渐降低,表明PdO含量增加,Pd0含量降低。催化剂臭氧分解活性与Pd/(Pd+PdO)比例呈正相关,但当催化剂表面仅有PdO时,催化剂亦具有一定的催化活性,可以推断Pd0和Pd2+均是臭氧分解反应的活性位点。由Pd/Al2O3催化剂的表面O1s XPS谱图分析可知,存在三种形态的氧物种,530.0 eV处的晶格氧(OⅠ)、531.0 eV处的表面羟基物种(OⅡ)及533.0 eV处的物理吸附水分子或氧缺陷(OⅢ)[26,29-31]。与具有丰富氧缺陷的锰氧化物催化剂不同,Pd/Al2O3催化剂表面物理吸附或化学吸附的氧物种含量较少,大部分氧物种以晶格氧形式存在,所以氧空穴并不是Pd/Al2O3催化剂分解臭氧的决定因素。但是,随着催化剂臭氧分解性能的提高,OⅡ/(OⅠ+OⅡ+OⅢ)值逐渐减小,即催化剂表面的羟基含量减小。相关研究已证实,锰氧化物表面的羟基物种会影响催化剂活性,且与催化剂失活机理密切相关[29-31]。Liu Y等[29]通过原位红外在Ce-MnO2表面探测到吸附的水分子和羟基基团,通过热处理减少表面羟基含量后,催化剂活性提高。这是因为在金属氧化物催化剂上,随着臭氧分解反应的进行,反应生成的中间氧物种无法及时脱附,同时会与催化剂表面的羟基反应生成H2O,对催化剂有一定的毒害作用,影响催化剂的活性。在Li Y等[32]研究中,Pd/TiO2-450R催化剂表面的羟基含量更多,促进了O2在TiO2表面的活化,成为甲醛在室温下氧化的活性位点,以上研究都表明金属氧化物表面的羟基与O2之间有较强的吸附作用。同样,在Pd/Al2O3催化剂上,随着Pd物种粒径的增加,催化剂表面羟基的含量逐渐提高,当O3分子在催化剂表面发生反应时,产生的O2分子还未及时脱附,就与表面羟基的反应生成了H2O分子,因此对其臭氧分解性能产生影响。
2.6 In situ CO DRIFTS
通过CO原位漫反射红外技术,检测了CO在不同Pd位点上的吸附,获得Pd/Al2O3催化剂表面Pd物种结构。在室温下,CO在Pd/Al2O3催化剂表面吸附30 min,然后用Ar吹扫表面后得到的红外光谱图,如图10所示。不同Pd/Al2O3催化剂的原位红外分析结果如表3所示。
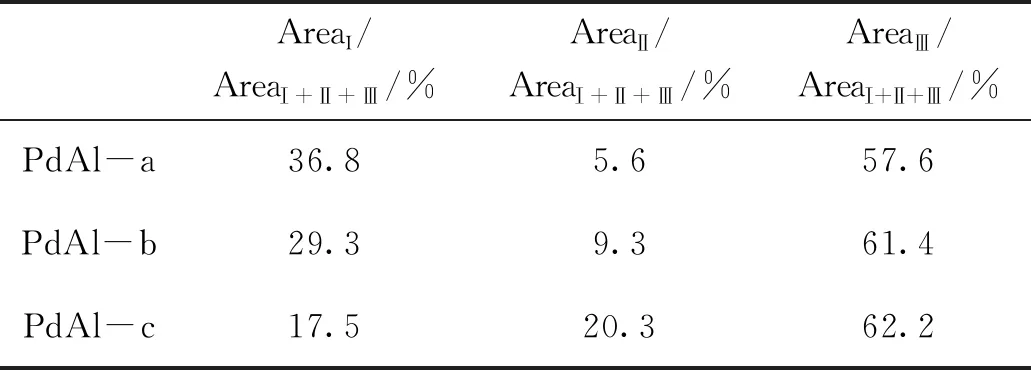
表3 不同Pd/Al2O3催化剂的原位红外分析结果

图10 Pd/Al2O3催化剂的原位CO 红外漫反射谱图
由图10可见,在PdAl-a、PdAl-b和PdAl-c催化剂表面,均检测到三种不同的CO振动吸收峰。(1 900~2 000) cm-1的振动吸收峰,归属于CO桥式吸附,(2 000~2 100) cm-1处的振动吸收峰归属于CO线式吸附[33]。其中,(1 930~1 934) cm-1处CO的吸附位点为Pd(111)晶面桥位和空位;(1 976~1 986) cm-1处吸附位点为Pd纳米簇的(111)/(100)晶面台阶位点;2 090 cm-1处的峰则归属于CO在Pd纳米簇拐角位点上的线式吸附。随着Pd纳米粒子的增大,红外光谱上的振动吸收峰强度明显减弱,特别是在PdAl-d样品上,几乎未检测到明显的CO桥式吸附的吸收峰。将1 930 cm-1、1 986 cm-1和2 090 cm-1处的振动吸收峰积分,峰面积分别记为AreaⅠ、AreaⅡ和AreaⅢ,积分峰面积的总和记为AreaⅠ+Ⅱ+Ⅲ。随着粒径增加,拐角位点上的线式吸附振动峰的峰面积所占比例逐渐由36.8%下降到29.3%,直至17.5%。
2.7 O2-TPD和H2O-TPD
Pd/Al2O3催化剂的O2-TPD和H2O-TPD谱图如图11所示。由O2-TPD谱图可以看出,PdAl-a样品101.1 ℃就出现一个氧气脱附峰,表明其具有强的活性氧物种迁移能力[34]。负载Pd后,Al2O3载体表面出现了更多能够吸附氧物种的位点,从而提高了臭氧分解性能。此外,氧物种的迁移能力也会影响反应过程中中间氧物种的脱附,高的活性氧物种迁移能力有助于提高催化剂的臭氧分解稳定性。

图11 Pd/Al2O3催化剂的O2-TPD和H2O-TPD谱图
通过H2O在催化剂表面的吸脱附实验,可以进一步阐明Pd/Al2O3催化剂耐湿性能的差异。由H2O-TPD谱图可以看出,不同催化剂上水的脱附温度与其耐水性能相关,温度越低,耐水性能越高[31]。4种Pd/Al2O3催化剂中,PdAl-a催化剂的脱附温度最低,峰面积最小;弱的水吸附性能(低的水脱附温度和少的吸水量),能减少H2O分子占据活性位,有助于H2O的脱附,从而提高其耐水性能。H2O分子容易在反应过程中脱附,而不占据反应的活性位点。因此,添加了Pd后的臭氧分解催化剂的抗水性均有提高。
3 结 论
采用等体积浸渍法和乙二醇还原法分别制备了不同Pd含量和不同Pd物种粒径的Pd/Al2O3催化剂。在30 ℃、空速600 000 mL·(gcat·h)-1和相对湿度RH<5%条件下,比较不同催化剂的活性,筛选出负载质量分数1.5%的Pd/Al2O3催化剂在7 h内显示出稳定的臭氧分解活性。在不同粒径的Pd/Al2O3催化剂对比中,使用浸渍法制备的PdAl-a催化剂在低湿度(RH<5%)和较高湿度(RH>90%)时均显示出最高的臭氧分解活性,这与其表面的Pd物种分散度较高和粒径较小有关。同时,Pd/Al2O3催化剂表面的Pd物种均以Pd0和PdO两种形式存在,均是臭氧分解的活性位点。粒径越小,Pd0相对含量越高,位于拐点位置的Pd纳米簇含量也越高,弱酸位点越多,催化剂性能随之提升。Pd的添加主要改善了催化剂对H2O的吸附量和吸附强度,因此改善了催化剂的耐水性能。
