基因检测在指导渝东北地区人工瓣膜术后华法林抗凝的价值
2022-04-28靳云洲潘仲惠
靳云洲 潘仲惠


[摘要] 目的 比较两种华法林剂量预测模式指导用量与实际达标剂量,分析两种预测模式的预测能力,并探讨其临床运用价值。方法 随机选取2020年5月至2021年5月在重庆大学附属三峡医院心脏大血管外科就诊的渝东北地区心脏人工瓣膜置换术后并进行基因检测(CYP2C9&VKORC1)的156例病患,按照基因检测结果分为4组,分别为CYP2C9*3 AA组(142例)、CYP2C9*3 AC组(14例)、VKORC1GA(GG)组(25例)、VKORC1AA组(131例)。分别采用两种不同的预测模式(国际華法林药物遗传学协与中国国家卫生健康委员会推荐的两种预测公式)计算出指导用量,然后将其分别与实际达标剂量对比,分析引起差别的因素,并对比两种预测方式的相关性。结果 1.国际华法林药物遗传学协推荐公式(方案1)与中国国家卫生健康委员会推荐公式(方案2)预测剂量与实际达标剂量的相关性,方案1(R2=0.606**)高于方案2(R2=0.550**);2.CYP2C9 *3 AC组、VKORC1GA(GG)组病例两种预测方案与实际达标剂量相关性不大,方案1相关性分别为(R2=-0.091,R2=0.257),方案2分别为(R2=-0.087,R2=0.304)。3.两种方案预测值及实际达标剂量,CYP2C9 *3 AC组用量显著低于CYP2C9 *3 AA组(P<0.05)、VKORC1GA(GG)组病患用量显著高于VKORC1AA组(P<0.01)。结论 国际预测方案更适合渝东北地区人群,但应警惕突变基因人群的抗凝风险性。
[关键词] 心脏人工瓣膜置换术后;华法林;基因检测;CYP2C9;VKORC1
[中图分类号] R446.1 [文献标识码] A [文章编号] 1673-9701(2022)07-0047-04
Value of genetic testing in guiding warfarin anticoagulation after prosthetic heart valve replacement in northeast Chongqing
JIN Yunzhou PAN Zhonghui
Department of Cardiovascular Surgery, Chongqing University Three Gorges Hospital, Wanzhou 404100, China
[Abstract] Objective To compare the guidance dosage of two warfarin dosage prediction models with the actual compliance dosage, analyze the predictive ability of the two prediction models, and explore their clinical application value. Methods A total of 156 patients underwent genetic testing (CYP2C9 & VKORC1) in the Department of Cardiovascular Surgery of Chongqing University Three Gorges Hospital from May 2020 to May 2021 were randomly selected. According to the test results, they were divided into 4 groups: the CYP2C9*3 AA group (n=142), the CYP2C9*3 AC group (n=14), the VKORC1GA (GG) group (n=25), and the VKORC1AA group (n=131). Two different prediction models (two prediction models recommended by the International Warfarin Pharmacogenetics Consortium and the National Health Commission of the People’s Republic of China) were used to calculate the guidance dosage. The guidance dosages were compared with the actual compliance dosages to analyze the factors that caused the difference. The correlation of the two prediction methods were compared. Results The model 1 (the model recommended by the International Warfarin Pharmacogenetics Consortium) (R2=0.606) had a higher correlation between the guidance dosage and the compliance dosage than the model 2 (the model recommended by the National Health Commission of the People’s Republic of China) (R2=0.550). There were no significant correlations between the guidance dosage and the compliance dosage in the CYP2C9 *3 AC group and the VKORC1GA (GG) group in both models (model 1 R2=-0.091 and R2=0.257, and model 2 R2=-0.087 and R2=0.304). The guidance dosages and actual compliance dosages in both models in the CYP2C9 *3 AC group were significantly lower than those in the CYP2C9 *3 AA group (P<0.05). The guidance dosages and actual compliance dosages in both models in the VKORC1GA (GG) were significantly higher than those in the VKORC1AA group (P<0.01). Conclusion The international prediction model is more suitable for the population in northeast Chongqing, but the risk of anticoagulation in the mutant gene population should be noticed.
[Key words] After prosthetic heart valve replacement; Warfarin; Genetic testing; CYP2C9; VKORC1
心脏人工瓣膜置换术是通过手术用人工瓣膜置换患者病变的瓣膜,以改善患者心功能,降低死亡率[1]。人工瓣膜置换术后患者均需要抗凝治疗[2],然而常用药物华法林安全有效窗口窄,有较高出血及栓塞风险,所以掌握华法林的剂量对降低华法林抗凝风险非常重要[3]。不同人群使华法林用药剂量受体重、年龄、身高、遗传、饮食生活习惯、基础疾病等多种因素影响,最近较多学者认为华法林用药剂量差异与华法林作用靶点CYP2C9、VKORC1 基因的变异有密切关系[4]。为了能更快速、更平稳地达到华法林达标剂量用药,世界范围内制定多种华法林预测方案。目前我国比较流行的是国际华法林药物遗传学协(IWPC)与中国国家卫生健康委员会推荐的两种预测公式。本文现在将这两种的计算公式分别运用于渝东北地区心脏人工瓣膜术后患者,分析两种方案的差异性及临床应用价值,分类汇总分析,现报道如下。
1 资料与方法
1.1 一般资料
随机选取2020年5月至2021年5月在重庆大学附属三峡医院心脏大血管外科就诊的渝东北地区心脏人工瓣膜置换术后并进行基因检测(CYP2C9&VKORC1)的156例病患,男57例,女99例;年龄33~82岁,平均(56.99±8.329)岁;身高141~174 cm,平均(159.12±6.577)cm,体重32~85 kg,平均(58.39±8.967)kg。
1.2 仪器与方法
1.2.1 基因检测 将选出的156例心脏人工瓣膜置换术后患者,采集空腹8 h以上的外周静脉血3 ml,采用荧光定量PCR法将其分组。即检测维生素K环氧化物还原酶亚单位1(vitamin K epoxide reductase com-plex1,VKORC1)(1639G-A)基因和细胞色素P450酶系(cytochrome P450 proteins)CYP2C9*2以及*3位基因。通过对患者CYP2C9及VKORC1基因进行检测后,其中所有患者CYP2C9*2(430>T)均为CC型(野生型)不作分组。CYP2C9*3(1075>C)基因型分成AC(杂合型)组和AA(野生型)组,其中CYP2C9*3 AC组14例(占8.97%),CYP2C9*3 AA组142例(占91.03%);VKORC1(-1639G>A)基因型中GG(野生型)组有3例(占1.92%);GA(杂合型)组有22例(占14.10%),以上25例统一简称VKORC1GA(GG)组,VKORC1 AA(突变型)组有131例(占83.97%)。
1.2.2 华法林达标方法检测 采集患者空腹8 h以上的外周静脉血 3 ml,然后采用凝固法检测患者服用华法林后PT-INR值(血浆凝血酶原时间)。门诊患者记录不同组患者服用华法林后PT-INR值稳定到1.5~2.5时华法林用量为实际达标剂量。住院术后患者记录患者出院时PT-INR稳定在1.5~2.5时华法林用量为实际达标剂量。分别记录体重、年龄、身高、干扰药物用药情况、实际达标剂量进行统计分析。
1.3统计学方法
采用SPSS 23.0软件对数据进行记录并分析。计数资料采用[n(%)]表示,计量资料采用(x±s)表示,独立样本均数的比较采用t检验,多样本均数的比较采用单因素方差分析,两变量相关性分析采用双变量线性回归分析,P<0.05为差异有统计学意义。
2 结果
2.1 各组患者体重、年龄、身高、用药情况比较
近些年研究成果提示,华法林用药剂量个体差异影响因素较多,除了受到个体的年龄、身高、性别及体重、用药情况、手术方式等影响之外,同时还受到CYP2C9、VKORC1等遗传基因变异影响[5-6]。由于华法林抗凝达标剂量受多种因素影响,因此本研究首先选择渝东北片区汉族人群,这样选择主要是减少生活习惯及饮食结构的影响;其次排除有重大疾病病史的病患;然后对选择人群的年龄、身高、体重等进行分析。各组间体重、年龄、身高比较,差异无统计学意义(P>0.05),具有可比性。另外通过记录各组患者常规影响华法林用量的药物观察,本研究病患均无阿司匹林、胺碘酮等用药史。目的是减少非遗传因素对研究结果的影响。见表1。
2.2 各组间华法林用药达标剂量比较
将CYP2C9*3 AC组与CYP2C9*3 AA组,VKORC1 GA(GG)组与VKORC1 AA组分别进行独立样本t检验,检验结果显示差异有统计学意义,其中CYP2C9*3AC组显著低于CYP2C9*3 AA组(P<0.05),VKORC1GA(GG)组显著高于VKORC1 AA组(P<0.0001),表明华法林用药量显著被基因影响,且CYP2C9*3AC组的用量显著较少,约0.5~1片(2.5 mg/片)。VKORC1GA(GG)组用量显著较大,约2~3片。见表2。
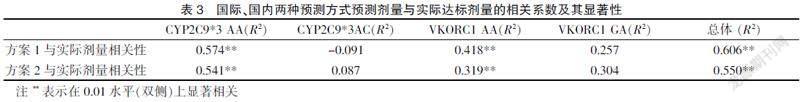
2.3 国际、国内两种预测方式预测剂量与实际达标剂量相关性比较
按照国际华法林药物遗传学协(IWPC)(简称国际)与中国国家卫生健康委员会(簡称国内)推荐的两种预测公式预测的华法林用药剂量(分别为方案1,方案2)与实际达标剂量的相关性对比见表3,由此可以看出两种方案预测值都与实际达标用量值显著相关,且国际预测值相关性较国内预测值更高。VKORC1 AA组及CYP2C9*3 AA组的两种预测方案都与实际达标值明显相关,国际预测值相关性更高。但是突变基因无论是CYP2C9*3AC组还是VKORC1GA(GG)组均与两种预测方案无相关性。
3 讨论
由于現代医学尤其是药物基因学的快速发展,在检测华法林作用靶点基因CYP2C9、VKORC1多态性的基础上,建立华法林用药预测方案成为了一个热点话题[7]。国外不少学者提出在基因检测的基础上创建华法林用药预测方案,其计算出的华法林的抗凝初始预测剂量与实际达标剂量更为贴近,能使患者快速地达到实际达标剂量,减少抗凝并发症[8]。多数学者认为,华法林抗凝效果受体重、年龄、身高、吸烟、饮酒、用药、基础疾病及遗传因素等多种因素影响。但是本研究入组病例,减小了体重、年龄、身高、生活饮食习惯、用药及基础疾病影响,采用基因检测技术将患者分为4组,分别为:CYP2C9 *3AC组、CYP2C9*3 AA组、VKORC1GA(GG)组、VKORC1 AA组。通过对其基因对比分析,得出突变基因显著影响华法林用量,其中CYP2C9*3AC组华法林达标剂量显著小于其他几组。有学者认为CYP2C9*3AC组基因组导致华法林药理学活性增加2.7~3.8倍[9]。由于本研究检测该基因突变为AC仅仅只有14例,需要更大样本数据来印证。VKORC1GA(GG)组华法林达标剂量显著高于其他几组。与丁征等(2020)[9-10]研究结论一致,即针对VKORC1基因型患者,至少携带1个G等位基因的患者,在其术后第2,3,4天的华法林总剂量较VKORC1-1639AA型明显更高[10]。针对VKORC1GA(GG)组患者给予一个较高的起始量估计达到达标剂量的速度更快。CYP2C9*3AC组基因型患者给予一个较低的起始量估计更加安全,这与陈洪晔等[11](2017)提出检测出CYP2C9 *3AC患者,并给予一个较低初始剂量,容易减少出血风险,尽快达到达标剂量,提供患者生存率一致。
通过各组患者两种方案预测剂量与实际达标剂量对比分析,总体来说两种方案都与实际达标剂量显著相关,但是国际华法林药物遗传学协(IWPC)的预测方案与实际达标剂量的相关性更高,其相关性高体现在未突变基因组。分析原因:目前华法林基因的研究仍然是一个热点研究[12],除了比较明确的CYP2C9 与VKORC1基因对华法林剂量的影响较大之外,还有其他基因比如CYP4F2、CYP2C基因簇(rs12777823) 等也可能影响华法林的用量,所以基因检测后再给予华法林用量预测有多大益处没有明确的定论[13-14]。因此也有学者提出不建议在使用华法林前常规进行基因检测,但在何种情况下需要进行基因检测下指导用药,却没有一致意见[15]。综合个人认为,以上两种基因型对华法林基因用量影响明显,突变基因差异较大。如果提前预测基因型,能更加警惕华法林用量不符导致的抗凝并发症。目前制约基因检测的原因主要还是费用较贵,医保不能报销[10]。但如果能降低检测费用,纳入医保,建议还是抗凝前给予预测基因型。
通过以上分析得出结论:①国际华法林药物遗传学协(IWPC)的预测方案比中国国家卫健委推荐的方案更加适合渝东北心脏人工瓣膜术后人群。②基因检测提示CYP2C9 *3AC组患者,可能需要更小剂量的实际达标剂量;VKORC1GA(GG)组的患者可能需要更加大剂量的实际达标剂量。③针对突变基因,目前两种预测方式与实际达标剂量相关性不显著,仍需要随时警惕其是否抗凝达标。④因为基因检测费用较高,医保不能报销。目前各种预测方案预测能力有限,不推荐大规模常规性检测。
[参考文献]
[1] 马建新,董兵,马建慧,等.CYP2C9和CYP4F2基因多态性对瓣膜置换术后华法林维持剂量的影响[J].实用医学杂志,2017,33(7):1120-1123.
[2] 吴宣,许雪清,汪家淑,等.不同剂量利伐沙班与华法林对高龄非瓣膜性心房颤动患者的抗凝治疗效果及安全性比较[J].中国当代医药,2021,28(3):90-94.
[3] 樊晖晖,范吉利,李宇,等.临床药师指导不同年龄段抗凝患者华法林治疗的效果分析[J].中国医药科学,2021, 11(10):68-70,74.
[4] 王威丽,张阳,李兴德,等.CYP2C9和VKORC1基因多态性对华法林抗凝疗效的影响[J].中国药物评价,2021, 38(1):25-29.
[5] 刘芃菲,卓钟灵,苏明,等.中国汉族人群CYP2C9 及VKORC1 基因多态性及其对华法林用药剂量的相关性研究[J].中华检验医学杂志,2020,43(1): 71-77.
[6] 杨思芸,梁婧,唐志立,等.川东北CYP2C9 和VKORC1 基因多态性对华法林剂量的影响[J].中国药业,2019, 28(5):30-32.
[7] 张舒羽,许哲,周守宁,等.VKORC1 和CYP2C9 基因多态性对华法林抗凝初期维持剂量及剂量波动的影响[J].中国医药导报,2019,16(30):34-36.
[8] Pengo V,Zambon CF,Fogar P,et al. A randomized trial of pharmacogenetic warfarin dosing in native patients with non-valvular atrial fibrillation[J].PLoS One,2015,10(12):e0145318.
[9] Khalighi K,Cheng G,Mirabbasi S,et al. Linkage dise- quilibrium between the CYP2C19*2,*17 and CYP2C9*1 alleles and impact of VKORC1,CYP2C9,CYP2C19 gene polymorphisms and gene- gene interactions on warfarin therapy[J].J Thromb Thrombolysis,2017,43(1):124-129.
[10] 丁征,闫婷婷,芦梦,等.VKORC1 基因分型对华法林初始抗凝治疗的影响和临床指导意义[J].药学与临床研究,2020,28(2):113-115.
[11] 陈洪晔,于波,谭启明,等.不同CYP2C9 及GGCX 基因型在人工瓣膜置换术后的抗凝效果比较[J].中国现代医学杂志,2017,27(18): 62-65.
[12] 钱正月,翟振国,赵莉.华法林个体化基因检测临床应用分析[J].心血管病学进展,2019,40(3):433-436.
[13] Munir P,Girvan B,Niclas E, et al. A randomized trial of genotype-guided dosing of warfarin[J].N Engl J Med,2013, 369( 24) : 2295-2303.
[14] Perera MA,Cavallari LH,Limdi NA, et al. Genetic var- iants associated with warfarin dose in African-American individuals:A genome-wide association study[J].Lancet,2013,382(9894):790-796.
[15] Johnson JA,Caudle KE,Gong L,et al. Clinical pharmac-ogenetics implementation consortium(CPIC) guideline for pharmacogenetics-guided warfarin dosing:2017 update[J]. Clin Pharmacol Ther,2017,102(3): 397-404.
(收稿日期:2021-10-08)
