分散液液微萃取–高效液相色谱法测定尿液中的阿替洛尔
2022-04-25刘红莉苗会娟张晨轩
刘红莉,苗会娟,张晨轩
(1.河北省药品职业化检查员总队,石家庄 050000; 2.河北省药品医疗器械检验研究院,石家庄 050000)
阿替洛尔是一种β 受体阻滞剂,用于治疗高血压﹑心绞痛和心肌梗死等疾病,在体内难以降解[1]。目前,阿替洛尔常用的检测方法有光谱方法﹑薄层色谱法﹑毛细管电泳﹑气相色谱法和液相色谱法等[2]。高效液相色谱法具有样品准备时间短﹑无需衍生化﹑多种物质可同时分析等优点,已成为测定阿替洛尔含量的重要手段。建立尿液中β 受体阻滞剂的快速检测方法具有较高的应用价值和较强的现实需求。样品处理是检测过程不可缺少的步骤,也是最耗时的环节。微萃取技术是一种新型的前处理技术,因其简便﹑快速﹑廉价﹑高回收率和高富集因子等优点,在提取痕量药物方面已经引起广泛关注[3]。分散液液微萃取基于由水相﹑非极性萃取溶剂﹑极性分散溶剂组成的三元溶剂组分体系,通过微升体积的萃取剂分散在溶液中,瞬间完成萃取[4–5]。分散液液微萃取因其简便﹑溶剂消耗少﹑浓缩能力强等优点,在尿液和血液等多种生物基质中均有应用[6]。然而,分散液液微萃取具有萃取剂毒性大﹑萃取剂不易收集等缺点。离子液体是一种新型溶剂,它是由有机阳离子与各种阴离子结合成的液体盐[7]。离子液体具有优异的性能,如高热稳定性﹑较宽的液态温度范围﹑相对较高的粘度以及能够溶解多种化合物[8]。离子液体也以其良好的溶剂化性质而闻名,蒸气压可忽略不计,而且毒性相对较低,被认为是良好的绿色溶剂[9]。离子液体迄今已成功用于多种微萃取技术,将离子液体与分散液液微萃取技术相结合,替代分散液液微萃取中所使用的高毒性萃取剂具有重要意义[10]。
离心步骤是收集萃取剂时最耗时的步骤,一般需要十分钟以上[11]。在离心后,萃取剂相和样品溶液相的界面不易观察,萃取剂相不易充分收集,从而影响整个方法的提取收率。利用萃取剂和样品溶液凝固点的差异,通过降温,将其中一相转化为固体,可以简化耗时的离心步骤,基于固液分离的原理高效充分地收集到萃取剂相,提高萃取效率。
笔者建立了离子液体–分散液液微萃取结合高效液相色谱–二极管阵列检测器测定尿液中阿替洛尔的方法。通过离子液体在样品中的分散实现了对阿替洛尔的萃取,优化了萃取条件,并将此方法应用于分析尿液样本中的痕量药物阿替洛尔。
1 实验部分
1.1 主要仪器与试剂
高效液相色谱仪:安捷伦1260 型,美国安捷伦科技有限公司。
阿替洛尔:纯度(质量分数)为98%,上海阿拉丁生化科技股份有限公司。
1-丁基-3-甲基咪唑六氟磷酸盐:纯度(质量分数)为97%,阿拉丁生化科技股份有限公司。
1-丁基-3-甲基咪唑四氟硼酸盐:纯度(质量分数)为97%,上海阿拉丁生化科技股份有限公司。
甲醇﹑乙腈和丙酮:色谱纯,上海阿拉丁生化科技股份有限公司。
1.2 色谱条件
色谱柱:Agilent ZORBAX SB–C18型色谱柱(250 mm×4.6 mm,5 μm,美国安捷伦科技有限公司);进样体积:20 µL;流动相:乙腈–0.1 moL/L磷酸缓冲溶液(pH 3.1),体积比为40∶60,流量为1.2 mL/min;检测波长:228 nm。
1.3 样品处理
将80 μL 的离子液体萃取剂1-丁基-3-甲基咪唑六氟磷酸盐和800 μL 的乙腈分散剂混合溶液快速注入含有5 mL 未经处理待测尿液的离心管中,离子液体1-丁基-3-甲基咪唑六氟磷酸盐均匀的分散在样品溶液中并完成萃取。将离心管转移到4 ℃的冰箱后,充分收集固化在离心管下层的1-丁基-3-甲基咪唑六氟磷酸盐,待其在室温融化后进样至高效液相色谱仪中进行定量分析。
2 结果与讨论
2.1 萃取条件的优化
为了获得最佳的提取条件,进行了一系列实验来研究提取条件对提取效率的影响,包括萃取剂的种类和体积﹑分散剂的种类和体积以及盐等影响因素。
2.1.1 萃取剂选择
在分散液液微萃取过程中,选择合适的萃取剂是影响提取效率的首要因素。萃取剂应具有比水密度大﹑在水中溶解度低﹑对目标分析物的萃取能力强等特点[12]。基于以上条件,笔者选取离子液体1-丁基-3-甲基咪唑六氟磷酸盐和1-丁基-3-甲基咪唑四氟硼酸盐作为萃取剂。结果表明,1-丁基-3-甲基咪唑六氟磷酸盐作为萃取剂表现出更高的萃取效率。因此选择1-丁基-3-甲基咪唑六氟磷酸盐作为萃取剂。
2.1.2 萃取剂体积选择
萃取剂的使用量是影响萃取回收率的重要因素,萃取剂过少会降低萃取效率,萃取剂过多会降低方法的灵敏度[13]。选取离子液体体积分别为50﹑60﹑70﹑80﹑90﹑100 μL 进行试验,结果见图1。

图1 离子液体体积对萃取效率的影响
由图1 可知,随着离子液体用量从50 μL 增加到80 μL,萃取效率显著提高,继续增加萃取剂的体积,萃取效率保持不变。因此,选择80 μL 的1-丁基-3-甲基咪唑六氟磷酸盐作为萃取剂。
2.1.3 分散剂选择
在分散液液微萃取过程中,萃取剂在分散剂的帮助下形成小液滴,增加与样品的接触面积,从而实现高效的萃取[14]。本实验选取了甲醇﹑乙腈和丙酮三种分散剂,比较其分散效果。结果表明,乙腈的分散能力显著高于甲醇和丙酮的分散能力,当乙腈作为分散剂时,提取效率较高。因此,选择乙腈作为萃取剂1-丁基-3-甲基咪唑六氟磷酸盐的分散剂。
2.1.4 分散剂体积选择
分散剂的体积也是影响萃取效率的重要因素。由于萃取剂是疏水的,只有足量的分散剂才能保证萃取剂在样品溶液中均匀分散,否则,由于分散剂体积不足,不能形成稳定的乳液体系,导致萃取效率下降[15]。选取分散剂的体积分别为200﹑400﹑600﹑800﹑1000﹑1200 μL 进行试验,结果见图2。由图2可知,分散剂用量从200 μL 增加到800 μL,萃取效率逐渐升高,继续增加分散剂的量,萃取效率逐渐降低。因此选择800 μL 的乙腈作为分散剂。

图2 乙腈体积对萃取效率的影响
2.1.5 盐的影响
加入盐会降低阿替洛尔在水溶液样品中的溶解度,促使阿替洛尔分配到有机相中,产生盐析效应[16]。另外,加入盐会改变离子强度,可能影响离子液体对阿替洛尔的萃取性能。本实验选取氯化钠的添加量分别为0﹑200﹑400﹑600﹑800﹑1 000﹑1 200 mg 进行试验,结果表明,随着氯化钠用量的增加,萃取效率没有显著的升高。因此本实验在分散液液微萃取过程中不添加氯化钠。
2.1.6 pH 选择
阿替洛尔在样品溶液中的存在形态常受pH 值的影响,pH 值影响阿替洛尔的分配系数从而改变阿替洛尔的提取效率。本实验调节样品溶液的pH值分别为3﹑5﹑7﹑9﹑11 进行试验。结果表明,随着pH 值的变化,阿替洛尔的萃取效率没有出现显著的变化。因此本实验在分散液液微萃取前无需调节样品的pH 值。
2.2 线性方程与检出限
为了评估本方法的分析性能,在最佳萃取条件下进行了线性﹑定量限和检出限的评价。用甲醇配制质量浓度为100 μg/mL 的阿替洛尔标准储备液,并逐级稀释制备不同浓度的加标尿液样品(0.01﹑0.02﹑0.1﹑0.2﹑1 μg/mL)考察本方法的线性关系,绘制了平均色谱峰面积对样品质量浓度的标准曲线。阿替洛尔在0.01~1 μg/mL 范围内与色谱峰面积具有良好的线性关系,以阿替洛尔的质量浓度(x,μg/mL)为横坐标,以色谱峰面积(y)为纵坐标绘制标准工作曲线,线性方程为y=328.6x+1.211,相关系数为0.995。以信噪比(S/N)分别为3 和10 计算,得检出限和定量限分别为0.003﹑0.010 μg/mL。
为了评估本方法的重复性,连续5 天对阿替洛尔样品进行重复测定,计算日间精密度。同一天内在5 个不同时间对阿替洛尔样品进行重复测定,计算日内精密度。日间试验的回收率分别为93.0%﹑94.2%﹑99.7%﹑103.8%﹑105.7%,精密度为5.7%(n=5);日内试验的回收率分别为94.1﹑94.4﹑99.8﹑101.8﹑103.2,精密度为4.3%(n=5),结果表明,所建立的方法具有良好的重复性。
2.3 加标回收与精密度试验
将本方法应用于尿液中阿替洛尔的定量分析以评估其准确性和适用性。尿液样品通过分散液液微萃取法提取,用高效液相色谱仪进行定量分析。在最佳萃取条件下进行了0.01﹑0.1﹑1 μg/mL 三个浓度的加标回收与精密度试验。标准色谱图与样品加标色谱图分别见图3﹑图4,加标回收与精密度试验结果如表1 所示。由表1 可知,阿替洛尔在尿样中的回收率为94.1%~101.6%,相对标准偏差为0.4%~3.9%(n=5),结果表明本方法具有良好的准确性和适用性。

表1 加标回收与精密度试验结果
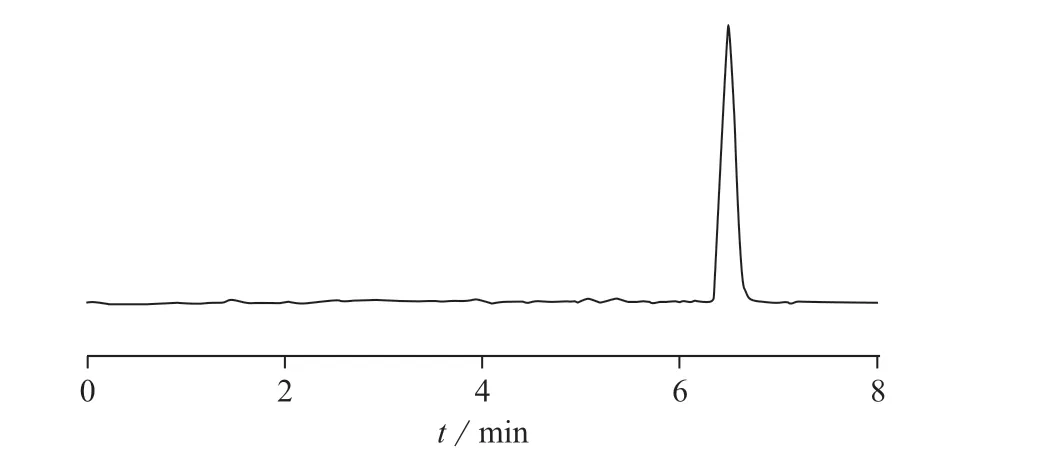
图3 标准溶液色谱图

图4 样品加标色谱图
3 结语
提出了一种结合离子液体和分散液液微萃取优点的新型样品处理技术,并采用固液分离方法收集萃取剂,应用高效液相色谱仪检测尿液中的阿替洛尔。在该方法中,萃取剂离子液体1-丁基-3-甲基咪唑六氟磷酸盐以微小液滴的形式分散到样本溶液中,快速高效地完成了萃取,同时避免使用高挥发性和高毒性的传统萃取溶剂。无需耗时的离心步骤便可实现萃取剂的高效收集。在最优的萃取条件下,本方法表现出了良好的线性﹑灵敏度﹑提取效率和重复性。离子液体–分散液液微萃取是一种简单﹑快速﹑高效的前处理方法,可用于生物样本中痕量药物的分析。
