帕金森病嗅觉识别障碍的临床特点及影响因素
2022-04-25翟志远郑金龙薛刘军
黄 悦 翟志远 郑金龙 薛刘军
1)徐州医科大学淮安临床学院,江苏 徐州 223300 2)南京医科大学附属淮安第一医院,江苏淮安 223300
帕金森病(Parkinson’s disease,PD)是一种临床表现具有广泛异质性的神经退行性疾病,可或先或后表现为不同的运动症状或(和)不同的非运动症状[1]。PD常见的运动症状包括运动迟缓、静止性震颤、肌强直和姿势步态不稳等,而非运动症状主要有嗅觉障碍(olfactory dysfunction,OD)、情绪障碍和自主神经障碍等,其中嗅觉障碍可早于典型运动症状5~10 a 出现,且约70%帕金森病人出现嗅觉障碍[2-3]。PD的嗅觉功能障碍主要涉及嗅觉阈值、嗅觉辨别、嗅觉识别和嗅觉记忆4个方面[4]。多项研究表明,嗅觉识别测试在诊断PD时较其他嗅觉功能测试具有更高的敏感性和特异性[5-7],此外,PD 患者的嗅觉识别障碍可能具有气味选择性[8],且伴嗅觉障碍的PD 患者可能具有一定的临床特征[9-10]。本研究旨在探讨PD患者嗅觉识别功能的临床特点及影响因素,为PD的临床评估和诊治提供指导。
1 对象与方法
1.1 研究对象 选取2019-09—2021-10 淮安市第一人民医院就诊的54例PD患者为研究对象,另选择同期健康检查者20名为对照组。PD患者纳入标准:(1)符合《中国帕金森病的诊断标准(2016 版)》中的PD 诊断标准。PD 组和对照组的排除标准:(1)嗅觉检测前2 周内有上呼吸道感染史;(2)既往有慢性鼻窦炎、鼻外伤或鼻窦疾病史者;(3)认知功能受损者[中学教育程度者:简易精神状态量表(mini-mental state examination,MMSE)<24 分;小学教育程度者<20分;文盲<17分];(4)伴精神疾病史及其他可能影响嗅觉功能的疾病,如精神分裂症、阿尔兹海默症、多发性硬化等。所有研究对象及家属签署知情同意书。
1.2 方法
1.2.1 资料收集:记录2组受试者的年龄、性别、吸烟史等基线资料,以及PD 患者病程、左旋多巴等效剂量(levodopa equivalent doses,LEDD)等临床资料。
1.2.2 嗅觉评估:采用江苏金森海默生物技术有限公司生产的PD嗅觉障碍辅助诊断卡(金帕默)评估受试者的嗅觉功能,该诊断卡由12种中国人群日常生活密切接触物品的气味测试卡片(嗅觉测试蜡块)组成,每个测试片题干均有4个备选答案,选出正确选项记一分,12道选项正确答案分别为香蕉、苹果、大料/八角茴香、玫瑰、菠萝、柠檬、酸奶/牛奶、薄荷、树脂、樟脑、木头、大蒜,该诊断方法共12分,总分<8分的PD患者纳入PD伴OD(PD with OD,PD-OD)组,总分≥8分PD患者纳入PD-NOD(PD with no OD,PD-NOD)组。
1.2.3 分型分期及非运动症状评估:(1)分型分期评估:所有患者均在“开”期时进行评估:依据统一帕金森病评定量表(unified Parkinson’s disease rating scale,UPDRS)中的震颤部分和非震颤部分评分平均值之比将患者分为震颤为主型(tremor dominant,TD),姿势不稳/步态障碍型(postural instability/gait difficulty,PIGD)和混合型(mixed type,MXT)亚组,当震颤项目平均分与非震颤评分比值≥1.5时,将病人归为TD 组,比值≤1 时归为PIGD 组,其余病人归为MXT 组,震颤评分包括项目震颤(2.16)和静止性震颤(3.20)、手部动作或姿势震颤(3.21),非震颤评分包括项目跌跤(2.13)、行走中冻结(2.14)、行走(2.15)、步态(3.29)、姿势的稳定性(3.30)[11]。运用修正的Hoehn-Yahr(H-Y)分级量表评估帕金森病人疾病严重程度。(2)非运动症状评估:依据罗马Ⅲ功能性便秘诊断标准评判患者是否存在便秘,运用Wexner 便秘评分系统对患者便秘程度进行评估,得分越高,便秘程度越严重。运用汉密尔顿抑郁量表(Hamilton depression scale,HAMD)-24项版本评估患者抑郁程度,HAMD≥8分判定为有抑郁症状。汉密尔顿焦量表(Hamilton anxiety scale,HAMA)-14 项版本评估患者焦虑程度,HAMA≥7 分判定为存在焦虑症状。运用快速眼动期睡眠行为障碍筛查问卷(rapid eye movement sleep behavior disorder screening questionnaire,RBDSQ)评估患者是否存在快速眼动期睡眠行为障碍(rapid eye movement sleep behavior disorder,RBD),评分≥6分判断存在RBD。
1.3 统计学处理 采用SPSS 25.0 统计学软件进行数据处理,符合正态分布的计量资料采用均数±标准差(±s)表示,非正态分布数据采用M(P25,P75)表示,分类变量采用n(%)表示。当资料符合正态分布及方差齐性时,组间比较采用两独立样本t 检验;不符合正态分布或方差齐性的资料采用非参数检验,组间比较采用Mann-Whitney U检验。分类变量采用卡方检验。采用Logistic 回归分析PD 患者嗅觉减退的影响因素。P<0.05为差异有统计学意义。
2 结果
2.1 PD 患者与对照组各项气味识别正确率比较PD 组和对照组性别构成、年龄、是否吸烟方面比较差异无统计学意义(P>0.05),PD组嗅觉得分较对照组低且差异有统计学意义(P<0.05),见表1。PD 患者与对照组相比,嗅觉评分中12 种气味选项的正确率均低,其中在苹果、玫瑰、薄荷、木头气味选项上差异有统计学意义(P<0.05),见图1。

表1 PD患者及对照组人口学资料及临床资料比较Table 1 Comparison of demographic and clinical data between PD patients and control group
2.2 伴和不伴嗅觉识别障碍PD 患者临床特征比较 PD患者中伴嗅觉障碍者40例(74.1%),PD伴嗅觉障碍组性别组成、年龄、病程、H-Y分期、LEDD、吸烟者占比与PD不伴嗅觉障碍组相比,差异无统计学意义(P>0.05);PD 伴嗅觉障碍组PIGD 型占比、便秘、HAMD、HAMA、RBDSQ 得分较PD 不伴嗅觉障碍组均高,差异有统计学意义(P<0.05)。见表2。
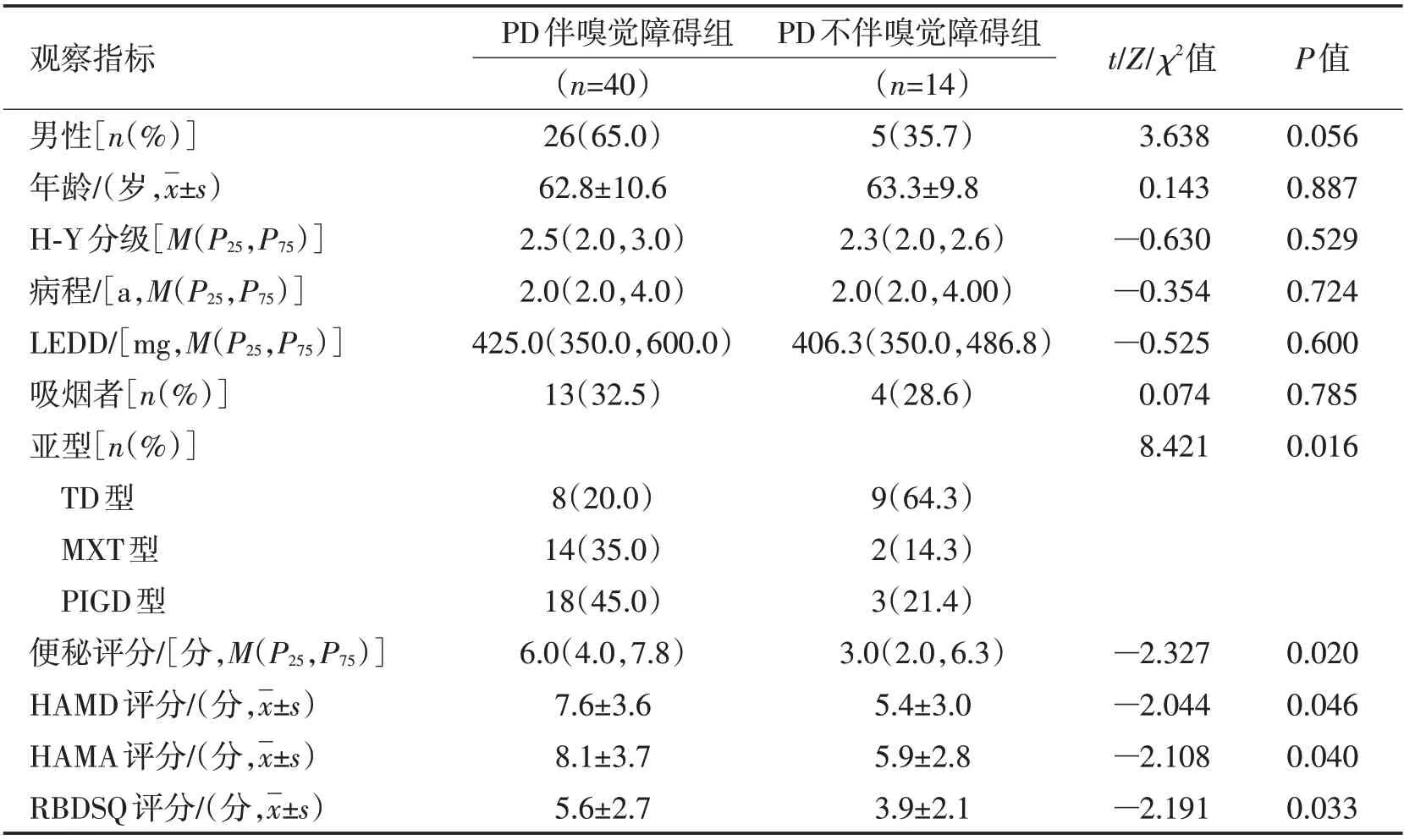
表2 伴和不伴嗅觉障碍PD患者组间人口学资料及临床资料比较Table 2 Comparison of demographic and clinical data between PD patients with and without olfactory disorder
2.3 伴和不伴嗅觉识别障碍PD 患者焦虑、抑郁、RBD 患病率比较 PD 伴嗅觉障碍组患者焦虑、便秘、RBD 发生率高于PD 不伴嗅觉障碍组,差异有统计学意义(P<0.05),2 组抑郁发生率比较差异无统计学意义(P>0.05),见表3。

表3 伴和不伴嗅觉障碍PD患者组间非运动症状患病率比较 [n(%)]Table 3 Comparison of the prevalence of non-motor symptoms between groups of PD patients with and without olfactory dysfunction [n(%)]
2.4 PD 患者嗅觉识别影响因素分析 将上述组间对比差异有统计学意义的焦虑、抑郁、RBD、便秘、TD亚型作为协变量,以嗅觉识别得分作为因变量做有序Logistic 回归分析,结果显示,TD亚型、无便秘是PD嗅觉识别功能的保护因素,而RBD得分为PD嗅觉识别功能的危险因素(P<0.05),见表4。

表4 PD患者嗅觉识别功能的影响因素分析Table 4 Analysis of influencing factors on olfactory recognition function in PD patients
3 讨论
本研究发现,PD患者的嗅觉识别能力较正常对照组减低,苹果、玫瑰、木头、薄荷气味选项用于区分PD 患者和正常对照组较为有效。伴嗅觉识别障碍的PD 患者非运动症状,如焦虑、抑郁、RBD、便秘程度较不伴嗅觉障碍的PD患者程度重,便秘和疾病亚型、RBD可能是影响PD患者嗅觉功能的因素。
嗅觉功能主要包括嗅觉阈值、嗅觉辨别、嗅觉识别和嗅觉记忆4个方面,PD患者嗅觉功能较正常对照全面减退[5,12],上述四方面功能均可通过嗅觉物理心理测试检测。研究证实,嗅觉识别测试在诊断PD时较其他嗅觉功能测试具有更高的敏感性和特异性[5-7],上述结果可能与嗅觉识别编码过程的脑域最为复杂有关,参与脑域包括内嗅皮质、海马、岛叶、眶额皮质、额下回、梨状皮质、丘脑和杏仁核等[13],上述任一部位受累均可能导致PD 患者出现嗅觉识别障碍。此外,嗅觉识别检测耗时相对较短、检测步骤相对简单[14],因此,在PD 的嗅觉障碍检测中的应用最为广泛[4]。本研究采用的帕金森病嗅觉障碍辅助诊断卡可用于评估受试者的嗅觉识别功能,得分情况与嗅觉功能相关,能初步判断嗅觉受损程度。一项针对中国PD 群体的病例对照研究表明,β-苯乙醇(表现为玫瑰气味)和异戊酸(表现为汗味)用于识别PD及正常对照组的敏感性较高[15]。另一项于多中心开展的大型研究将Sniffin’s ticks嗅觉检测法中16项气味选项替换为该测试法中8 项最佳识别气味选项(甘草、茴香、薄荷、肉桂、香蕉、菠萝、玫瑰和咖啡)后,新方法用于区分PD 及对照组时仍具有较高的敏感性(83.3%)和特异性(82.0%)[16]。本研究使用的嗅觉障碍辅助诊断卡中苹果、玫瑰、木头、薄荷气味选项正确率在PD组及对照组的对比差异有统计学意义,提示该4 项气味用于鉴别PD 患者时作用最佳,但本研究涉及的PD患者及正常患者样本量均较小,未来需要开展更大规模的研究探讨最佳嗅素,进一步优化嗅觉测试量表、确立PD患者嗅觉障碍界定值。
国内外已有研究表明,PD伴嗅觉障碍者可能具有一定的临床特征。疾病亚型可能影响PD嗅觉功能,伊朗的一项研究对104例PD患者行伊朗嗅觉识别测试,结果显示,TD组患者嗅觉得分高于PIGD组[17]。韩国的一项研究使用跨文化嗅觉鉴定试验对98 例PD 患者行嗅觉评估发现,嗅觉正常的PD 患者多表现为TD型[18]。同时期的大量临床研究表明,PIGD型患者除表现为更重的嗅觉障碍外,疾病进展更迅速,还具有更多的焦虑、抑郁倾向及更重的便秘表现[19-21]。既往关于PD 疾病亚型的病理学、影像学研究表明,与TD型患者相比,PIGD型患者存在更为严重的弥漫性神经变性[22-24],推测这也是导致不同预后的原因。本研究结果与上述研究结果一致,但由于PD亚型随病程进展可能改变[25],因此,疾病亚型与PD 嗅觉功能关系的研究不能局限于横断面,而应进行长时间随访观察。
目前PD 嗅觉障碍的发病机制尚不明确,根据Braak假说,α-突触核蛋白异常折叠形成的路易小体首先出现于嗅球及前嗅核、肠道黏膜下神经丛等部位,此即Braak病理分期一期。随着PD病情进展,路易小体逐步逆行至中脑黑质及大脑皮质[26],依据该假说,嗅觉及肠道系统的最先累及可导致嗅觉障碍及便秘症状的早期出现。大量临床研究也表明,PD患者的便秘症状与嗅觉障碍密切相关[27-29]。本研究表明,便秘是PD 嗅觉障碍的影响因素,依据脑肠轴理论,肠道微生物群可通过神经、内分泌、免疫等过程介导中枢神经系统和肠神经系统之间的双向交流[30],推测肠道微生物群失衡不但表现为便秘症状,还可向上累及梨状皮层、杏仁核等嗅觉中枢从而加重嗅觉障碍。
现有研究表明,PD患者的情绪障碍可能与嗅觉障碍有关。一项针对中国PD 人群的病例对照研究表明,伴嗅觉障碍的PD 患者HAMD-17 评分高于不伴嗅觉障碍的PD 患者[31]。荷兰的一项研究则提示PD患者嗅觉得分与抑郁、焦虑得分具有显著的负相关性[32]。参与PD 情绪障碍的神经回路包括额顶叶皮层、杏仁核、纹状体、内侧丘脑、颞叶、前扣带回和边缘区域[33],上述区域的代谢减低、功能失调均可能导致PD患者出现焦虑、抑郁症状[34],额叶眶回、杏仁核、边缘叶海马旁回同样参与嗅觉信号传导,故共同神经传导通路的受累可能解释PD 嗅觉障碍和情绪障碍关联的产生[34]。
RBD 作为共核蛋白病中常见的非运动症状,它的出现不但可预测疾病的发生,对预后评估也具有潜在价值。日本的一项病例对照研究显示,伴RBD的PD患者嗅觉识别得分显著低于不伴RBD的PD患者[35]。RBD 主要以快速眼动(rapid eyemovment,REM)睡眠期肌肉迟缓消失为表现,控制REM 睡眠期肌张力的神经网络主要包括脑桥背外侧被盖下核及桥脚核,上述结构均存在大量胆碱能受体分布,而边缘系统胆碱能神经元又在嗅觉传导中发挥重要作用,因此,PD 嗅觉障碍与RBD 相关的机制可能与胆碱能通路损伤有关。
苹果、玫瑰、木头、薄荷气味选项用于辨识PD的嗅觉识别障碍最为有效,伴嗅觉识别障碍的PD患者其焦虑、抑郁、RBD等非运动症状更重,疾病亚型、便秘、RBD可能是PD嗅觉识别的影响因素。在临床实践中,不应忽略PD 存在的嗅觉障碍,对于存在嗅觉障碍的PD 患者应更加关注其可能的亚型分组及合并存在的便秘、抑郁、RBD症状。
本研究仍存在一些不足:(1)样本量偏小;(2)PD嗅觉功能的4 个方面,本研究只评估了嗅觉识别部分,未来如果有条件可行完整评估,并分别探讨嗅觉其他部分与其他临床特征的相关性;(3)本文是基于横断面的研究,未对病人进行随访评估,因此未能探讨嗅觉功能与疾病进展的关系。总之,关于PD嗅觉功能障碍的病理改变、嗅觉功能障碍与PD其他症状的关系及其机制目前仍有待进一步探讨。
