人β- 防御素- 3调控呼吸道合胞病毒致哮喘幼鼠的气道重塑及白细胞激活
2022-04-25蔡昌君黄惠敏桂冬梅尹杨艳
蔡昌君,黄惠敏,桂冬梅,尹杨艳
(海南医学院第一附属医院 儿科,海南 海口 570100)
哮喘是一种常见的气道慢性炎症性疾病,近年来该疾病在全球范围内发病率急剧增加,且在儿童期发病率最高。呼吸道合胞病毒(respiratory syncytial virus,RSV)、鼻病毒(rhinovirus,RV)和流感病毒(influenza,FLU)是小儿哮喘发作的重要诱因。85%的哮喘急性发作与RSV感染有关,RSV感染是哮喘反复发作和加重的独立危险因素,能够诱导哮喘恶化如促进炎症反应、气道高反应性和气道重塑[1- 2]。目前,糖皮质激素和白三烯调节剂作为防治RSV诱发哮喘的主要药物,对控制哮喘症状、减少哮喘急性发作次数有一定作用[3]。然而这些药物并不能完全治愈哮喘,还存在各种副作用,因此迫切需要寻找安全有效的哮喘临床治疗方法。
人β- 防御素- 3(human β- defensin- 3,hBD3)是一种由45个氨基酸组成的小分子阳离子抗菌肽,具有抗菌谱广、活性高、安全性好等特点,还能联系固有的免疫应答,因此被研究者们认为是最有前途的抗菌肽之一[4]。此外,hBD3表现出多种宿主防御功能,参与心血管疾病、胃肠道感染及关节炎等病理过程[5- 7],但是其在哮喘中的潜在作用及相关机制尚不明确。本研究采用卵清白蛋白(OVA)合并RSV感染建立幼鼠哮喘模型,观察hBD3对哮喘幼鼠疾病过程的影响,以期阐明其在支气管气道重塑和白细胞激活方面发挥的作用及其可能机制,为哮喘诊疗研究提供实验依据。
1 材料与方法
1.1 实验动物
健康、SPF级BALB/c幼鼠,4周龄,体重(14±2)g,雌雄各半,购于北京科兴中维生物技术有限公司,动物生产许可证号为SCXK(京)2019- 0009。饲养环境设置为温度22~24 ℃、相对湿度(50±5)%、12 h/12 h明暗周期,期间正常饮食。适应性饲养1周后开始实验。本研究经我院伦理委员会审批通过。
1.2 主要试剂
hBD3购自美国PeproTech公司,地塞米松(DXM)购自上海泽叶生物科技公司,OVA购自美国Sigma公司,RSV的Long株来源于中国武汉病毒研究所。瑞氏染色、HE染色和PAS染色试剂盒购自北京雷根生物有限公司,Masson染色和免疫组化染色试剂盒购自上海翊圣生物科技有限公司,特异性ELISA试剂盒购自南京凯基生物公司,RIPA裂解液、BCA蛋白测定试剂盒及ECL化学发光液购自上海碧云天生物研究所,兔抗人α- 平滑肌肌动蛋白(α- SMA)、血管内皮生长因子(VEGF)、转化生长因子- β1(TGF- β1)、胰岛素样生长因子- 1(IGF- 1)单克隆抗体、兔抗GAPDH多克隆抗体及辣根过氧化物酶(HRP)标记的山羊抗兔IgG购自英国Abcam公司。
1.3 方法
1.3.1 动物模型制备及给药 将40只幼鼠按照数字随机表法分为对照组、模型组、hBD3组及DXM组(阳性对照)4组,每组10只。参考文献[8]制备RSV感染致哮喘模型,除对照组外,其余3组幼鼠在第1天采用多点致敏法分别于两后足跖、腹股沟、背部、颈部及腹腔皮下注射含2%OVA与2%氢氧化铝的致敏剂。第14天起,各组腹腔注射0.2 ml致敏剂以加强致敏。第21天后,将幼鼠置于密闭容器内,雾化吸入1% OVA 30 min激发,每日1次,连续10 d,与此同时,hBD3组以100 μg·kg-1·d-1hBD3溶液灌胃,DXM组以0.5 mg·kg-1·d-1DXM溶液灌胃,对照组和模型组灌胃等体积生理盐水,连续14 d。于第21、35天分别用含1×106PFU的RSV悬液50 μl滴鼻,对照组在造模过程中腹腔注射或雾化吸入等量生理盐水,并以生理盐水滴鼻。
1.3.2 肺泡灌洗液(BALF)制备及细胞计数 实验处理结束后麻醉幼鼠,仰卧位固定,消毒后在颈部正中切口,打开胸腔分离皮下组织和肌肉,暴露气管。在右侧甲状软骨与第一、二软骨环之间进行缝线结扎,在第四、五软骨环之间做 “T”形切口,插入输液针头至气管腔内,缝线固定,将适量生理盐水注入肺部,轻柔按摩胸前区,停留30 s后将灌洗液导出,再缓慢注入,重复灌洗3次,收集灌洗液。4 ℃下以2 000 r·min-1离心15 min,弃上清留沉淀,生理盐水稀释,滴入细胞计数板,通过显微镜(400倍)计数白细胞总数,涂于载玻片,干燥后进行瑞氏染色,随机选择5个不同视野,分类计数嗜酸粒细胞、中性粒细胞、淋巴细胞数目。
1.3.3 ELISA试验 收集各组幼鼠腹部静脉血和BALF,离心后提取上清液,采用特异性ELISA试剂盒检测BALF及血清中免疫球蛋白lgE、白细胞介素(IL)- 4、IL- 5、肿瘤坏死因子- α(TNF- α)水平,严格按照试剂盒说明书操作。
1.3.4 HE染色 处死幼鼠取其肺组织,清洗后在4%多聚甲醛中固定,常规石蜡包埋,冰冻切片机上制成4 μm切片,进行HE染色,切片复温,脱蜡脱水,苏木精染色5 min,流水冲洗,伊红染色3 min,流水再次冲洗,程序化脱水、透明,中性树胶封片;光镜观察肺组织并拍照。
1.3.5 气道形态变化分析 取制备的肺组织切片,显微镜下获取肺内支气管横断面,采用Image- Pro Plus软件分析染色标本,分别测量气管内周长(Pi)、管壁面积(WAt)、支气管平滑肌面积(WAm)以及支气管平滑肌细胞核数目(N)。测量值通过Pi进行标准化,分别记为WAt/Pi、WAm/Pi和N/Pi。
1.3.6 PAS染色 取制备的肺组织切片,脱蜡脱水,置于阿利新蓝溶液浸泡10 min,流水冲洗,加过碘酸溶液氧化处理5 min,再浸入Leagene Schiff Reagent液中染色10 min,流水冲洗,苏木素染核,酸性乙醇分化,加入氨水返蓝,流水冲洗后程序化脱水、透明,中性树胶封片;光镜观察肺组织染色情况并拍照;随机选择5个不同视野,计数杯状细胞数目。
1.3.7 Masson染色 取制备的肺组织切片,脱蜡脱水,使用weigert铁苏木素溶液染色10 min,1%盐酸乙醇分化,流水冲洗,Masson染液返蓝,蒸馏水洗涤后加丽春红酸性品红液染色5 min,1%磷钼酸水分化,苯胺蓝溶液染色5 min,1%冰醋酸水溶液浸泡并洗涤,程序化脱水、透明,中性树胶封片;光镜观察肾组织胶原沉积并拍照;Image- Pro Plus软件分析染色面积比例。
1.3.8 免疫组化染色 肺组织切片经脱蜡脱水后,0.3%过氧化氢处理30 min,高温(98 ℃)加热5 min进行抗原修复,加山羊血清室温封闭1 h,将切片与兔抗人α- SMA单克隆抗体(1∶200)在4 ℃共同孵育过夜;次日PBS清洗,加入对应的山羊抗兔IgG抗体(1∶5 000),室温下孵育1 h,滴加DAB显色,自来水清洗,苏木素复染,程序化脱水、透明,中性树胶封片;光镜观察肺组织染色情况并拍摄图像,胞质染成黄色至棕色即为阳性;随机选择5个不同视野,Image- Pro Plus软件统计阳性染色面积。
1.3.9 蛋白质印迹实验 取肺组织在无菌环境下剪碎,研磨匀浆,添加RIPA裂解液,提取组织总蛋白,BCA法测定总蛋白浓度。制备10%SDS- PAGE凝胶,各组分别取30 μg总蛋白上样,通过电泳分离(电压50 V,60 min),再将蛋白电转至PVDF膜(温度75 ℃,电压50 V,60 min),室温下用5%脱脂奶粉封闭1 h,TBST洗膜,加入一抗抗体,4 ℃孵育过夜;次日加入对应HRP标记的二抗抗体,室温孵育1 h;TBST洗膜,加入ECL化学发光液避光反应30 min;凝胶图像采集系统进行蛋白显影,Image- Pro Plus统计软件对条带进行分析;以内参GAPDH为基准,计算各蛋白的相对表达水平。
1.4 统计学处理
2 结 果
2.1 hBD3对哮喘幼鼠BALF白细胞分类计数的影响
与对照组比较,模型组BALF中细胞总数显著增加,嗜酸粒细胞、中性粒细胞、淋巴细胞的比例也均高于对照组(P<0.05);与模型组比较,hBD3组和DXM组的BALF中细胞总数及嗜酸粒细胞、中性粒细胞、淋巴细胞的比例均显著降低(P<0.05)。见表1。
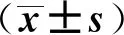
表1 各组幼鼠BALF白细胞分类计数比较
2.2 hBD3对哮喘幼鼠BALF和血清中细胞炎症因子水平的影响
ELISA检测结果如表2、3所示。与对照组比较,模型组BALF和血清中IgE、IL- 4、IL- 5及TNF- α水平均显著升高(P<0.05);与模型组比较,hBD3组及DXM组BALF和血清中IgE、IL- 4、IL- 5、TNF- α水平均显著降低(P<0.05)。
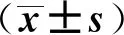
表2 各组幼鼠BALF中细胞炎症因子水平
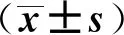
表3 各组幼鼠血清中细胞炎症因子水平
2.3 hBD3对哮喘幼鼠肺组织病理学的影响
HE染色结果显示,对照组肺组织未见明显的病理损伤,间质间基本无炎症细胞浸润;模型组肺组织发生损伤,基底膜增厚,可见大量炎症细胞浸润;hBD3组和DXM组肺组织损伤较模型组明显减轻,炎症细胞浸润减少。见图1。
PAS染色后可见对照组肺组织结构完整,模型组肺组织内有大量杯状细胞增生,较对照组显著增加(P<0.05);hBD3组和DXM组肺组织内杯状细胞均较模型组显著减少(P<0.05)。见图1。

a 与对照组比较,P<0.05; b 与模型组比较,P<0.05
2.4 hBD3对哮喘幼鼠肺组织纤维化的影响
Masson三色染色结果如图2所示。对照组肺组织中蓝染面积小,胶原纤维较少;模型组肺组织中蓝染面积分布较对照组显著增加,胶原纤维增多,组织纤维化现象十分明显(P<0.05);与模型组比较,hBD3组和DXM组肺组织中蓝染面积显著缩小,胶原纤维减少,组织纤维化程度减轻(P<0.05)。
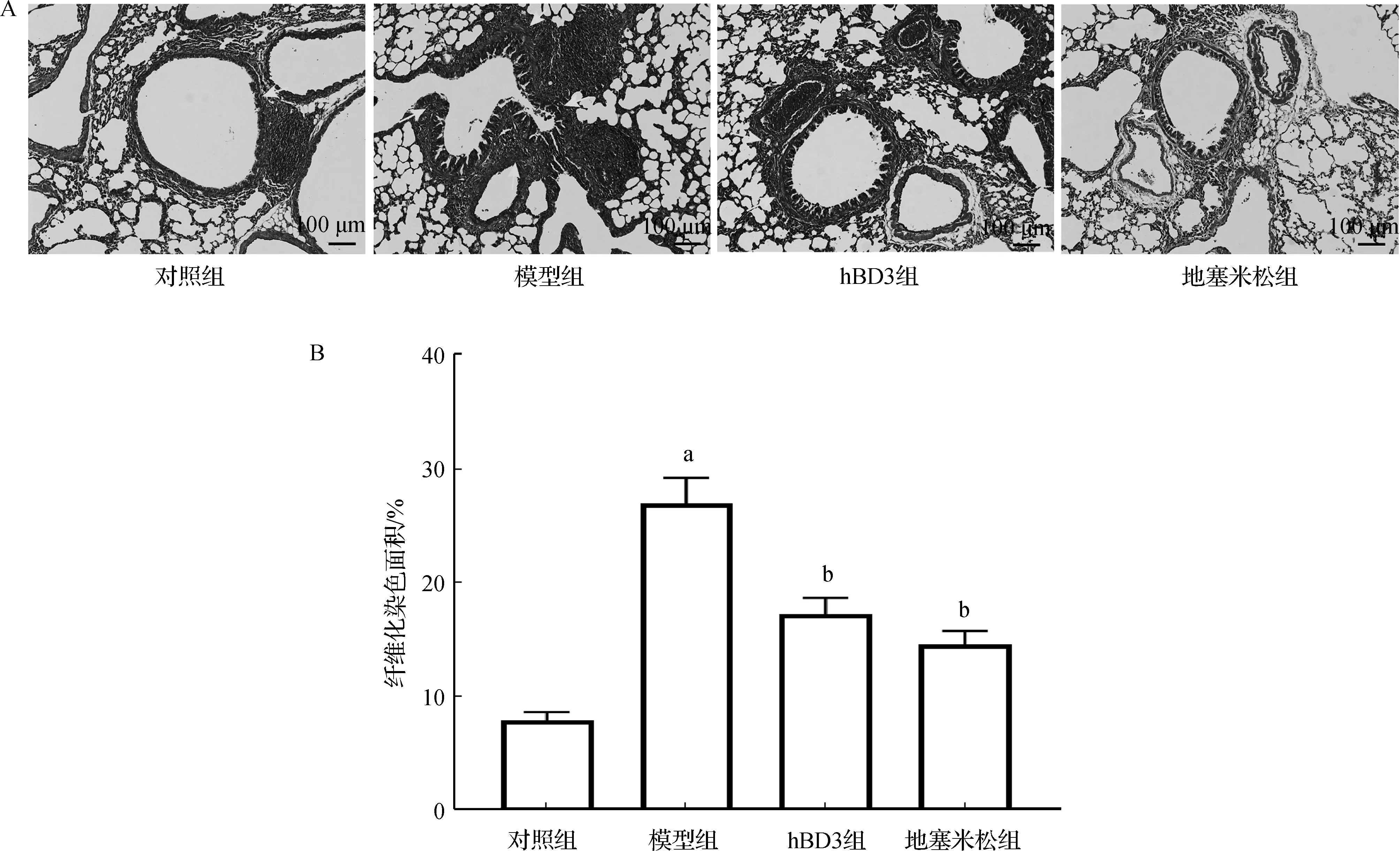
a 与对照组比较,P<0.05; b 与模型组比较,P<0.05
2.5 hBD3对哮喘幼鼠气道重塑程度的影响
各组肺内支气管各参数检测结果显示,模型组肺组织WAt/Pi、WAm/Pi、N/Pi均显著高于对照组(P<0.05);而hBD3组和DXM组肺组织WAt/Pi、WAm/Pi、N/Pi均显著低于模型组(P<0.05)。见图3。
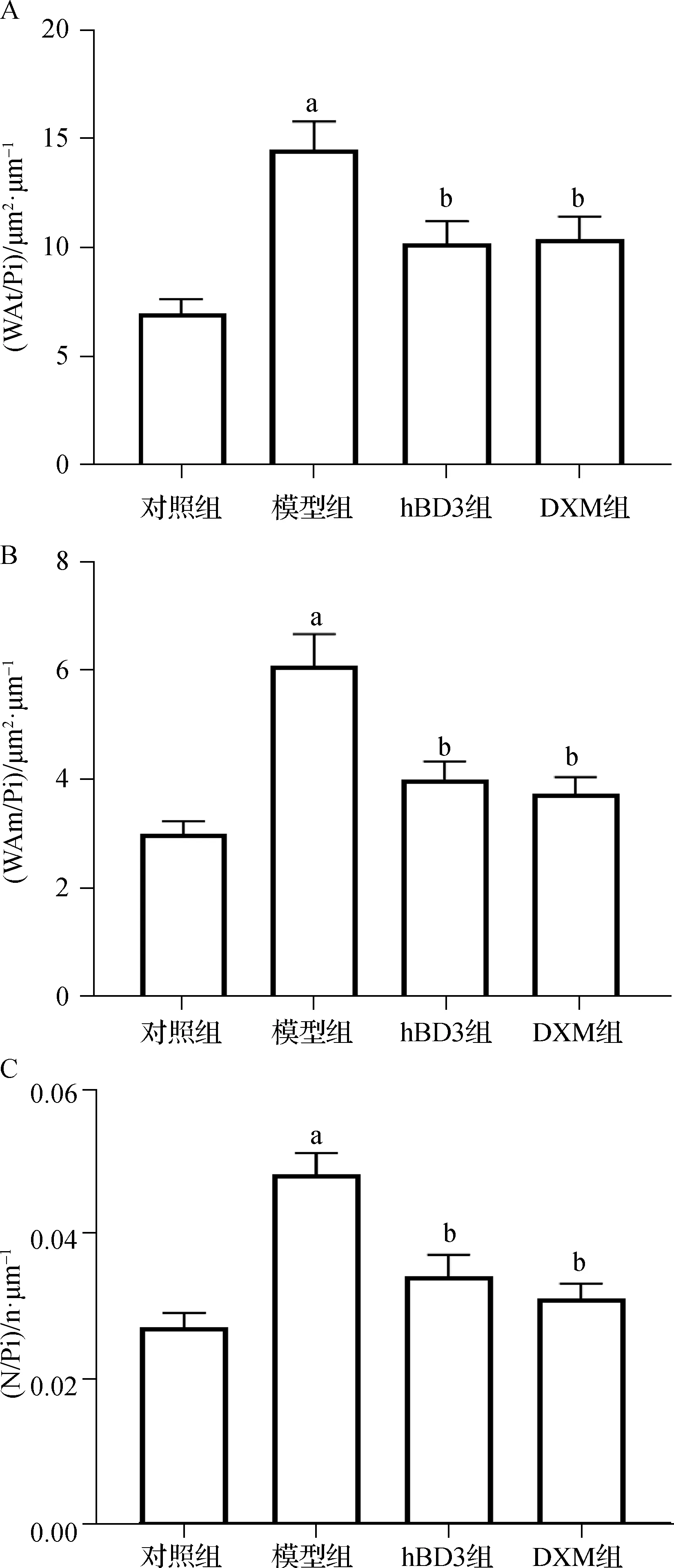
a 与对照组比较,P<0.05;b 与模型组比较,P<0.05
2.6 hBD3对哮喘幼鼠肺组织α- SMA表达的影响
免疫组化染色结果如图4所示。与对照组比较,模型组肺组织染色加深,染色面积增加,α- SMA阳性表达率显著升高(P<0.05);与模型组比较,hBD3组和DXM组肺组织染色变浅且面积缩小,α- SMA阳性表达率显著下降(P<0.05)。
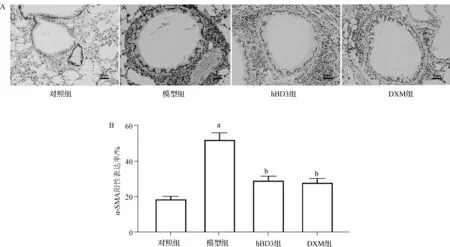
a 与对照组比较,P<0.05; b 与模型组比较,P<0.05
2.7 hBD3对哮喘幼鼠肺组织生长因子及自噬相关蛋白表达的影响
与对照组比较,模型组肺组织中VEGF、TGF- β1、IGF- 1蛋白表达水平均显著上升(P<0.05);与模型组比较,hBD3组和地塞米松组肺组织中VEGF、TGF- β1、IGF- 1蛋白表达水平均显著下降(P<0.05)。见图5。
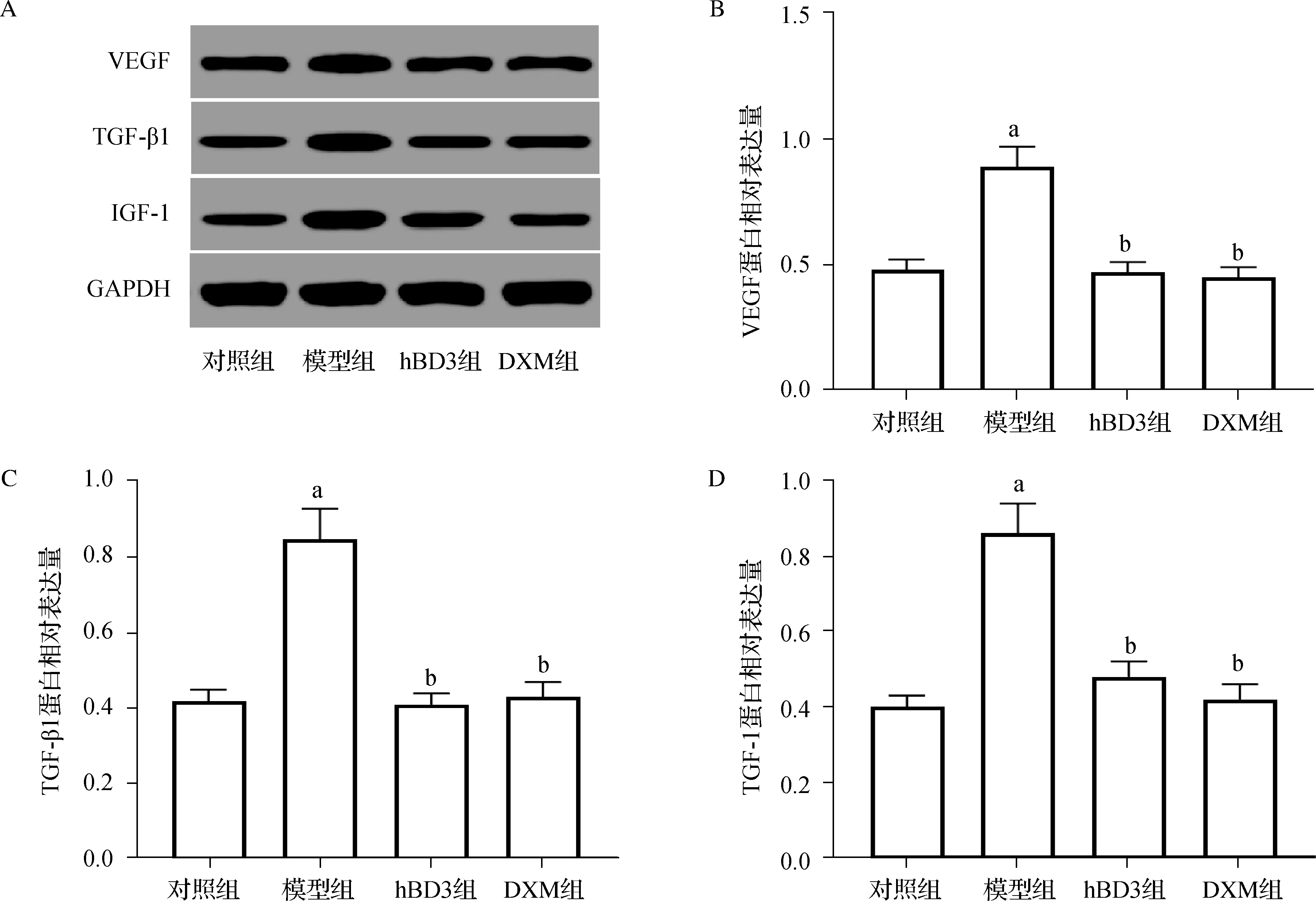
a 与对照组比较,P<0.05; b 与模型组比较,P<0.05
与对照组比较,模型组肺组织内LC3- Ⅱ、Beclin- 1蛋白表达水平均显著上升(P<0.05),P62蛋白表达水平显著下降(P<0.05);而hBD3组和地塞米松组肺组织内LC3- Ⅱ、Beclin- 1蛋白表达水平均较模型组显著下降(P<0.05),P62蛋白表达水平则显著上升(P<0.05)。见图6。
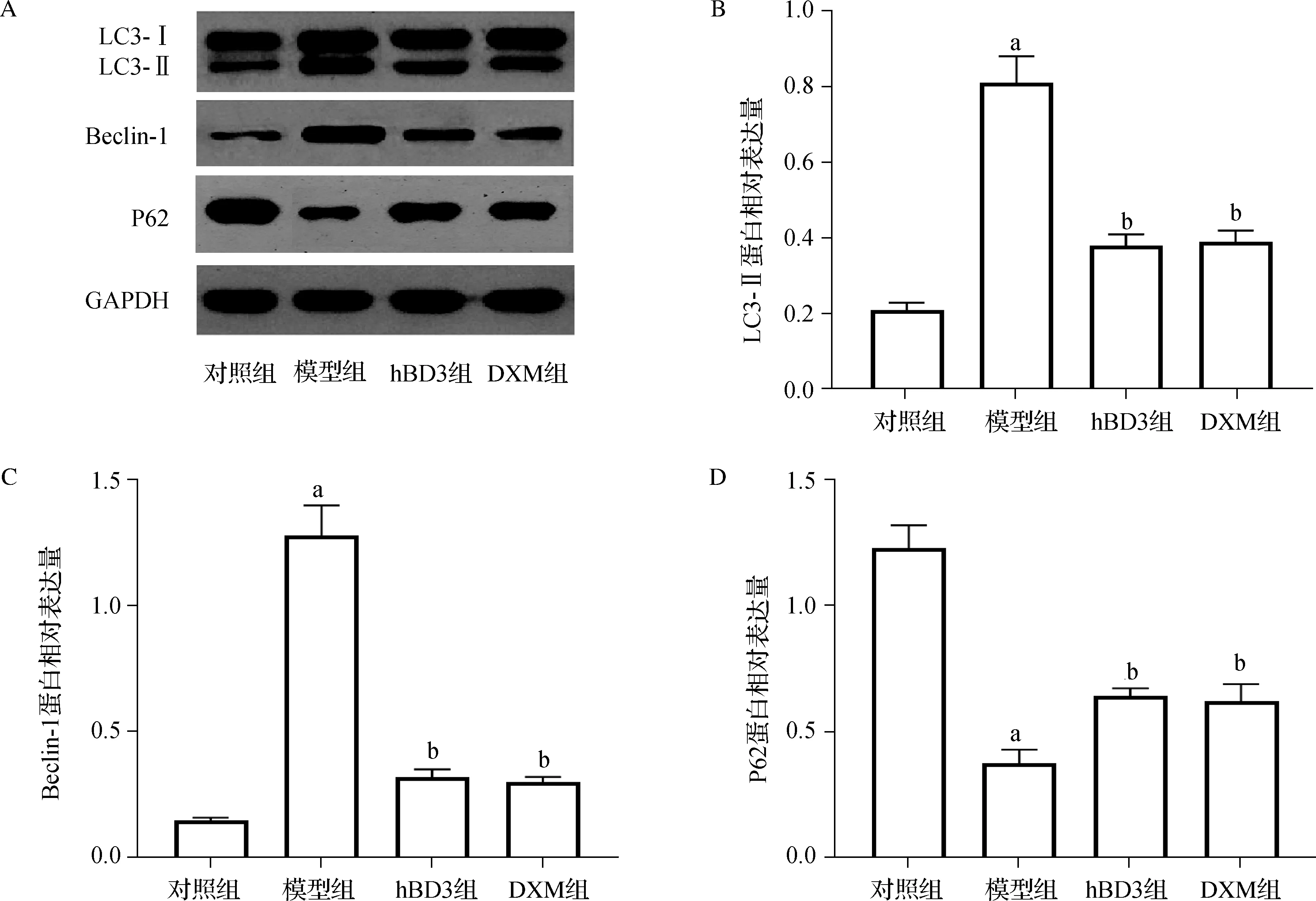
a 与对照组比较,P<0.05; b 与模型组比较,P<0.05
3 讨 论
防御素是天然免疫系统的重要组成分子,具有广泛的抗菌、抗病毒和免疫调节特性。人类防御素分为α- 防御素和β- 防御素两大类。人β- 防御素主要由黏膜和上皮细胞产生,hBD3作为β- 防御素家族的成员之一,也能在内皮细胞中表达,对宿主细胞毒性低。近年来,越来越多的研究表明了hBD3参与多种生理病理过程:hBD3可以诱导肠上皮细胞迁移,并降低坏死性小肠结肠炎新生大鼠模型的严重程度和死亡率[9];hBD3能够减轻TNF- α刺激的人脐静脉内皮细胞的炎症反应和氧化损伤,抑制单核细胞黏附和细胞黏附分子的表达,其作用可能与抑制NF- κB和MAPK信号传导途径相关[10];hBD3还能够抑制RAW264.7细胞向M1表型极化,在体内和体外均表现出抗牙周炎特性[11]。因此本研究探究hBD3对RSV感染诱发哮喘幼鼠的影响,实验结果提示,hBD3能够有效缓解哮喘幼鼠的炎症反应和气道重塑,提示其对哮喘幼鼠具有良好的治疗效果。
在哮喘的发病机制中,外界刺激作用下的支气管痉挛起着关键作用,同时炎症也是导致哮喘发作的原因,另一个显著因素是气道重塑。慢性呼吸道上皮炎症会导致微血管发生变化、支气管壁增厚和支气管气流受限,引发通气受损。在哮喘病理过程中,气道重塑与许多结构变化有关,例如上皮损伤、皮下纤维化、血管生成、肌成纤维细胞和肌细胞肥大以及气道平滑肌细胞中平滑肌纤维的数量增加[12- 13]。因此寻找有效的控制气道重塑的药物并阐明其分子机制对治疗哮喘具有重要意义。VEGF是一种多功能血管生成调节因子,在哮喘患者中过度表达,其表达水平与疾病活动度呈正相关,并与支气管直径及气道高反应性(AHR)呈负相关。相关实验证据表明,VEGF能够在小鼠气道和肺组织中诱导血管生成,促进肺组织结构重塑和炎症反应[14]。作为调节气道重塑的主要因子之一,TGF- β1可以促进成纤维细胞前体分化为肌成纤维细胞,并促进肌成纤维细胞的增殖,TGF- β1还有助于气道平滑肌细胞迁移到上皮层进而促进组织重塑[15]。IGF- 1可以提高胶原蛋白和弹性蛋白含量,增加平滑肌厚度,并在肺组织损伤修复和气道重塑中发挥重要作用[16]。因此VEGF、TGF- β1及IGF- 1是气道重塑的经典标志物。本研究结果显示,经过hBD3作用的哮喘幼鼠,肺组织基底膜增厚、炎症细胞浸润以及纤维化现象均明显减轻,杯状细胞数目减少,同时肺组织中VEGF、TGF- β1、IGF- 1蛋白表达水平均下降,由此推测,hBD3能够有效抑制哮喘幼鼠的气道重塑过程。
白细胞的调节募集是先天免疫反应不可或缺的要素,白细胞激活后能够释放大量的促炎症细胞因子、蛋白水解酶、自由离子基和活性氧等,造成内皮细胞破坏,加重组织损伤[17]。本研究结果显示,哮喘幼鼠的BALF中细胞总数增加,其中嗜酸粒细胞、中性粒细胞、淋巴细胞的比例也均明显升高,经hBD3作用的哮喘幼鼠BALF中细胞总数以及嗜酸粒细胞、中性粒细胞、淋巴细胞的比例均明显降低,此外BALF和血清中IgE、IL- 4、IL- 5和TNF- α水平也均显著降低。由此反映出hBD3能够抑制哮喘中白细胞激活,并有效降低促炎细胞因子表达进而调控病理生理过程。
自噬是细胞利用溶酶体途径降解受损细胞器和大分子的过程,能够维持体内正常的细胞稳态,并参与多种疾病的病理生理过程。近期研究强调了自噬在哮喘发展中的重要作用。Ban等[18]证实,重度哮喘患者痰和外周血嗜酸粒细胞的自噬水平高于非重度哮喘患者和健康对照者中的自噬水平;Kim等[19]研究发现,布地奈德可以通过介导自噬对人鼻病毒发挥抗病毒作用,从而有效预防哮喘发作,而利用氯喹抑制自噬显著降低了布地奈德对人鼻病毒的抗病毒和抗炎作用。本研究检测结果显示,RSV感染诱发哮喘幼鼠的肺组织内自噬相关蛋白LC3- Ⅱ和Beclin- 1的蛋白表达水平均升高, P62蛋白表达水平下降,而经过hBD3作用的哮喘幼鼠肺组织中LC3- Ⅱ和Beclin- 1的蛋白表达水平均明显受到抑制,也促进了P62蛋白表达,由此推测hBD3可能通过调控自噬发挥对哮喘幼鼠的保护作用。
综上所述,本研究推测hBD3能够改善RSV感染诱发哮喘幼鼠的炎症和气道重塑,降低白细胞激活程度,其机制可能是通过调控自噬实现的,这预示了hBD3对支气管哮喘的临床治疗价值,然而关于自噬如何影响哮喘发展的机制仍有待进一步研究阐明。
