Erenumab预防性治疗成人偏头痛疗效和安全性的Meta分析
2022-04-24丁锐陈显建周婧李国倩李国春
丁锐 陈显建 周婧 李国倩 李国春
西南医科大学附属中医医院,四川 泸州 646000
偏头痛(migraine)为反复发作的中重度搏动性头痛,是一种单侧发作或双侧发作的慢性、严重和致残性的神经系统疾病,并伴有恶心、畏光、畏音等症状,常规体力活动后可导致头痛加重,对人们的正常学习,工作和生活造成严重影响[1]。流行病学调查研究显示,偏头痛的全球年发病率为14.7%,在我国的年发病率约为9.3%,女性高于男性[2]。目前,预防性治疗偏头痛的药物包括非甾体抗炎药、钙通道阻滞药、β受体阻滞药、抗癫痫药以及抗抑郁药等,但上述药物不良反应相对较大,导致患者治疗依从性差,复发率较高[3]。因此,对于现有治疗失败的患者,需要新的、有效的、安全的、可耐受的预防性治疗。近年来大量研究显示,降钙素基因相关肽(CGRP)是一种由37个氨基酸组成的神经肽,血管活性很强[1],通过三叉神经血管系统的疼痛调节机制,在偏头痛的中枢和外周病理生理机制中起关键作用[4,5]。截至2021年3月,已有4种CGRP单克隆抗体被开发用于预防性的治疗偏头痛,Erenumab作为第一个完全人源化的单克隆抗体,该药物选择性靶向CGRP受体[6],于2018年5月获得美国食品药品监督管理局(FDA)批准,用于成人偏头痛的预防治疗。目前Erenumab已经获得CFDA批准,正在国内进行临床试验;为此本研究采用系统评价的研究方法,探讨Erenumab在成人偏头痛方面预防性治疗的有效性和安全性,为该药在我国的上市及临床应用提供循证数据支持。
1 研究方法
1.1 纳入与排除标准
1.1.1 研究类型。使用Erenumab预防性治疗偏头痛的随机对照试验(RCT),语种限定为中文和英文。
1.1.2 研究人群。根据国际头痛学会分类第3版(ICHD-3)[7],有偏头痛病史(有或无先兆)时间≥12个月,18~65岁年龄患者,种族、性别不限。
1.1.3 排除标准。包括:患者有偏瘫性偏头痛和集丛性偏头痛史;正在使用1种以上的偏头痛预防性药物;对2个以上的偏头痛预防药物没有治疗反应;开放性试验;动物试验;非RCT;综述;延伸性研究。
1.1.4 干预措施。试验组:Erenumab(70mg/月,140mg/月);对照组:安慰剂。
1.1.5 结局指标。主要疗效指标:①月平均偏头痛天数较基线的变化(MMD);②月平均偏头痛天数较基线减少≥50%的患者例数(MMD 50);③月平均急性偏头痛特异性用药天数较基线的变化(MSMD);次要结局指标,偏头痛物理功能影响日记(MPFID)评分;④对日常活动的影响(MPFID-EA);⑤对身体的影响(MPFIDPI);⑥对日常活动的总体影响(MPFID-OIEA);⑦头痛影响测试(HIT-6)。安全性指标:(1)总不良反应发生率;因不良反应终止率;(2)严重不良反应发生率;(3)鼻咽炎发生率;(4)上呼吸道感染发生率;(5)注射部位疼痛发生率;(6)疲劳发生率等。
1.2 检索策略 通过计算机检索中国知网、万方、维普、PubMed、Cochrane Library、Web of Science(SCI)等数据库。检索时间为该数据库建库至2021年3月。英文检索词:Erenumab,AMG334,monoclonalcalcitoningenerelated peptide antibodies,CGRPreceptor inhibitor,migraine。中文检索词:Erenumab,AMG 334,CGRP单克隆抗体,偏头痛。
1.3 筛选文献和提取数据 根据纳排标准,由两名研究者独立阅读文献,进行文献初步筛选,对符合的文献再次详细阅读并确定是否纳入,如遇分歧则通过交叉核对并商讨或通过第三名研究员决定。提取数据包括:基本特征(第一作者,发表年限,病例数,患者年龄),研究基线特征、干预措施、治疗疗程、每月偏头痛发作时间、结局指标等。
1.4 质量评价 采用偏倚风险评价工具,并采用改良的Jadad量表评价文献质量,评价项目包括随机序列生成、分配隐藏、盲法、盲评结果、选择性报道和数据完整性。
1.5 统计学方法 本文数据通过Rev Man5.1与Stata 12.0软件进行分析。采用均数差(MD)作为连续性变量的效应指标,比值比(OR)作为二分类变量采用的效应指标,区间估计值均采用95%可信区间(95%CI)表示。对纳入的研究使用卡方检验对纳入数据进行异质性检验,若I2<50%,则提示各研究间异质性不显著,采用固定效应模型进行统计分析;反之,则认为各研究间异质性显著,采用随机效应模型进行统计分析;同时,文章还绘制倒漏斗图并采用Egger检验进行发表偏倚风险分析。
2 结果
2.1 文献检索结果 共检索文献456篇,阅读文献题目和摘要后排除文献435篇,进一步仔细阅读全文,排除包括开放性研究以及延长性试验共15篇,最终纳入文献6篇[8-13],共计3 079例患者,均为英文文献。文献筛选流程及结果见图1,纳入Meta分析所有研究的基本特征见表1。
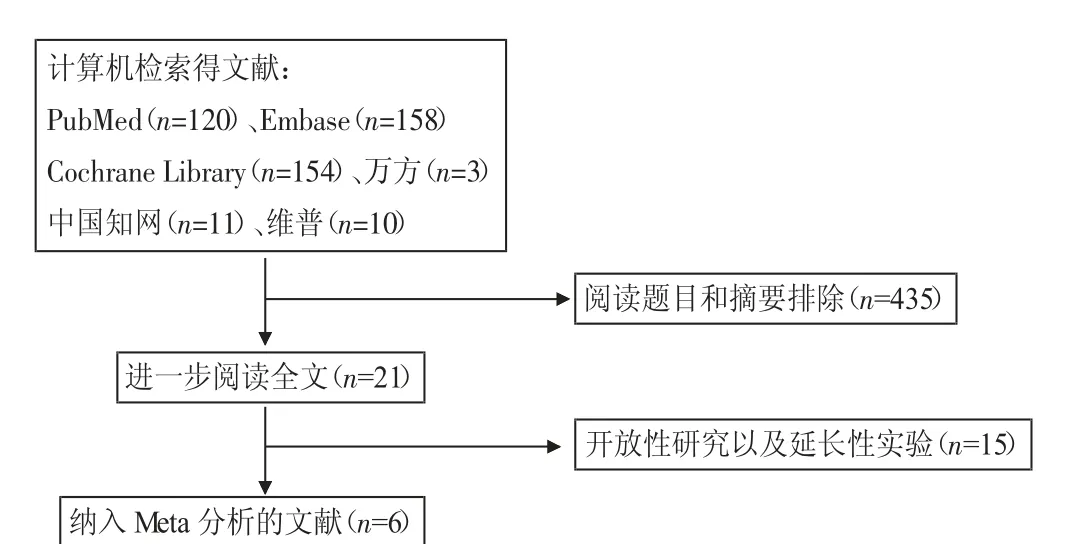
图1 文献筛选流程图
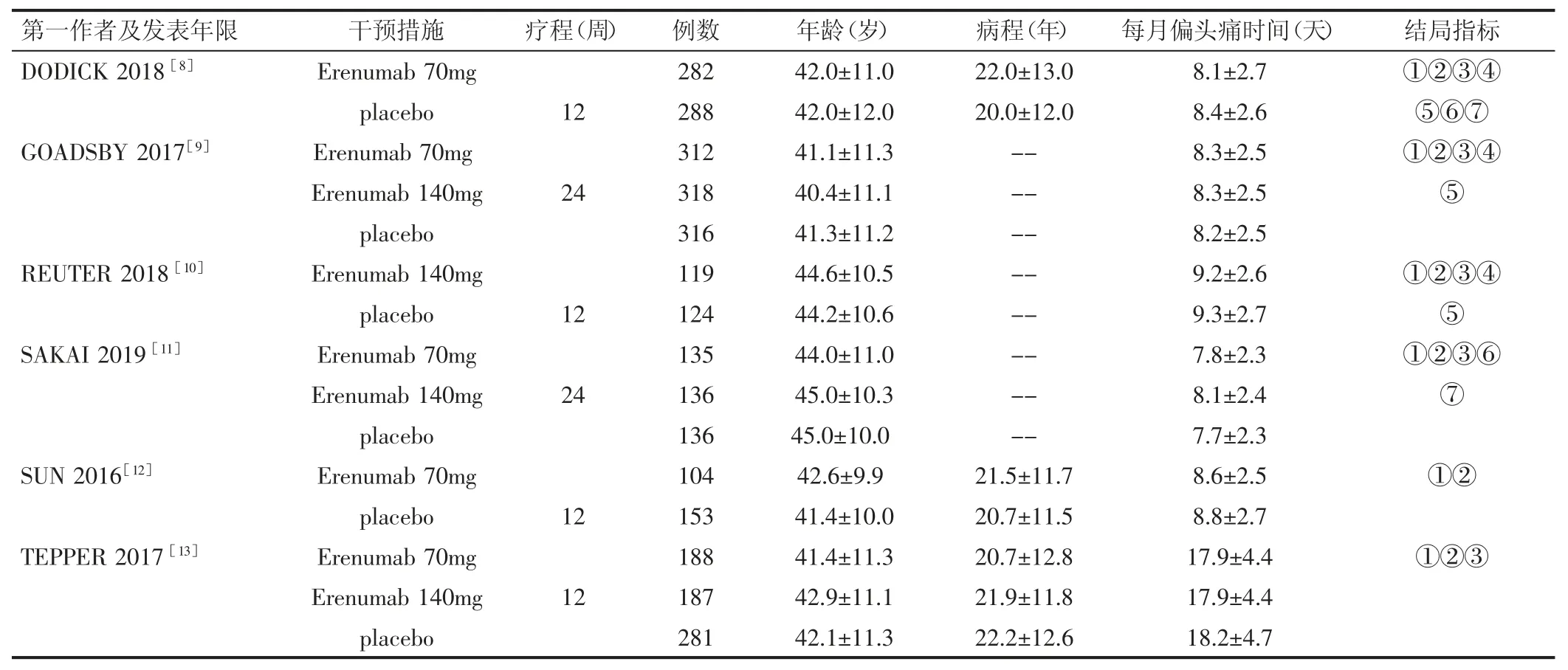
表1 纳入Meta分析所有研究的基本特征
2.2 纳入文献质量评价 本课题纳入的6项研究均为随机、双盲、多中心的RCT[8-13],纳入各研究的详细评价见表2、图2和图3。
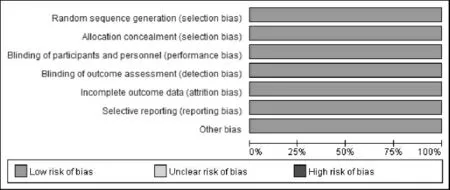
图2 各项研究偏移风险条形图

图3 各项研究偏移风险图

表2 纳入研究的质量评价表
2.3 Meta分析结果
2.3.1 MMD。6项研究[8-13](3 079位患者)均报道了Erenumab与安慰剂比较的MMD,各研究间异质性较小(P=0.08,I2=42%),通过固定效应模型分析显示,试验组减少MMD与安慰剂组间的差异具有统计学意义[MD=-1.68,95%CI(-1.92,-1.44),P<0.00001];按照试验组给药剂量不同对比安慰剂组进行亚组分析,结果显示:①70mg剂量组减少MMD显著多于安慰剂组,差异具有统计学意义[MD=-1.53,95%CI(-1.84,-1.21),P<0.00001];②140mg剂量组减少MMD显著多于安慰剂组,差异有统计学意义[MD=-1.91,95%CI(-2.30,-1.53),P<0.00001]。见图4。
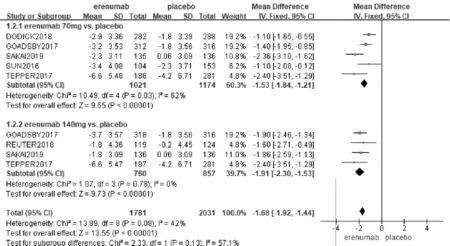
图4 Erenumab与安慰剂比较月平均偏头痛天数较基数变化(MMD)的森林图
2.3.2 MMD 50。6项研究[8-13](3079位患者)均报道了Erenumab与安慰剂比较的MMD 50,结果显示,各研究间异质性较小(P=0.07,I2=45%),通过固定效应模型分析,试验组的MMD 50显著高于安慰剂组,差异有统计学意义[OR=2.32,95%CI(2.01,2.68),P<0.00001];按照试验组给药剂量不同对比安慰剂组进行亚组分析,结果显示:①70mg剂量组减少MMD 50显著多于安慰剂组,差异有统计学意义[OR=2.07,95%CI(1.72,2.49),P<0.00001];②140mg剂量组减少MMD 50显著多于安慰剂组,差异有统计学意义[OR=2.75,95%CI(2.19,3.45),P<0.00001]。见图5。
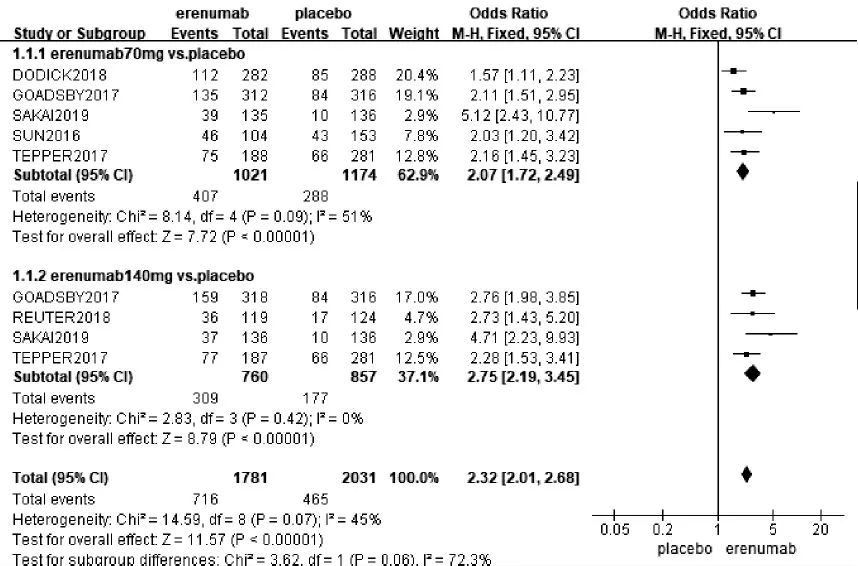
图5 Erenumab与安慰剂比较月平均偏头痛天数较基数减少≥50%的患者比例(MMD 50)的森林图
2.3.3 MSMD。5项研究[8-11,13](2 822位患者)报道了Erenumab与安慰剂比较的MSMD,各研究间有显著的异质性(P<0.00001,I2=88%),通过随机效应模型分析显示,试验组减少MSMD显著多于安慰剂组[MD=-1.59,95%CI(-2.03,-1.14),P<0.00001];按照试验组给药剂量不同对比安慰剂组进行亚组分析,结果显示:①70mg剂量组减少MSMD显著多于安慰剂组,差异有统计学意义[MD=-1.29,95%CI(-1.88,-0.70),P<0.00001];②140mg剂量组减少MSMD显著多于安慰剂组,差异有统计学意义[MD=-1.88,95%CI(-2.39,-1.36),P<0.00001]。见图6。
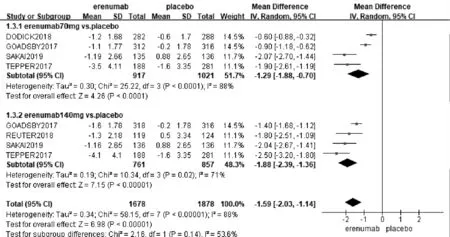
图6 Erenumab与安慰剂比较月均急性偏头痛特定用药天数较基线变化(MSMD)的森林图
2.3.4 其余指标。其余疗效指标的Meta分析结果见表3。
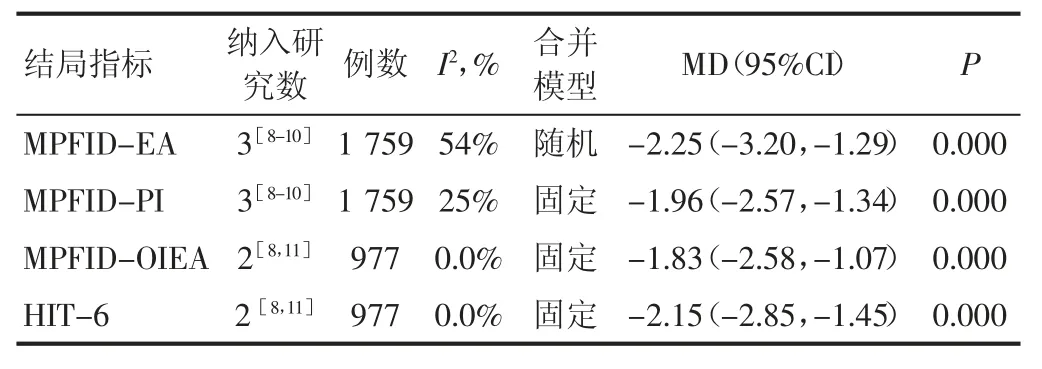
表3 其余疗效指标的Meta分析结果
2.3.5 安全性评价。6项研究[8-13](3 079位患者)均报道了Erenumab与安慰剂总不良反应发生率的比较结果,各研究间无显著异质性(P=0.16,I2=32%),通过固定效应模型分析,结果显示,Erenumab组与安慰剂间差异无统计学意义[OR=0.95,95%CI(0.83,1.08),P=0.39]。
2.3.6 其余安全性指标。其余安全性指标的Meta分析见表4。
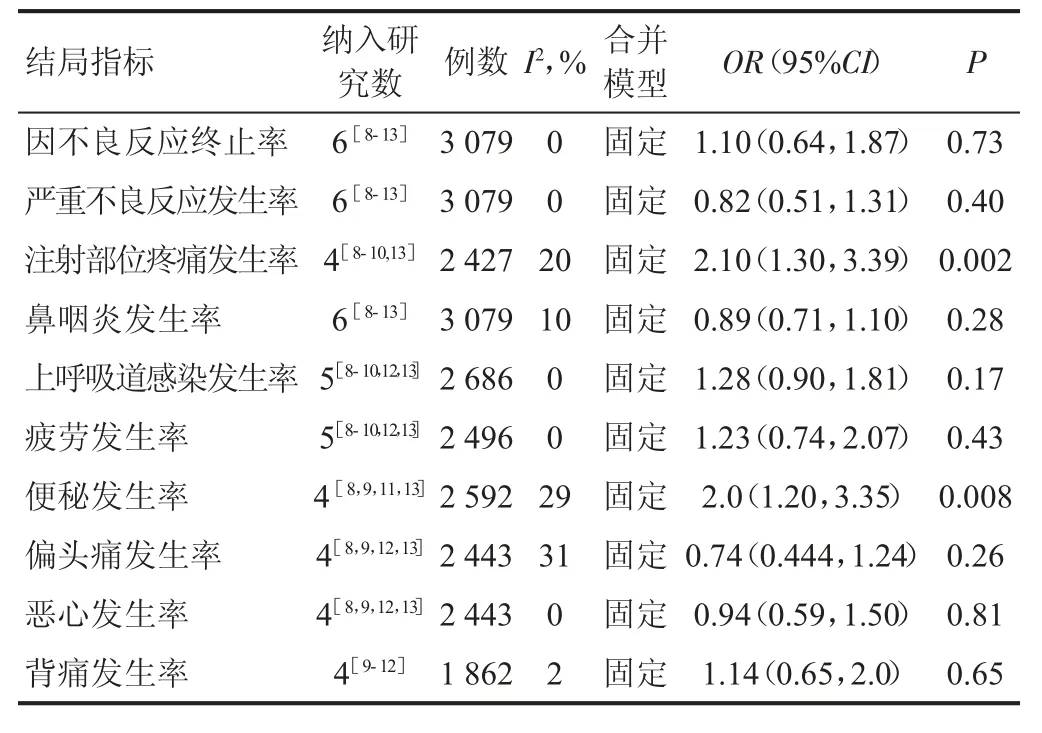
表4 其余安全性指标的Meta分析结果
2.4 发表偏倚分析 以结局指标MMD 50和总不良反应率为指标绘制倒漏斗图,详见图7(A、B),可见图中各点基本呈对称分布在倒漏斗图范围内。通过Stata中的Egger检验对Erenumab与安慰剂比较的结局指标MMD 50以及总不良反应发生率进行发表偏倚风险分析,结果提示:MMD 50的Egger检验P=0.963,总不良反应发生率的Egger检验P=0.635,再次说明纳入的研究存在发表偏倚风险的可能性较低。
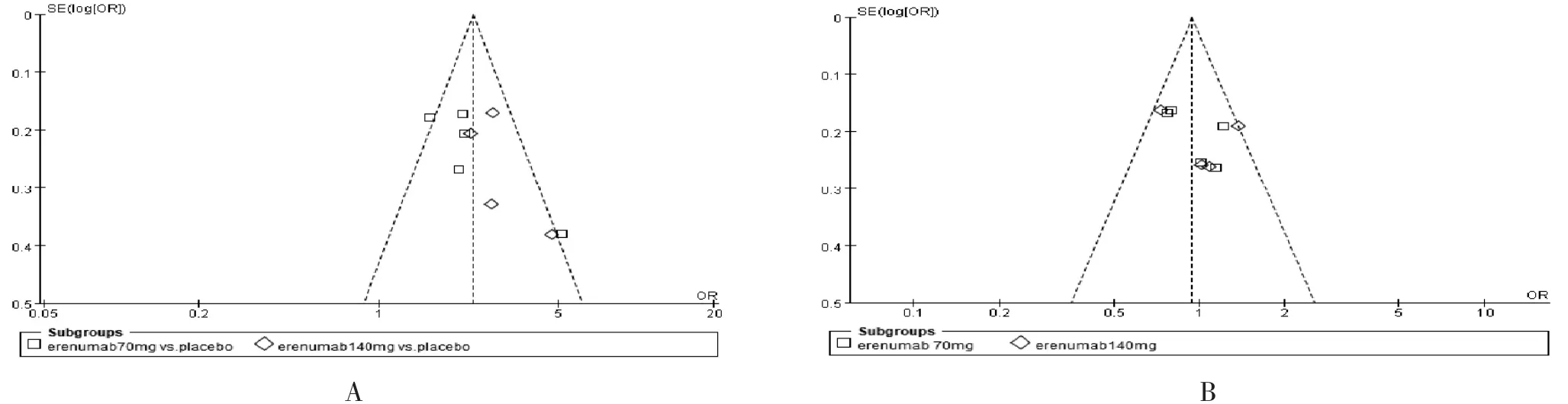
图7 MMD 50(A)和不良反应发生率(B)的倒漏斗图
3 讨论
CGRP作为一种具有37个氨基酸的神经肽,已被证实是一种在偏头痛发作中释放的重要神经递质[1,4],是目前国际上研究偏头痛的预防和治疗的重要靶点。目前偏头痛的病理生理机制包括血管源性学说和神经学说及遗传学说;三叉神经血管学说认为,三叉神经系统在偏头痛发作时,激活并释放血管活性神经肽,尤其是CGRP,它能引起硬脑膜和颅外的血管舒张以及神经源性炎症,从而引起典型的搏动性偏头痛[4,14]。CGRP受体被激活后,通过腺苷酸环化酶途径使得环磷酸腺苷(cAMP)浓度增加,激活环化核苷酸调控通道,引起兴奋性升高,兴奋阈值降低,进而产生动作电位,产生痛觉[15]。抑制过量CGRP信号对预防偏头痛发作至关重要,Erenumab通过靶向拮抗CGRP受体,抑制过量CGRP释放,减少胞内腺苷酸环化酶的增加,降低神经细胞兴奋性,从而起到预防偏头痛发作的作用[5]。
本研究对Erenumab预防性治疗偏头痛的疗效和安全性进行Meta分析结果显示:疗效方面,与安慰剂相比,Erenumab在MMD、MMD 50、MSMD、MPFID-EA、MPFID-PI、MPFID-OIEA、HIT-6等方面均显著优于安慰剂(P<0.05)。
安全性方面:从严重不良反应发生率、总不良反应发生率以及因不良反应终止试验方面看,Erenumab组和安慰剂组之间并没有显著差异。不良反应轻微,常见不良反应包括鼻咽炎,注射部位疼痛,上呼吸道感染,便秘,疲劳,偏头痛等,且都易耐受。
依从性方面:Erenumab的规格为每支70mg/mL,预填充式注射器,推荐给药方案为每月皮下注射70mg(1支)或者一次性注射140mg(2支)作为预防。患者可自行采用自动注射器给药,极大地提高了患者的依从性。Lipton[16]等对Erenumab做了成本效益-分析,反映出该药的高昂治疗费用,可能对患者依从性有较大影响。
本研究共纳入6项RCT研究(共计3 079例患者),均为随机、双盲、多中心的高质量研究,Jadad评分均为7分,但是,本研究还是存在一定的局限性:(1)纳入的研究数量有限,尚需更多设计严谨,样本量更大的RCT对其疗效和安全性作更加全面的研究;(2)由于文献限制,尚未对偏头痛作分型分析,加之限定了语种,由于条件限制,尚未对日文数据库进行检索;(3)6项研究均是与安慰剂作对比研究,尚需要阳性对照药物对其疗效做更全面的对比研究;(4)随访周期较短,需要更多设计严格,大样本,多中心的研究对其疗效安全性做更全面的评价。
综上所述,Erenumab在预防治疗成人偏头痛方面显著优于安慰剂组,且不良反应轻微可耐受,对于应用传统药物治疗无效的患者来说,Erenumab可能会成为预防和治疗偏头痛的新的选择。
