计算机辅助手术系统在胸腔镜肺结节切除术中的应用
2022-04-08邹志强李俊萍李玉财
李 兵,邹志强,李俊萍,张 伟,李玉财
(1.潍坊医学院,山东 潍坊,261053;2.中国人民解放军第960医院胸外科;3.淄博市市立医院胸心外科;4.淄博市市立医院肿瘤科)
随着CT技术的广泛应用,肺结节的检出率明显攀升,临床上越来越多的孤立性肺部小结节被检出。胸腔镜肺段手术为肺结节的治疗提供了新的微创治疗方式[1]。大多数直径<1 cm或胸膜下深度超过5 mm的小结节,术中无法通过视觉、手指触诊、腔镜器械滑行进行定位,使得结节定位不准确,手术本身的操作时间延长、手术难度增加[2-3],增加了术中血管损伤、中转开胸的概率,术前如何准确定位病灶,以帮助术中顺利寻找病灶、实现准确定位显得尤为关键。肺小结节的定位方法大体上可分为注入液体材料介导定位、经皮置入固态材料介导定位、影像介导定位[4-5]等。计算机辅助手术(computer-assisted surgery,CAS)系统此前已有用于胃、肝脏、胆囊及肾脏等器官手术中成功的案例,现探讨CAS系统在胸腔镜肺结节切除术中的应用价值。
1 资料与方法
1.1 临床资料 选取2018年1月1日至2021年10月1日解放军第960医院胸外科收治的以肺结节入院行胸腔镜肺段切除术的患者。将患者分为实验组(n=96,应用CAS系统进行术前评估)与对照组(n=92,未应用CAS系统)。纳入标准:(1)胸部CT检查提示结节直径≤20 mm,磨玻璃样影实性成分<50%,手术方式为解剖性肺段切除术;(2)心肺功能正常;(3)排除其他系统恶性疾病;(4)部分行头颅MRI、上腹部彩超或CT、发射型计算机断层显像骨扫描或正电子发射计算机断层显像-CT等排除远处转移;(5)两组患者完善术前检查,均行血常规、尿常规、肝肾功能、凝血功能、血型、肺功能、心电图等常规检查,无手术禁忌证。排除标准:(1)病变直径>20 mm;(2)病变直径<20 mm、磨玻璃样影实性成分>50%;(3)术中快速病理证实为实性癌或微乳头癌需行肺癌根治术;(4)合并其他脏器的严重并发症不能耐受检查或手术;(5)合并神经及精神系统疾病不能配合检查;(6)临床资料缺失。
1.2 术前准备 术前患者均行胸部CT平扫+增强扫描检查。将CT图像导入CAS系统软件,通过提取与分割肺血管、支气管区域进行三维重建(图1~图3),通过体积计算、胸廓及肺切除的虚拟模拟提取肺结节,以可视化切除表面及手术切缘的范围,对患者进行术前评估。确定单纯肺段切除的边距及肺结节准确定位,即能达到完全切除时病变组织与切缘之间具有足够的无病变组织的边界,并通过三维重建模型制定明确的手术路线,根据手术辅助系统定位结节位置,减少不必要的操作,降低手术风险。

图1 肺段模型重建 图2 结节在肺段定位 图3 结节与动静脉、支气管毗 邻关系
1.3 手术方法 采用双腔气管插管全身麻醉,健侧肺通气。患者取侧卧位,采用3个切口施术(腋中线第7~8肋间为胸腔镜观察孔,腋前线锁骨中线间3~4肋间为主操作孔,腋后线7肋间为副操作孔)。
1.4 观察指标 观察记录两组患者年龄、性别、吸烟史、第一秒用力呼气量/用力肺活量、最大通气量、肺结节位置与直径、手术时间、术中出血量、术后引流量、引流管拔除时间、术后住院时间、术后病理结果、术后并发症发生率等指标。
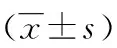
2 结 果
2.1 两组患者术前一般资料的比较 年龄、性别、吸烟史、术前合并症、第一秒用力呼气量/用力肺活量、最大通气量、肺结节直径差异无统计学意义(P>0.05),见表1。
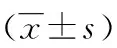
表1 两组患者临床资料的比较
2.2 术中、术后相关指标的比较 两组均顺利完成胸腔镜肺段切除术。实验组均发现结节,对照组中2例未发现结节,无中转开胸或二次手术病例,无住院期间死亡病例。两组手术时间、术中出血量、术后引流量、拔除引流管时间、住院时间差异有统计学意义(P<0.05),见表2。两组术后病理结果差异无统计学意义(P>0.05),见表3。
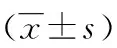
表2 两组患者围手术期指标的比较

表3 两组患者术后病理结果的比较(n)
2.3 并发症的比较 实验组术后并发症发生率为5.2%,其中肺不张1例、肺部感染3例、心律失常1例。对照组术后并发症发生率为6.5%,其中漏气1例、肺部感染4例、心律失常1例,通过用药物控制感染、控制心律失常、延长引流管放置时间等措施,患者均康复,两组并发症发生率差异无统计学意义(χ2=2.358,P=0.792)。
3 讨 论
肺部小结节的外科治疗趋向常态化,解剖性肺段切除术具有淋巴结清扫彻底、切除精准、预后好等优点。肺组织可获得更多的保留,对肺功能的影响较小,可提高手术精准性。但肺部磨玻璃样结节密度接近周围肺组织密度且可能无胸膜牵拉标志性特征,胸腔镜下部分病变难以探查到具体位置,肺内支气管、肺动静脉之间存在错综复杂的解剖结构,变异较多,个体差异性大,普通薄层CT扫描多无法明确肿瘤部位及靶段支气管、肺动静脉的走行,难以明确段间平面,易损伤重要脏器或造成大出血,增加手术风险,影响术后恢复。
术前利用肺成像技术进行提前规划,是获得手术满意效果的必要条件[6-7]。在解剖性肺段切除术中尤为关键[7]。Chen-Yoshikawa等[8]对胸外科手术进行CT三维重建术前模拟,还原出3D几何图形,重建各个肺段的形态,用不同的颜色标记区分支气管、肺静脉、肺结节、肺动脉等,能360°旋转重建图像,经多角度、多层次观察判断,了解肺段支气管、血管等解剖结构的个体化差异,找到最佳手术入路,为临床制定个体化的手术方案提供了依据[9]。对于肺部结节而言,手术方式一般采用肺叶切除术、肺楔形切除术、解剖性肺段切除。在未应用CAS系统前,对于肺结节的定位方法多样,依靠扩大肺叶或肺段切除面积达到手术目的[10]。本研究采用CAS系统定位法,通过将术中探查到的肺血管、支气管解剖形态与术前三维重建的血管、支气管图像进行对比,发现两者基本相符[11]。其中术前三维重建结节部位定位成功率100%[12]。肺结节营养血管符合率为96.67%[13-14],肺结节毗邻支气管符合率为96.42%[15]。与未应用CAS系统组相比,可缩短手术时间、减少术中出血量、缩短术后胸腔引流时间、减少术后引流量、缩短住院时间。CAS系统出现后,建立个体化肺结节三维数字化模型[16],利于制定肺结节模拟手术规划,可于术前明确肺结节与支气管、动静脉的位置关系。而邻近亚段、肺段动脉或支气管的结节位于亚段或肺段的中央区域,邻近段间静脉结节位于相邻肺段之间,在保证切缘的前提下通过单亚段、单肺段或不同的肺段组合方式实现靶区域解剖性切除。术中段间平面的确定及分离,在切断段气管前,将肺段确认无误后膨肺通气,再次确认靶肺段气管,同时观察剩余肺段通气情况,确保不伤及其他肺段气管。离断靶段气管及靶段动脉、静脉后,可使用纯氧膨肺后单肺通气,待段间界限明显,选择直线切割缝合器或电刀分离段间肺组织,如接近段间平面的肿瘤,确保手术切缘,降低手术切缘阳性率[17],使用直线切割缝合器分离段间平面时,需背离邻近肺段,必要时可能会牺牲段间静脉。最大限度保留正常组织[18],减轻手术创伤,减少手术并发症,提高患者术后生存质量[19]。CAS系统已有用于消化系统、泌尿系统等术前规划的报道,并取得了较好的手术效果;应用于呼吸系统手术的报道较少,本研究验证了CAS系统在肺结节胸腔镜手术中的应用价值。
本研究的不足在于回顾时间较长,随着单中心手术数量的增加、术者技术的进步,手术时间会逐渐缩短。本研究限于单中心小样本研究,期待有多中心大样本研究加以验证补充。综上,对于直径≤2 cm的肺结节患者,胸腔镜肺段切除术前应用CAS系统具有一定的临床价值。
