改良FOLFOXIRI方案在结直肠癌治疗中的效果和安全性分析
2022-04-02汪彤王沚萱
汪彤 王沚萱


【摘要】 目的:探析改良FOLFOXIRI方案治疗结直肠癌患者的效果和安全性。方法:选取2019年1月-2020年10月鞍山市中心医院收治的70例结直肠癌患者,依据不同治疗方法将患者分为观察组和对照组,每组35例。观察组予以改良FOLFOXIRI方案治疗,对照组予以标准FOLFOXIRI方案治疗。比较两组治疗效果及不良反应的发生情况。结果:观察组客观缓解率(ORR)为60.00%(21/35),高于对照组的34.29%(12/35),差异有统计学意义(P<0.05)。观察组疾病控制率(DCR)为88.57%(31/35),高于对照组的74.29%(26/35),差异无统计学意义(P>0.05)。观察组Ⅲ级不良反应发生率为11.43%(4/35),低于对照组的45.71%(16/35),差异有统计学意义(χ=10.080,P<0.05)。观察组粒细胞减少发生率低于对照组,差异有统计学意义(χ=8.824,P<0.05)。结论:改良FOLFOXIRI方案治疗结直肠癌的近期疗效较好,且安全性较高。
【关键词】 改良FOLFOXIRI方案 结直肠癌 不良反应
Effect and Safety of Modified Folfoxiri Regimen in the Treatment of Colorectal Cancer/WANG Tong, WANG Zhixuan. //Medical Innovation of China, 2022, 19(07): -127
[Abstract] Objective: To investigate the effect and safety of modified FOLFOXIRI in the treatment of colorectal cancer patients. Method: A total of 70 patients with colorectal cancer admitted to Anshan Central Hospital from January 2019 to October 2020 were selected, and they were divided into observation group and control group according to different treatment methods, with 35 cases in each group. The observation group was treated with modified FOLFOXIRI regimen, and the control group was treated with standard FOLFOXIRI regimen. The therapeutic effect and the occurrence of adverse reactions were compared between two groups. Result: The objective response rate (ORR) of the observation group was 60.00% (21/35), which was higher than 34.29% (12/35) of the control group, the difference was statistically significant (P<0.05). The disease control rate (DCR) of the observation group was 88.57% (31/35), which was higher than 74.29% (26/35) of the control group, the difference was not statistically significant (P>0.05). The incidence of grade Ⅲ adverse reactions in the observation group was 11.43% (4/35), which was lower than 45.71% (16/35) in the control group (χ=10.080, P<0.05). The incidence of granulocytopenia in the observation group was lower than that in the control group, the difference was statistically significant (χ=8.824, P<0.05). Conclusion: The modified FOLFOXIRI has good short-term effect and high safety in the treatment of colorectal cancer.
[Key words] Modified FOLFOXIRI Colorectal cancer Adverse reactions
First-author’s address: Anshan Central Hospital, Liaoning Province, Anshan 114000, China
doi:10.3969/j.issn.1674-4985.2022.07.029
结直肠癌是临床常见的一种恶性肿瘤,其在我國的发病率与死亡率分别占所有恶性肿瘤的第六位及第五位[1-2]。目前临床治疗结直肠癌的一线化疗药物以氟尿嘧啶、伊立替康及奥沙利铂为主,其中单用氟尿嘧啶治疗的患者生存时间仅10~12个月,联合应用伊立替康或奥沙利铂治疗可将生存时间提高至14~16个月[3]。但有报道显示,将氟尿嘧啶/亚叶酸钙、奥沙利铂及伊立替康三种药物联合(FOLFOXIRI方案)应用与仅应用一种或两种药物治疗的患者相比生存时间更长,甚至可达20个月左右[4-5]。不过由于该方案毒性反应较大,而我国与欧美人群存在体质及耐受性的差异,可能会影响治疗效果,导致生存时间无法获得有效延长,因此该方案在我国未得到广泛应用[6]。基于此,本研究通过结合国外关于FOLFOXIRI方案的经验,将标准FOLFOXIRI方案中的用药剂量进行改良,并观察其在结直肠癌患者中的疗效及安全性,旨在为临床治疗提供理论基础,现报道如下。
1 资料与方法
1.1 一般资料 选取2019年1月-2020年10月鞍山市中心医院收治的70例结直肠癌患者。纳入标准:(1)均经病理学或组织学确诊为无法手术的结直肠癌;(2)年龄18~75岁;(3)经美国东部肿瘤协作组(ECOG)评分为0~2分,预计生存时间≥3个月,距辅助放化疗结束时间≥6个月;(4)治疗前常规心电图及血常规检查无异常。排除标准:(1)合并心、脑、肝等重要脏器严重损伤;(2)肿瘤复发或转移后接受过抗肿瘤治疗。(3)伴有久泻不止的短肠综合征或活动性感染;(4)中途退出研究。依据不同治疗方法将患者分为观察组和对照组,每组35例。本研究获医院医学伦理主管部门批准,患者及家属均知情且同意。
1.2 方法 对照组予以标准FOLFOXIRI方案治疗:第1天,伊立替康(生产厂家:江苏恒瑞医药股份有限公司,批准文号:国药准字H20040711,规格:100 mg)165 mg/m2静脉滴注;奥沙利铂[生产厂家:齐鲁制药(海南)有限公司,批准文号:国药准字H20093167,规格:50 mg]85 mg/m2加入5%葡萄糖注射液500 mL静脉滴注,时间在3 h以内;第1、2天,5-氟尿嘧啶(生产厂家:山西普德药业有限公司,批准文号:国药准字H20051113,规格:0.25 g)400 mg/m2静脉滴注,亚叶酸钙(生产厂家:江苏恒瑞医药股份有限公司,批准文号:国药准字H32022391,规格:0.1 g)200 mg/m2静脉滴注,以14 d为1个周期,连续治疗12个周期。观察组予以改良FOLFOXIRI方案治疗:第1天,伊立替康150 mg/m2静脉输注90 min,续接奥沙利铂85 mg/m2、亚叶酸钙200 mg/m2,然后持续泵入48 h氟尿嘧啶2 800 mg/m2,以14 d为1个周期,直到发生肿瘤进展、肿瘤根治切除或不良反应且无法耐受时。两组均预防性给予5-羟色胺3受体阻滞剂防治呕吐;出现胆碱能反应则应用皮下注射阿托品(生产厂家:浙江瑞新药业股份有限公司,批准文号:国药准字H33020465,规格:1 mL︰0.5 mg)
0.25 mg治疗;出现腹泻则给予口服洛哌丁胺(生产厂家:西安杨森制药有限公司,批准文号:国药准字H10910085,规格:2 mg)2 mg治疗;若患者出现Ⅲ级及以上腹泻,则将伊立替康减量25%;若出现Ⅲ级及以上胃炎及皮炎,则将氟尿嘧啶减量15%;若出现Ⅱ级以上的周围神经毒性反应且持续14 d以上,则暂停使用奥沙利铂直至毒性反应消失;若出现Ⅲ级及以上血小板减少且持续3 d以上,则将所有药物减量15%。
1.3 观察指标及判定标准 (1)比较两组疗效。应用实体瘤的疗效评价标准(response evaluation criteria in solid tumors,RECIST)进行评估,包括4个条目,即完全缓解(complete response,CR)、部分缓解(partial response,PR)、疾病稳定(stable disease,SD)、疾病进展(progressive disease,PD),其中治疗后病灶完全消失为CR,治疗后有可测量目标病灶的直径总和低于基线≥30%为PR,治疗后出现新病灶或者所有可测量目标病灶的直径总和高于基线≥20%为PD,治疗后靶病灶减小的程度没达到PR或者增加的程度也没达到PD水平为SD。其中客观缓解率(objective response rate,ORR)=CR+PR,疾病控制率(disease control rate,DCR)=CR+PR+SD,两组均于治疗4个周期后进行评估[7]。(2)比较两组不良反应发生情况。通过记录治疗期间不良反应的发生情况以评价其安全性,依据美国国立癌症研究所(NCI)制定的常见不良反应分级标准(common terminology criteria adverse events,CTCAE)进行分级,分为0~4级[8]。
1.4 统计学处理 采用SPSS 24.0对本研究数据资料进行处理,计量資料行t检验,以(x±s)表示,计数资料采用χ检验,以(%)表示。以P<0.05为差异有统计学意义。
2 结果
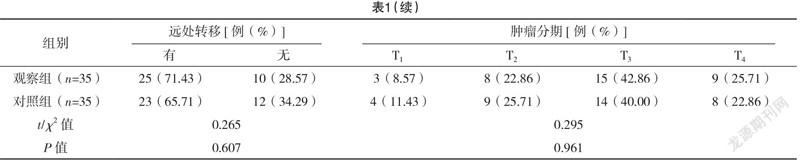
2.1 两组一般资料比较 两组一般资料比较,差异均无统计学意义(P>0.05),具有可比性,见表1。
2.2 两组近期疗效比较 观察组ORR为60.00%(21/35),高于对照组的34.29%(12/35),差异有统计学意义(P<0.05)。观察组DCR为88.57%(31/35),高于对照组的74.29%(26/35),差异无统计学意义(P>0.05)。见表2。
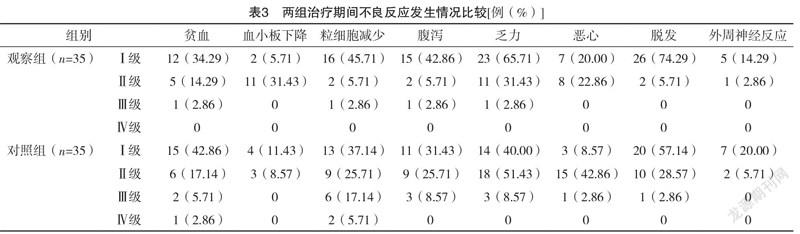
2.3 两组治疗期间不良反应发生情况比较 治疗期间,观察组Ⅲ级不良反应发生率分别为11.43%(4/35),低于对照组的45.71%(16/35),差异有统计学意义(χ=10.080,P<0.05)。观察组Ⅳ级不良反应发生率为0,低于对照组的8.57%(3/35),差异无统计学意义(χ=3.134,P>0.05)。观察组粒细胞减少发生率低于对照组,差异有统计学意义(χ=8.824,P<0.05)。两组贫血、血小板下降、腹泻、乏力、恶心、脱发及外周神经反应发生率比较,差异均无统计学意义(χ=0.919、0.134、1.472、1.061、0.915、0.971、0.170,P>0.05)。见表3。
3 讨论
目前,NCCN指南及ESMO指南均推荐将FOLFOXIRI方案作为结直肠癌治疗的一线方案[9-10]。但仍有部分患者在经过该方案的规范治疗后出现了复发及转移;另外,由于结直肠癌起病隐匿,早期并无典型临床症状,就诊时大部分患者已属中晚期,失去了最佳治疗时机。因此,如何选择合适的辅助化疗方案,进而提高治疗有效率并延长患者生存时间,已成为当今研究热点。
Sunakawa等[11]對日本进展期结直肠癌患者应用FOLFOXIRI方案的Ⅰ期研究中表明,对该方案中的药物剂量进行相应调整后,其在治疗中产生的毒性反应是可控的,且该方案中的推荐剂量是适用于东方人的。刘捷等[3]为适用于中国人体质及耐受性亦将原方案进行改良,且治疗后患者ORR为51.1%,DCR为85.1%,与国外报道结果相似。本研究中观察组患者ORR为60.00%,DCR为88.57%,略高于上述研究结果,可能与本研究样本量较小有关。GONO研究显示,FOLFOXIRI方案较FOLFIRI方案相比显著提高了患者的无进展生存期、生存时间及有效率;但HORG研究则显示两种方案对患者的ORR、生存时间及中位无进展生存期的影响无显著差异[4,12]。推测与HORG研究中氟尿嘧啶的给药方式保留了静脉推注,所以导致腹泻等毒副反应发生率未显著减少有关,因此本研究方案中均将氟尿嘧啶的给药方式改为静脉滴注。此外,粒细胞减少与腹泻作为该方案中的剂量限制性毒性,与伊立替康的活性代谢产物SN-38所产生的细胞毒性有一定相关性[13-14]。SN-38会在肝脏UGT1A1的糖基化作用下发生葡萄糖醛酸化失活进而生成SN-38G,随着胆汁排泄进入肠道,并被肠道内细菌产生的酶重新分解成SN-38,继而对肠道黏膜造成损伤,引发腹泻[15-16]。还有研究显示,UGT1A1的表达是可变的,因此会引起不同患者间SN-38糖化反应的速率相差较大,导致个体间不良反应程度的不同,且UGT1A1*28的多态性与预测伊立替康相关毒性反应之间存在相关性,因此将伊立替康剂量下调可能有利于减轻毒性反应[17-19]。既往研究中,Ⅲ、Ⅳ级粒细胞下降的发生率为35.0%~55.0%,Ⅲ、Ⅳ级腹泻的比例为20.0%~27.7%[4,12]。本研究中观察组Ⅲ级不良反应发生率为11.43%,且无一例Ⅳ级不良反应发生,其中Ⅲ级粒细胞下降发生率为2.86%,Ⅲ级腹泻发生率为2.86%,均低于上述研究结果且低于对照组,可能与本研究方案中将伊立替康及氟尿嘧啶进行调剂且研究中还给予药物进行预防有关。
综上所述,本研究在国外关于FOLFOXIRI方案治疗结直肠癌患者相关研究的经验上,初步改良了用药剂量及给药方式,较标准FOLFOXIRI方案相比提高了治疗有效率,降低了不良反应的发生率。但本研究样本量较小,可能存在统计偏移,且未对其进行远期疗效观察,尚有待进一步大样本量多中心研究进行深入验证。
参考文献
[1]陈万青,郑荣寿,张思维.中国恶性肿瘤的动态变化[J].科技导报,2014,32(26):65-71.
[2]何美,李必波,杜佳.2012-2016年重庆市城市人群结直肠癌筛查结果分析[J].中国肿瘤,2020,29(6):430-433.
[3]刘捷,林榕波,范南峰,等.改良FOLFOXIRI方案一线治疗晚期结直肠癌的疗效及生存预后分析[J].现代肿瘤医学,2017,25(7):1083-1088.
[4] FALCONE A,RICCI S,BRUNETTI I,et al.Phase Ⅲ trial of infusional fluorouracil,leucovorin,oxaliplatin,and irinotecan (FOLFOXIRI) compared with infusional fluorouracil,leucovorin,and irinotecan (FOLFIRI) as first-line treatment for metastatic colorectal cancer:the Gruppo Oncologico Nord Ovest[J].J Clin Oncol,2007,25(13):1670-1676.
[5]胡俊,王银华,叶斌,等.FOLFOXIRI联合Kras基因靶向治疗方案对晚期结直肠癌预后的影响[J].现代消化及介入诊疗,2019,24(2):146-149.
[6] MASI G,VASILE E,LOUPAKIS F,et al.Triplet combination of fluoropyrimidines,oxaliplatin,and irinotecan in the first-line treatment of metastatic colorectal cancer[J].Clin Colorectal Cancer,2008,7(1):7-14.
[7] RONOT M,BOUATTOUR M,WASSERMANN J,et al.
Alternative Response Criteria (Choi, European association for the study of the liver, and modified Response Evaluation Criteria in Solid Tumors [RECIST]) Versus RECIST 1.1 in patients with advanced hepatocellular carcinoma treated with sorafenib[J].Oncologist,2014,19(4):394-402.
[8] DUECK A C,MENDOZA T R,MITCHELL S A,et al.Validity and reliability of the us national cancer institute’s patient-reported outcomes version of the common terminology criteria for adverse events (PRO-CTCAE)[J].JAMA Oncol,2015,1(8):1051-1059.
[9] BENSON A B,VENOOK A P,AL-HAWARY M M,et al.
NCCN guidelines insights:colon cancer,version 2.2018[J].J Natl Compr Canc Netw,2018,16(4):359-369.
[10] VAN C E,CERVANTES A,NORDLINGER B,et al.
Metastatic colorectal cancer:ESMO clinical practice guidelines for diagnosis,treatment and follow-up[J].Ann Oncol,2014,25(S3):iii1-iii9.
[11] SUNAKAWA Y,FUJITA K,ICHIKAWA W,et al.A phase Ⅰ study of infusional 5-fluorouracil,leucovorin,oxaliplatin and irinotecan in Japanese patients with advanced colorectal cancer who harbor UGT1A1*1/*1,*1/*6 or *1/*28[J].Oncology,2012,82(4):242-248.
[12] SOUGLAKOS J,ANDROULAKIS N,SYRIGOS K,et al.
FOLFOXIRI (folinic acid, 5-fluorouracil, oxaliplatin and irinotecan) vs FOLFIRI (folinic acid, 5-fluorouracil and irinotecan) as first-line treatment in metastatic colorectal cancer (MCC):A multicentre randomised phase Ⅲ trial from the Hellenic Oncology Research Group (HORG)[J].Br J Cancer,2006,94(6):798-805.
[13]杨雷,廖洪,徐克强.伊立替康致迟发性腹泻的机制和治疗进展[J].中国医药导报,2015,12(32):30-33.
[14]姜志超,张雯,孙永琨,等.FOLFOXIRI改良方案一线治疗晚期胃癌疗效及安全性分析[J].中国肿瘤临床,2020,47(9):438-441.
[15]夏晖,王璇,王之彝,等.1例伊立替康致迟发性腹泻的病例分析[J].中国药师,2016,19(3):543-545.
[16]梅丹,陆俊国,顾海娟,等.伊立替康化疗相关性腹泻发生的特点与危险因素分析[J].中国医院药学杂志,2019,39(2):191-195.
[17] LIU X,CHENG D,KUANG Q,et al.Association of UGT1A1*28 polymorphisms with irinotecan-induced toxicities in colorectal cancer:A meta-analysis in Caucasians[J].Pharmacogenomics J,2014,14(2):120-129.
[18] ETIENNE-GRIMALDI M C,BOYER J C,THOMAS F,et al.
UGT1A1 genotype and irinotecan therapy:general review and implementation in routine practice[J].Fundam Clin Pharmacol,2015,29(3):219-237.
[19]梅丹,陸俊国,顾海娟,等.伊立替康联合替吉奥方案化疗致严重迟发性腹泻1例分析[J].中国药物警戒,2020,17(6):373-376.
(收稿日期:2021-09-06) (本文编辑:张明澜)
