化学发光法与液相色谱串联质谱法测定多囊卵巢综合征女性体内性激素的比较分析
2022-03-30葛佳佳杨娜张潇莉沈山梅葛卫红中国药科大学南京鼓楼医院南京0008南京大学医学院附属鼓楼医院南京0008南京中医药大学南京00
葛佳佳,杨娜,张潇莉,沈山梅,葛卫红*(.中国药科大学南京鼓楼医院,南京 0008;.南京大学医学院附属鼓楼医院,南京 0008;.南京中医药大学,南京 00)
多囊卵巢综合征(polycystic ovary syndrome,PCOS)是一种常见的生殖内分泌疾病,发病率介于5%~20%,表现为月经稀发、闭经、不孕、高雄激素血症、多毛、痤疮和卵巢多囊样改变等。其发病机制复杂且尚未明确,可能与性激素代谢紊乱相关。其中高雄激素血症被普遍认为是PCOS 关键的病理生理改变,雄激素水平尤其是睾酮(testosterone,T)指标的准确定量对PCOS 的诊断至关重要。在临床,医师还会对其他PCOS 相关的性激素水平进行评估以加强诊断和鉴别诊断。雌激素是类固醇激素代谢的下游物质,与雄激素的代谢紧密相关。雌二醇(estradiol,E2)是生物活性最强的一种雌激素,也是PCOS诊断和药物治疗的一项重要评估指标。
液相色谱串联质谱分析(liquid chromatography-tandem mass spectrometry,LC-MS/MS)法是雄激素测定的金标准。该方法结合了液相色谱仪器的分辨力以及质谱的高特异性,可从少量样品中分析多种物质,具有更高的准确度、精密度和灵敏度。但在实际的临床实践中,医院多采用化学发光免疫法(chemiluminescent immunoassay,CLIA)测定性激素。它是一种结合化学发光和免疫分析的检测方法,操作简单、检测速度快,而且具备较高的检测灵敏度。本研究使用LCMS/MS 法测定与PCOS 发生、诊断最为密切相关的T 和E2 两种性激素水平,并与临床上CLIA法的检测结果进行比较分析。
1 材料
为提高一致性检验的准确程度,根据Bland等的推荐,采用Bland-Altman 分析的样本量最好达到100 例。因此,本研究收集了2020年1—6月就诊于南京大学医学院附属鼓楼医院妇科门诊并符合2003年鹿特丹诊断标准的PCOS 患者100 例。纳入标准:① 稀发排卵或无排卵;②高雄激素血症或高雄激素临床表现(脂溢性皮炎、多毛、痤疮等);③ 任意一侧卵巢内直径2 ~9 mm 的未成熟卵泡>12 个或卵巢体积>10 mL;符合以上任意两条即可。排除标准:① 其他引起类似PCOS 症状的疾病,如甲亢、高泌乳素血症、肾上腺疾病等;② 合并其他重大疾病、肿瘤患者;③ 妊娠女性。
2 方法
2.1 化学发光免疫法
采用CLIA 法测定血清中T 和E2 的浓度。所用仪器为西门子全自动化学发光免疫分析仪(德国,Atellica/IH01375),检测所需试剂均为配套试剂,按规定的要求操作。剩余血清于-80℃冰箱保存,留作LC-MS/MS 分析法测定。
2.2 LC-MS/MS 法
使用Waters ACQUITY UPLC I-Class/XEVO TQD 超高效液相色谱质谱联用仪测定T 和E2 的浓度。 对照品T(纯度:99.2%, 批号:G157843,德国DR.E),E2(纯度:96.3%,批号:100182 ~201205,中国食品药品检定研究院),内标睾酮-d3(T-d3,纯度 98%,美国Sigma)和雌二醇-d4(E2-d4,纯度 98%,加拿大TRC)。参考本实验室前期建立的方法,采用液液萃取方法进行前处理,色谱柱为Waters BEH C(2.1 mm×100 mm,1.7 μm),流动相为0.1%甲酸水(A)-乙腈(B),等度洗脱(70%B)。质谱采用电喷雾离子源,MRM 离子对分别为:T:289.3 →97.04,T-d3:292.32 →97.03,E2:506.27 →171.05,E2-d4:510.27 →171.05。本方法T 和E2 的线性范围均为3 ~300 nmol·L(r
>0.995)。该LC-MS/MS 方法已由本实验室参考生物样品定量分析方法验证指导原则完成方法学考察。2.3 统计方法
采用 SPSS 26 软件,两种方法测得的数据采用均值±标准差表示。两种方法测定数据的差值符合正态分布且差值不随均值增大而增大时,使用Medcalc 软件直接进行Bland-Altman 分析;当差值明显随着均值增大而增大时,对数据进行对数转换后进行Bland-Altman 分析,以评估CLIA 法与LC-MS/MS 法的一致性。使用配对t
检验和Pearson 相关性分析进行整体数据的比较,P
<0.05 为差异有统计学意义。3 结果
3.1 两种检测方法的结果比较
将CLIA 法和 LC-MS/MS 法测定的T、E2血清浓度进行比较分析,结果见图1。CLIA 法检测T、E2 浓度的平均值分别为(1.45±0.43)nmol·L和(0.17±0.08)nmol·L。LC-MS/MS 法测定的T、E2 的平均值分别为(1.48±0.74)nmol·L和(0.11±0.07)nmol·L。将两组检测结果进行配对样本t
检验,结果两种检测方法测得T 浓度差异无统计学意义(P
=0.54),测得E2 浓度差异有统计学意义(P
<0.001)。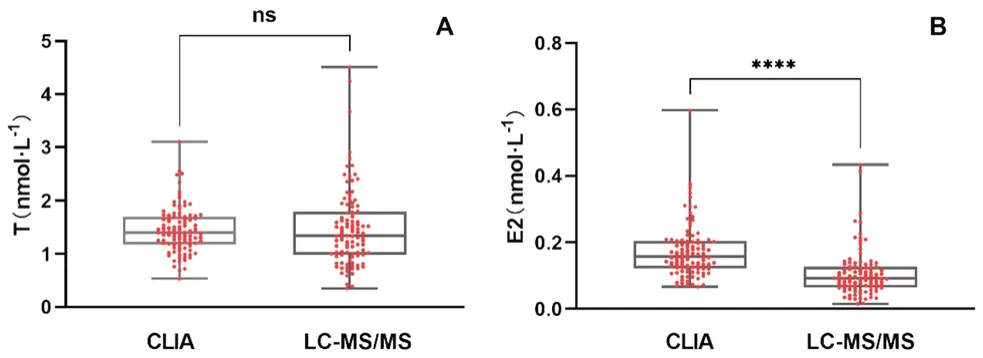
图1 CLIA 法和LC-MS/MS 法测定的结果(****P <0.0001)Fig 1 Results of CLIA method and LC-MS/MS method(****P <0.0001)
3.2 两种检测方法的相关性和一致性分析
为进一步比较 CLIA 法和 LC-MS/MS 法的测定结果,利用100 个样本分别进行Pearson 相关性分析和Bland-Altman 一致性分析。在Pearson相关性分析中,T 和E2 的相关系数分别为 0.774和0.883(P
均<0.001),两种检测方法的结果呈强度相关。在Bland-Altman 一致性分析中,100 例配对数据的T 的比值的均数是104.95%(95%CI
:98.97%~111.28%),一致性下限为58.83%(95%CI: 53.19% ~65.04%), 一致性上限为187.2%(95%CI
:169.32% ~207.0%);100 例配对数据的E2 的差值的均数是0.065(95%CI
:0.057 ~0.072),一致性下限为-0.009(95%CI
:-0.022 ~0.004),一致性上限为0.139(95%CI
:0.126 ~0.152),Bland-Altman 图见图2。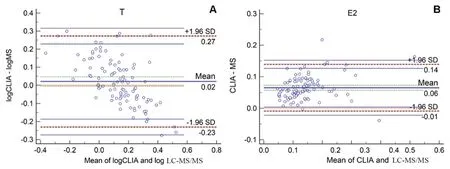
图2 两种检测方法测定结果的Bland-Altman 图Fig 2 Bland-Altman diagram of detection results by 2 methods
从图中可以看出,T 和E2 均有4%(4/100)的点在一致性界限外。在一致性界限范围内,T 比值的最大值为1.87,最小值为0.58。说明CLIA 法测量的T 是LC-MS/MS 法的0.58 ~1.87倍,即CLIA 法的测量结果与LC-MS/MS 测量结果最大相差87%;在一致性界限范围内,E2 差值的最大值为0.144 nmol·L,两种测量方法的E2 平均值为0.141 nmol·L;从临床上考虑,T 和E2 测量结果相差的幅度均是不能接受的,两种检测方法的一致性不佳。
3.3 两种检测方法对高雄激素血症诊断的分析
依据2018年多囊卵巢综合征诊治内分泌专家共识,高雄激素血症是PCOS 的诊断内容之一,且由于不同的测定方法和参考范围,测定值高于当地女性参考范围的正常上限即可考虑高雄激素血症,故采用本院根据当地女性T 浓度制订出来的参考区间:0.3 ~1.66 nmol·L,即CLIA 法采用T >1.66 nmol·L诊断为高雄激素血症。CLIA 法共确定了28 名(28%)高雄激素血症患者。LC-MS/MS 法的结果采用Yang 等在中国人群中利用质谱法建立的高雄激素血症标准:T >1.85 nmol·L。使用 LC-MS/MS 方法最终确定24 名(24%)高雄激素血症的PCOS 患者。
值得注意的是,尽管通过CLIA 法与LC-MS/MS 法识别为高雄激素血症的 PCOS 女性的百分比相似,但在将个体分配到高雄激素血症和非高雄激素血症的类别中存在一定的不匹配(见图3)。以金标准(LC-MS/MS)作为参考,总共100 名女性中有16 名(16%)被CLIA 法不恰当地分类。其中,10 例患者出现假阳性,6 例患者出现假阴性。

图3 PCOS 女性通过CLIA 测定方法确定为高雄激素血症或非高雄激素血症的情况Fig 3 PCOS women identified as hyperandrogenemic or normoandrogenemic by CLIA assay
4 讨论
性激素的测定,尤其是T 对PCOS 的临床诊断和治疗具有一定的参考价值,其最终的结果必须准确、特异和灵敏。本研究通过CLIA 法和 LCMS/MS 法对100 名PCOS 患者的血清T、E2 进行测定,并进行两组数据的比较和分析。结果表明,尽管两种检测方法之间存在总体适度的相关性,但并不能充分反映它们之间的一致性。Bland-Altman 一致性分析的结果表明,CLIA 法和LC-MS/MS 法在测定性激素水平方面一致性不佳,CLIA 法测定的性激素水平普遍偏高,高雄激素血症的假阳性率和假阴性率也较高。
高雄激素血症对PCOS 的诊断具有重要参考意义。卵巢中膜细胞的雄激素生成增加已被证明,在PCOS 中进行准确的雄激素测量非常重要。本研究结果与Salameh 等的研究一致,通过LC-MS/MS 和免疫测定法的T 指标具有较强的相关性。但是在一致性评价中,与金标准LC-MS/MS 测定法相比,CLIA 法并没有表现出一致的检测水平。而且对PCOS 患者进行个体评估时,可能会受到某些因素的影响而发生数据偏差,CLIA 法的假阳性率为15.2%,假阴性率为25%,这与Tosi 等的研究结果相似。可能是由于CLIA 法极易受环境影响,稳定性差的原因。
此外,结果还显示两种检测方法测定的E2水平存在显著差异,在以往的文献中尚未有类似的研究。人们多关注雄激素的变化,但在整个类固醇代谢谱中,雌激素、孕激素和雄激素的变化紧密关联。测定雌激素等其他性激素对PCOS 的诊断和治疗也是十分必要的。本研究中CLIA 法测得的雌激素水平明显被高估,这可能是因为性激素之间的化学结构高度类似,CLIA 法容易发生免疫交叉反应,无法特异性区分E2 和其他性激素。
目前,CLIA 法因其操作简便、易实现自动化等优势在许多实验室和医院中广泛使用。但由于易受相关内源性物质、外界环境、基质效应等的干扰,其对于性激素测定的特异性和可靠性存在疑问。相比于免疫测定方法,LC-MS/MS 法具有所需样品体积小、灵敏度和特异性大大提高,动态范围大,可同时检测多种性激素的优势,成为定量性激素的金标准,并逐渐被应用于一些具备条件的临床实验室中。在未来,越来越成熟的LC-MS/MS 法将取代各种免疫法成为性激素研究的主要方法,临床上应积极满足建立LC-MS/MS 法相关的设备、软件、训练有素的员工等条件,将LC-MS/MS 技术广泛应用于精确的性激素的测定等临床项目。
