高纯稀土氧化物的制备试验研究
2022-03-29崔建国侯睿恩陈禹夫
乔 军,崔建国,王 哲,侯睿恩,陈禹夫
(1.包头稀土研究院 白云鄂博稀土资源研究与综合利用国家重点实验室,内蒙古 包头 014030;2.稀土冶金及功能材料国家工程研究中心,内蒙古 包头 014030)
市售稀土氧化物中铁、铅、铜、锌等重金属杂质质量分数偏高,难以适应新材料领域要求。用硫化物沉淀法可以去除重金属杂质元素[1-5],但对于从稀土溶液中去除重金属杂质的研究报道较少[6]。课题组近十年来一直进行相关研究。
试验研究了采用硫化物沉淀法从稀土料液中去除杂质获得纯净稀土料液,以制备高纯稀土氧化物,提高稀土收率。
1 试验部分
1.1 原料与试剂
工业草酸:质量分数>99.6%,乌海恒昌化工有限责任公司。工业草酸中含有一定量重金属杂质,使用前先用结晶法去除[7-11]。
氯化镧料液:ρ(La2O3)/ρ(REO)≥99.99%,ρ(La3+)=283.0 g/L,ρ(Cu2+)=12.3 mg/L,ρ(Zn2+)=926.0 mg/L,ρ(Fe3+)=0.5 mg/L,ρ(Pb2+)=1.1 mg/L,盐酸体系,pH=3,取自北方某稀土生产企业。
氯化铈料液:ρ(CeO2)/ρ(REO)≥99.99%,ρ(Ce3+)=327.0 g/L,ρ(Fe3+)=1.5 mg/L,ρ(Zn2+)=2.8 mg/L,ρ(Pb2+)=1.0 mg/L,ρ(Cu2+)=1.1 mg/L,盐酸体系,pH=3,取自北方某稀土生产企业。
硝酸镧料液:ρ(La2O3)/ρ(REO)≥99.99%,ρ(La3+)=316.0 g/L,ρ(Fe3+)=7.5 mg/L,ρ(Pb2+)=4.5 mg/L,ρ(Zn2+)=156.1 mg/L,ρ(Cu2+)=3.6 mg/L,硝酸体系,pH=3,取自北方某稀土生产企业。
硫化铵溶液:质量浓度(以S计)78 g/L,分析纯,天津化工试剂厂。
硝酸:分析纯,天津化工试剂厂。
水:由Heal Force型超纯水仪制备,二次水,电阻率大于18.0 MΩ·cm。
Y2O3,Pr6O11:市售,江阴加华新材料资源有限公司;
Gd2O3,Dy2O3:市售,广东从化市建丰稀土有限公司;
Er2O3,Tm2O3,Yb2O3,Lu2O3:市售,深圳鸿博稀土新材料有限公司。
稀土氧化物原料的化学组成见表1。

表1 稀土氧化物原料的化学组成
1.2 试验设备
电动搅拌器:JB90-S型,上海梅颖普公司;循环水真空泵:SHB-Ⅲ型,西安太康生物科技有限公司;电子天平:HZF-B型,2 000 g/0.1 g,福州华志科学仪器有限公司;电子天平:HZF-C 8 000 g/1 g,福州华志科学仪器有限公司;万用电炉:DL型,12 kW,北京永光明医疗仪器有限公司;封闭电炉:FL-2 1.5 kW,北京永光明医疗仪器有限公司;封口机:SF-300型,温州市兴业机械设备有限公司。
1.3 分析方法
稀土氧化物中的REO和纯度分别采用容量法、质谱法测定,稀土溶液中REO浓度采用EDTA配合滴定法测定;杂质铁、铅、锌、铜离子以原子吸收及质谱法测定。
1.4 试验方法
工业草酸经二次纯水溶解后,过滤除去可见杂物,滤液浓缩蒸发并冷却后析出草酸晶体,风干后备用;草酸沉淀母液循环使用。
取一定体积稀土溶液,加水稀释,搅拌条件下加入硫化铵溶液,持续搅拌一段时间后,用定量滤纸过滤,得到稀土滤液和硫化物沉淀。以结晶草酸为沉淀剂沉淀稀土草酸盐,稀土草酸盐通过灼烧得到低重金属杂质含量的高纯稀土氧化物。
稀土料液包括生产线上的氯化镧、氯化铈、硝酸镧3种料液,以及用硝酸溶解工业稀土氧化物得到的硝酸镨、硝酸钇、硝酸钆、硝酸镝、硝酸铒、硝酸铥、硝酸镱、硝酸镥8种料液。铁、铅、锌、铜杂质在工业稀土氧化物中以氧化物形式存在,硝酸溶解过程中被溶出。
工业稀土氧化物硝酸溶解反应如下:

(Ln:Y,Gd,Dy,Er,Tm,Yb,Lu);
(1)

(2)

(3)

(4)

(5)

(6)
稀土料液中杂质金属硫化沉淀反应:
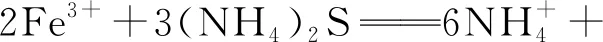
(7)
(8)
(9)
(10)
高纯溶液中草酸沉淀稀土反应:

Ln2(C2O4)3·9H2O↓+6HNO3,
(Ln:La,Ce,Pr,Y,Gd,Dy,Er,Tm,Yb,Lu)。
(11)
稀土草酸盐灼烧反应:

(Ln:La,Y,Gd,Dy,Er,Tm,Yb,Lu);
(12)

(13)

(14)
试验中,以某杂质元素对最终稀土氧化物纯度的影响最为显著为原则,影响较小的元素不予跟踪。跟踪杂质:工业草酸和结晶草酸选定Fe2O3、PbO,氯化镧料液杂质选定CuO、ZnO,氯化铈料液选定ZnO、Fe2O3,硝酸镧料液选择Fe2O3、PbO,稀土氧化物原料、硝酸稀土溶液和最终稀土氧化物选定Fe2O3、PbO、ZnO和CuO。
2 洁净稀土料液的制备
常见稀土料液为氯化镧、氯化铈及硝酸镧溶液。基于硫离子能与大部分非稀土重金属离子形成沉淀,而与稀土离子共存的原理,去除重金属离子。金属硫化物在水溶液中的溶度积Ksp见表2。

表2 不同金属硫化物在水中的Ksp
针对氯化镧料液,考察镧离子浓度、反应温度、反应时间、硫化铵质量浓度对杂质离子去除率和镧离子收率的影响;针对氯化镧、氯化铈、硝酸镧3种料液,考察硫化铵溶液用量对杂质离子去除率和稀土离子收率的影响;针对氧化镨、氧化钆、氧化镝、氧化钇、氧化铒、氧化铥、氧化镱、氧化镥8种常见工业稀土氧化物,考察硫化沉淀法除杂提纯效果。结合生产实际,选取2种主要影响产品质量的杂质元素跟踪考察其去除效果。
2.1 氯化镧料液除杂
2.1.1 氯化镧质量浓度对杂质离子去除率和La3+收率的影响
试验条件:硫化铵溶液质量浓度(以S2-计,下同)26 g/L,硫化铵溶液加入量0.4%(相对于料液体积),室温,反应时间15 min。氯化镧质量浓度对杂质离子去除率和La3+收率的影响试验结果如图1所示。

图1 氯化镧质量浓度对杂质离子去除率和La3+收率的影响
由图1看出:随氯化镧质量浓度升高,杂质离子去除率及La3+收率均降低。体系中氯化镧质量浓度升高,则含水量降低,加入碱性硫化铵溶液后,pH快速升高,致使一些La3+水解产生胶状沉淀La(OH)3,导致La3+收率下降3%,且CuS、ZnS沉淀反应明显受阻,Cu2+、Zn2+去除率下降。综合考虑,确定氯化镧质量浓度以100 g/L为宜。
2.1.2 温度对杂质离子去除率和La3+收率的影响
试验条件:氯化镧质量浓度100 g/L,硫化铵质量浓度26 g/L,硫化铵溶液加入量0.4%(相对于料液体积),反应时间15 min。温度对杂质离子去除率和La3+收率的影响试验结果如图2所示。

图2 温度对杂质离子去除率和La3+收率的影响
由图2看出:随温度升高,杂质离子去除率和La3+收率均下降;反应温度为20 ℃时,Cu2+、Zn2+去除率最高;温度升到40 ℃,部分硫离子会发生水解,产生硫化氢气体逸出,导致部分硫离子未能参与反应;同时,La3+在40~60 ℃下也易水解成La(OH)3沉淀,使La3+收率降低。综合考虑,确定除杂在室温下进行即可。
2.1.3 反应时间对杂质离子去除率和La3+收率的影响
试验条件:氯化镧质量浓度100 g/L,硫化铵质量浓度26 g/L,硫化铵溶液加入量0.4%(相对于料液体积),室温。反应时间对杂质离子去除率和La3+收率的影响试验结果如图3所示。
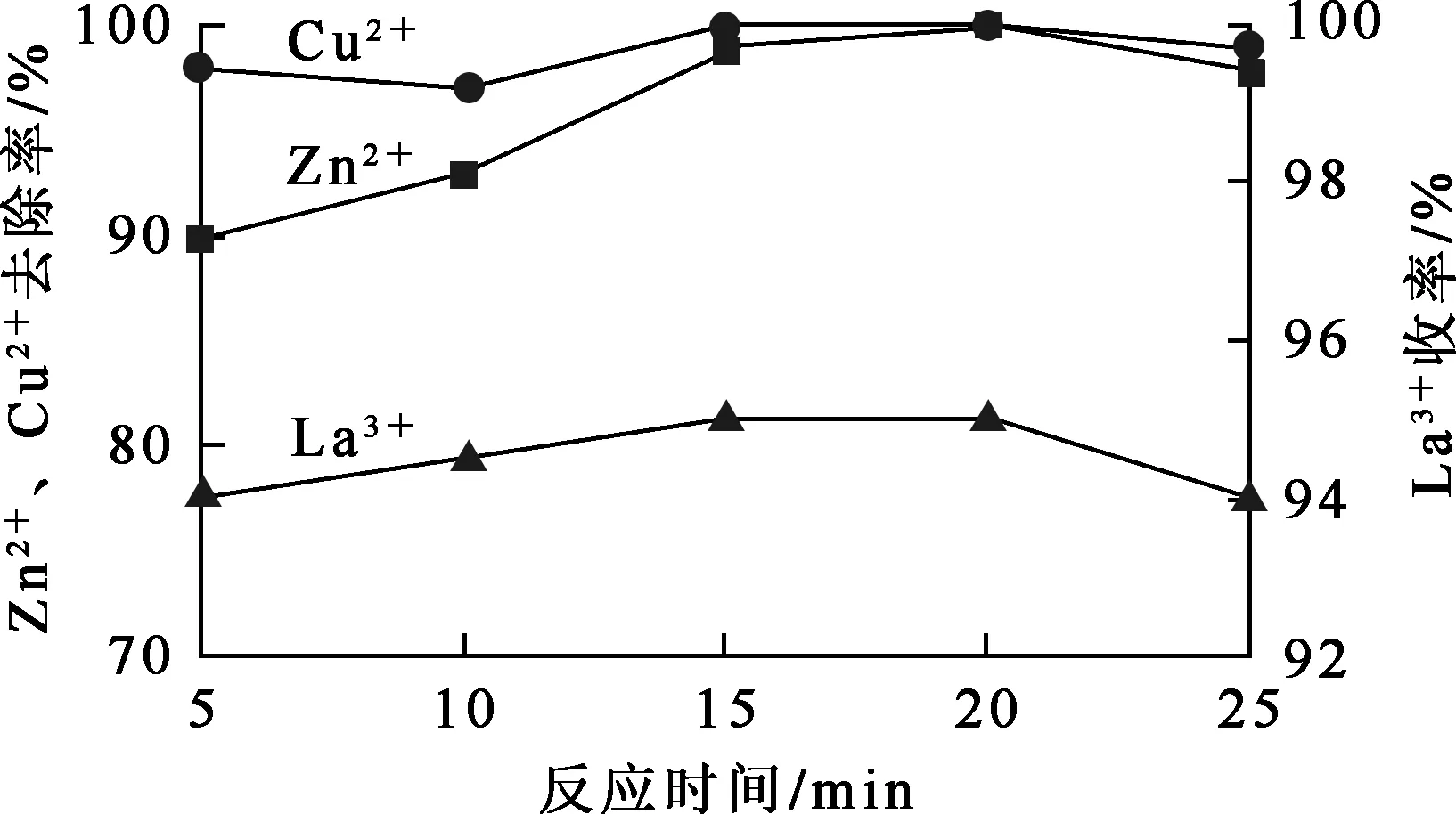
图3 反应时间对杂质离子去除率和La3+收率的影响
由图3看出:随反应时间延长,Cu2+去除率略有提高但幅度不大,Zn2+去除率从90%提高到100%,之后略有下降。硫化物沉淀反应速度相对较慢,反应时间短时,反应不完全;但反应时间过长,已生成的硫化物又会发生溶解,使沉淀去除率略有降低。La3+收率稳定在95%左右,反应时间影响不大。综合考虑,确定反应时间以15 min为宜。
2.1.4 硫化铵质量浓度对杂质离子去除率和La3+收率的影响
试验条件:氯化镧质量浓度100 g/L,硫化铵溶液加入量0.4%(相对于料液体积),反应时间15 min。室温下,硫化铵质量浓度对杂质离子去除率和La3+收率的影响试验结果如图4所示。

图4 硫化铵质量浓度对杂质离子去除率和La3+收率的影响
由图4看出:随硫化铵质量浓度升高,Cu2+去除率略有下降,而Zn2+去除率大幅下降至90%左右,La3+收率从100%降为90%。硫化铵质量浓度升高,体系pH快速升高,易使La3+水解生成La(OH)3沉淀,并导致Zn2+沉淀效果变差;但硫化铵质量浓度也不能过低,否则会给后续草酸沉淀工序造成压力。综合考虑,确定S2-质量浓度以26 g/L为宜。
2.2 硫化铵溶液加入量对3种稀土料液杂质离子去除率和稀土离子收率的影响
试验条件:3种料液(氯化镧溶液,ρ(La3+)=100 g/L;氯化铈溶液,ρ(Ce3+)=100 g/L;硝酸镧溶液,ρ(La3+)=100 g/L)各取250 mL,硫化铵质量浓度26 g/L,室温,反应时间15 min。硫化铵溶液加入量对3种料液杂质离子去除率和稀土离子收率的影响试验结果如图5~7所示。
由图5看出:对于氯化镧料液,随硫化铵溶液加入量增加,Zn2+去除率逐渐升高,Cu2+去除率较为稳定。硫化铜溶度积8.9×10-35远低于硫化锌溶度积8.9×10-25,Cu2+更易生成硫化物沉淀。La3+收率呈下降趋势,因为随硫化铵溶液加入,体系pH逐渐升高,少量La3+会发生水解形成氢氧化镧沉淀,造成收率下降。综合考虑,对于氯化镧料液,确定硫化铵溶液加入量以3.0 mL(相对于料液体积1.2%)为最佳。

图5 硫化铵溶液加入量对氯化镧料液杂质离子去除率和La3+收率的影响
由图6看出:对于氯化铈料液,随硫化铵溶液加入量增加,Zn2+去除率由65%逐渐升至100%,Fe3+去除率由35%升至近100%。硫化锌溶度积为8.9×10-25,低于硫化铁溶度积4.9×10-18,更容易沉淀。Ce3+收率呈下降趋势,因为S2-的水解使体系局部碱性增大,部分Ce3+会水解为氢氧化铈沉淀。综合考虑,硫化铵溶液加入量以2.0 mL(相对于料液体积0.8%)为最佳。
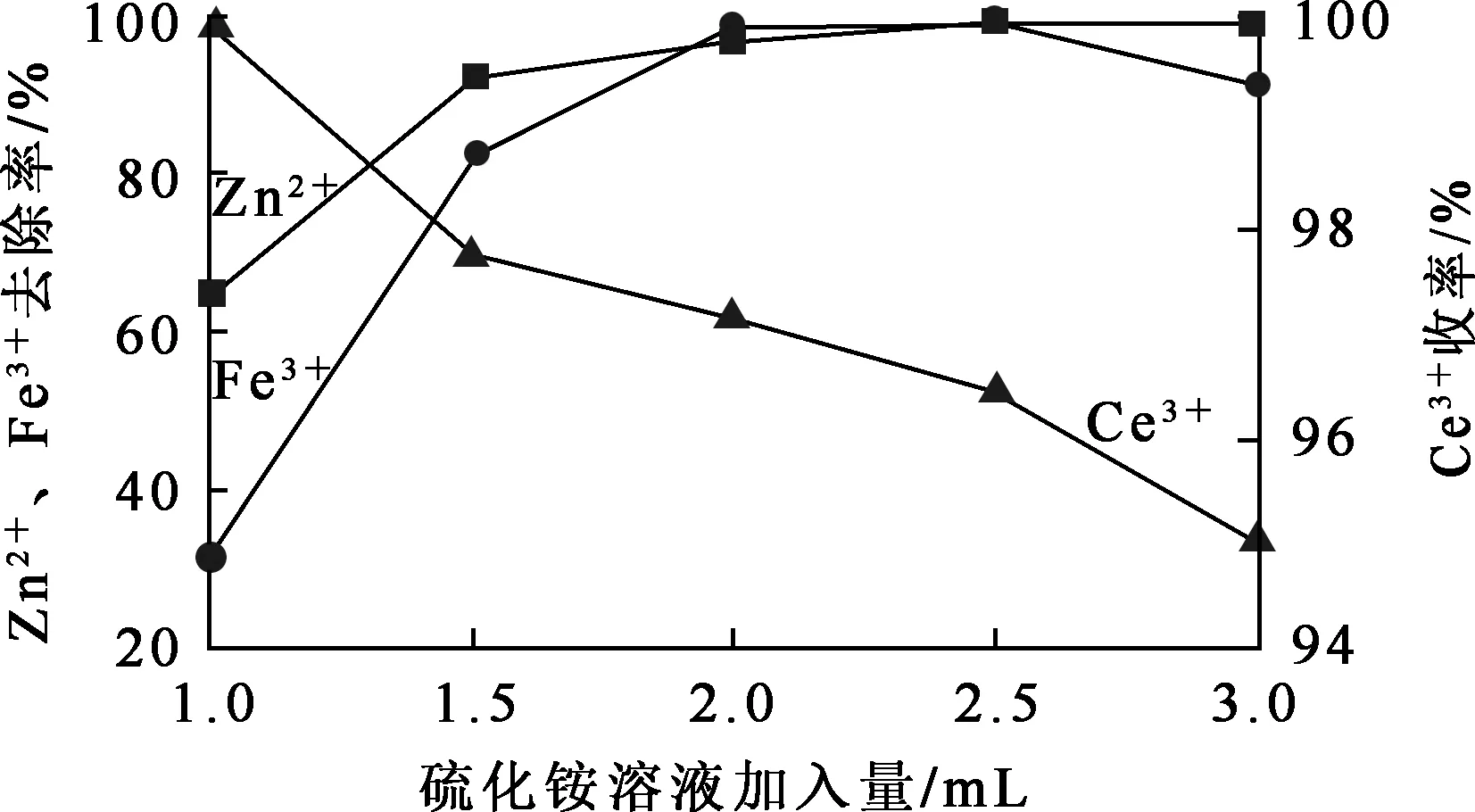
图6 硫化铵溶液加入量对氯化铈料液杂质离子去除率和Ce3+收率的影响
由图7看出:对于硝酸镧料液,随硫化铵溶液加入量增加,Fe3+去除率由55%升至近98%,Pb2+去除率由88%升至100%。硫化铅溶度积9.3×10-28远低于硫化铁溶度积4.9×10-18,更容易沉淀。La3+收率在硫化铵溶液加入量1.0 mL后呈下降趋势,氢氧化镧沉淀的生成会造成La3+损失。综合考虑,硫化铵溶液加入量以1.8 mL(相对于料液体积0.72%)为最佳。

图7 硫化铵溶液加入量对硝酸镧料液杂质离子去除率和La3+收率的影响
2.3 硫化铵除杂工艺对工业稀土氧化物的提纯
针对8种工业稀土氧化物进行除杂提纯。因镧系稀土元素性质相似,稀土精矿中又以镧、铈为主,所以除杂试验中除考察硫化铵溶液加入量条件外,其他试验条件的考察均采用3种生产料液。
8种工业稀土氧化物(氧化镨、氧化钆、氧化镝、氧化钇、氧化铒、氧化铥、氧化镱、氧化镥)各25 g,硝酸溶解后加水稀释至250 mL,分别加入硫化铵溶液除杂,在室温下反应时间15 min,硫化铵质量浓度(以S2-计)26 g/L,硫化铵溶液加入量均为3.5 mL。反应后过滤,得8种硝酸稀土溶液,分析结果见表3。可以看出:硫化铵溶液加入量为料液体积1.4%时,各溶液中杂质离子均可以有效去除;其中,Cu2+最易被去除,其次是Pb2+、Zn2+,而Fe3+最难被去除;稀土离子收率均大于95%。硫化铵溶液加入量为料液体积的1.4%,大于3种生产料液除杂时的硫化铵溶液加入量(氯化镧料液1.2%、氯化铈料液0.8%、硝酸镧料液0.72%),因为工业稀土氧化物料液较生产线料液的杂质元素含量更低,更难被去除,需要硫化铵溶液稍微过量。
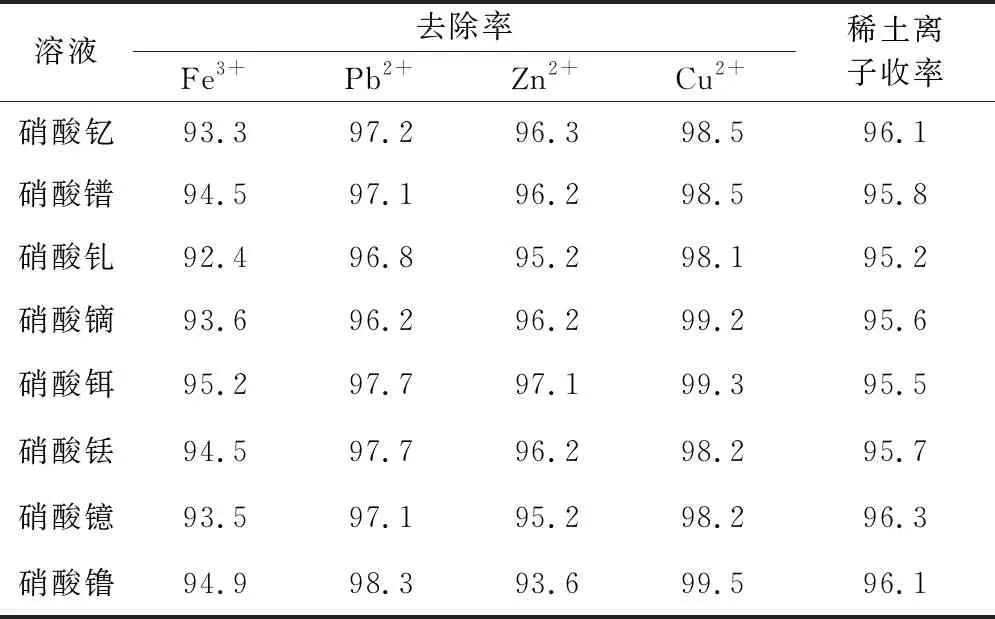
表3 硝酸稀土溶液中杂质离子去除率和稀土离子收率 %
2.4 从净化稀土溶液中沉淀草酸稀土
适宜条件下,以工业草酸制备分析纯结晶草酸,并用以作为沉淀剂从净化后的稀土料液中沉淀稀土草酸盐,然后通过灼烧,得到高纯稀土氧化物。所得稀土氧化物的化学组成见表4。
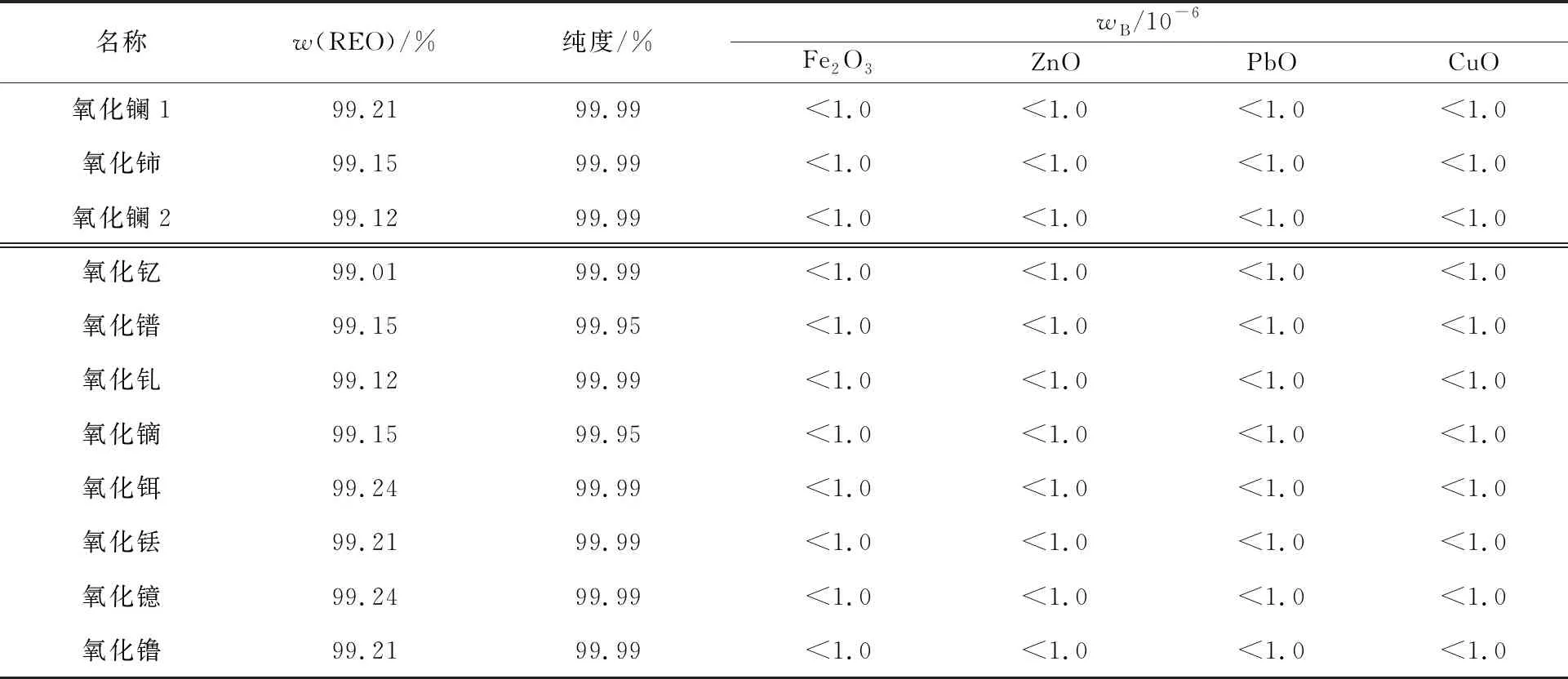
表4 高纯稀土氧化物化学组成
3 放大试验
取8种工业氧化物各10 kg进行硫化铵除杂试验,结果见表5。可以看出:高纯稀土氧化物收率均大于96%,杂质元素氧化物质量分数均小于1×10-6。

表5 放大试验中高纯稀土氧化物化学组成
4 结论
采用硫化铵溶液沉淀法可有效去除稀土氧化物和稀土料液中的铁、铅、锌、铜杂质离子,净化后料液通过草酸沉淀和灼烧,可获得高纯稀土氧化物,其中杂质质量分数均低于1.0×10-6。工艺中用到的草酸以工业草酸通过结晶法制备,生产成本大大降低,且生产过程无废物产生,绿色环保。
