用CTAB改性膨润土从低浓度废水中吸附去除U(Ⅵ)
2022-03-29张益硕周仲魁杨顺景李荆瑜
张益硕,周仲魁,杨顺景,李荆瑜
(1.东华理工大学 核资源与环境国家重点实验室,江西 南昌 330013;2.东华理工大学 水资源与环境工程学院,江西 南昌 330013)
铀是一种天然放射性重金属元素,环境中如存在铀,会对人及动植物造成辐射伤害[1-5],因此,含铀废水经处理后才能排放[6]。铀在水溶液中主要以U(Ⅵ)形式存在。常见的含铀废水处理方法有电化学法、离子交换法、化学沉淀法、膜分离法、吸附法等[4]。吸附法因效率高、操作简单、环保及能耗低而得到广泛应用[7-8]。膨润土是一种以蒙脱石为主要成分的含水材料,价格低廉、性质稳定、比表面积大、多孔、阳离子交换容量大、膨胀性强、吸附能力强,可用作吸附材料;但未经改性的膨润土通常带有负电荷,其吸附阳离子的能力较差。对膨润土进行改性,可以提高其吸附能力,用于吸附去除有害物质[9-11]。目前,膨润土改性工艺较复杂,成本较高,因此,研究一种制备方法简单、成本低廉且可用于从废水中吸附去除U(Ⅵ)的改性膨润土有重要意义。
CTAB(十六烷基三甲基溴化铵)为阳离子表面活性剂,可将大量疏水官能团引入到膨润土层间,改善膨润土的表面性能和结构,提高其对水体中污染物的吸附能力[12-13]。试验研究了用CTAB改性膨润土,并用于从低浓度废水中吸附去除U(Ⅵ),以期为含铀废水的处理提供一种可用吸附剂。
1 试验部分
1.1 试剂与仪器
主要试剂:碳酸钠、氢氧化钠、盐酸、U(Ⅵ)标准溶液、CTAB(十六烷基三甲基溴化铵)、乙二醇、5%HNO3(ICP-OES使用),均为分析纯。
主要仪器:电热鼓风干燥箱(DHG-9070A),pH计(ST3100),恒温空气摇床(ZWYR-240),双光束紫外分光光度计(UV-1400PC),集热式恒温加热磁力搅拌器(DF-101S),高速离心机(Gl-21m),电感耦合等离子体发射光谱仪(ICP-OES,Agilent 5100),红外光谱仪分析仪(BRUKER VERTEX70),扫描电镜(TESCAN MIRA4)。
1.2 CTAB改性膨润土
对天然钙基膨润土进行研磨,筛分过50目筛。取5.0 g钙基膨润土,加入适量碳酸钠,再加入350 mL超纯水,磁力搅拌一定时间后,静置陈化,得钠基膨润土。取钠基膨润土于1 000 mL烧杯中,于333.15 K水浴锅上加热搅拌。CTAB为有机试剂,在超纯水中几乎不溶解,根据相似相溶原理,用乙二醇辅助CTAB使其溶解完全,之后加入到装有钠基膨润土的烧杯中,保持水温333.15 K,继续搅拌4 h。之后,于室温下静置48 h,抽滤,离心洗涤(防止乙二醇干扰),洗涤液用1%硝酸银溶液检测无沉淀,滤饼于328.15 K烘箱中烘干,制得CTAB改性钠基膨润土。
1.3 改性膨润土吸附U(Ⅵ)
取一定质量浓度U(Ⅵ)溶液50 mL于锥形瓶中,用盐酸或氢氧化钠溶液调pH,加入一定量改性膨润土,在适宜温度下进行吸附,然后取吸附尾液用针头滤膜过滤,对滤液用ICP-OES测定U(Ⅵ)质量浓度,并按式(1)、(2)计算U(Ⅵ)去除率(y)和吸附量(qt)。
(1)
(2)
式中:ρ1—吸附前U(Ⅵ)质量浓度,mg/L;ρ2—吸附后U(Ⅵ)质量浓度,mg/L;V—溶液体积,L;m—改性膨润土质量,g。
2 试验结果与讨论
2.1 材料表征
2.1.1 SEM表征
改性前、后膨润土的SEM照片如图1所示。

a—改性前;b—CTAB改性后。
由图1看出:改性前的膨润土表面光滑,有细微层状突起;而改性后的膨润土表面较粗糙,有大量凸起,层间空隙明显扩大,轮廓与空隙更明显,比表面积增大,表明CTAB已成功与钠基膨润土结合。
2.1.2 FT-IR表征
改性前、后膨润土的FT-IR分析图谱如图2所示。

图2 改性前、后膨润土的FT-IR分析图谱
由图2看出:改性前、后的膨润土均在3 618 cm-1处出现较宽的—OH伸缩振动峰,在796 cm-1处出现Si—O伸缩振动峰和较弱的Si—O—Si吸收振动峰,在988 cm-1处出现较强的Si—O伸缩振动峰,在1 632 cm-1处出现—OH和层间水伸缩振动峰。改性膨润土在1 648 cm-1处出现H—O—H弯曲振动峰,表明改性前后膨润土中都含有结晶水。改性膨润土在2 917 cm-1处出现C—H伸缩振动吸收峰,在2 850 cm-1处出现C—H弯曲振动吸收峰[14-15],表明膨润土改性成功。改性膨润土在993 cm-1处出现Si—O—Si吸收振动峰,且改性前、后峰形变化较小,表明改性并没有改变膨润土原有的层状硅氧骨架结构。
2.2 膨润土对U(Ⅵ)的吸附性能
2.2.1 改性膨润土对U(Ⅵ)的吸附性能
分别将改性前、后的膨润土0.3 g加入到50 mL、初始U(Ⅵ)质量浓度10 mg/L、pH=7.26的模拟废水中,室温下振荡一定时间,吸附试验结果见表1。可以看出:改性膨润土对U(Ⅵ)的吸附去除率和吸附量分别为92.58%和2.02 mg/g,是改性前的3.78倍,去除效果较好。后续试验均采用改性膨润土作吸附剂。

表1 膨润土改性前后对U(Ⅵ)的吸附性能比较
2.2.2 废水pH对改性膨润土吸附U(Ⅵ)的影响
废水体积50 mL,初始U(Ⅵ)质量浓度10 mg/L,改性膨润土用量6 g/L,振荡速率121 r/min,振荡时间180 min,室温下,废水pH对改性膨润土吸附U(Ⅵ)的影响试验结果如图3所示。

图3 废水pH对改性膨润土吸附U(Ⅵ)的影响
由图3看出:在pH=1.17强酸条件下,改性膨润土对U(Ⅵ)的吸附率较低,随pH升高,U(Ⅵ)去除率升高;pH升高到3以后,U(Ⅵ)去除率变化不大。改性膨润土吸附U(Ⅵ)的pH范围较宽,可在不改变中性废水pH条件下使用。强酸条件下,因为H+与U(Ⅵ)发生竞争吸附,使得吸附率较低;随pH升高,溶液中H+浓度逐渐降低,吸附率快速升高。综合考虑,确定改性膨润土吸附去除U(Ⅵ)时可不必调整废水pH。
2.2.3 改性膨润土用量对吸附U(Ⅵ)的影响
废水体积50 mL,初始U(Ⅵ)质量浓度10 mg/L,废水pH=6.77,室温下,振荡速率121 r/min,振荡时间180 min,改性膨润土用量对吸附U(Ⅵ)的影响试验结果如图4所示。可以看出:随改性膨润土用量增加,U(Ⅵ)去除率总体呈先升高后下降趋势;改性膨润土用量为0.8 g/L时,U(Ⅵ)去除率最大,为96.95%,之后随膨润土用量增加而逐渐降低。随改性膨润土用量增加,其所提供的吸附位点相应增多,吸附的U(Ⅵ)也随之增加,但单位改性膨润土的吸附量相应下降;改性膨润土用量过大时易发生团聚,导致吸附能力下降。综合考虑,改性膨润土适宜用量为0.8 g/L。
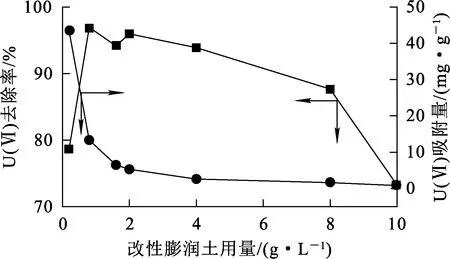
图4 改性膨润土用量对吸附U(Ⅵ)的影响
2.2.4 吸附时间对改性膨润土吸附U(Ⅵ)的影响
废水体积200 mL,初始U(Ⅵ)质量浓度10 mg/L,废水pH=6.86,改性膨润土用量0.8 g/L,振荡速率121 r/min,室温下,吸附时间对改性膨润土吸附U(Ⅵ)的影响试验结果如图5所示。

图5 吸附时间对改性膨润土吸附U(Ⅵ)的影响
由图5看出:随反应时间延长,U(Ⅵ)去除率提高,355 min时达最大,之后趋于稳定。综合考虑,确定适宜吸附时间为355 min。
2.2.5 初始U(Ⅵ)质量浓度对改性膨润土吸附U(Ⅵ)的影响
废水体积50 mL,pH=6.86,改性膨润土用量0.8 g/L,室温,振荡速率121 r/min,振荡时间355 min,初始U(Ⅵ)质量浓度对改性膨润土吸附U(Ⅵ)的影响试验结果如图6所示。可以看出:改性膨润土对U(Ⅵ)的去除率和吸附量均随初始U(Ⅵ)质量浓度升高先升高后下降;初始U(Ⅵ)质量浓度为10 mg/L时,U(Ⅵ)去除率达最大,为96.74%;初始U(Ⅵ)质量浓度在5~10 mg/L范围内,其去除率均超过90%。改性膨润土用量一定时,其吸附位点一定,所能吸附的U(Ⅵ)的量也一定,达到饱和后不再继续吸附。

图6 初始U(Ⅵ)质量浓度对改性膨润土吸附U(Ⅵ)的影响
2.2.6 温度对吸附U(Ⅵ)的影响
废水体积50 mL,初始U(Ⅵ)质量浓度10 mg/L,废水pH=6.89,改性膨润土用量0.8 g/L,振荡时间475 min,温度对改性膨润土吸附U(Ⅵ)的影响试验结果如图7所示。可以看出:随温度升高,U(Ⅵ)去除率提高;室温下,U(Ⅵ)去除率为80%;温度升至453.15 K后,U(Ⅵ)去除率达最高,之后快速下降。温度过高,有可能会破坏改性吸附剂的结构,从而导致吸附能力下降。推断改性膨润土对U(Ⅵ)的吸附反应为吸热反应。

图7 温度对吸附U(Ⅵ)的影响
2.3 吸附动力学及等温线
2.3.1 吸附动力学
对室温下的试验数据进行吸附动力学与等温模型拟合。吸附动力学模型为准一级动力学和准二级动力学模型,拟合结果见表2和图8。

表2 室温下改性膨润土吸附U(Ⅵ)的动力学拟合参数

图8 改性膨润土吸附U(Ⅵ)的准一级和准二级动力学模型拟合曲线

2.3.2 吸附等温线
对改性膨润土吸附U(Ⅵ)的试验数据用Langmuir和Freundlich等温吸附方程进行拟合,拟合参数见表3,吸附等温曲线如图9所示。可以看出:室温下,Langmuir方程的相关系数为0.994 9,大于Freundlich的相关系数0.977 1,表明改性膨润土吸附U(Ⅵ)的过程更符合Langmuir等温吸附模型,吸附过程为单分子层吸附,最大吸附量为27.25 mg/g。

表3 室温下改性膨润土吸附U(Ⅵ)的等温吸附模型参数

图9 改性膨润土对U(Ⅵ)的平衡吸附量与平衡质量浓度之间的关系
3 结论
用CTAB改性膨润土从废水中去除U(Ⅵ)是可行的,适宜条件下,U(Ⅵ)去除率可达96.95%,吸附过程符合准二级动力学模型,以化学吸附为主;室温下,吸附反应更符合Langmuir等温吸附模型,以单分子层吸附为主,最大吸附量为27.25 mg/g。
