基于真实情境的“价-类”思维的构建*
2022-03-17熊娟
熊娟






摘要:“价-类”思维可以预测物质的性质和设计物质间的转化,对于元素化合物的学习有重要作用。以“医生给缺铁性贫血的病人开药”为情境,设计一系列情境问题,利用“价-类”二维图讨论铁盐和亚铁盐的化学性质,通过实验探究解决问题。培养学生利用“价-类”思维学习元素化合物知识,提高学生科学探究的学科素养,体会化学与生活紧密联系,增强社会责任感。
关键词:真实情境;“价-类”二维图;实验探究
文章编号:1008-0546(2022)03x-0050-05 中图分类号:G632.41 文献标识码:B
doi:10.3969/j.issn.1008-0546.2022.03x.012
“价-类”分别指元素价态和物质类别。2019年人教版教材化学必修第一册特别指出“物质类别和元素价态,是学习元素及其化合物性质的重要认识视角”[1]。基于物质的“价-类”思想,可以预测物质的性质和设计物质间的转化,对于元素化合物的学习有重要作用。
一、教学内容及教学现状分析
1.教学内容
“铁盐和亚铁盐”是2019年人教版教材化学第一册第三章“铁金属材料”第一节的内容。主要内容有:铁盐和亚铁盐的性质;铁盐和亚铁盐的转换;铁盐和亚铁盐的检验及应用;运用“价-类”思维分析和解决问题。
2.教学现状分析
《普通高中化学课程标准(2017年版2020年修订)》(以下简称“新课标”)在必修课程内容主题2“常见的无机物及其应用”中指出“结合真实情境中的应用实例或通过实验探究,了解铁及其重要化合物的主要性质,了解它们在生产生活中的应用”[2]。本节内容将知识、实验、应用紧密结合,培养学生模型认知和证据推理、科学探究和创新意识、科学态度和社会责任的核心素养。但在实际教学中存在3个不足:(1)实验探究不足,不能应开尽开。(2)通过“铁三角”关系及化學方程式的书写强调物质的性质和转化,忽视了知识在真实情境中的应用。(3)“价-类”思维渗透不充分,忽视了元素化合物的知识素养化。
二、教学思想与创新
1.创设情境,提出问题
本节课的引入是学生自己主演,自己录制的25秒情景剧。大屏幕中有熟悉的同学,再加上字幕、图片等后期特效,同学们瞬间把注意力集中到课堂上了。提出问题:补铁药片是否含有亚铁?贫血的病人是否缺维生素C?引入问题作为情境主线,推动后续的讨论和探究,使堂课各个环节有机结合。
2.实验探究,解决问题
学生分组讨论,然后进行实验探究,解决具体情境问题,再应用本节课的知识检验生活中常见食品和药物中的亚铁离子,将化学知识与生活实际结合,体现化学学科的应用性。
3.“价-类”结合,素养提升
在铁盐和亚铁盐任务讨论探究中,构建铁元素的“价-类”二维图。“价-类”二维图和氧化还原原理结合,为实验探究提供原理支持,建立元素化合物的证据推理核心素养。
三、教学目标
1.通过实验探究铁盐和亚铁盐的化学性质,体会实验对认识和研究物质性质的重要作用,形成证据意识,培养科学素养。
2.掌握铁盐和亚铁盐的转化关系、检验方法,将元素化合物的性质系统化、网络化。
3.逐步形成“价-类”思维,学会用“价-类”的视角认识有变价元素物质间的转化关系,建立模型认知和证据推理的素养,丰富研究物质的思路和方法。
4.学会用化学方法检验生活中含亚铁离子的食品和药物,学以致用,培养运用知识解决问题的能力以及科学态度和社会责任的核心素养。
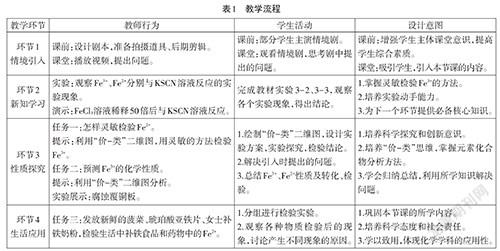
四、教学流程
根据教学目标,本节课的学习过程分为四个环节:情境引入→新知学习→性质探究→生活应用。具体教学流程见表1。
五、教学实录
1.创设情境
【情境】播放自制情境视频。A穿着白大褂扮演医生,B扮演病人。见图1。
B(难受):医生,我最近烦躁、易怒、注意力不集中,头发干枯脱落,请问我得了什么病?
A(自信):你这是缺铁性贫血。
B(开心):我是不是应该多吃点菠菜?
A(摇头):我建议你多吃点猪肝。如果很不舒服,我给你开点琥珀酸亚铁片、维生素C,服用一周后看效果。
B(感谢):谢谢医生!
【学生】进入情境,思考问题。
2.灵敏检验铁离子的方法
【教师】要想解决B同学的问题,我们先要了解一些重要的知识。请同学们完成教材中的实验3-2、实验3-3,观察两个实验现象,讨论实验结果。
【学生实验】氯化铁、氯化亚铁溶液分别与KSCN溶液反应,观察实验现象、讨论实验结果。
【结论】氯化铁和硫氰化钾溶液混合后溶液变成血红色,见图2、图3。氯化亚铁和硫氰化钾溶液混合后无现象。Fe+3SCN=Fe(SCN)(血红色)
【教师】利用溶液变成血红色这个特别的现象,可以用KSCN溶液检验铁离子。KSCN溶液可以非常灵敏地检验铁离子。
【演示实验】取一支洁净的试管,滴入两滴氯化铁溶液,然后用蒸馏水稀释50倍,摇匀。再滴入1mL KSCN溶液,溶液由无色变成淡血红色。
【教师】试管中铁离子的浓度非常小,滴入KSCN溶液后,溶液由无色变成淡血红色。能非常灵敏地检验出铁离子。
3.Fe和Fe的化学性质
【过渡提问】补铁需要的是亚铁离子,可以用什么方法灵敏地检验出亚铁离子呢?有了正确的方法,就可以检验补铁片中是否有亚铁离子。
【任务一】怎样灵敏检验Fe?
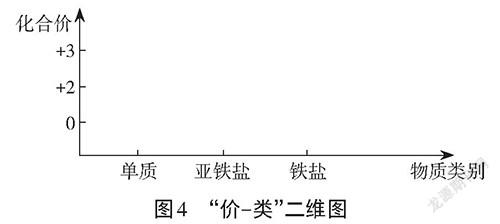
【方法指导】(1)将铁及其化合物标在“价-类”二维图上,见图4,预测Fe的性质。(2)利用灵敏检验Fe的方法。
【讨论交流、实验探究】根据图中的信息讨论灵敏检验Fe的方法。根据各组的设计、提供实验仪器和药品完成实验探究。
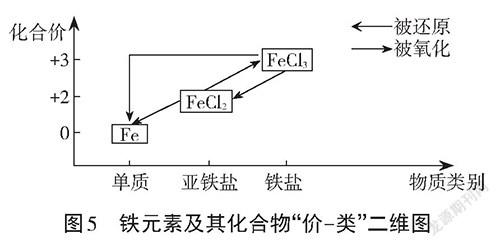
【成果分享】分享实验成果和结论,见图5。
根据二维图的信息,可以将Fe氧化成Fe,再通过检验Fe的存在检验Fe。具体实验步骤有两种。
方法一:取氯化亚铁溶液,加入KSCN溶液,再加入氯水,溶液变血红色。
方法二:取氯化亚铁溶液,加入氯水,再加入KSCN溶液,溶液变血红色。
【教师提问】实验现象一样,但是加试剂顺序不一样。请问哪一个小组是正确的?
【学生分析】方法一是正确的。先加氧化剂,再加KSCN溶液,可能原溶液是Fe,故不能确定原溶液中一定有Fe。
【教师追问】同学们成功完成任务一,解决了B同学的第一个问题。B同学还问到“我还缺维生素C吗?”同学们知道维生素C的用途是什么吗?
【学生分析】Fe有还原性,容易被氧化。维生素C还原性更强,可以做抗氧化剂,防止Fe被氧化。
【教师追问】刚才同学们做实验的时候,有同学问我FeCl溶液底部是什么物质?大家根据Fe的性质可以推测出这是什么物质吗?有什么用途吗?
【学生分析】Fe容易被氧化,溶液中放入Fe粉,可防止Fe被氧化。
【学生总结】Fe的化学性质:(1)强还原性(2)弱氧化性。Fe的用途:人体补铁剂、生产生活中还原剂。
【过渡提问】同学们根据“价-类”二维图预测了Fe的化学性质,并用实验进行了证明。同学们能否再根据“价-类”二维图预测一下Fe的化学性质,并用实验证明你的预测是否正确。
【任务二】探究铁离子的化学性质。
【实验探究】根据“价-类”二维图,预测Fe性质;根据提供的实验仪器和药品设计实验步骤,完成实验探究。
【成果分享】根据“价-类”二维图,Fe有氧化性,可以被还原成Fe或Fe。
方法一:取氯化铁溶液加入KSCN溶液,溶液变血红色,再加入铁粉,振荡,血红色褪去,溶液变浅绿色。
方法二:取氯化铁溶液加入KSCN溶液,溶液变血红色,再加维生素C粉末,振荡,红色褪去,溶液变浅绿色。
【分析总结】Fe的化学性质:强氧化性。
【教师追问】Fe有强氧化性,那么Fe的有哪些用途呢?
【学生回答】可以制作印刷电路板。
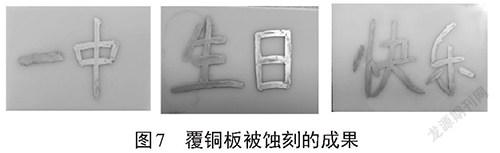
【实验展示】由于课堂时间不够,化学兴趣小组的同学在课余时完成了覆铜板制作“一中”的蚀刻实验。实验现象见图6。
他们用同样的方法又做了两块蚀刻覆铜板,见图7。有兴趣的同学可以课后一起完成这个实验。
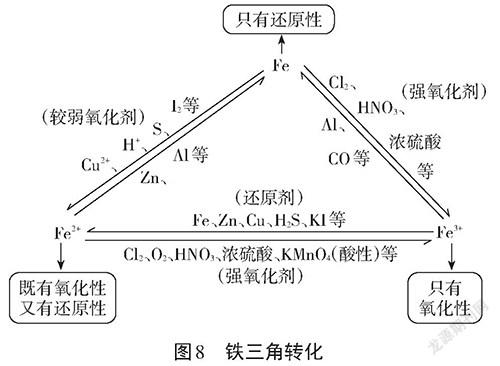
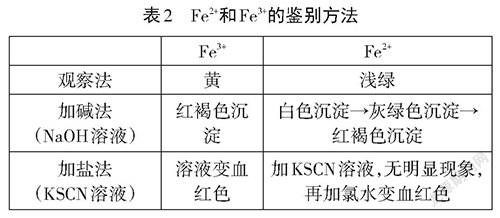
【总结提问】1、Fe、Fe、Fe三者之间可以怎样转化?
2、哪些方法可以鉴别Fe和Fe?
【交流总结】见图8、表2。
4.生活中常见补铁物质的检验
【任務三】生活中有很多补铁(Fe)的食品和药物,如菠菜、女士补铁奶粉、琥珀酸亚铁片等等。我们利用本节课学到的方法,检验这些补铁食品和药物中是否真的含有Fe。
【教师】发放新鲜的菠菜、琥珀酸亚铁片、女士补铁奶粉。提醒学生菠菜、补铁片分别放在研钵中研磨,奶粉放入烧杯中加水溶解后进行检验实验。
【实验检验】分组对各物质进行现场检验,对比实验现象。见图9、图10。
【交流总结】这些食品和药物都有Fe。根据溶液变色的情况,菠菜中的含铁量最少,琥珀酸亚铁片中的含铁量最多。A医生说缺铁性贫血吃菠菜的效果不如吃补铁片剂是有科学道理的。很多食品和药物都有专门的质量检测机构对标注的成分进行检验,检验不合格的食品和药物不能销售。
【教师总结】本节课我们学会利用“价-类”二维图预测Fe和Fe的化学性质,并用实验证明。学会了检验Fe和Fe的方法,并检验了生活中常见补铁食品和药物中是否有Fe。希望在以后其它元素化合物的学习中,同学们也能利用“价-类”二维图的思维模式进行分析,用求真精神进行科学探究,用社会责任感解决生活中的问题。
【课后作业】进一步扩充铁及其化合物的“价-类”二维图,见图11。将铁的氧化物、氢氧化物等类别的物质补充完整。结合化合价复习这些物质的化学性质,总结不同类物质相同价态的共同点、不同价态相同种类物质的共同点。
六、教学反思
1.情境丰富,贯穿课堂
情境是体现知识的发现过程、应用条件和意义价值的场景[3]。新课标在铁及其化合物教学内容的“情境素材建议”特别提到:补铁剂;实验室中硫酸亚铁的保存与使用;印刷电路板的制作;菠菜中铁元素的检测等等情境[2]。本节课从补铁剂是否含有Fe 的情境开始,穿插Fe保存、Fe印刷电路板等情境,通过实验检验菠菜、补铁片、加铁奶粉中含有Fe结束。在丰富的情境中,学生学会利用化学知识解决问题,体会到化学在生产生活中的广泛应用,增强社会责任感。
2.实验探究,科学精神
本节课学生实验环节丰富,完成了新教材中“实验”“探究”“研究与实践”。在教材的基础上进一步挖掘,设计了KSCN溶液灵敏检验氯化铁溶液,检验补铁片和加铁奶粉中是否有Fe等,体现了课堂的广度。实验活动对学生实验行为要求较高,除了观察实验现象,还要求对现象进行归纳总结,回答实验有关问题,部分实验达到了要求学生设计实验步骤的高阶行为[4],体现了课堂的深度。学生通过实验探究,进一步掌握Fe和Fe的化学性质,相互转化、离子检验等核心知识,培养了学生的科学探究和创新意识。
3.“价-类”思维,知识素养化
新课标铁及其化合物教学内容的“学业要求”特别提到:能依据物质类别和元素价态的角度列举某种元素的典型代表物、预测物质的性质和变化并设计实验进行初步验证、说明物质转化路径等等[2]。“价-类”二维图将物质类别和元素价态综合在二维坐标图中,有利于对物质的性质进行系统科学分析。本节课Fe和Fe的性质预测都是通过“价-类”二维图得出的,图中的物质类别和元素价态还可以拓展。学生“价-类”思维初步建立,为元素化合物的系统构建奠定了基础,实现了知识素养化。
参考文献
[1]人民教育出版社,课程教材研究所,化学课程教材研究开发中心.普通高中教科书(化学必修第一册)[M].北京:人民教育出版社,2019:69.
[2] 教育部.普通高中化学课程标准(2017年版2020年修订)[S].北京:人民教育出版社,2020.
[3]张景雪,袁金芳.化學核心素养下的情景教学设计及反思[J].中学化学教学参考,2019(7):35-36.
[4]黄海清.人教版高中化学必修模块教学生实验活动的分析与比较[J].化学教育(中英文),2021,42(13):8-14.
3639500589296
