DDP-4抑制剂与GLP-1受体激动剂治疗2型糖尿病患者的有效性研究
2022-03-16崔艳敏宋岳涵
崔艳敏 宋岳涵
2型糖尿病是临床最为常见的慢性内分泌疾病,我国>20岁的糖尿病患病率为9.7%,其中绝大多数为2型糖尿病[1]。本病的发生发展与胰岛功能的衰退密切相关,出现胰岛素分泌减少和机体胰岛素抵抗,长期发展可引发诸多严重并发症,致残及致死率较高。2012年的ADA/EASD的血糖管理共识推荐,对于经二甲双胍单药治疗3个月后糖化血红蛋白(HbA1c)仍未达标者,可联合磺酰脲类、噻唑烷二酮类、胰高血糖素样肽-1(GLP-1)受体激动剂、二肽基肽酶-4(DDP-4)抑制剂、胰岛素等5种药物进行治疗[2]。GLP-1是一种肠促激素,受进食及神经内分泌等多种因素调节,由远端小肠和结肠内 L 细胞分泌,人体天然的GLP-1半衰期仅为1.5~2 min,可被DPP-4 酶快速裂解而失去活性,导致内源性GLP-1无法达到治疗浓度[4]。GLP-1和DDP-4抑制剂均属于肠促胰素类药物,均基于体内GLP-1生理活性来发挥降糖作用。GLP-1受体激动剂通过外源性补充GLP-1,DDP-4抑制剂通过抑制DDP-4酶的活性,减少GLP-1降解。而二甲双胍可抑制胰岛β细胞中DDP-4的活性、上调GLP-1的表达,因此,其作用机制与GLP-1受体激动剂、DDP-4抑制剂完美契合,联合应用可协同增效[4]。本研究进一步分析GLP-1受体激动剂与DDP-4抑制剂在治疗2型糖尿病患者中的有效性及空腹血糖(FBG)、餐后2 h血糖(2hPG)水平的影响,报道如下。
1 资料与方法
1.1 一般资料 将2019年1月至2020年6月在我院内分泌科治疗的126例2型糖尿病患者随机分为观察组和对照组,每组63例。观察组中,男33例,女30例;年龄34~76岁,平均年龄(47.4±11.2)岁;病程1~8年,平均(4.5±1.7)年;体重指数(BMI)25.2~30.7 kg/m2,平均(28.1±1.4)kg/m2。对照组中,男34例,女29例;年龄35~78岁,平均年龄(47.8±11.5)岁;病程1~9年,平均(4.7±1.8)年;BMI 25.3~30.9 kg/m2,平均(28.3±1.5)kg/m2。2组的年龄、性别比、病程、BMI等具有均衡性。见表1。

表1 2组患者基线资料比较 n=63
1.2 纳入与排除标准
1.2.1 纳入标准:①所有患者符合《中国2型糖尿病防治指南(2017年版)》[5]中关于2型糖尿病诊断标准;②血糖明显升高,伴有2型糖尿病典型症状,如口渴、乏力、多饮、多尿等;③任意2次FPG≥7.8 mmol/L,或FPG<7.8 mmol/L,但任意2次口服糖耐量试验的2hPG≥11.1 mmol/L,以及口服75 g葡萄糖1次间期血糖≥11.1 mmol/L;④入院前3个月未使用任何降糖药;⑤甲状腺超声检查正常;⑥本研究经我院伦理委员会批准,所有患者均知情同意,自愿加入研究。
1.2.2 排除指标:①合并严重急慢性糖尿病并发症者;②合并其他内分泌疾病者,如甲状腺功能低下、多囊性卵巢、性腺功能减退症等;③合并原发性心肺、肝肾严重疾病;④未能控制的高血压;⑤合并无症状低血糖症;⑥药物过敏;⑦精神疾病、意识障碍者。
1.3 方法 2组均服用二甲双胍片(中美上海施贵宝制药有限公司生产,国药准字H20023370),初始剂量0.5 g/次,2次/d,每周增加0.5 g,直至增加至2 g/d,分早晚2次服用;均于治疗期间维持原来降糖、调脂、降压方案,严格控制饮食、规范运动量及运动强度。
1.3.1 对照组:服用西格列汀片(Merck Sharp & Dohme Italia SPA,国药准字J20140095),早餐前服用100 mg,1次/d[6]。
1.3.2 观察组:使用利拉鲁肽注射液[诺和诺德(中国)制药有限公司生产,国药准字J20160037],于每日午餐前注射1次,起始剂量0.6 mg,7 d后增加剂量至1.2 mg/d,并维持治疗[7]。治疗期间采用强生稳豪血糖仪监测血糖变化,维持各点血糖≥4.4 mmol/L。2组均治疗16周后评价疗效。
1.4 观察指标 (1)治疗前、治疗16周后检测FBG、2hPG、HbA1c、体重、腰围、BMI:采用己糖激酶法测定FBG、2hPG,电化学发光法测定HbA1c,测定腰围、身高、体重,计算BMI;(2)治疗前、治疗16周后测定收缩压(SBP)、舒张压(DBP)、总胆固醇(TC)、三酰甘油(TG)、高密度脂蛋白胆固醇(HDL-C)、低密度脂蛋白胆固醇(LDL-C),采用全自动生化分析仪测定血脂各指标;(3)治疗期间观察有无不良反应发生,并检测肝肾功能各指标,统计低血糖、恶心呕吐、腹胀腹泻、头晕、上呼吸道感染、鼻咽炎等不良反应发生率,以血糖<2.77 mmol/L判断为低血糖[8]。

2 结果
2.1 2组治疗前后血糖及体重各指标比较 观察组治疗后FBG、HbA1c、体重、腰围、BMI明显低于对照组(P<0.05),但2组2hPG比较差异无统计学意义(P>0.05)。见表2。

表2 2组治疗前后血糖及体重各指标比较
2.2 2组治疗前后血压及血脂各指标比较 观察组治疗后SBP、TC、TG、LDL-C水平明显低于对照组,而HDL-C水平明显高于对照组(P<0.05),但2组治疗后DBP水平差异无统计学意义(P>0.05)。见表3。

表3 2组治疗前后血压及血脂各指标比较
2.3 2组不良反应发生率比较 2组低血糖发生率比较,差异无统计学意义(P>0.05),但观察组恶心呕吐、腹胀腹泻、头晕、上呼吸道感染、鼻咽炎等不良反应发生率明显高于对照组(P<0.05)。见表4。
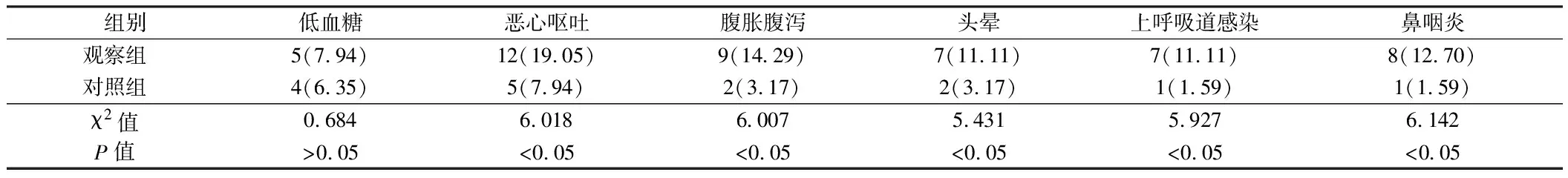
表4 2组不良反应发生率比较 n=63,例(%)
3 讨论
随着超重及肥胖2型糖尿病患者的比例越来越高,传统口服降糖药物和胰岛素治疗的效果一般,且无法有效控制BMI,导致血压、血脂等异常升高,进一步加重机体胰岛素抵抗,降低外周胰岛素敏感性,使得病情呈恶性循环[9]。因此,如何在理想控制血糖的同时减少低血糖及BMI增加风险,改善胰岛β细胞功能,抑制病情进展,是临床研究的重点。
GLP-1是由结肠和远端小肠的L细胞分泌的一种肠促胰素,而GLP-1受体在体内分布广泛,二者结合后可发挥促进胰岛素的合成和分泌作用,保护胰岛β细胞功能,抑制凋亡,促进其增殖和新生,还具有抑制胰高血糖素分泌、增加外周组织葡萄糖利用率、减少食物摄取、延缓胃排空、减少肝糖输出等生理作用[10]。因此,增加机体合成和分泌GLP-1成为临床2型糖尿病治疗的方向。但人体天然的GLP-1存在时间短,导致增加体内GLP-1的合成和释放无法达到治疗目的,而通过外源性补充GLP-1成为了临床治疗的新选择[11]。
利拉鲁肽是一种GLP-1受体激动剂,比天然GLP-1多一个特殊脂肪酸侧链,使得利拉鲁肽与血浆白蛋白之间的作用具有可逆性,从而不易被DPP-4裂解,从而增加了外源性GLP-1浓度,使体内GLP-1浓度能够达到药理学水平,并延长GLP-1活性,达到治疗2型糖尿病的目的[12]。其作用机制为:(1)调节血糖:GLP-1的作用呈葡萄糖依赖性,即机体血糖升高时GLP-1 刺激胰岛β细胞,增加胰岛素的分泌,促进血糖降低,当血糖<4.5 mmol/L时,GLP-1停止对胰岛β细胞进行刺激[13]。同时,GLP-1还可刺激胰岛α细胞,在血糖升高时胰高糖素的分泌,反之增加减少胰高糖素的分泌,达到调节血糖平衡的效果[14]。(2)降低BMI:GLP-1可在中枢神经系统内合成,直接作用于中枢神经,发挥脑神经肽作用,延缓胃排空,增加饱腹感,减轻BMI。同时GLP-1还是一种厌食信号肽,作用于大脑中调节食欲的信号,抑制食物摄取,增加能量消耗,减轻BMI[15]。(3)减少脂肪堆积:GLP-1可作用于稳定型自然杀伤T细胞,增加白色脂肪棕色化和产热,增加脂肪组织内FGF-21的表达及产热,从而减少内脏脂肪,改善内脏脂肪含量,缩减腰围,降低BMI[16]。
DPP-4是一种位于细胞表面的丝氨酸肽酶,可降解体内多种活性物质,如GLP-1、降血糖素、神经肽Y等。因此,抑制DPP-4活性,减少GLP-1降解,提高血浆中GLP-1的含量和活性,有利于维持GLP-1的功能,提升降糖效果,减少肝糖原分解,延缓胃排空[17]。DPP-4抑制剂即通过这一药理作用达到降糖效果,其通过抑制GLP-1的降解,提高空腹和餐后GLP-1水平,延长其活性,对葡萄糖的调控达葡萄糖依赖性,可调节性刺激胰岛素分泌,降低血糖[18]。西格列汀是代表性的DPP-4抑制剂,是一种口服吸收的小分子药物,不仅抑制DPP-4活性,升高GLP-1的含量和活性,增加胰岛素的释放量,还可降低胰高血糖素的分泌,抑制内源性血糖的生成,但对胃动力影响较小,因此治疗后体重改变较小[19]。其次,可降低HbA1c。小鼠试验表明,西格列汀治疗4周HbA1c下降0.6%,治疗8周HbA1c下降1.1%[20]。再者,可调节血脂。西格列汀可减轻机体胰岛素抵抗,增加胰岛素敏感性,从而改善机体糖脂代谢紊乱,减少TC、TG在胰腺的沉积。
本研究结果显示,观察组治疗后FBG、HbA1c、体重、腰围、BMI明显低于对照组(P<0.05),但2组2 hPG比较差异无统计学意义(P>0.05)。说明GLP-1受体激动剂在降糖及将BMI效果上优于DPP-4抑制剂。因GLP-1受体激动剂可减少食物的摄入,增加饱腹感,使得将BMI效果更为明显。观察组治疗后SBP、TC、TG、LDL-C水平明显低于对照组,而HDL-C水平明显高于对照组(P<0.05),但2组治疗后DBP水平差异无统计学意义(P>0.05);2组低血糖发生率比较,差异无统计学意义(P>0.05),但观察组恶心呕吐、腹胀腹泻、头晕、上呼吸道感染、鼻咽炎等不良反应发生率明显高于对照组(P<0.05)。说明GLP-1受体激动剂对心血管的保护作用更好,可以扩张外周血管,降低血管阻力,还可抑制远端肾小管对尿钠的重吸收,促进尿钠的排泄,发挥降压作用。同时,GLP-1受体激动剂增加了内源性脂肪的消耗,有助于降低内脏和外周脂肪含量,达到降低血脂的效果。但在胃肠道不适及感染等不良反应发生率上相对较高,一般程度较轻,临床应做好相关的防治工作。
综上所述,GLP-1受体激动剂在治疗2型糖尿病患者中的有效性更佳,对FBG、2hPG、HbA1c、BMI等均有良好抑制效果,特别适合超重或肥胖2型糖尿病患者的治疗,但DPP-4抑制剂的耐受性更好,不良反应发生率更低,临床应结合患者的具体病情选择适宜的治疗药物。
