帕博利珠单抗致剥脱性皮炎1例的临床诊治并同期应用帕博利珠单抗44例皮肤毒性分析
2022-03-11黄佳圆潘半舟梅静峰范朝晖
黄佳圆,潘半舟,纪 红,梅静峰,范朝晖,周 云
(江苏省肿瘤医院 江苏省肿瘤防治研究所 南京医科大学附属肿瘤医院 a.肿瘤内科;b.放疗科;c.胸外科,南京 210009)
近年来,肿瘤免疫治疗已逐渐成为恶性肿瘤治疗领域的重要手段,免疫检查点抑制剂(immune checkpoint inhibitors, ICIs)通过抑制免疫检查点活性,激活T细胞免疫应答,参与肿瘤免疫逃逸机制的调控,达到抗肿瘤的目的[1]。目前ICIs联合细胞毒药物化疗已被证实有效[2],而ICIs在改善提高肿瘤治疗效果同时也导致一些特殊的不同于化疗的不良反应,称为免疫相关毒副作用(immune-related adverse events,irAEs),可见于全身各系统[3-4],皮肤反应是最常见的irAEs,包括瘙痒、皮疹、皮炎、红斑、荨麻疹、光敏反应等,严重的皮肤不良反应也可能直接威胁患者生命[5]。研究结果表明,使用帕博利珠单抗和纳武利尤单抗的患者中皮肤不良事件发生率约为34%~40%,3~4级皮疹较少见[6],皮肤irAEs可能提示积极的预后因素。近日我院1例食管癌患者在接受两周期帕博利珠单抗联合紫杉醇、洛铂治疗后发生剥脱性皮炎并成功治愈,现将临床诊治并同期应用帕博利珠单抗44例皮肤毒性进行分析,并对免疫相关性不良反应皮肤毒性的文献进行复习。
1 临床资料
1.1病史资料 患者女性,75岁,身高165 cm,体重45 kg,体表面积1.49 m2。2020年4月无诱因出现进食哽噎感,进干食时明显,后梗阻逐渐加重,当地医院行胃镜活检病理:食管鳞癌。2020年7月在我院行胃造瘘术,术后行肠内营养治疗,营养状况改善。2020-09-22及2020-10-24于我院胸外科行帕博利珠单抗100 mg静脉滴注+紫杉醇180 mg静脉滴注+洛铂30 mg静脉滴注治疗2周期。2020-10-30因“全身皮疹”复诊,2020-11-02皮损进一步加重再次入院,表现为面部、前胸部及四肢多处皮肤脱落,可见肌肉组织,渗血压痛。院内会诊考虑剥脱性皮炎,转入我科治疗。既往无糖尿病、高血压、冠心病史,无结核、肝炎病史,无药物过敏史,无吸烟、饮酒史。
体格检查:体温37 ℃,脉搏98次/min,呼吸19次/min,血压123/80 mmHg(1 mmHg=0.133 kPa),疼痛评分4分,意识清,精神欠佳,头面部皮肤破溃、大面积渗血、渗液,睁眼、张口受限,背部皮肤大面积剥脱伴渗液,双足及会阴部布满水泡,躯干部广泛水肿性红斑伴有大量脱屑。双肺呼吸音清,未闻及干湿性啰音。心率98次/min,律齐,各瓣膜听诊区未闻及杂音。腹部平坦,未见包块,无压痛及反跳痛,肝脾肋下未及。四肢肌力肌张力正常,双下肢无水肿。生理反射存在,病理反射未引出。
实验室检查:血常规:白细胞9.41×109/L,中性粒细胞计数8.90×109/L,血红蛋白92 g/L,血小板183×109/L;生化:肌酐40 μmol/L,血糖9.67 mmol/L,总蛋白56.1 g/L,白蛋白25.5 g/L,白球比0.8, 谷丙转氨酶、谷草转氨酶正常;降钙素原0.322 ng/mL。
诊断:食管鳞癌化疗免疫治疗后,剥脱性皮炎 ECOG评分:4分。
1.2治疗经过 患者转入我科后,予鼻饲流质饮食,同时予护胃、输注白蛋白、静脉营养支持,维持水电平衡。结合病史、体征及检查结果,考虑帕博利珠单抗治疗所致剥脱性皮炎,同时合并皮肤感染,予甲泼尼龙120 mg静脉滴注 d1-4,100 mg静脉滴注d5-7,80 mg静脉滴注d8-10,40 mg静脉滴注d11-13, 20 mg静脉滴注d14-17;予头孢曲松钠他唑巴坦钠2 g静脉滴注、每天2次 d1-14抗感染。2020-11-06患者胃造瘘管滑脱,不能再次植入,改全静脉营养支持。2020-11-09及2020-11-10先后输注病毒灭活血浆425 ml、475 ml。2020-11-12患者小便难解,考虑长期大量应用皮质类固醇及三代头孢抗炎,易并发霉菌感染,加用氟康唑抗霉菌治疗,用药前行中段尿培养。2020-11-17患者全身皮肤全面好转,头面部结痂基本脱落,双足及会阴部水泡吸收好转,其余部位红斑好转,水肿消退,行鼻饲营养管植入,改肠内营养。
局部治疗贯穿整个治疗过程,糜烂渗出明显部位予3%硼酸湿敷;干燥部位瘙痒明显时予氧化锌油、复方曲安奈德乳膏外用。治疗期间每日更换被褥、定期空间消毒。
目前患者全身皮肤基本好转(图1),鼻饲流质,生活自理,每日散步2小时。
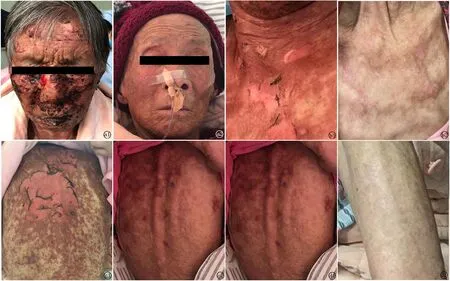
图1 帕博利珠单抗致剥脱性皮炎患者治疗前后 a1.头面部治疗前;a2.头面部治疗后;b1.颈部治疗前;b2.颈部治疗后;c1.背部治疗前;c2.背部治疗后;d1.肢体治疗前;d2.肢体治疗后
1.3同期应用帕博利珠单抗患者皮肤毒性分析 收集我院2020-09-01至2020-11-30期间应用帕博利珠单抗治疗的患者共计44例(包括上述患者),包括食管癌9例,肺癌28例,子宫内膜癌1例,直肠癌1例,卵巢癌1例,纵膈恶性肿瘤1例,宫颈癌2例,胰腺癌1例。其中联合化疗32例,联合放疗8例,联合放化疗同步2例,单用帕博利珠单抗2例。这些患者中男性27例,女性17例,年龄大于60岁(包括60周岁)的29例,低于60周岁的15例。我们对这部分患者的皮肤毒性情况进行了随访观察,大多数患者接受帕博利珠单抗治疗后未出现明显皮肤毒性反应,见表1。

表1 帕博利珠单抗治疗患者的免疫相关性皮肤反应的发生情况及转归
2 讨 论
根据第5版常见不良事件评价标准(CTCAE)对临床判断皮肤不良事件的分级标准,我院44例应用帕博利珠单抗治疗患者中仅少数表现为皮肤瘙痒、皮疹,多为G1、G2级,给予局部应用润肤剂、中等强度的糖皮质激素软膏、口服抗过敏药物或泼尼松0.5~1 mg/(kg·d)治疗效果良好,不影响帕博利珠单抗的继续使用。本次收集患者中仅1例出现严重剥脱性皮炎,积极治疗后好转,停用免疫治疗。在欧洲肿瘤内科学会(ESMO)指南免疫治疗毒性管理中提到,当使用ICIs的患者可能出现相关皮肤不良事件时,首先需要除外如感染、其他药物反应或其他疾病皮肤表现的原因,应对皮肤黏膜全面仔细检查,评估是否合并发热、淋巴结肿大等伴随症状,必要时检测血常规、肝肾功能、炎性指标等。当出现皮肤病急重症时,如伴嗜酸性粒细胞增多和系统症状的药疹(DRESS)、急性发热性中性粒细胞增多性皮肤病(Sweet综合征)、Stevens-Johnson综合征或中毒性表皮坏死松解症等致命情况时,应永久停用ICIs,同时立刻住院对症治疗。必要时应当请皮肤科医师会诊,协助进行详细的皮肤病学评估及专科局部治疗。本例剥脱性皮炎患者的诊治完全符合指南,且治疗转归理想。
人源化高亲和力单克隆PD-1抗体帕博利珠单抗2014年被批准应用于临床,在恶性黑色素瘤、肺癌、膀胱癌等恶性肿瘤均证实疗效确切[7],食管癌是紧随其后免疫原性最强的肿瘤类型。KEYNOTE-181研究结果提示,PD-L1(CPS≥10)食管鳞癌患者中位生存期可以达到10.3个月,客观缓解率也有所提高。其中中国人群中PD-L1(CPS≥10)食管鳞癌患者中位OS可以达到12个月,较传统治疗组延长6.6个月,提示中国人群存在获益优势[8]。因此2020年6月帕博利珠单抗获批单药用于通过充分验证的检测评估肿瘤表达PD-L1(CPS≥10)的、既往一线全身治疗失败的、局部晚期或转移性食管鳞状细胞癌(ESCC)患者的治疗,成为首个用于食管癌的免疫治疗药。
帕博利珠单抗在KEYNOTE 006、KEYNOTE 010等多个临床试验中均提示安全性良好[9-11],但免疫治疗过程中可能过度激活T细胞活化,诱发免疫相关不良反应[12],且机制未明,有研究认为,细胞毒性损伤诱发机体释放炎症因子,激发全身炎症反应系统[13],免疫相关性皮肤毒性主要与T细胞介导异常活化有关[14]。皮肤毒性是最常见的irAEs,通常出现在首次用药起效后3~6周左右的治疗早期,为剂量限制性。虽然发生率高,但大多轻微可逆,在支持治疗下通常可控。研究发现,通过评估82例接受过抗PD-1治疗的转移性黑色素瘤患者发现,49%的患者出现了新发皮肤不良反应,包括苔藓样反应、湿疹和白癜风,其中苔藓样口腔黏膜病变涉及舌头、口腔黏膜、嘴唇和(或)牙龈的糜烂,在统计学上表现出明显的合并而非单独出现的趋势[15]。某46岁男性患者在帕博利珠单抗治疗后双手手掌上出现局限、播散性的红色丘疹,表面具有光泽,手背皮肤活检病理提示过度角化的楔形棘皮病,表皮下有致密性苔藓样小淋巴细胞浸润[16]。现有文献报道的皮肤不良事件的发生时间为4~10个月不等,往往自限性,仅局部使用类固醇就容易控制[17],双联合免疫治疗可能会加重皮肤毒性的发生率及发生频率[18]。
皮肤不良事件的严重程度根据常见毒性反应标准进行分级[19],所有级别的皮肤不良事件在大约1/3以上免疫治疗患者中均有所发现,更严重的不良反应发生在约2.4%的患者中。本例患者第1周期使用帕博利珠单抗后出现Ⅰ~Ⅱ级皮肤毒性,予对症抗过敏治疗后症状缓解。第2周期治疗后1周再次出现皮肤反应,症状和程度均较前加重,对症治疗未见缓解,皮损进展迅速,数日内即发展为全身皮肤破溃、渗血、渗液,水泡和大量脱屑。根据免疫相关性皮肤不良事件的分级,患者出现剥脱性皮炎,评估属于Ⅳ级严重不良反应,应当永久停药,同时立即予大剂量激素冲击治疗,辅以消炎、维持水电平衡、营养支持及积极护理干预,后患者逐渐好转后平稳缓慢减量激素。在出现严重免疫相关不良反应时,大剂量类固醇激素使用及联合丙种免疫球蛋白为主要治疗药物。值得临床医师注意的是,激素减量过程中需要警惕病情出现反复。
免疫治疗的临床广泛应用使疾病控制和总体生存优势提升。临床医生在应用免疫治疗前应详细交代可能发生的包括皮肤毒性在内的多种irAEs,提醒可能出现导致治疗中断,甚至危及生命的严重irAEs。重视皮肤毒性的发生,在治疗过程中尽早发现、及时诊断、限制剂量和毒性,加强支持对症治疗及多学科协作,采取合适的护理干预措施,对患者的疗效及生存质量具有重要影响。
