白蛋白结合型紫杉醇致妇科恶性肿瘤患者周围神经病变的临床和相关因素分析*
2022-03-11徐圣秋
曲 珍,徐圣秋
徐州市第一人民医院 药学部,徐州 221100
白蛋白结合型紫杉醇是使用纳米技术,将人血清白蛋白作为载体,与疏水性紫杉醇相结合,与溶剂型紫杉醇相比更易在体内分解,且具有相对靶向性。本品2005 年在美国上市,2009 年进入中国,可用于多种恶性肿瘤的治疗,如妇科各种癌症、肺癌、胰腺癌等[1],尤其是治疗妇科恶性肿瘤(包括卵巢癌、宫颈癌和子宫内膜癌)的基本药物。较之于传统的溶剂型紫杉醇,白蛋白结合型紫杉醇剂量使用范围更大(80~375 mg·m-2),过敏反应更少,用药前无需抗过敏预处理,使用方便。化疗所致的周围神经病变(chemotherapy-induced peripheral neuropathy,CIPN)是紫杉醇类药物的较常见不良反应,对患者的生活质量造成严重影响。肢端呈手套-袜套状麻木是紫杉醇所致周围神经病变的特征表现,往往局部有灼热感、刺痛或肌肉痛,严重者造成深腱反射消失,发生率约60%,一般在用药后24~72 h 出现,重度CIPN 发生率达10%[2]。本研究分析使用白蛋白结合型紫杉醇化疗妇科癌症患者的CIPN 发生情况及不同年龄、癌症类型、合并基础疾病与联用神经毒性药物等临床因素与周围神经病变发生率的相关性,旨在为白蛋白结合型紫杉醇的安全用药提供理论依据。
1 资料与方法
1.1 研究对象
此研究在本院伦理委员会监督下进行,纳入2018 年10 月~2020 年10 月本院应用白蛋白结合型紫杉醇方案治疗的妇科癌症患者共180 例,其中,年龄34~84 岁,平均年龄(60.12±9.08)岁。卵巢癌121 例,宫颈癌43 例,子宫内膜癌16 例。
1.2 纳入标准
①经病理或细胞学检查确诊,转移癌经X 线、CT、MRI 骨扫描等检查确诊;②资料齐全;③预计生存期超过半年;④PS 评分低于2 分;⑤接受含白蛋白结合型紫杉醇化疗方案。⑥化疗前患者的血常规、肝肾功能及心电图检查基本正常。
1.3 排除标准
①联用伽马刀、放疗患者;②化疗疗程不足2周期或者化疗周期间隔2 个月以上的患者;③药物过敏史患者;④有其他周围神经病变病史。
1.4 化疗方案及化疗周期[3]
所有患者使用白蛋白结合型紫杉醇260 mg·m-2(年长体弱者予175 mg·m-2),第1 天给药(21 d 为1个化疗周期),用药前不予抗过敏预处理,每次静脉滴注30 min,化疗期间观察并记录患者的不良反应。
1.5 观察指标
通过本院电子病历系统收集患者年龄、肿瘤类型、伴随基础疾病、给药方案等信息,以及化疗后患者周围神经病变发生情况及程度,对使用白蛋白结合型紫杉醇方案化疗后周围神经病变的发生率和相关危险因素进行研究及作关联性分析。
CIPN 评定标准:评估标准按照国际惯例,采用美国国家癌症研究所常见不良反应术语评定标准[4](National Cancer Institute -Common Terminology Criteria for Adverse Events,NCI-CTCAE)进行评价:①0 级:表现正常;②1 级:腱反射消失或感觉异常(包括刺痛觉);③2 级:感觉改变或异常(包括刺痛觉),影响肢体功能、但不影响日常生活;④3 级:感觉改变或异常(包括刺痛觉),影响日常生活;⑤4级:生命危险,需紧急治疗。⑥5 级:死亡。
1.6 统计学处理
2 结果
2.1 临床生理、病理因素
患者治疗方案如下:①白蛋白结合型紫杉醇单药治疗42 例(占23%);②白蛋白结合型紫杉醇双药治疗方案127 例(占71%),其中联合顺铂9 例(占5%),卡铂80 例(占44%),奈达铂19 例(占11%),洛铂2 例,奥沙利铂6 例,吉西他滨11 例(占6%);③白蛋白结合型紫杉醇联合抗血管生成靶向药物11 例(占6%),其中贝伐珠单抗和卡铂6 例,联合阿帕替尼5 例,上述靶向药物均按药品说明书指示用药。白蛋白结合型紫杉醇平均单次输注剂量240 mg·m-2,平均累积剂量(736.84±405.5)mg·m-2,平均治疗3 个疗程。化疗2~4 周期收集患者不良反应信息。180 例患者使用含白蛋白结合型紫杉醇治疗方案整体耐受性良好且不良反应可控制,CIPN 发生率为42.78%(77/180),使用过程中也无过敏反应及超敏反应的发生。不同临床生理、病理因素间的周围神经病变发生率比较,见表1。

表1 不同生理病理因素下的白蛋白结合型紫杉醇致CIPN 的情况
2.2 多因素Logistic 回归分析周围神经病变的危险因素
以是否周围神经病变为因变量;将单因素分析中筛选出的影响CIPN 相关因素纳入多因素Logistic 分析,分别以年龄、肿瘤类型(卵巢癌)、合并糖尿病、联用神经毒性药物、单次剂量、累积剂量为自变量,建立二元Logistic 回归模型。结果显示,年龄、合并糖尿病、联用神经毒性药物、单次剂量较大(260 mg·m-2)、累积剂量601~900 mg·m-2、累积剂量901~1200 mg·m-2在模型中均有统计学意义(P<0.05),见表2。
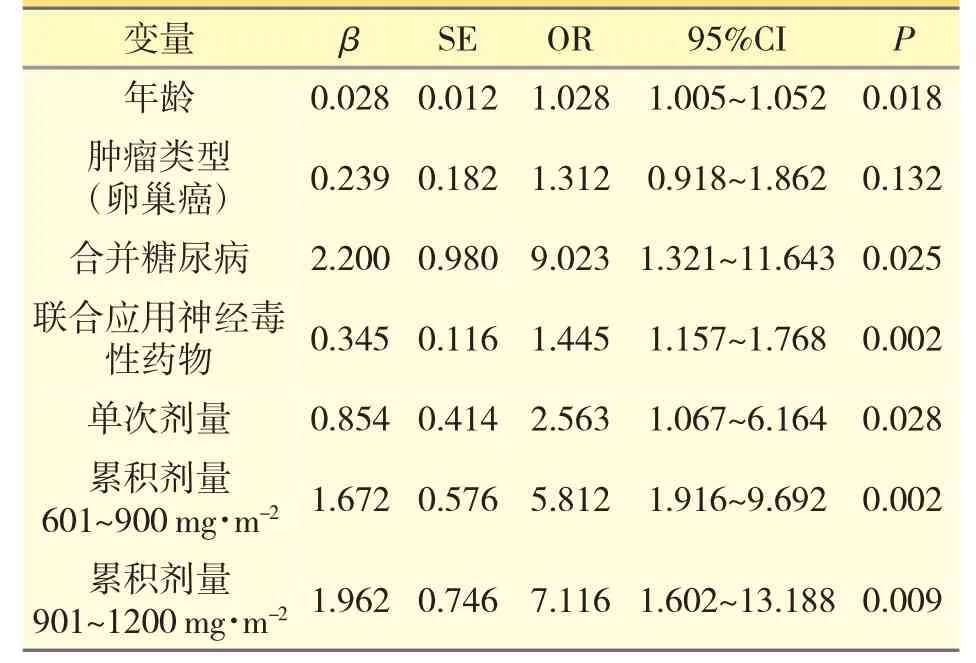
表2 白蛋白结合型紫杉醇致周围神经病变影响因素的多因素Logistic 回归分析
2.3 严重(3 级及以上)周围神经病变的影响因素
在180 例患者中,发生1 级CIPN 38 例(占21.11%),包括手指/手麻木、手指/手或脚趾/脚不舒适感、脚趾/脚麻木、对冷温度敏感;2 级CIPN 24 例(占13.33%)包括肢体麻木、疼痛灼热;3 级CIPN 15 例(占8.33%),包括触觉减退或消失、双下肢肌力减退、很难保持身体平衡;4 级和5 级CIPN 均为0 例。
在180 例患者中,发生3 级及以上CIPN15 例(发生率8.33%),相关影响因素见表1。与多因素Logistic 回归分析得出的危险因素一致。
年龄>65 岁患者的3 级及以上CIPN 发生率明显高于年龄≤65 岁的患者(P<0.05);糖尿病患者的3 级及以上CIPN 发生率明显高于非糖尿病患者(P<0.05);联用神经毒性药物患者的3 级及以上CIPN 发生率明显高于非联用周围神经毒性药物患者(P<0.05)。CIPN 严重程度呈剂量依赖性与累积性的特点,即白蛋白结合型紫杉醇高剂量组(单次剂量260 mg·m-2)3 级及以上CIPN 发生率高于低剂量组(单次剂量175 mg·m-2),且累积剂量越高,越容易发生3 级及以上的CIPN。
2.4 周围神经病变的药物因素
由表1 可见,CIPN 呈剂量依赖性与累积性的特点,即白蛋白结合型紫杉醇高、低剂量组间CIPN 发生率以及白蛋白结合型紫杉醇不同累积剂量组间,CIPN 发生率差异有统计学显著意义。
关于联合用药相关性,在180 例患者中,白蛋白结合型紫杉醇单药治疗42 例,发生CIPN17 例(发生率40.48%);联合用药时CIPN 的发生情况见表3。

表3 白蛋白结合型紫杉醇联合用药时周围神经病变的发生情况[n(%)]
当白蛋白结合型紫杉醇联合不同药物时,CIPN的差异无统计学意义(P>0.05)。
3 讨论
CIPN 是白蛋白结合型紫杉醇的常见不良反应,其发生与多种因素有关,目前化疗的单次剂量及累积剂量被公认是主要的危险因素,其他危险因素为患者年龄、癌症类型、合并糖尿病、周围神经病变史等。CIPN 的发病机制目前尚不清楚,可能与微管结构异常、神经元线粒体受损[5]、人群代谢酶的基因多态性[6]等有关。也有研究[7]表明,CIPN 风险增加可能与血药浓度、年龄、肥胖、合并症、吸烟史、饮酒史以及有神经系统疾病病史相关。
本研究表明,老年(年龄>65 岁)、合并糖尿病、联用神经毒性药物以及单次剂量和/或累积剂量高的妇科癌症患者应用白蛋白结合型紫杉醇更易发生CIPN。尤其以高血糖(OR 9.023)和高累积剂量(OR 分别为5.812 和7.116)风险程度最高。有报道[8]表明,白蛋白结合型紫杉醇的单次剂量>175 mg·m-2即发生CIPN,累积剂量达400 mg·m-2可发生严重的CIPN,表现为肢体麻木、触觉减退或消失、疼痛灼热、双下肢肌力减退等,停药一段时间可缓解。在本研究中,患者白蛋白结合型紫杉醇平均单次输注剂量为240 mg·m-2,平均累积剂量为(736.84±405.5)mg·m-2,临床以下肢受累为主,知觉减退,与文献报道一致。
综上,白蛋白结合型紫杉醇致CIPN 发生率高,剂量有蓄积性,用药前应注意关注上述危险因素,结合患者的具体病情及用药情况进行药学监护和患者宣教,维护患者用药安全。