HPLC- MS/MS法同时测定牛肉中80种兽药及其代谢物
2022-03-10李永琴卜宁霞
李永琴, 卜宁霞, 陈 娟, 马 岩, 杨 奇
(宁夏兽药饲料监察所, 宁夏 银川 750011)
优质农产品的供给成为农业高质量发展的迫切需求,但伴随而来的质量安全问题也成为阻挠畜产品高质量发展的绊脚石,其中最突出的就是兽药残留问题。兽药是一把“双刃剑”,兽药在动物养殖环节防治动物疾病、促进生长的同时,对靶动物安全、接触者的安全、环境生态安全、动物性食品安全以及公共卫生安全等都将构成复杂而深刻的影响,兽药不规范的使用,不可避免地会在动物体内造成不同程度的残存,过量残存的兽药或兽药代谢物,相当一部分还保留有一定的生物活性,如果通过食物链进入人体内产生蓄积,即可对人体正常生理机能构成影响,甚至引起直接的毒害作用[1-2]。兽药残留检测分析是目前保障畜产品安全的有效手段,受兽药种类、前处理方法、畜产品本身基质等因素影响我国兽药残留检测仍面临前处理方法复杂耗时、检测效率低、多种类药物残留联检技术缺乏等技术瓶颈,当前兽药残留检测工作仍难以实现对畜产品兽药残留质量安全风险的全面分析与评价。因此,在兽药残留检测中开发快速、简便的前处理技术及具有高灵敏度、高选择性和良好重现性的检测技术已成为未来兽药残留检测的趋势。
近年来动物源性产品中多种类兽药残留的联检技术成为研究热点,Desmarchelier等[3]建立了乳制品、鱼类、蛋类食品中154种药物残留的LC- MS/MS检测方法,涉及105种抗生素、41种抗寄生虫药、5种抗炎药和3种镇静剂类药物;Bessaire等[4]利用QuEChERS方法建立了鸡蛋、牛奶、肉类等食品中23种内酰胺类药物的快速筛查方法;Goessens等[5]采用UHPLC- Orbitrap-HRMS对水产品中林可酰胺类、青霉素类、头孢菌素类、二氨基嘧啶类、截短侧耳素类和苯酚类等11类46种抗菌药物残留进行全扫描快速筛查分析;孙雷等[6]利用超高压液相色谱- 三重四级杆/线性离子阱串联质谱开展了猪肉中14类92种兽药残留的高通量筛查和定量方法的研究,并采用MRM- IDA- EPI扫描模式提升了方法筛查准确度;蒋定之等[7]针对禽蛋产品建立了磺胺及其增效剂类、喹诺酮类、硝基咪唑类、喹乙醇代谢物、吩噻嗪类等14类48种兽药残留的快速筛查检测方法,以应对鸡蛋中禁限用药物的快速检测;李娜等[8]利用改进的QuEChERS方法建立了禽肉、猪肉中4类29种禁限用兽药残留的检测方法,解决了四环素类兽药难与其他类兽药同时检测的难题;徐伟等[9]使用WondaPak QuEChERS多兽药残留专用提取包和净化包建立了猪肉中8类125种药物残留的检测方法,使前处理操作在20 min即可完成。这些国内外研究均专注于通过建立快速的前处理技术和仪器全扫描分析模式,应用一种检测方法去实现畜产品中多种类药物残留的快速测定,以提升兽药残留检测工作效率。
本研究为提升宁夏地区兽药残留分析工作效率和监测水平,全面保障宁夏滩羊、肉牛、奶产业等特色畜产品质量安全,研建符合宁夏畜产品质量安全保障工作需求的兽药残留检测方法,从生产环节实际兽药使用种类和国家规定禁限用药物种类入手,确定筛查药物种类。首先通过宁夏兽药信息化监管平台对兽药经营和使用环节的药物使用情况进行大数据统计分析与调研,同时综合考虑农业农村部禁停用药物名录和GB 31650—2019《食品安全国家标准 食品中兽药最大残留限量》中规定的有最大残留限量的药物,筛选确定生产环节不规范用药可能会对宁夏肉牛产业高质量发展带来风险隐患的兽药种类,共12类。利用超高效液相色谱- 串联质谱多反应监测技术与Oasis PRiME HLB固相萃取快速净化前处理技术建立牛肉中多组分兽药残留联检应用技术,开发一次进样可同时识别并分析12类80种兽药及其代谢物的高通量检测方法,实现检测效率提升、参数扩增、覆盖面扩大,希望为宁夏优势特色肉牛产业高质量发展和牛肉产品质量安全监管提供重要的技术支撑。
1 材料与方法
1.1 材料与试剂
Oasis PRiME HLB固相萃取柱(200 mg,6 mL),美国Waters公司;0.22 μm微孔亲水性聚丙烯滤膜,美国Waters公司;甲酸、乙腈、甲醇均为色谱纯,美国Fisher公司;实验用水均为超纯水;标准品分别购于德国DrEhrenstorfer GmbH公司、德国WITEGA公司及中国兽医药品监察所。
1.2 仪器与设备
ACQUITY UPLC- Xevo TQ- S micro型超高效液相色谱- 串联质谱联用仪,美国Waters公司;AE- 205型电子天平,瑞士Mettler Toledo公司;CT15RT型高速冷冻离心机,日本HITACHI公司;氮吹仪,美国Organomation Associates公司。
1.3 实验方法
1.3.1标准工作液的配制
精密称取标准品各约10 mg,分别置于10 mL棕色容量瓶中,用甲醇溶解并定容至刻度,混匀,配制质量浓度为1 mg/mL的标准储备液。分别准确量取1 mg/mL的各标准储备液1 mL,于10 mL容量瓶中,用甲醇定容至刻度,配制成质量浓度为100 μg/mL的标准工作液。准确量取100 μg/mL标准工作液各500 μL,于50 mL容量瓶中,用甲醇稀释定容至刻度,混匀,配制成质量浓度为1 μg/mL的混合标准工作液。
1.3.2检测条件
1.3.2.1 液相色谱条件
色谱柱使用Waters HSS T3色谱柱(2.1 mm×100 mm×1.8 μm),流动相A为φ(甲酸)0.1%的水溶液,流动相B为φ(甲酸)0.1%的甲醇溶液,柱温为45 ℃,样品盘温度为10 ℃,进样量为2 μL,流动相流速为0.45 mL/min。HPLC的梯度洗脱程序见表1。
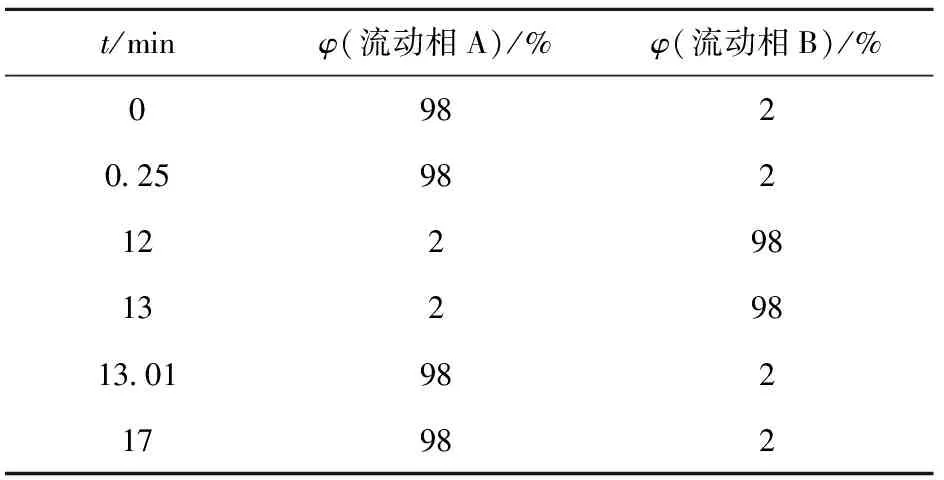
表1 HPLC的梯度洗脱程序Tab.1 Gradient elution program of HPLC
1.3.2.2 质谱条件
电喷雾正离子源(ESI+);多反应监测(MRM)采集模式;毛细管电压3.5 kV;离子源温度150 ℃;脱溶剂气温度600 ℃;脱溶剂气流速度1 000 L/h;锥孔气150 L/h;碰撞气流速0.15 mL/min。80种兽药及其代谢物的质谱监测参数见表2。
1.3.3前处理方法
准确称取2.50 g(精确至0.01 g)均质好的牛肉样品,置于50 mL聚丙烯离心管中,加入φ(甲酸)=0.2%且φ(乙腈)=80%的水溶液10 mL,旋涡振荡,12 000 r/min高速离心5 min,取上清液待净化。取Oasis PRiME HLB固相萃取柱(200 mg,6 mL),不需要活化与平衡,直接取3 mL上清液过固相萃取柱,保持1秒1滴的流速,收集全部流出液,然后再准确量取2 mL流出液,氮气吹干,1 mLφ(甲酸)=0.1%且φ(甲醇)=10%的水溶液溶解,过0.22 μm微孔亲水性聚丙烯滤膜,用HPLC- MS/MS测定分析。
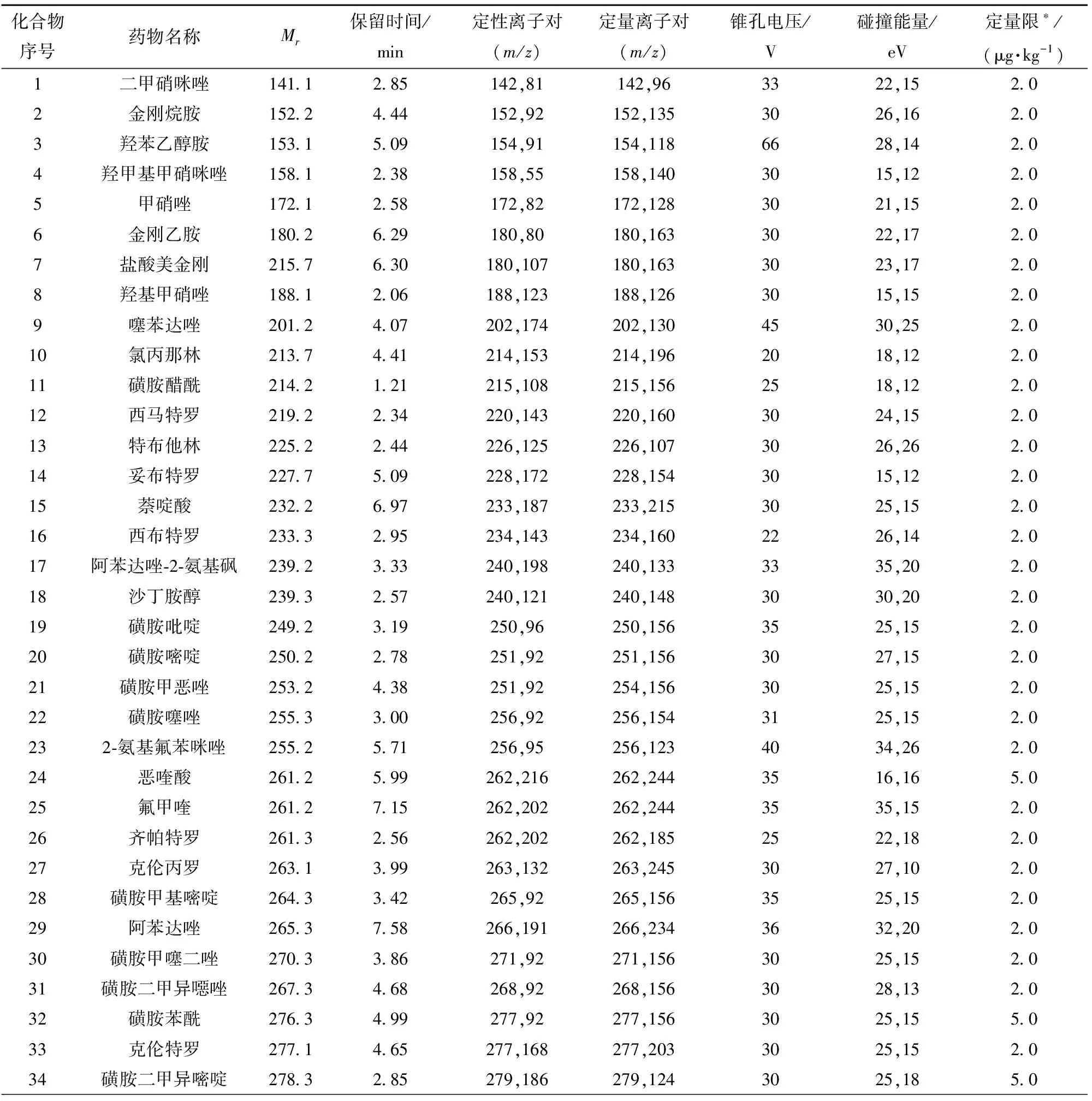
表2 80种兽药及其代谢物的质谱监测参数Tab.2 Mass spectrometry monitoring parameters of 80 veterinary drugs and their metabolites
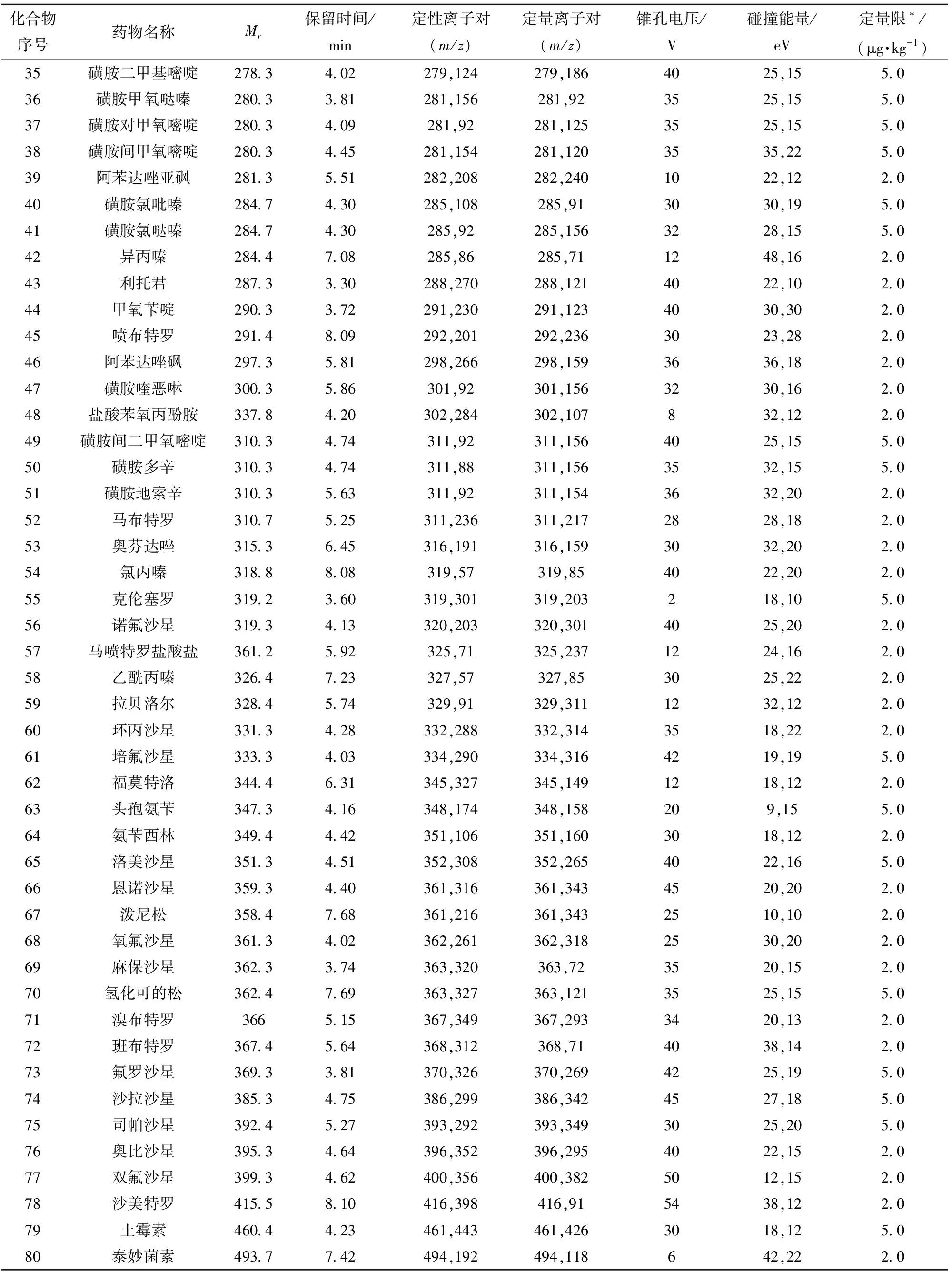
续表2
2 结果与分析
2.1 测定药物的选择依据
本研究在检测药物的选择从3个方面考虑,一是GB 31650—2019《食品安全国家标准 食品中兽药最大残留限量》中明确规定有最大残留限量的药物及其同类药物,在考虑国标规定药物的同时,将部分药物的同类药物纳入选择范围,以紧追行业发展趋势,充分覆盖养殖环节使用兽药种类,包括8种氟喹诺酮类(表2中化合物序号15、24、25、69、73、75、76、77)、4种硝基咪唑类(化合物序号1、4、5、8)、2种激素类(化合物序号67、70)、7种苯并咪唑类(化合物序号9、17、23、29、39、46、53)、3种镇静剂类(化合物序号42、54、58)、21种磺胺类(化合物序号11、19、20、21、22、28、30、31、32、34、35、36、37、38、40、41、44、47、49、50、51)和泰妙菌素(化合物序号80)药物;二是农业农村部第2292号公告、250号公告中明确规定停止、禁止在养殖环节使用的药物及其他化合物[10],包括4种氟喹诺酮类(化合物序号56、61、65、68)、21种β-激动剂类(化合物序号3、10、12、13、14、16、18、26、27、33、43、45、48、52、55、57、59、62、71、72、78)和金刚烷胺类(化合物序号2、6、7)药物;三是通过宁夏兽药信息化管理平台大数据统计掌握的在宁夏养殖环节大量使用,且不规范使用会造成兽药残留风险的药物,包括3种氟喹诺酮类(化合物序号60、66、74)、土霉素(化合物序号79)、氨苄西林(化合物序号64)、头孢氨苄(化合物序号63)药物,共涉及12大类80种兽药及其代谢物。此方法涉及药物种类多,涵盖参数广,突破了传统检测方法只能够对已知药物的单一筛查,能够实现对畜产品兽药残留质量安全风险隐患的全方位评价分析。
2.2 前处理条件的优化结果
2.2.1提取溶剂的优化结果
实验中选取不同溶剂提取化合物,包括乙腈、甲醇、φ(甲酸)=0.2%的乙腈溶液(以下称为甲酸乙腈溶液)、φ(甲酸)=0.2%且φ(乙腈)=80%的水溶液(以下称为甲酸乙腈水溶液)4种溶剂。结果表明:乙腈与甲醇相比,提取效率更高,上机后化合物整体峰形和提取率都偏高,但仍不能完全满足正离子化合物检测需求;不同体积分数的甲酸乙腈和甲酸乙腈水溶液比较,甲酸乙腈水溶液更适合多种类药物提取,能够显著提高喹诺酮类、四环素类等常规适宜水相溶剂提取的药物;选择不同体积分数的甲酸乙腈水溶液进行目标化合物提取,实验中发现甲酸浓度过高会对磺胺类等化合物回收率有影响,当甲酸乙腈水溶液作为提取溶剂时80种兽药及其代谢物的回收率均可保持在60%~120%范围内,能够充分满足GB/T 27417—2017《合格评定 化学分析方法确认和验证指南》中对化合物分析正确度的要求[11],且提取效果明显高于其他溶剂,故本实验最终选取甲酸乙腈水溶液作为提取液。不同提取溶剂时80种兽药及其代谢物结果见图1。
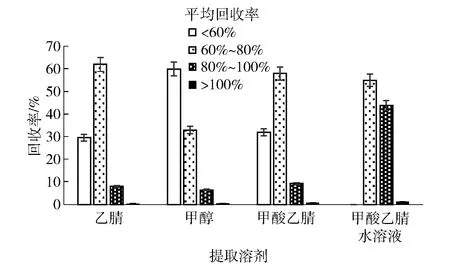
图1 不同提取溶剂时80种兽药及代谢物平均回收率Fig.1 Average recoveries of 80 veterinary drugs and their metabolites with different extraction solvents
2.2.2固相萃取柱的优化结果
固相萃取技术是一种简单、快速、准确的分离技术,能够选择性去除干扰杂质,获得高灵敏度,是兽药残留分析中最常用的净化方式。动物源性食品样品中存在大量的磷脂,非常容易干扰部分化合物分析定量,同时影响色谱柱寿命及仪器维护成本。本研究利用Oasis PRiME HLB固相萃取小柱进行样品净化,能有效去除磷脂等干扰杂质,提高检测工作的准确性[12-13]。同时,其通过式的净化处理策略能极大提高样品分析通量,使样品流速更快且不容易被堵,也极大地提高了检测效率,使样品处理过程简单高效,非常适用于检验检测机构大批量的日常分析检测。
2.3 方法定量限与线性范围
准确量取100 μg/L混合标准溶液于2.50 g空白牛肉组织中制成1.0、2.0、5.0、10.0、50.0、100.0 μg/kg添加,前处理后上机测定,依据信噪比(S/N)≥10,综合各类药物的精密度和准确度,保证每种兽药及其代谢物都能够满足检测定性定量要求,确定12大类80种药物及代谢物的定量限在2.0~5.0 μg/kg,见表2。
准确量取混合标准工作液适量,用φ(甲酸)=0.1%且φ(甲醇)=10%的水溶液配制成浓度为1.0、2.5、5.0、25.0 、50.0 μg/L的系列混合标准工作液,取空白样品前处理氮吹后的残留物5份,依次加入配制好的系列混合标准工作液1 mL,充分溶解后得空白基质匹配系列标准工作液,过滤后上机测定,可最大程度降低基质影响。每个浓度进3针,以特征离子质量色谱峰面积为纵坐标(y),基质匹配标准溶液浓度为横坐标(x),绘制标准曲线。80种药物及代谢物在1.0~50.0 μg/L呈现良好的线性关系,相关系数均大于0.990,见表3。
2.4 方法精密度与准确度
将空白牛肉样品进行 2.0、5.0、50.0、100.0 μg/kg质量浓度混合标准工作液加标后,按照前处理方法处理后上机,平行测试5份样品,重复3 次考察回收率和相对标准偏差,结果见表3。从表3中实验结果可以看出本方法牛肉中80种药物及代谢物在2.0 μg/kg加标浓度的平均回收率为 60.0%~103.0%,批间RSD为0.4%~18.7%;5.0 μg/kg加标浓度的平均回收率为69.8%~99.5%,批间RSD为0.3%~17.1%;50 μg/kg加标浓度的平均回收率为67.7%~99.7%,批间RSD为0.4%~19.6%;100 μg/kg加标浓度的平均回收率为 64.5%~92.5%,批间RSD为0.4%~18.1%。牛肉中80种兽药及其代谢物的加标回收率与精密度见表3。
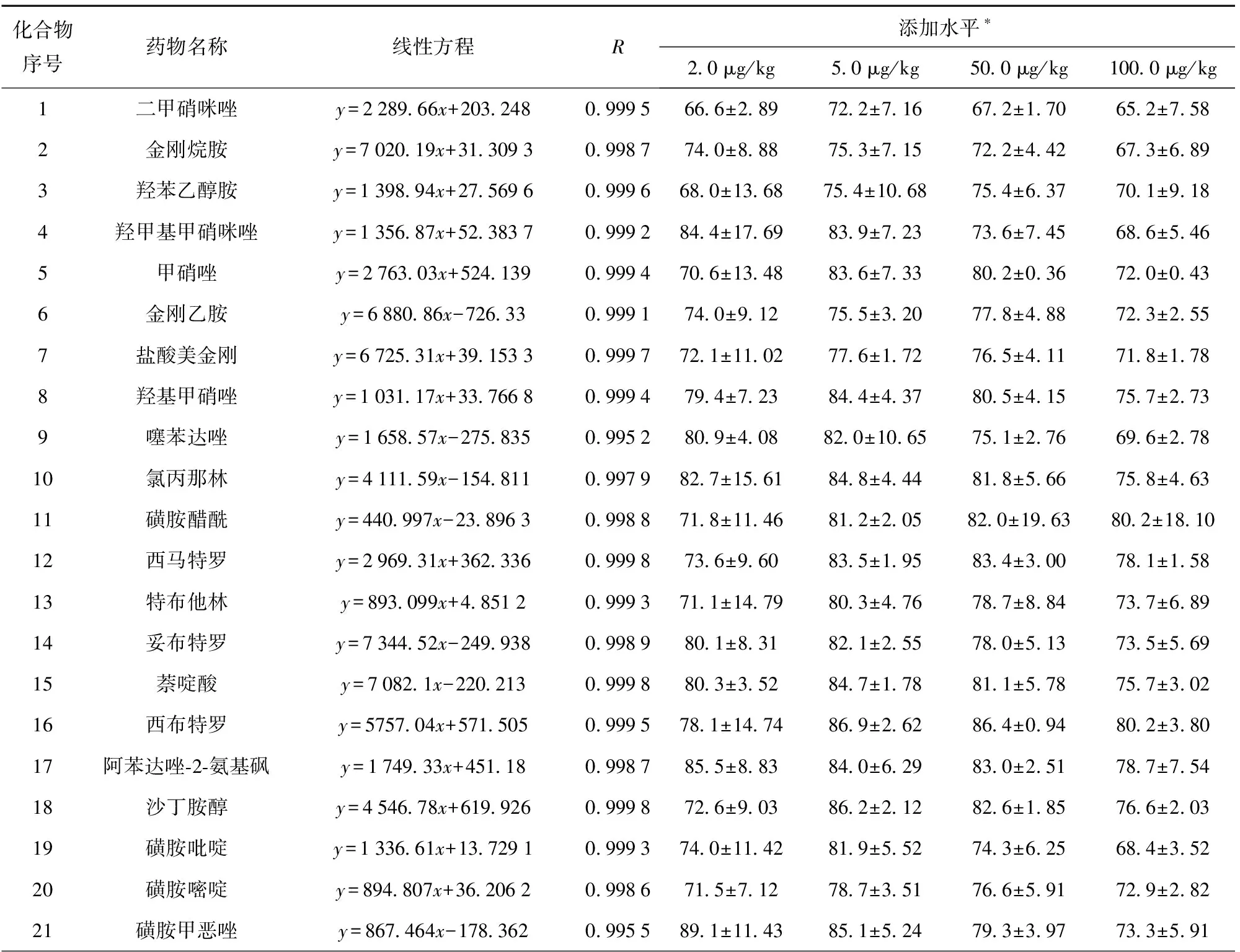
表3 牛肉中80种兽药及其代谢物的加标回收率与精密度Tab.3 Recovery rate and precision of 80 veterinary drugs and their metabolites in beef %
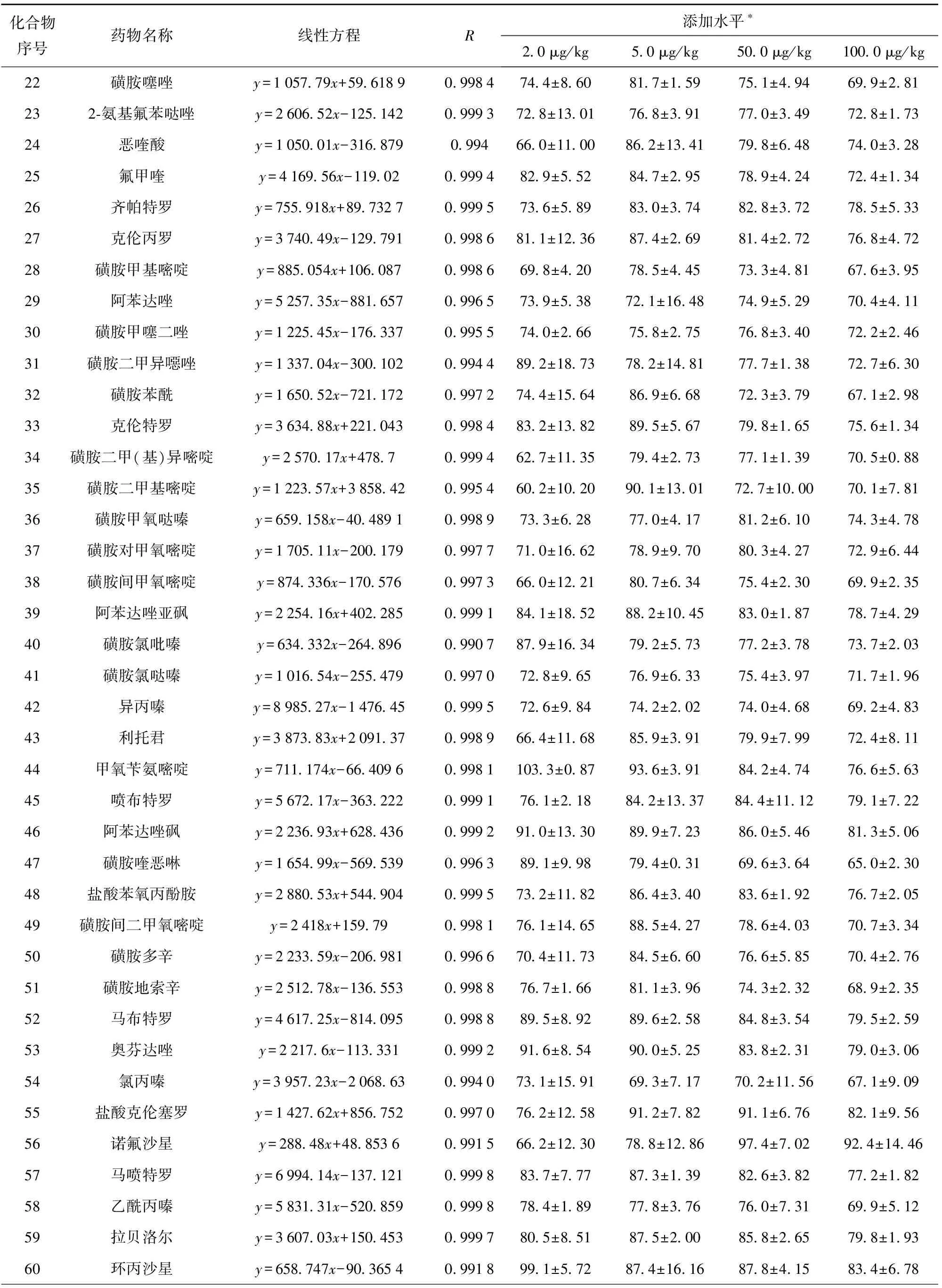
续表3
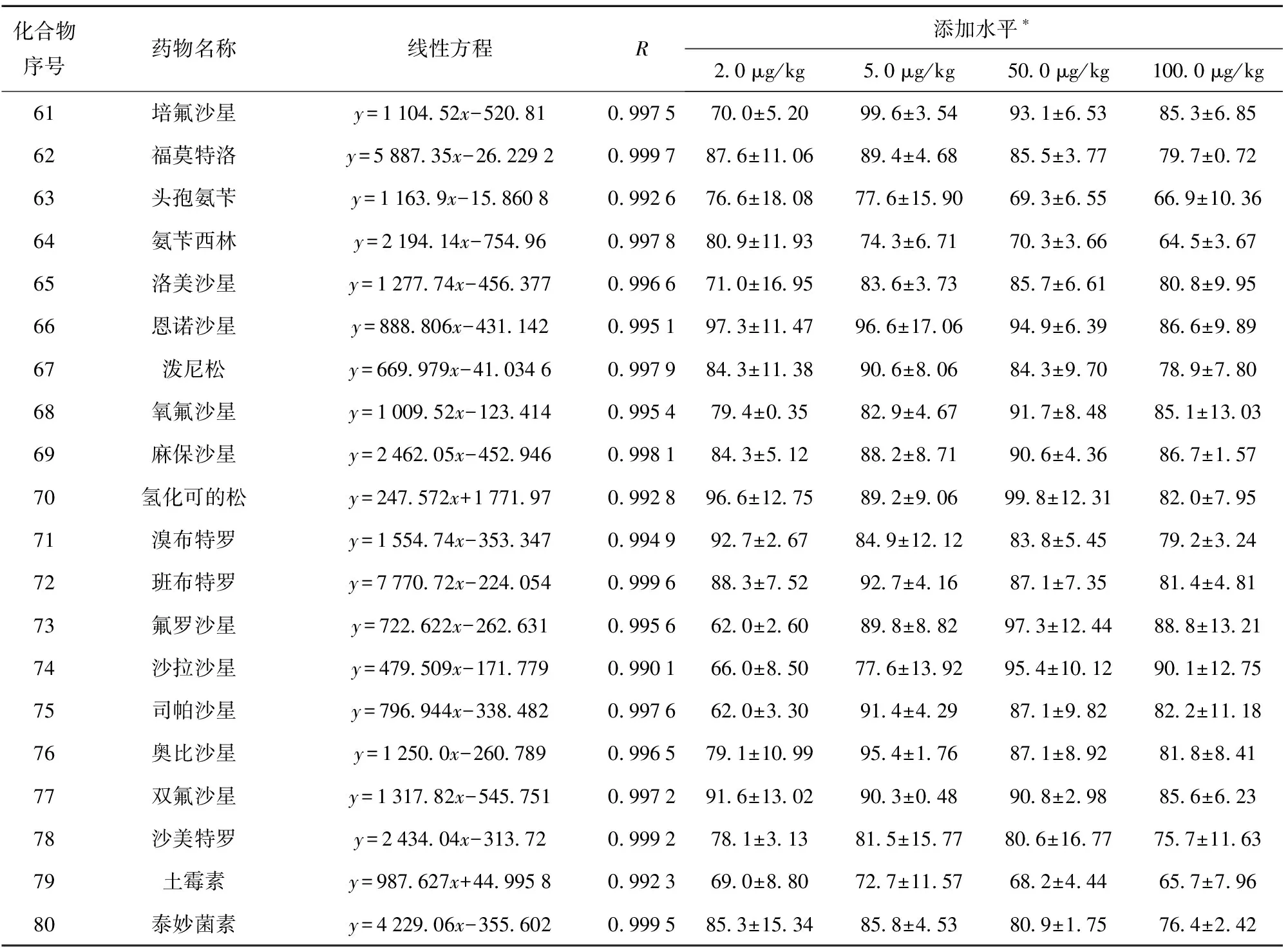
续表3
2.5 实际样品检测结果
利用本方法对来自农贸市场和屠宰场的40批牛肉进行药物残留检测,结果按照国家标准GB 31650—2019《食品安全国家标准 食品中兽药最大残留限量》中各类药物及其代谢物的最大残留限量进行判定。结果显示,有1批牛肉样品中检出土霉素残留,残留量为54.5 μg/kg,GB 31650—2019中规定牛肉肌肉组织中其最大残留限量为100 μg/kg,属合格产品;2批样品检出磺胺类药物,残留量分别为磺胺间甲氧嘧啶23.3 μg/kg和35.4 μg/kg,GB 31650—2019中规定牛肉肌肉组织中磺胺类药物最大残留限量为100 μg/kg,属于合格产品;1批检出恩诺沙星残留,残留量为118 μg/kg,GB 31650—2019中规定牛肉肌肉组织中其最大残留限量为100 μg/kg,属于不合格产品。本研究同时应用国标方法GB/T 21317—2007《动物源性食品中四环素类兽药残留量检测方法 液相色谱- 质谱法》[14]、GB/T 20759—2006《畜禽肉中十六种磺胺类药物残留量的测定 液相色谱- 串联质谱法》[15]和GB/T 21312—2007 《动物源性食品中14种喹诺酮药物残留检测方法 液相色谱- 质谱 质谱法》[16]3种方法分别对检测结果为阳性的牛肉样品进行复检,4份阳性样品检测结果分别为土霉素残留58.6 μg/kg,2份磺胺间甲氧嘧啶残留分别为26.1 μg/kg和31.2 μg/kg,恩诺沙星残留115 μg/kg。从牛肉阳性样品经国标检测方法检测验证表明:本研究方法定性定量结果准确可靠,能够满足动物源性食品残留检测的需求。
3 结 论
本检测方法选择甲酸乙腈水作为提取溶剂,采用通过式固相萃取净化技术,有效去除样品中的蛋白、磷脂等干扰杂质,建立快速、高效的样品前处理方法。采用Waters公司HSS T3色谱柱提升多种类化合物的分离度和灵敏度,利用超高效液相色谱- 串联质谱多反应监测模式实现对80种兽药及其代谢物的准确定性定量分析。
本方法根据欧盟2002/657/EC和我国农牧发[2003]1号文规定进行残留量测定方法学考察验证,方法的线性范围、回收率和精密度等参数均能满足我国和欧盟的规定,方法具有较高的重现性和可操作性,能够满足对牛肉中80种药物及代谢物残留定性和定量分析的要求。本方法可以实现一针进样同时测定80种兽药及代谢物的残留,解决了使用常规检测标准多类药物多种前处理方法复杂耗时的技术难题,有效提升了兽药残留检测效率,通过方法在牛肉产品质量安全监测中的应用,可有效提升牛肉兽药残留风险隐患的排查能力。
