扩张型心肌病伴房颤并多脏器梗死和消化道出血1例
2022-03-08闫晓凤刘江华
闫晓凤 刘江华
扩张型心肌病(dilated cardiomyopathy,DCM)是一种异质性心肌病,以左心室或双心室扩大伴心肌收缩功能降低为特征。DCM常伴心律失常,心房纤颤(atrial fibrillation, AF)是常见的不良预后。DCM合并AF最严重的并发症是各种血栓栓塞。AF可致的动脉栓塞大多数为脑动脉栓塞(缺血性脑卒中),极少数是体循环动脉栓塞。AF合并体循环动脉栓塞由于症状缺乏特异性、可自愈性及临床医生警惕性不高,极容易漏诊。本文报道1例DCM伴AF并发多脏器梗死和消化道出血病例的诊疗过程,以期提高对此类疾病的诊疗及日常管理认识。
1 病例资料
病人男,农民,64岁,因“腹痛1 d”于2020年5月11日10:24急诊入院。病人入院前1 d无诱因下出现难以忍受的腹中部持续性刺痛,疼痛与进食及体位无明显联系,无放射,伴恶心、非喷射性呕吐4次,呕吐物为胃内容物,无呕血,无发热、腹泻、腹胀等不适,当日凌晨至当地医院就诊,查腹部平片示:左中腹结节影,心电图示AF(快速型),考虑不能除外肠系膜栓塞,遂被送至我院急诊就诊,急诊行全腹CT血管造影术(CTA)示:脾梗死;脾动脉脾内上分支闭塞。既往:2015年3月因“心悸、气促2月,双下肢水肿5 d”在我院治疗,当时查动态心电图示:(1)AF;(2)频发室性早搏(多源性、部分成对、短阵室性心动过速)。行心脏超声检查示:(1)静息状态下室壁运动普遍减弱;(2)二尖瓣、主动脉瓣轻度关闭不全;(3)三尖瓣轻度关闭不全(呈中度肺动脉高压表现)。行冠脉造影术可见:正常右优型冠脉,左右冠脉管壁光滑,管腔通畅。当时诊断:(1)AF,心功能Ⅲ~Ⅳ级;(2)DCM。出院后病人未规范服药治疗,平素仍有轻微活动后气促症状,未予重视。入院查体:急性病容,心界向左下扩大,心律绝对不齐,心音强弱不等,脉率小于心率,心率90次/min。全腹稍紧张,压痛、反跳痛明显,肠鸣音减弱,双下肢不肿。辅助检查(5月11日10:24急诊):心电图提示AF(见图1),血红蛋白为122.20 g/L,血小板为100.70×109/L,中性粒细胞百分比为0.835,D二聚体为1031 ng/mL,血淀粉酶类为199 U/L,肌酸激酶为908 U/L,肌酸激酶同工酶为67 U/L。胸部CT平扫+全腹部血管成像:(1)心脏增大,主动脉、冠状动脉硬化;(2)肝多发囊肿;(3)脾梗死(见图2);(4)双肾囊肿;(5)脾动脉脾内上分支闭塞。诊断:(1)脾动脉分支闭塞并脾梗死;(2)DCM;(3)AF,心功能Ⅳ级。

图1 心电图示AF
收住入院(5月11日17:20)急查白细胞为5.96×109/L,红细胞为5.29× 1012/L,血红蛋白为125.0 g/L,血小板为86×109/L ,中性粒细胞百分比为0.747,凝血酶原时间为16.20 s,凝血酶原活动度为60%,国际标准化值为1.36,D-二聚体为874 ng/mL,脑利钠肽前体为11010.0 pg/mL,心电图示AF。本例病人入院时已发病1 d,错过溶栓治疗窗,故未予溶栓治疗。予吸氧,监护,卧位,应用华法林钠片3 mg、低分子肝素钙5000 IU抗凝,地佐辛注射液2 mL静脉泵入缓解疼痛,以及抗炎、护胃等对症治疗。
病人入院13 h后解一次砖红色尿,约500 mL, 急查尿常规潜血(+++),白细胞(+),尿蛋白(+++),胆红素(+)。入院17 h(5月12日12:00)病人诉腹胀,无排便、排气,予开塞露塞肛后解1次暗红色烂便共约600 mL,考虑存在消化道出血,不排除抗凝治疗所致出血及肠系膜栓塞可能,继续禁食,予艾司奥美拉唑钠抑酸等对症支持治疗。同时停用华法林,继续低分子肝素抗凝治疗。
入院后19 h复查血常规:白细胞为7.05×109/L,红细胞为5.37×1012/L,血红蛋白为126.00 g/L, 血小板为87.0×109/L,中性粒细胞百分比为0.798,凝血酶原时间为22.4 s,凝血酶原活动度为39%,国际标准化值为1.86, D-二聚体为1855 ng/mL,超敏肌钙蛋白为0.033 ng/mL,血淀粉酶为224 U/L,超敏C反应蛋白为188.0 mg/L。大便潜血阳性。全腹部CT平扫+增强+血管成像示:(1)脾梗死、左肾梗死(见图2、图3);(2)肝多发囊肿;(3)肝内胆管、主胰管轻度扩张,请结合临床;(4)双肾囊肿;(5)脾动脉脾内上分支、左侧肾动脉前支中段闭塞。腹部站立正位片示:肠梗阻。见图4。

图2 全腹CT平扫示脾脏、肾脏梗死

图3 全腹CTA示肾脏梗死
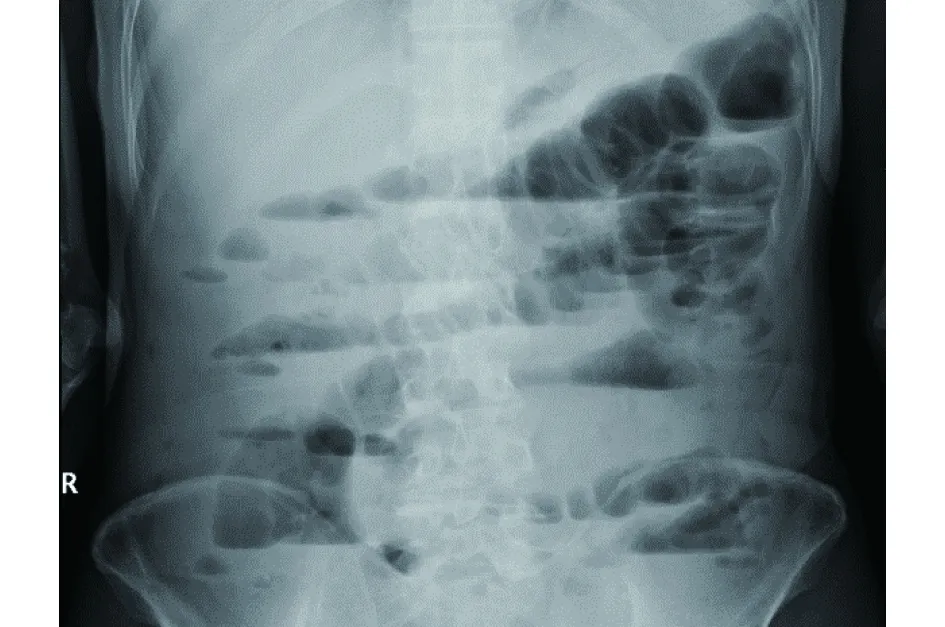
图4 腹部正位片示肠梗阻
入院后21 h病人血压下降至84/60 mmHg,将病情告知病人家属并建议送至重症监护室继续治疗,家属表示理解但要求出院。出院后随访,该病人在出院1周后于家中离世。
2 讨论
本例病人以急性腹痛起病,既往有明确的DCM合并AF病史,入院后多次查心电图提示AF发作,腹部CTA提示脾梗死和肾梗死,腹部立位片提示肠梗阻。脾梗死是脾动脉或其分支阻塞而导致的部分或全部脾脏坏死,主要原因有血栓形成、动脉粥样硬化斑块脱落、动脉内皮白细胞浸润、微循环阻塞等[1]。肾梗死是肾动脉主干或分支的急性栓塞而使肾组织缺血坏死,常见于AF、附壁血栓形成、心脏瓣膜病者[2]。肠梗阻,尤其是血运性肠梗阻是由于肠系膜血管栓塞或血栓形成,使肠管发生血运障碍,肠失去蠕动能力而导致的缺血坏死[3]。肠系膜血管栓塞与血栓形成几乎都是在高凝状态、血流缓慢、各种心源性疾病及动脉硬化性阻塞或狭窄的基础上发生。心源性病人大多伴有AF。AF增加缺血性脑卒中及体循环动脉栓塞的风险, 其年发生率分别为1.92%和0.24%[4]。体循环栓塞常见部位依次为下肢、肠系膜及内脏、上肢,60%左右的病人需要介入或外科手术干预, 事件发生30 d内致残率为20%, 致死率为25%[5]。当既往有明确AF病史的病人突发急腹症时,一定要警惕内脏及肠系膜栓塞的可能。
我们发现血栓栓塞是脾梗死、肾梗死和血运性肠梗阻发病的共同原因,本例病人考虑系由其原发病DCM合并AF长期未得到规范和规律治疗所致。
当DCM 病人是窦性心律时,血栓事件发生率为14%,在AF 时则为33%[6]。所以,临床上在治疗DCM时应尽早控制心力衰竭和心律失常,延缓心肌重构,预防猝死和栓塞发生[7]。对于已合并AF的病人CHADS2-VASC评分男性≥2分,女性≥3分,应考虑接受口服抗凝治疗,可使用华法林或新型抗凝药,预防血栓形成及栓塞[8]。抗凝治疗在降低血栓栓塞事件风险的同时, 增加了出血事件的发生风险[4]。目前临床医生常借用AF病人抗凝治疗的风险评估方法对DCM病人进行风险评估[9]。AF病人的血栓栓塞风险是连续且不断变化的, 对于AF病人应定期评估其血栓栓塞风险[10]。 HAS-BLED评分能很好地预测AF病人的出血风险, HAS-BLED≥3分较0分病人的出血风险高8.56倍[11]。而通常出血风险增高者发生血栓栓塞事件的风险往往也高, 这些病人接受抗凝治疗的临床净获益可能更大[12]。因此HAS-BLED评分增高并非抗凝治疗的禁忌,只要病人具备抗凝治疗适应证仍应进行抗凝治疗。
总之,降低DCM合并AF病人的再入院率、心血管事件发生率及死亡率,提高病人生存率和生活质量,需要形成一整套系统的综合管理模式。WHO提出心血管疾病防治的主要工作之一是以社区为基础进行综合管理[13]。而基层医生直接接触到DCM合并AF较少,这类疾病通常病情复杂多变,容易出现急危重的情况,这就要求我们一定要拓展诊疗思路,提高对该疾病系统的认识和诊治能力,增强对该疾病相关危害的认识和重视。对已经确诊为DCM合并AF的病人,应积极做好AF相关栓塞预防,所有病人均应进行终生的管理和治疗:通过卒中风险评估(在大多数病人中)选择合适的口服抗凝药物,进行AF相关症状评估,进行心率、节律控制、监测和治疗及伴随心血管疾病的防治[14]。同时还应加强健康教育和定期随访,特别是在促进病人对抗凝治疗的了解和减轻使用抗凝药物的顾虑方面,一定要建立规范的管理系统,从而增加病人的依从性,降低心力衰竭的发作频率及并发症的发生概率。期待更多的医务人员重视这类病人的综合管理,减少类似事件发生。
