溶液配制中洗涤操作的实验探究
2022-03-08马力赵雯吕春辉
马力 赵雯 吕春辉
摘要: 借助氯离子数字化传感器,对配制一定物质的量浓度的溶液实验中洗涤2~3次操作的实际效果进行实验探究,发现第一次洗涤并转移能够将绝大部分溶液残留转移,洗涤2次并转移则能够基本将溶液残留完全转移,定量且直观地验证了教材中“需用少量蒸馏水洗涤烧杯内壁和玻璃棒2~3次”的实验要求,证据性强,易于学生理解。此外,通过对使用不同容积的烧杯以及不同溶解用水量等因素的探究,得出配制一定物质的量浓度的溶液的实验中烧杯内溶液的残留主要与烧杯和溶液的接触面积等因素有关。
关键词: 物质的量浓度; 溶液配制; 实验探究
文章编号: 10056629(2022)02007104
中图分类号: G633.8
文献标识码: B
1 问题的提出
《普通高中化学课程标准(2017年版2020年修订)》在必修课程主题1“化学科学与实验探究”中将配制一定物质的量浓度的溶液列为了学生必做实验[1]。人教版[2]、鲁科版[3]、苏教版[4]、沪科版[5]四个版本教材均不约而同地将配制一定物质的量浓度的溶液作为高中学生首个必做实验,其重要程度可见一斑。而作为高中学生首个必做实验,其承载的并不单单是实验本身的,还有初高中衔接、定性到定量思维融合等更深层次的教学意义。在四个版本的教材中,人教版、苏教版、沪科版均在实验操作步骤中提到了“用少量蒸馏水洗涤烧杯内壁和玻璃棒2~3次”;鲁科版则是以留白的方式要求学生“将溶解后的溶质全部转移到容量瓶中”;人教版、沪科版更是在实验的问题讨论中要求学生思考“用少量蒸馏水洗涤烧杯内壁和玻璃棒2~3次”的原因。
为什么要用少量蒸馏水洗涤烧杯内壁和玻璃棒?通过简单推理似乎并不困难,学生也能较轻松地去理解转移时溶液残留的问题。但为什么需要洗涤的次数为2~3次,不仅仅是学生理解存在困难,教师往往也只能凭借经验进行讲解。由于配制一定物质的量浓度的溶液作为学生在高中阶段接触到的第一个定量实验,能否通过定量的手段说明需要洗涤2~3次的原因,从而培养学生的定量思维,值得我们思考。通过查阅文献,笔者发现对此类问题的定量研究极少,基于此,笔者进行了以下的实验设计及探究。
2 实验设计及探究
2.1 实验设计
在本实验的设计过程中,考虑到由于在配制一定物质的量浓度的溶液实验中存在多个环节可能造成实验误差,以及数字传感器量程限制的问题,因此在本实验中主要通过检测每次洗涤烧杯内壁和玻璃棒后的洗涤液中氯离子浓度,从而从数字化角度直观展现转移时溶液残留等问题,帮助学生更好地理解洗涤2~3次操作的相关意义。
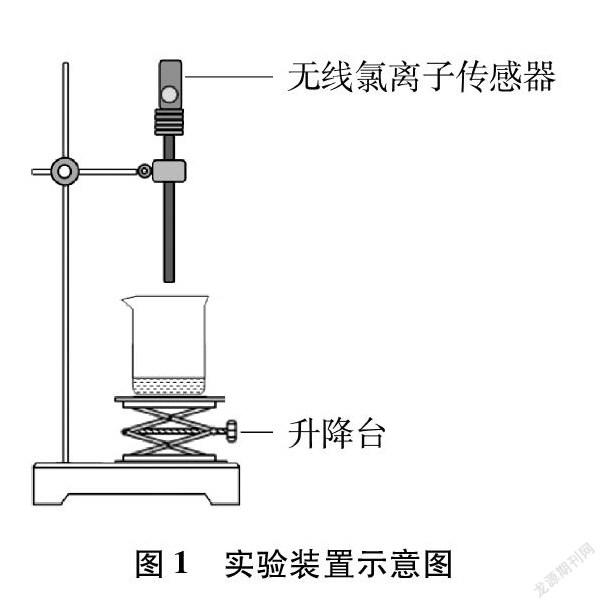
实验采用Vernier无线氯离子传感器(量程1~35000mg/L)对洗涤液中氯离子浓度进行测定。实验中将Vernier无线氯离子传感器通过铁架台予以固定(如图1所示),由升降台升降盛有洗涤液的烧杯进行测定,从而尽可能避免手持传感器不够稳定而造成测量数据的偏差。
鉴于各版本教材对配制一定物质的量浓度的溶液实验的要求存在细微差异,如人教版中要求配制100mL 1.00mol/L NaCl溶液,沪科版中则是要求配制100mL 1.000mol/L NaCl溶液,魯科版中要求配制100mL 0.400mol/L NaCl溶液,苏教版则是要求配制100mL 0.100mol/L Na2CO3溶液。四个版本的教材只有人教版对溶解固体溶质的蒸馏水体积规定为40mL,其他版本的教材仅仅是提及用适量蒸馏水进行溶解,沪科版、苏教版教材还对溶解过程中使用烧杯的规格定为100mL等。因此在本实验的探究中,选择以配制氯化钠溶液为例,并综合溶解度等多方面因素的考虑,选取溶解时使用不同规格烧杯(50mL、 100mL)、溶解时加入不同体积蒸馏水(40mL、 30mL、 20mL)、配制不同浓度溶液(1.000mol/L、 0.400mol/L),分别对3次洗涤后洗涤液中氯离子的浓度进行检测。此外,实验中为了确保NaCl完全溶解,在肉眼观察到NaCl固体完全溶解后,均静置5分钟,再进行转移、洗涤、测量等操作。洗涤时控制每次蒸馏水用量均为15mL,并尽可能保证每次洗涤的方式、频率、时间一致。
2.2 实验分析与结果
2.2.1 多次洗涤后洗涤液中氯离子浓度的变化
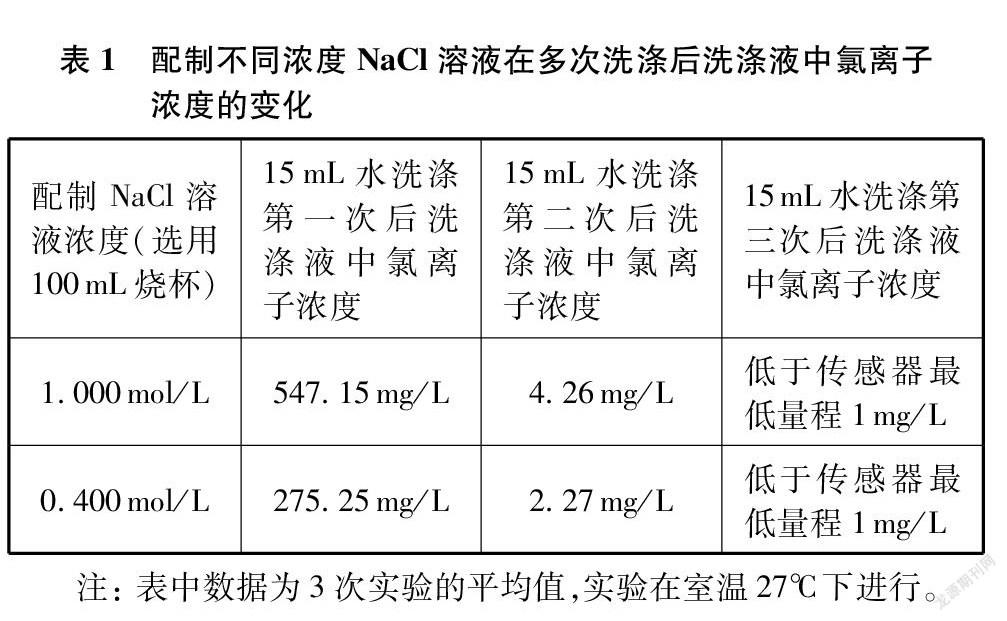
由于烧杯中溶液在转移后,残留在烧杯中溶液的量存在一定的随机性,会导致测量结果存在较大差异,因此本实验过程中则以转移至烧杯中不存在肉眼可见的明显液滴后再进行洗涤测量,并通过三次平行实验以减小误差。实验中对烧杯的洁净程度要求较高,不够洁净的烧杯也往往会存在较多溶液挂壁的现象,导致测量结果差异较大。表1为配制1.000mol/L与0.400mol/L NaCl溶液(选用100mL烧杯),均加入40mL蒸馏水溶解后,各用15mL蒸馏水洗涤三次时,每次洗涤液中氯离子浓度的变化情况。
通过分析表1数据不难发现,无论是配制1.000mol/L还是0.400mol/L的NaCl溶液,第一次洗涤后洗涤液中氯离子浓度均较高,而第二次洗涤后洗涤液中氯离子浓度则大幅下降,均维持在个位数,可见第一次洗涤能够大幅度减少溶液残留。由于本次实验中选用的Vernier无线氯离子传感器,其量程为1~35000mg/L,当3次洗涤后洗涤液中氯离子浓度已降至传感器最低量程1mg/L以下,故记录为低于传感器最低量程1mg/L。由此也可以得出,用15mL水洗涤1次并转移时已能将绝大部分溶液残留转移,洗涤2次并转移则能够基本将溶液残留完全转移。当然如若在前述溶液转移过程中存在较多溶液挂壁现象以及洗涤时可能存在加入蒸馏水较少等情况,洗涤3次并转移则可以有效保证溶液残留完全转移。可见,教材中规定的用少量蒸馏水洗涤烧杯内壁和玻璃棒2~3次,是有科学道理的。
2.2.2 溶解时加入不同体积蒸馏水对溶液残留的影响
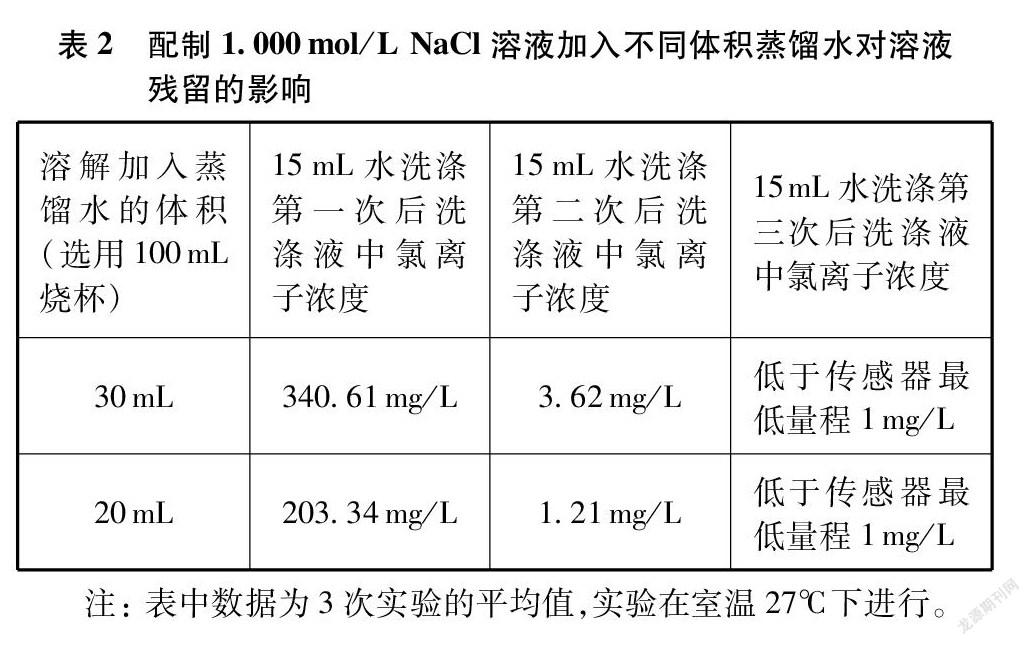
人教版对溶解固体溶质的蒸馏水体积规定为40mL,其他版本的教材则仅仅是提及用适量蒸馏水进行溶解。那么溶解时加入不同体积蒸馏水对溶液残留又会有怎样的影响呢?考虑到氯化钠的溶解度,选择溶解时分别加入40mL(实验数据见2.2.1表1第一行)、30mL、 20mL蒸馏水进行实验。表2为配制1.000mol/L NaCl溶液(选用100mL烧杯)加入不同体积蒸馏水溶解,静置5分钟后再进行转移,并各用15mL蒸馏水洗涤3次时,每次洗涤液中氯离子浓度的情况。
结合表1配制1.000mol/L NaCl溶液加入40mL蒸馏水溶解、洗涤后对应测得的数据,以及表2加入30mL、 20mL蒸馏水溶解、洗涤后对应测得的数据进行分析,可以发现溶解时加入不同体积的蒸馏水确实对溶液残留存在影响。但是有趣的是,随着溶解水量的减少,洗涤液中的氯离子浓度也随之减小。这与我们预想的因为溶解所用水量少,使得残留溶液的浓度高,从而导致测得洗涤液中的氯离子浓度高,并不一致。分析其原因则可能是当溶解加入蒸馏水量较少时,其溶液与烧杯的接触面积相对较小,溶液残留也相对较少,从而导致洗涤后洗涤液中的氯离子浓度相对较小。
而通过表1、表2中的相关数据,我们似乎可以得出在配制1.000mol/L NaCl溶液的实验中加入20mL蒸馏水进行溶解,其溶液残留相对较少,但是我们也可以发现在多次洗涤后,原来溶解时加入不同体积蒸馏水对溶液残留的影响已是微乎其微。
2.2.3 溶解时选用不同规格的烧杯对溶液残留的影响
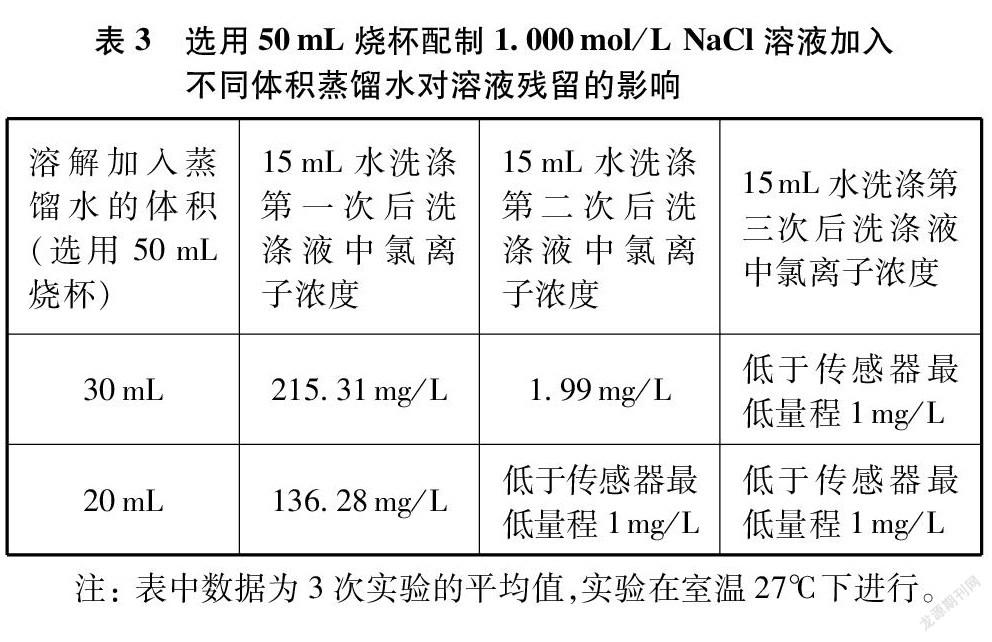
沪科版、苏教版教材对溶解过程中使用烧杯的规格定为100mL,人教版、鲁科版教材则未有规定。那么配制1.000mol/L NaCl溶液选用不同规格的烧杯对溶液残留是否存在影响呢?于是我们选择50mL烧杯加入不同体积蒸馏水溶解,静置5分钟后再进行转移、洗涤,并测量各用15mL蒸馏水洗涤3次时每次洗涤液中氯离子浓度的情况,与前述选用100mL烧杯的实验进行对照。
通过分析表3数据,在一定程度上进一步验证了前述实验结论。而对比表2、表3数据我们则可以发现,选用50mL烧杯进行溶解时,其溶液残留量均小于100mL烧杯。以50mL烧杯底部直径4.7厘米、100mL
烧杯底部直径5.2厘米计算,我们可以发现,盛装相同体积液体时,液体与50mL烧杯的接触面积会小于与100mL烧杯的接触面积,溶液残留相对较少,从而造成上述数据的差异。当然,通过比较,我们似乎可以得出,在配制1.000mol/L NaCl溶液实验中选用50mL烧 杯进行溶解,其溶液残留相对较少,但是在多次洗涤后,却早已消除了其影响。
3 实验总结与思考
本实验通过探究每次洗涤后洗涤液中氯离子浓度的变化,尝试从定量的角度分析配制一定物质的量浓度的溶液中各次洗涤操作的效果,得出了以下结论:
(1) 分析实验数据发现第一次洗滌并转移已能够将绝大部分溶液残留转移(以本实验历次数据最大值计算,其溶液残留造成误差仅为0.0024%),洗涤2次并转移则能够基本将溶液残留完全转移,验证了教材中“需用少量蒸馏水洗涤烧杯内壁和玻璃棒2~3次”的实验要求是有科学道理的。
(2) 通过对使用不同容积的烧杯以及不同溶解用水量等因素的探究,发现这些因素虽然对最终洗涤并转移后的结果影响不大,但烧杯中的溶液残留还是与烧杯和溶液的接触面积等因素有关。
本实验探究的目的并不止于此。笔者在此基础上还进行了以下思考:
(1) 在本实验教学中教师可以尝试引导学生亲自进行实验,在实验中体验科学探究的一般过程,体会、认识手持技术手段对化学科学创新的重要价值。其实,在任何实验探究中教师都不应该把知识仅仅当成结论告知给学生,而是让学生在自我需求的驱动下,通过在实验中的合作和探究自主完成知识的建构、实现认知的转变和发展[6],力求通过实验真正让“静”的知识“动”起来,促成知识的动态生成。
(2) 配制一定物质的量浓度的溶液是中学化学教材中的经典实验之一。然而,越经典的实验,教师在日常教学中越容易忽略对实验本身的思考。在信息化、数字化高度发展的今天,教师更应该利用好教材以及教材中的经典实验,借助数字化仪器设备,不断思考创新,设计开发出更富时代特征、更符合素养发展的实验探究活动,使经典实验在传承的同时能够与时俱进、焕发新生。
参考文献:
[1]中华人民共和国教育部制定. 普通高中化学课程标准(2017年版2020年修订)[S]. 北京: 人民教育出版社, 2020.
[2]王晶, 毕华林主编. 普通高中教科书·化学·必修第一册[M]. 北京: 人民教育出版社, 2019: 61~62.
[3]王磊主编. 普通高中教科书·化学·必修第一册[M]. 济南: 山东科学技术出版社, 2019: 25~26.
[4]王祖浩主编. 普通高中教科书·化学·必修第一册[M]. 南京: 江苏凤凰教育出版社, 2020: 39~40.
[5]麻生明, 陈寅主编. 普通高中教科书·化学·必修第一册[M]. 上海: 上海科学技术出版社, 2021: 30~31.
[6]王程杰. 对中学化学实验教学作用的重新认识[J]. 教学仪器与实验, 2001, (4): 4~6.
