氨基酸对淀粉结构形貌及热致相变行为的影响
2022-03-07许慧娴朱芷仪韦惠莹赖晓宁钟航宇刘宏生贾晓江
许慧娴,朱芷仪,韦惠莹,赖晓宁,钟航宇,刘宏生,贾晓江
(1.华南理工大学食品科学与工程学院,广东 广州 510640)(2.石家庄君乐宝乳业有限公司,河北 石家庄 050221)
淀粉是食品的主要组成成分,可提供人类生命活动所需的能量。天然淀粉存在一些缺点,如易成糊、糊粘度高、冻融稳定性差等。这些缺点增大了淀粉的加工难度,同时导致淀粉类食品产生不良风味和口感[1],在实际生产中通常需要对其进行改性处理。常见的改性方式主要包括化学、物理及酶法改性,其中绿色、安全的物理改性方式一直备受关注[2]。近年来越来越多研究聚焦于天然食品成分(如糖类、蛋白质、多酚、氨基酸等)对淀粉的物理改性修饰作用研究。氨基酸作为蛋白质的基本组成单元,是一种极性小分子物质,易与淀粉发生物理相互作用从而改变其理化性质。已有研究表明氨基酸与淀粉之间存在静电相互作用,可显著影响淀粉的加工和储藏性能。采用合适的氨基酸作为添加剂,可达到改善淀粉类食品品质的目的[3,4]。
氨基酸在水溶液中以偶极离子的形式存在,即一个氨基酸中同时包含能给出质子的 NH3+和接受质子的 COO-。根据氨基和羧基的相对数量,氨基酸通常分为酸性、碱性和中性氨基酸三大类,其中酸碱性氨基酸也被称为带电氨基酸。已有研究表明带电氨基酸显著提高淀粉糊化相变温度、并抑制淀粉回生,这些现象归因于淀粉分子和氨基酸分子间的静电相互作用[5-8]。在氨基酸/淀粉共混体系中,不同比例的氨基酸使体系呈不同的酸碱性,pH值对淀粉结构及性质具有显著影响。同时氨基酸的比例也会影响其与淀粉分子、水分子之间的非共价相互作用(静电相互作用、氢键相互作用)强度,进而影响淀粉的相变行为。然而,现有研究大多集中于单一添加量的氨基酸对淀粉加工性质的影响,相关讨论主要基于氨基酸的电荷性质,针对不同氨基酸和添加量对淀粉结构形貌和相变行为机制影响的报道较少。
本文以玉米淀粉为研究对象,选用三种具有代表性的氨基酸-中性甘氨酸(Gly)、碱性赖氨酸(Lys)和酸性谷氨酸(Glu)作为添加剂,系统研究了氨基酸种类及氨基酸添加量(0、3%、6%、10%、15%、20%)对淀粉的聚集态结构形貌及其热致相变行为的影响规律,为功能性淀粉类食品的开发及生产提供理论参考。
1 材料与方法
1.1 材料与试剂
普通玉米淀粉,澳大利亚Penford公司;甘氨酸、赖氨酸和谷氨酸,北京太阳生物科技有限公司。
1.2 仪器与设备
FE20数显pH计,梅特勒托利多有限公司;EV010扫描电子显微镜,德国ZEISS;BHS-2型偏光显微镜,日本Olymplus公司;D8 ADVANCE型X射线衍射仪,德国Bruker公司;IS50 FT-IR Nicolet傅立叶转换红外光谱仪,美国Thermo Fisher公司;DSC-8000差示扫描量热仪,美国Perkin-Elmer公司;Micro Visco-Amylo-Graph布拉班德黏度仪,德国Brabender公司。
1.3 实验方法
1.3.1 样品制备
分别将0.6 g、1.2 g、2.0 g、3.0 g和4.0 g氨基酸加入50 mL的蒸馏水中,充分搅拌使氨基酸溶解后加入20.0 g玉米淀粉,在30 ℃条件下磁力搅拌90 min,转速为800 r/min,使氨基酸与淀粉充分作用后转移至玻璃培养皿中。随后在40 ℃的对流烘箱中干燥48 h后研磨得到粉末样品。在相同条件下制备不含氨基酸的淀粉样品作为对照。
1.3.2 pH值测定
参照GB/T 10468-1989,用pH计在室温下直接测定氨基酸和淀粉共混乳液的pH值。
1.3.3 扫描电子显微镜观察
将样品置于高真空条件下,用离子溅射镀膜仪进行喷金镀膜,用扫描电镜进行观察并拍照,加速电压为10 kV。
1.3.4 热台偏光显微镜观察
称取一定量的氨基酸淀粉混合样品,加入少量蒸馏水搅拌均匀制成乳液。将适量乳液置于载玻片上并用专用胶密封,放入热台中加热;起始温度为30 ℃,升温速率为2 ℃/min,加热至偏光十字完全消失。加热过程中,每隔1 ℃交替拍摄淀粉颗粒在正常光和偏振光下的图像,在线观察淀粉颗粒的形态和偏光十字变化。拍摄像素设置为1024×768,放大倍数为10×50,曝光时间控制在0.01 s内。
1.3.5 X射线衍射测定
采用 X射线衍射仪探究氨基酸对淀粉晶体的影响,特征射线铜靶,管压和电流分别为40 kV和40 mA,扫描范围为4°~40°,扫描速度为2°/min,步长为0.02°。参照 Amparo Lopez Rubio等[9]的方法,采用MDI Jade 6.0软件计算淀粉样品的相对结晶度。
1.3.6 红外光谱分析
取1.3.1中的混合样品配置成水分含量为70%的乳液,置于95 ℃水浴锅中加热40 min后冷冻干燥。取适量干燥样品与KBr按照1:100的比例研磨,压片后置于红外光谱仪上测试。测试条件为:扫描波数范围为4000~400 cm-1,分辨率为2 cm-1,扫描次数为64次。用OMNIC 8.2软件对红外图谱进行基线校正、平滑以及自动去卷积处理,去卷积参数选择半峰宽为36.2 cm-1,增强因子为3.0。
1.3.7 膨胀度测定
本研究中淀粉膨胀度的测量参考 Pan等[10]的方法。测量过程主要包括以下程序:(1)通过偏光显微镜获得淀粉颗粒在加热过程中不同温度下的颗粒图像(方法同 1.3.4);(2)将淀粉颗粒图像导入计算机数据库并通过Canny边缘检测算法精准识别,得到淀粉颗粒边缘信息;(3)通过淀粉形态智能分割算法分割已识别的颗粒图像,并测量所有颗粒的像素(面积)变化,得到颗粒面积随温度变化的规律。通过公式计算得到淀粉的膨胀度(SC),计算公式如下:
式中:
A0、Ai——起始时刻、特定时间的淀粉颗粒在对应显微图中的像素(面积)。
以普通玉米淀粉为例,淀粉膨胀度测量原理如图1所示。在滤除背景的冗余信息后,从显微图像中很好地提取出所有淀粉颗粒的全面轮廓并以白色像素的形式呈现(图1a);识别并提取颗粒程序完成后,图像中保留了两种像素:淀粉颗粒的白色像素和背景的黑色像素,分别以1和0标记这两种像素。根据加热过程中像素(面积)的变化,得出了淀粉膨胀度随温度的变化(图1b)。
1.3.8 差示扫描量热仪(DSC)测试
准确称取1.3.1中制备的样品6.5 mg(干基),置于30 μL的铝盘(PE No.B0169320)中,用10 μL的移液枪向铝盘中注入约 16 μL去离子水并密封。在DSC测试之前,将制好的样品在室温下平衡24 h使其达到均匀状态。将待测样品和参比盘分别放入DSC样品室左侧和右侧的热皿板上,设置扫描温度范围为30~120 ℃,升温速率为5 ℃/min进行测试。
1.3.9 布拉班德粘度测试
准确称取一定量1.3.1中制得的样品(干基),加入蒸馏水配置浓度为 6%的淀粉乳,搅拌均匀后倒入测量容器中。测试盒选择350 cmg,转子速度为250 r/min,以7.5 ℃/min的升温速率从30 ℃升温至95 ℃,保温5 min,随后以同样的速率将温度降至50 ℃,保温5 min。
1.3.10 分子动力学模拟
采用GROMACS 5.1.4进行了分子动力学模拟。以 26个呈规则螺旋结构的葡萄糖残基片段代表直链淀粉分子,三种氨基酸(谷氨酸、赖氨酸、甘氨酸)分子模型的拓扑文件由LigParGen服务器在OPLSAA力场下生成,同时选用在OPLSAA力场下兼容性更好的TIP4P四点水模型[11,12]。淀粉分子、水分子及三种氨基酸分子结构如图2所示。
采用周期边界条件并且以淀粉片段为中心建立一个边长为5.73 nm的正方体盒子,随后随机插入0、40和80个氨基酸分子,分别表示不同添加量的氨基酸体系,使用TIP4P水模型对每个系统进行溶剂化处理。体系进行充分的能量极小化后,在323.15 K,以及1 bar的大气压下,采用蛙跳算法以2 fs的步长进行50 ns的模拟。采用Verlet算法对所有的键长进行限制,PME方法则用于静电相互作用的计算,静电力和范德华力均在1 nm处截断[11]。
1.3.11 数据处理
采用 IBM SPSS 21.0统计分析软件对数据进行Turkey检验,显著性水平设为p<0.05;采用Origin 8.0绘图。
2 结果与分析
2.1 氨基酸种类和添加量对共混体系pH值的影响
表1为氨基酸种类和添加量对淀粉/氨基酸体系pH值的影响。由表可知,对照组(无添加氨基酸样品)的pH值为7.13。氨基酸在溶液中的电离会改变体系pH值,随着中性甘氨酸添加量的增大,共混体系pH值有所降低,呈现弱酸性;而随着赖氨酸和谷氨酸添加量的增大,体系的碱性和酸性明显逐渐增强。当氨基酸添加量为20%时,赖氨酸和谷氨酸共混体系的pH值分别变为9.72和3.27,此时体系分别呈现较强碱性和酸性。

表1 氨基酸种类和添加量对淀粉/氨基酸体系pH值的影响Table 1 Effects of amino acid type and content on pH value of starch/amino acid system
氨基酸溶液酸碱性与氨基和羧基基团对质子传递作用密切相关[13]。酸性的谷氨酸分子和碱性的赖氨酸分子分别比中性甘氨酸分子多一个羧基和氨基,使三种氨基酸体系的pH值呈现明显差异。氨基酸在溶液中的质子传递形式及甘氨酸、赖氨酸、谷氨酸的分子结构式如图3所示。甘氨酸溶液呈弱酸性,这主要是由于氨基正离子的质子解离能力大于羧基负离子接受质子的能力,即 Ka(NH3+)>Kb(COO-)。在谷氨酸溶液中,其中一个未电离的羧基给出质子的能力大于另一个已解离的羧基负离子接受质子的能力,因此溶液显酸性。同理,对于赖氨酸分子,其两性离子中未质子化的氨基从水溶液中得到质子的能力大于另一个已质子化的氨基正离给出质子的能力,因此溶液显碱性。
2.2 氨基酸种类和添加量对淀粉颗粒形貌的影响
氨基酸的种类及其添加量对淀粉颗粒形貌具有不同的影响。如图4所示,玉米原淀粉颗粒呈大小不一的圆形或多角形,粒径位于5~20 μm之间。少量淀粉颗粒表面分布密集的小孔,这些孔通常在淀粉合成过程中产生[14]。淀粉的颗粒形貌会随着氨基酸分子的种类及浓度的不同呈现不同的变化,而导致其变化的因素可能主要是氨基酸溶液的pH值变化引起的。
从结果中可以看出,不同浓度添加量(0~20%)的中性甘氨酸对淀粉颗粒表面形貌均无显著影响,这主要是由于甘氨酸添加量对体系pH值影响不大,即使其添加量提高至20%,体系仍呈弱酸性,有研究表明,轻微的酸性处理并不会对颗粒结构的整体稳定性造成明显影响[15]。而酸性的谷氨酸和碱性的赖氨酸分子则随着添加量的变化,对淀粉颗粒及形貌呈现破坏作用,当其添加量大于10%后,淀粉颗粒表面逐渐变粗糙,孔径增大,且谷氨酸体系中颗粒表面出现明显凹陷。已有研究表明,淀粉颗粒经较强的酸碱性溶液处理后,其无定型结构会发生降解,从而导致颗粒表面孔隙增多、孔径增大[16-18]。在本研究中,高添加量(>10%)的非中性氨基酸使淀粉体系的酸碱性发生明显改变,颗粒无定型结构遭到不同程度破坏,颗粒形貌发生较明显变化。Ji等[19]在研究赖氨酸和天冬氨酸对玉米淀粉消化性质的影响时,同样发现玉米淀粉颗粒表面变粗糙。
2.3 氨基酸种类和添加量对淀粉结晶结构的影响
偏光显微镜和X射线衍射仪是用于分析淀粉结晶结构的常用设备。淀粉颗粒独特的球晶结构在偏振光的照射下会呈现出清晰明亮的偏光十字[20]。X射线衍射仪则可用于表征淀粉结晶结构的类型和相对结晶度。图5显示的是在室温条件下(30 ℃)经不同浓度甘氨酸、赖氨酸和谷氨酸处理后淀粉偏光十字的对比图片。玉米原淀粉颗粒呈现清晰明亮的偏光十字。经不同浓度的三种氨基酸处理后,淀粉颗粒的偏光十字没有明显变化,表明常温下氨基酸处理的淀粉仍然保留完整的球晶结构,这与Ji等[19]的研究结果一致。同时,X射线衍射仪分析结果也表明氨基酸添加量及种类对淀粉结晶结构无明显影响。如图6所示,原淀粉在 15°、17°、18°和 23°处分别有一个强的衍射特征峰,是典型的A型结晶衍射图谱。经不同浓度的三种氨基酸处理后,玉米淀粉的A型特征衍射峰没有明显变化,说明氨基酸不改变淀粉的晶体结构类型。
然而随着氨基酸浓度的变化,不同种类处理淀粉的相对结晶度会随之发生变化。如表2所示,随着碱性赖氨酸和酸性谷氨酸浓度的增大,处理后的淀粉相对结晶度升高,当赖氨酸和谷氨酸添加浓度达到20%时,相对结晶度分别升高了1.00%和1.96%,而不同浓度的中性甘氨酸对淀粉结晶度影响不大。显然,非中性氨基酸体系中淀粉相对结晶度的升高可能是由共混体系酸碱性的增强引起的。在酸碱处理中,淀粉无定型区会优先水解从而导致其结晶度升高[21,22]。Chen等[6]研究了氨基酸对土豆淀粉理化性的影响,发现添加10%的赖氨酸使淀粉的相对结晶度提高了1.69%,表明氨基酸对淀粉结晶结构的影响还与淀粉的结晶类型有关,土豆淀粉的B型结晶结构比玉米淀粉的A型结晶结构更为松散,使氨基酸小分子更容易进入晶体结构中,因此对淀粉相对结晶度的影响更明显。
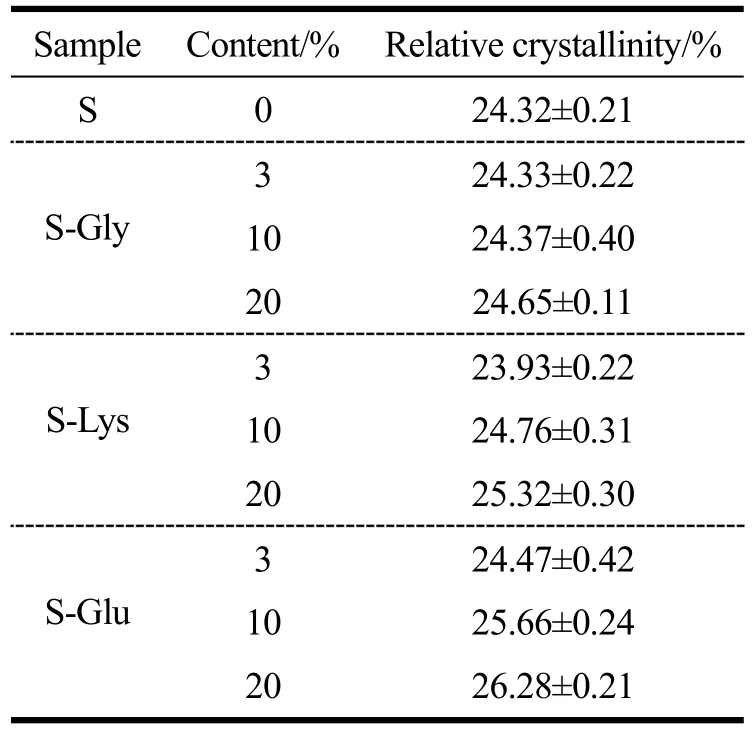
表2 经不同浓度甘氨酸、赖氨酸和谷氨酸处理后淀粉样品的相对结晶度Table 2 Relative crystallinity of starch samples treated by glycine, lysine and glutamic acid with different contents
2.4 氨基酸种类和添加量对淀粉短程有序结构的影响
为了进一步探究氨基酸与淀粉分子间的相互作用和氨基酸种类及其添加量对淀粉短程有序结构的影响,采用傅立叶红外光谱仪对氨基酸与淀粉共混样品进行测定。如图7所示,淀粉在3340 cm-1附近有一个强且宽的吸收峰,该峰由缔合羟基O-H键的伸缩振动产生,2930 cm-1、1646 cm-1、1340 cm-1、1013 cm-1附近的峰分别为 C-H的伸缩振动、O-H的弯曲振动、C-OH的弯曲振动和C-O的伸缩振动[23,24]。三种氨基酸均使3340 cm-1处的吸收峰向低波数方向发生红移,表明氨基酸与淀粉分子间存在氢键相互作用,且谷氨酸和赖氨酸与淀粉分子间的氢键相互作用比甘氨酸更强,这是因为甘氨酸分子结构中可发生氢键作用的极性基团数量较少。随着三种氨基酸浓度的增大,3340 cm-1处的吸收峰偏移量逐渐增大,表明体系中氢键的密度和强度逐渐增大,氨基酸分子与淀粉分子之间的氢键相互作用强度与氨基酸浓度呈正相关。而经过三种氨基酸处理后的淀粉均未出现新的吸收峰,说明淀粉和氨基酸混合未衍生化,二者主要发生非共价键相互作用。
1045 cm-1与1022 cm-1处的红外特征吸收峰分别与淀粉的有序结构和无定型结构有关,1045 cm-1与1022 cm-1处峰强的比值(R1045/1022)已被广泛用于评估淀粉短程结构有序性,比值越大,表明结构有序性越高[25,26]。对 1200~800 cm-1范围的波谱进行去卷积处理,相应图谱如图8所示,淀粉的R1045/1022值列于表3中。研究结果表明,氨基酸种类和添加量对淀粉短程结构有序性的影响大小与氨基酸、淀粉分子间的氢键相互作用程度相关:氢键相互作用越强,淀粉短程结构有序性越低。三种氨基酸均使淀粉的R1045/1022值降低,且赖氨酸和谷氨酸影响大于甘氨酸,随着甘氨酸、赖氨酸和谷氨酸添加量由0增大至20%,淀粉的R1045/1022由0.87分别降低至0.69、0.62和0.59。Wan等[5]的研究发现谷氨酸、赖氨酸和甘氨酸同样能降低大米淀粉的短程结构有序性,且三种氨基酸对淀粉短程结构有序性的影响大小与本文一致。氨基酸与淀粉分子间的氢键相互作用可能是导致淀粉短程结构有序性降低的主要原因,氨基酸分子通过占据淀粉链上的氢键作用位点来抑制淀粉分子内氢键形成,进而导致淀粉短程结构有序性降低。

表3 不同浓度甘氨酸、赖氨酸和谷氨酸对淀粉R1045/1022值的影响Table 3 Effects of glycine, lysine and glutamic acid with different contents on the R1045/1022 values of starch
2.5 氨基酸种类和添加量对淀粉膨胀度的影响
氨基酸种类和添加量也会对淀粉糊化过程中的膨胀度产生影响。如图9所示,淀粉的膨胀分为两个阶段:缓慢膨胀阶段(30~60 ℃)和快速膨胀阶段(60~70 ℃)。第一阶段主要是淀粉无定型区的可逆吸水膨胀,第二阶段主要是晶体结构的热无序化过程。三种氨基酸均能抑制淀粉膨胀,谷氨酸的抑制作用最大。随着三种氨基酸添加量提高,淀粉膨胀度表现出先减小后增大的规律,在10%处达到最低。70 ℃时,含量为10%的甘氨酸、赖氨酸和谷氨酸体系中,淀粉膨胀度分别降低了 21.13%、21.48%、25.95%。氨基酸对淀粉膨胀度的影响与氨基酸改变体系中水分子的分布及氨基酸与淀粉间相互作用相关。
淀粉颗粒水合和膨胀的能力取决于淀粉分子与水分子间的氢键相互作用强度[27,28]。在水溶液中,水分子快速进入淀粉颗粒内部与其形成氢键,导致淀粉颗粒结构被破坏。添加氨基酸后,氨基酸分子由于体积较大,优先与水分子作用,导致淀粉溶剂化所需水分子数量减少[29],从而抑制淀粉颗粒的水合膨胀。这与蔗糖分子抑制淀粉膨胀度的作用机制类似[30]。随着氨基酸浓度提高,与氨基酸水合的水分子数量不断增加,抑制膨胀作用越来越显著。当氨基酸含量为10%时,淀粉分子与水分子相互作用最弱,膨胀度最低。增加氨基酸浓度增大了其与淀粉分子作用的可能性,也会对淀粉分子内氢键产生破坏作用,从而会导致淀粉的膨胀度的升高。除氢键相互作用外,当谷氨酸和赖氨酸的添加量大于10%时,溶液中较强的酸性或碱性使淀粉无定型区结构不稳定,也会加速淀粉分子与水分子的相互作用。值得注意的是,中性甘氨酸的添加量大于10%后,淀粉的膨胀度同样表现为升高,表明氨基酸的极性基团与淀粉分子、水分子间的非共价相互作用是影响淀粉溶胀的主要原因,而氨基酸的酸碱性是影响淀粉溶胀的次要因素。
2.6 氨基酸种类和添加量对淀粉糊化相变的影响
氨基酸的种类和添加量对淀粉糊化相变温度及焓值的影响作用不同。如图10所示,玉米原淀粉在67 ℃附近有一个较宽的吸热峰,添加氨基酸后,淀粉的吸热峰均向高温区偏移,表明三种氨基酸均能抑制糊化相变进程,且谷氨酸和赖氨酸影响更显著。随着氨基酸浓度的增大,糊化相变温度表现为先增大后减小的趋势,在10%处达到最大值(表4)。经10%的甘氨酸、赖氨酸和谷氨酸处理后,淀粉峰值温度分别提高了3.71 ℃、6.00 ℃和5.58 ℃。与本结果稍有不同的是,Chen等[8]研究发现谷氨酸和赖氨酸能显著提高土豆淀粉的起始糊化温度,而对峰值糊化温度和终止糊化温度无显著影响,这可能是由氨基酸浓度和淀粉结构差异导致的。本研究中氨基酸浓度更大,而且玉米淀粉的晶体结构更稳定。起始糊化温度表示最弱微晶的熔融温度,土豆淀粉的晶胞能容纳更多水分子,最弱微晶破坏后,低比例的氨基酸分子抑制水分子对晶体结构的破坏作用不明显,因此淀粉的峰值糊化温度和终止糊化温度无明显变化。玉米淀粉的晶胞较致密,其双螺旋结构在糊化过程中逐渐展开,起始糊化温度的滞后会导致峰值糊化温度和终止糊化温度同步滞后。
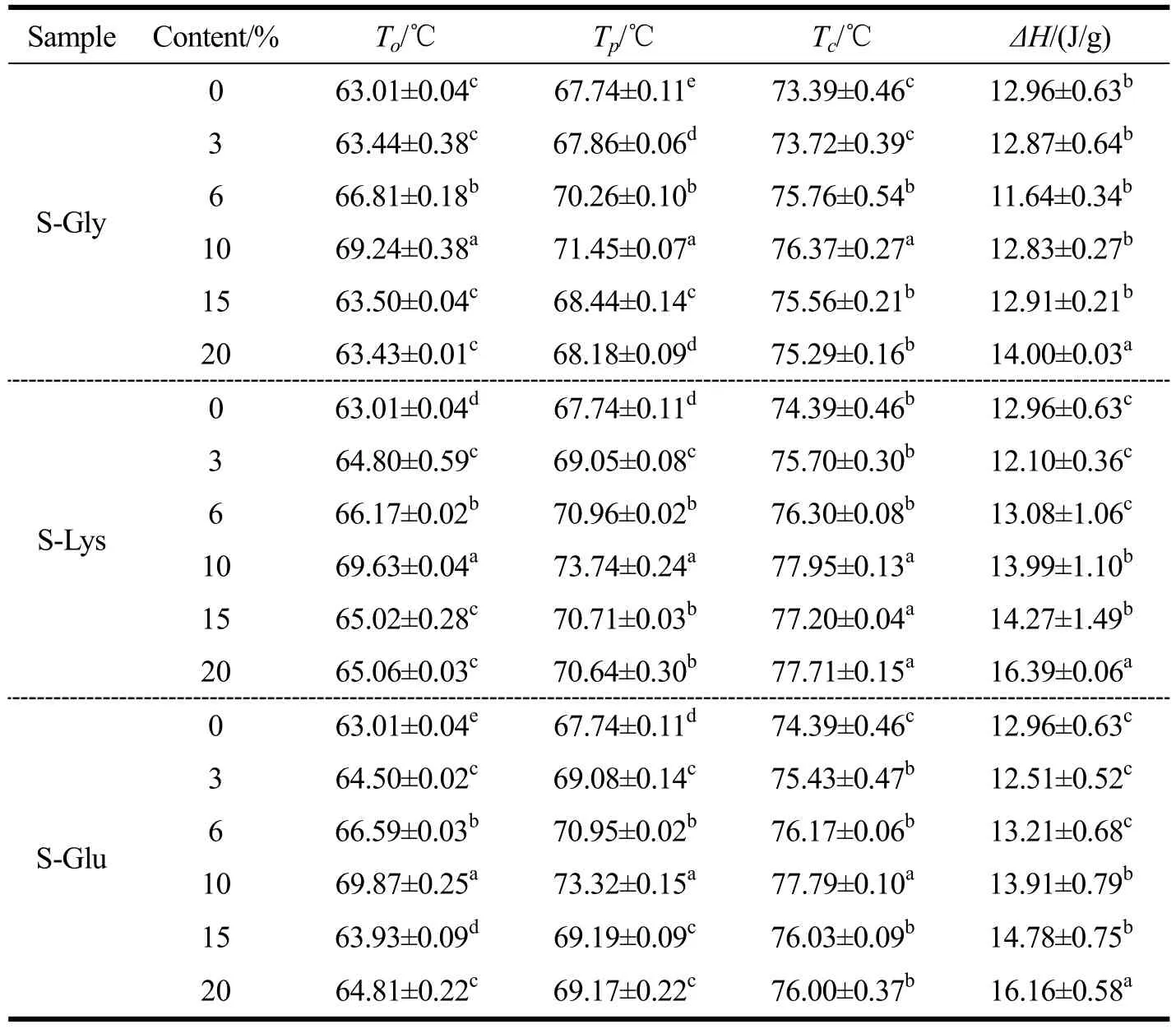
表4 不同浓度甘氨酸、赖氨酸和谷氨酸对淀粉糊化相变参数的影响Table 4 Effects of glycine, lysine and glutamic acid with different contents on the gelatinization characteristics of starch
淀粉葡萄糖残基之间的氢键相互作用是维持其螺旋结构的关键,相变是淀粉分子内氢键被破坏的动态演变过程[31,32]。氨基酸偶极离子和中性盐离子性质相似,与水分子之间的静电相互作用会改变体系中水分子的存在状态,进而间接影响淀粉的相变行为[33]。氨基酸的水合作用抑制了淀粉颗粒膨胀,使淀粉糊化滞后,因此表现为更高的糊化温度。然而高添加量(>10%)溶液中氨基酸分子与淀粉分子之间的氢键相互作用导致淀粉结构变弱,使糊化温度有所降低,与膨胀度结果一致。糊化焓值与淀粉晶体的熔化和双螺旋的破坏有关[34,35]。高添加量(>10%)的氨基酸使淀粉糊化焓值显著提高,这可能是由于高比例的氨基酸分子与淀粉分子之间形成较强的氢键网络,需要更高的能量使淀粉糊化。
2.7 氨基酸种类和添加量对淀粉糊粘度的影响
经不同浓度甘氨酸、赖氨酸和谷氨酸处理的淀粉样品的布拉班德粘度曲线如图11所示,特征粘度参数分别列于表5、表6和表7中。除3%的甘氨酸无显著影响外,其他氨基酸均显著提高淀粉的起糊温度,降低淀粉的特征粘度。随着三种氨基酸添加量的增大,淀粉起糊温度(PT)表现为先增大后减小的趋势,而峰值粘度(PV)、谷值粘度(TV)和终值粘度(FV)呈现出单调递减的趋势。玉米原淀粉的起糊温度为71.81 ℃,添加10%的甘氨酸、赖氨酸和谷氨酸能最大限度抑制淀粉糊化,使起糊温度分别提高了6.02 ℃、6.92 ℃和10.06 ℃,而峰值粘度分别降低了37.95 BU、56.78 BU、81.67 BU。三种氨基酸对淀粉糊粘度性质的影响大小为:谷氨酸>赖氨酸>甘氨酸。Galkowska等[3]的研究发现相同结果,氨基酸与水分子、淀粉分子间的物理相互作用可能是影响淀粉糊粘度性质的主要原因。
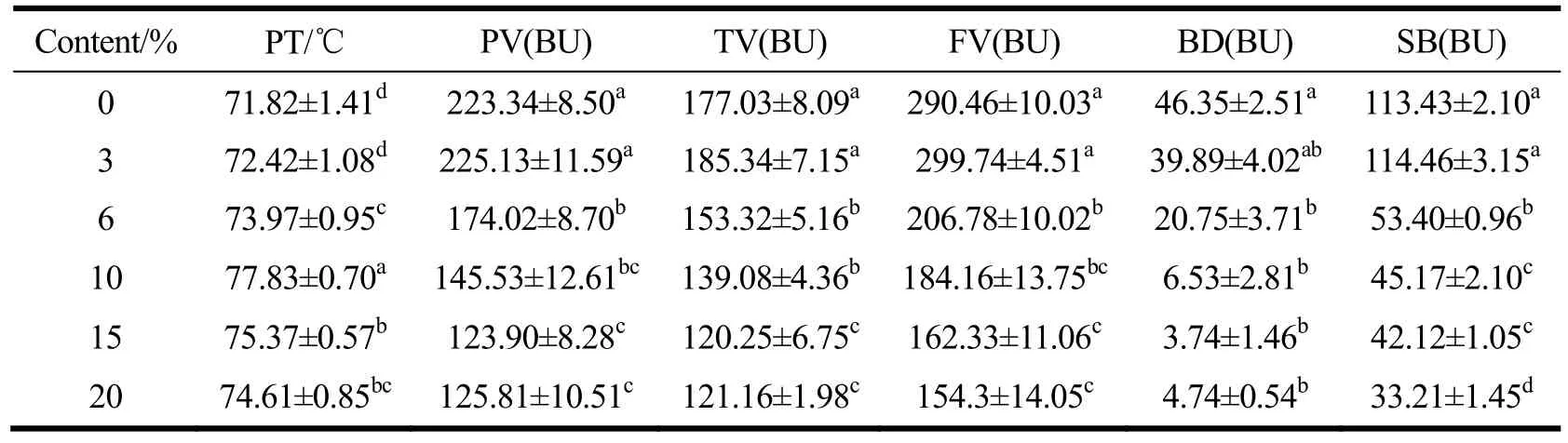
表5 不同浓度甘氨酸对淀粉布拉班德粘度参数的影响Table 5 Effects of glycine acid with different contents on the Brabender viscosity characters of starch

表6 不同浓度赖氨酸对淀粉布拉班德粘度参数的影响Table 6 Effects of lysine acid with different contents on the Brabender viscosity characters of starch
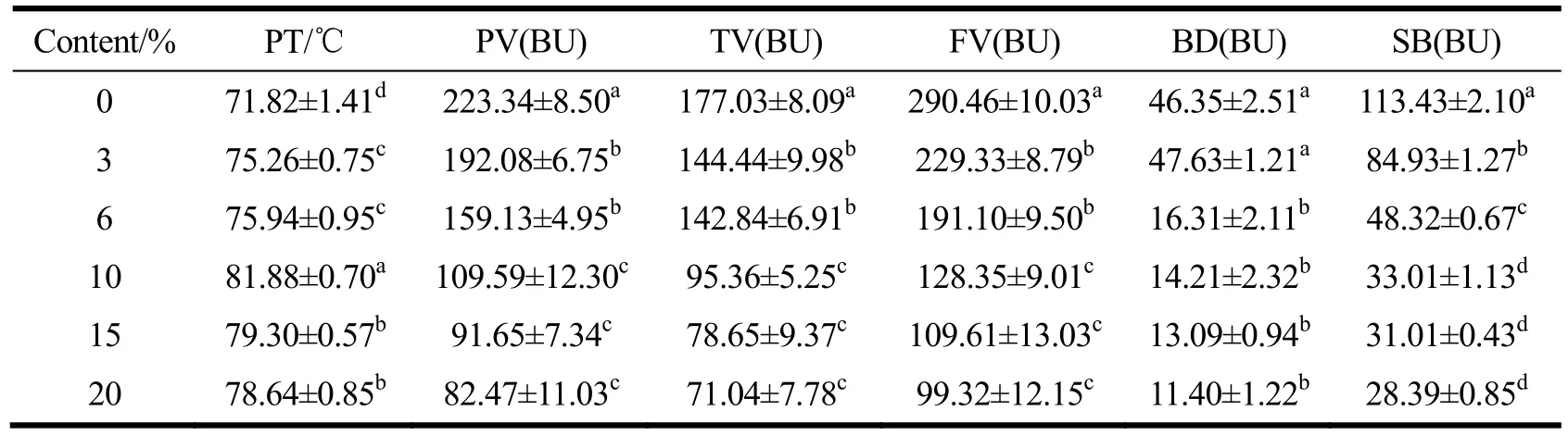
表7 不同浓度谷氨酸对淀粉布拉班德粘度参数的影响Table 7 Effects of glutamic acid with different contents on the Brabender viscosity characters of starch
在本文中,由于氨基酸浓度的变化导致淀粉体系的酸碱性发生改变。因此,除物理相互作用之外,氨基酸的酸碱性也会影响淀粉的粘度。氨基酸对粘度的影响可能主要是由以下两方面引起的:一方面,氨基酸分子与水分子的作用减少了游离水分子数目,使部分淀粉颗粒保持相对稳定,淀粉颗粒之间的表面相互作用较弱,表现为较低的粘度[36,37];另一方面,酸性谷氨酸在水中电离的 H+会使分散在体系中的直链淀粉分子水解成更短的分子链[38],而碱性赖氨酸则使直链淀粉羟基去质子化,导致淀粉链间排斥力增大。淀粉链长的降低及链间斥力的增大均不利于其缠绕聚集,因而淀粉糊粘度更低。经氨基酸处理后,淀粉的崩解值(BD)和回生值(SB)均一定程度降低,表明氨基酸提高了淀粉的热糊稳定性并抑制短期回生。短期回生主要是直链淀粉链通过氢键重新缔合形成有序结构的过程[39]。在较强酸碱性的环境中,淀粉链的降解或淀粉链之间的排斥作用均抑制淀粉链的聚集重排。另一方面,糊化后的淀粉羟基的暴露促进氨基酸分子与之发生氢键作用,阻碍了淀粉链缔合重排,导致回生粘度降低。
2.8 分子动力学模拟
为了从分子水平分析氨基酸种类和添加量影响淀粉分子结构及相变行为的分子作用机理,采用分子动力学模拟分析了淀粉分子链在不同浓度甘氨酸、赖氨酸及谷氨酸水溶液体系中的构象稳定性及氨基酸分子、水分子、淀粉分子之间的相互作用关系,采用均方根偏差、螺旋二面角分布、淀粉分子与水分子的径向分布函数及溶液体系氢键行为和相互作用能等方法进行统计分析,为氨基酸影响淀粉结构与性质的分子间作用机制提供理论解释。
2.8.1 螺旋二面角分析
淀粉是由葡萄糖分子通过α-1,4糖苷键聚合而成的高分子聚合物。糊化过程中淀粉分子链的螺旋结构逐渐伸展为柔性的随机链段,处于α-1,4糖苷键位置的两个二面角 φ (O5-C1-O4′-C4′)和 ψ (C1-O4′-C4′-C3′)角度会随着淀粉结构变化而变化,研究二面角的分布可以更加清楚地反映糖苷键的变化情况,进而分析淀粉分子螺旋结构在溶液中的退化程度。
图12是50 ns内不同浓度的甘氨酸、赖氨酸和谷氨酸溶液体系中二面角随时间的分布情况(以 10 ns为一个时间单位,不同时间单位的二面角分布用不同颜色表示)。如图所示,在模拟的前10 ns内水溶液中淀粉的二面角(φ,ψ)由(105°,115°)迅速减小至(95°,105°),在 20~50 ns期间,每一个时间单位的二面角分布范围几乎相同,表明淀粉构象在前 10 ns发生剧烈转变,螺旋结构降解速度快。相比于水溶液,加入三种氨基酸后淀粉链二面角的变化速度均放缓(角度逐渐向低角度范围偏移),而谷氨酸和赖氨酸抑制二面角变化的作用大于甘氨酸。随着三种氨基酸添加量的提高,二面角的变化速度均逐渐变慢,说明在一定浓度范围内,高浓度的氨基酸可更好地维持溶液体系中淀粉分子的螺旋结构。氨基酸抑制淀粉螺旋结构的降解行为在宏观上表现为抑制淀粉糊化,与DSC实验结果一致。
2.8.2 径向分布函数
径向分布函数(Radial Distribution Function,RDF)用于描述其他目标粒子对应于参考点距离变化的函数。其定义为以参考粒子为圆心,半径为r的范围内出现另外一个粒子的概率密度与该粒子随机分布的概率密度的比值。通过考察体系中目标粒子与参考粒子之间的相对分布情况,可以反映粒子之间的相互作用。
如图13所示,水溶液及不同氨基酸溶液体系中淀粉径向分布函数的特征峰均出现在 0.27 nm,表明淀粉分子与水分子间存在较强的氢键相互作用,淀粉分子被水分子溶剂化程度高[40]。随着氨基酸种类和浓度的变化,该特征峰的强度有所不同。三种氨基酸溶液体系中特征峰的峰值均比水溶液体系的小,表明氨基酸分子抑制了淀粉分子和水分子的相互作用,减小了水分子的溶剂化作用。当添加相同量的氨基酸分子时,0.27 nm处特征峰的峰值按照甘氨酸、赖氨酸、谷氨酸的顺序依次减小,谷氨酸对淀粉周围水分子的分布影响最大,而甘氨酸影响最小。随着氨基酸浓度增大,峰强逐渐变弱,表明在一定浓度范围内,氨基酸分子数量越多,与之发生作用水分子数量就越多。相应与淀粉分子发生作用的水分子就越少。水分子是淀粉加工体系中有效增塑剂[41],抑制水分子与淀粉分子相互作用将有效抑制淀粉相变的发生。
2.8.3 氢键相互作用
淀粉分子螺旋结构的稳定性主要依赖于分子内氢键[42]。分子内氢键数目可用于衡量淀粉螺旋结构稳定性,氢键数目越多,螺旋结构越稳定。为了考察不同浓度甘氨酸、赖氨酸和谷氨酸溶液体系中淀粉分子内氢键数目变化及氨基酸与淀粉、水分子之间的氢键相互作用情况,表8统计和分析了50 ns内不同体系中淀粉分子内及各组分分子之间的氢键数目及淀粉-氨基酸、淀粉-水分子的相互作用能(均以50 ns内的平均值计)。随着氨基酸分子数量增多,淀粉分子内氢键数目和淀粉-氨基酸分子间的氢键数目略微增大,但是淀粉-水分子间的氢键数目明显减小,同时氨基酸-水分子间的氢键数目明显增大。淀粉-水分子和淀粉-氨基酸分子的相互作用能结果与氢键数目的统计结果一致,即分子间氢键数目越多,相互作用能越大。以上结果表明,氨基酸分子和水分子在与淀粉分子发生氢键相互作用时存在竞争关系,但是由淀粉-水分子间氢键数目远大于淀粉-氨基酸分子间氢键数目可知,淀粉溶剂化效应主要由水分子主导,而大部分氨基酸分子与水分子作用减少了淀粉分子周围水分子的分布密度,导致与淀粉作用的水分子数量减少,进而影响淀粉的宏观性质。

表8 不同浓度甘氨酸、赖氨酸和谷氨酸溶液体系中各组分分子之间的氢键数目及相互作用能Table 8 Hydrogen bond number and Interactional energy between different molecules in glycine, lysine and glutamic acid solutions with different contents
3 结论
本文系统研究了甘氨酸、赖氨酸及谷氨酸在不同含量条件下(0、3%、6%、10%、15%、20%)对玉米淀粉结构形态及相变行为的影响。研究结果表明,氨基酸种类和添加量均会影响淀粉的结构与性质,三种氨基酸影响作用大小呈现以下趋势:谷氨酸>赖氨酸>甘氨酸,且当氨基酸浓度为 10%左右,影响最为显著。甘氨酸对淀粉的结构无显著影响,但是酸性的谷氨酸和碱性的赖氨酸使淀粉颗粒表面变粗糙,并促使淀粉相对结晶度提高,这主要是由于非中性氨基酸体系中较强的酸碱性对淀粉无定型结构产生了破坏作用。三种氨基酸均会抑制淀粉糊化及回生,这主要是氨基酸与水分子、淀粉分子之间的氢键相互作用导致。氨基酸分子通过与水分子作用减少水分子对淀粉分子的塑化作用,使糊化行为滞后,糊化后淀粉分子链的展开有利于氨基酸分子与之形成氢键,阻碍了淀粉分子链重排,导致回生程度降低。
