冰片促灯盏乙素透体外血-视网膜内屏障的作用研究*
2022-03-03李志林郑祖杰黎晓冬曾洁萍
李志林,郑祖杰,黎晓冬,曾洁萍
(1.成都中医药大学 成都 610075;2.成都中医药大学附属医院 成都 610075)
青光眼是以视网膜神经节细胞(Retinal ganglion cells,RGCs)及其轴突进行性丢失为病理基础的神经变性性疾病,临床上青光眼的主要治疗措施是降低眼压,但临床发现某些眼压得到有效控制的青光眼患者,仍然存在视功能继续受损的情况,单纯控制眼压无法遏止RGCs凋亡[1]。故如何在眼压控制后继续对视神经保护成为国内外研究热点,在既往研究中已有采用各种中药对视神经保护的研究,诸如枸杞多糖、雷公藤、白藜芦醇等[2]。也有研究证实活血通络中药如灯盏细辛提取物对急性眼内压升高的大鼠RGCs具有确切的保护作用[3-4]。同时临床上研究表明灯盏花素注射液对于部分青光眼滤过术后患者的视野有部分改善作用[5],然而口服制剂(灯盏花素片)临床却未达到预期效果,这可能是因为口服很难透过血眼屏障而在眼内达到有效浓度,注射给药方式又难以长期持续给药从而临床疗效不理想有关。
口服药品经吸收后通过血液到达全身,想要进入视网膜内,需要首选通过血-视网膜屏障。既往研究发现冰片作为中医外科的常用药,可经眼、皮肤等部位吸收[6]。张瑞涛等[7]研究表明,经鼻腔将冰片给药可明显提高鼻腔黏膜血管和脑血管的通透性,在一定浓度范围内,伊文思蓝(Evans blue,EB)的通透性与冰片使用浓度呈线性关系。而血-视网膜屏障由内屏障和外屏障组成:内屏障由视网膜毛细血管内皮细胞及其间的紧密连接构成。因此本研究通过构建内屏障模型观察冰片对药物的促透过作用。
1 HBSS中灯盏乙素含量测定方法学建立
1.1 实验仪器及药物
1.1.1 实验仪器
API4000型HPLC-MS/MS仪(ABSCIEX公司),十万分之一电子分析天平(SHIMADZU公司),H2050R低温高速离心机(湖南湘仪),EKUP-II-150L型超纯水仪(四川宜科),多规格可调移液器(Sartorius);实验药品灯盏乙素(纯度98.54%),批号AF8051821;冰片,批号AF8040412;黄芩苷(纯度99.31%,内标),批号AF9062402,均购自于成都埃法生物科技有限公司。实验用甲醇、甲酸、乙腈均为HPLC级。实验中所用纯水为超纯水。
1.1.2 测定对象
灯盏乙素CAS#:27740-01-8;分子式:C21H18O12;分子量:462.36。黄芩苷CAS#:21967-41-9;分子式:C21H18O11;分子量:446.36
1.2 检测方法
1.2.1 色谱条件
HPLC-MS/MS系统由Aglient公司1260型HPLC仪和AB SCIEX公司API 4000型三重四极杆串联质谱(ESI离子源)组成。选择Agilent ZORBAX C18色谱柱(2.1e100 mm,3.5 µm,批号959793-902),柱温30℃。流动相A为0.1%的甲酸溶液,流动相B为0.1%的乙腈溶液。梯度洗脱(见表1)。
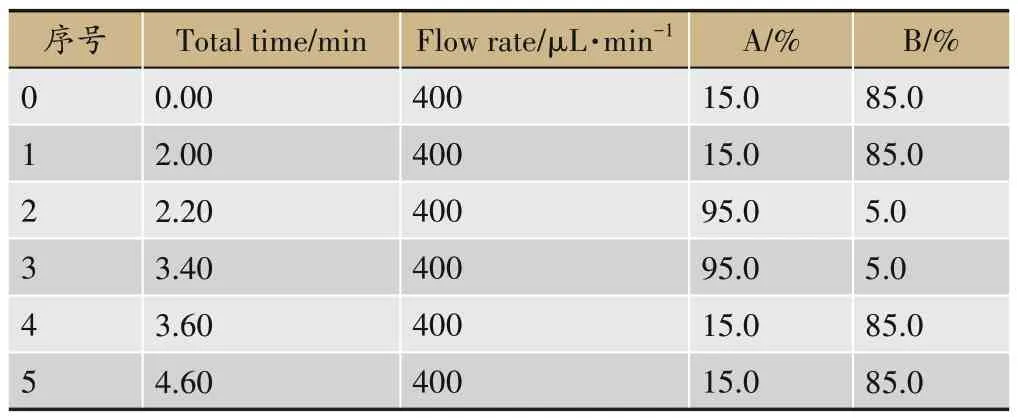
表1 梯度洗脱流动相
1.2.2 质谱条件
以选择性负离子对监测模式(MRM)测定灯盏乙素(m/z 461.3/285.2)的浓度,黄芩苷作内标(m/z 445.1/268.9),质谱参数见表2,灯盏乙素质谱product碎片离子扫描图见图1,黄芩苷质谱product碎片离子扫描图见图2。
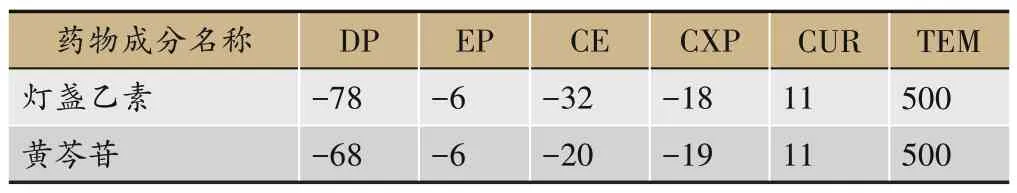
表2 质谱参数

图1 灯盏乙素质谱product碎片离子扫描图(m/z 461.3/285.2)

图2 黄芩苷质谱product碎片离子扫描图(m/z 445.1/268.9)
1.2.3 样本预处理
取待测样本10 µL,加入0.1%甲酸水溶液:0.1%甲酸乙腈溶液=15∶85的溶液90 µL,混匀后,再加入50 µL内标工作液(1000 ng·mL-1的黄芩苷甲醇溶液),混匀后于4℃、12000 r·min-1离心5 min后,取上清液50 µL上样,进样5 µL分析。
1.2.4 数据处理
采用Analyst色谱工作站,自动计算待测成分与内标的峰面积、峰面积比值、标准曲线、测定浓度以及偏差。浓度单位为ng·mL-1,标准曲线加权设置为1/c2。以标准曲线进样后的色谱峰面积比值对应其理论浓度建立标准曲线方程,未知样本进样后得到的色谱峰面积比值代入次标准曲线方程即可反算出其浓度。
1.3 方法学验证
1.3.1 标准曲线
先用天平称取灯盏乙素10.15 mg标准品,相当于灯盏乙素10 mg,用甲醇配制灯盏乙素储备液(100 µg·mL-1),储存条件-35℃冰箱。取储备液,临用前先用流动相即0.1%甲酸水溶液:0.1%甲酸乙腈溶液=15∶85溶液稀释出标准曲线系列工作液STA-STG。基质标准曲线范围为5000-400 ng·mL-1,最低定量限为400 ng·mL-1,标准曲线工作液具体配置见表3,标准曲线见图3。

图3 标准曲线图
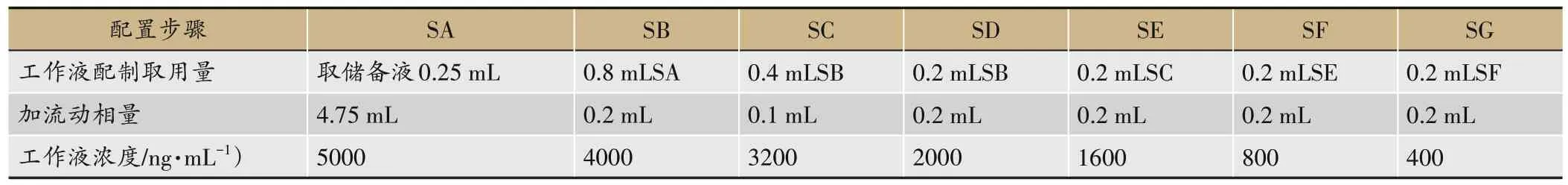
表3 标准曲线工作液配制表
1.3.2 准确度和精密度
用甲醇配制灯盏乙素质控储备液(200 µg·mL-1)并用50%甲醇水溶液稀释出质控工作液HQC、MQC、LQC(含灯盏乙素4000、2000、400 ng·mL-1)。取这3个浓度水平的质控基质样本,经预处理后进样。共测定3个分析批,每批每个浓度各测定6次,计算准确度和精密度。批内精密度CV 0.91%-1.59%,批间精密度CV 3.70%-7.58%,准确度为98.03%-99.87%。
1.3.3 预处理回收率
取HQC、LQC质控基质样品各3份,经预处理挥干后复溶进样。另取空白HBSS基质经预处理后挥干,加入标准工作液复溶,配制成同理论浓度的样品直接进样,比较两组样品的峰面积,计算预处理回收率。灯盏乙素的预处理回收率为97.3-99.5%,内标的预处理回收率为98.7%。
1.3.4 特异性与基质效应
取6个不同来源未混合的空白HBSS基质,经预处理后分别进样检测,考察空白基质对待测物和内标的出峰干扰情况,结果均未发现干扰。灯盏乙素和内标的保留时间为1.5 min,空白基质图见图4,标准曲线图谱见图5,实测样本图见图6。

图4 空白基质图谱(Blank HBSS)

图5 标准曲线图谱(SD sample)

图6 实测样本图谱(Unknown sample)
将6个不同来源的空白HBSS基质经预处理后挥干,加入标准工作液复溶分别配制HQC、LQC两个浓度水平的基质效应考察样本,进样。另配制同理论浓度的纯溶液样本,进样。比较两组样品的峰面积,考察基质效应。每个浓度平行测定3份,计算经内标校正后的基质效应因子,结果各基质的内标归一化基质效应因子分别为0.989-1.003,符合要求。
1.3.5 稳定性
分别考察了储备液和工作液于-30℃保存31天的稳定性(偏差为(-0.60%)-(-0.84%))、储备液和工作液于室温保存24 h的稳定性(偏差为(-3.30%)-(-0.57%))、基质样本室温保存22 h稳定性(偏差为(-1.83%)-(3.53%))、基质样本在-30℃冰箱冷冻保存60天的稳定性(偏差为(-0.75%)-(-4.05%))、基质样本反复冻融5次的稳定性(偏差为(-1.37%)-(5.33%))、处理后的样本重复进样稳定性(偏差为(1.21%)-(2.34%))和在进样室(11℃)保存24 h的稳定性(偏差为(-0.96%)(4.27%)),其结果均符合要求。
1.3.6 其他
我们还考察了仪器的进样携带污染率(Carryover)、样本稀释的可靠性(稀释系数5、10)等,其结果均符合2015版《中国药典》中《9012生物样品定量分析方法验证指导原则》。所有样本的采集、处理、保存和检测过程均控制在方法学验证有效的时效范围内。
2 大鼠原代视网膜血管内皮细胞的分离培养
2.1 实验所需材料
2.1.1 主要仪器
TDZ4-WS台式低速离心机(湖南湘仪实验室仪器开发有限公司),SW-CJ-2FD双人单面垂直净化工作台(苏州博莱尔净化设备有限公司),AE31型生物显微镜(麦克奥迪实业有限公司),MCO-15AC型二氧化碳培养箱(三洋电机株式会),FB124电子天平(上海舜宇恒平科学仪器有限公司),DSX-280B型手提式压力蒸汽灭菌器(上海申安医疗器械),另外需要尼龙筛网200目(Corning),15 mL离心管及50 mL离心管,Transwell(24孔8 µm及0.4 µm),一次性针头过滤器PES进口(33 mm,0.22 µm),眼科手术剪,眼科手术镊,加样枪及枪头、培养瓶、碘伏、棉签等若干。
2.1.2 主要试剂
Gibco公司生产胎牛血清,DMEM/F12,HBSS缓冲液,Sigma公司的II型胶原酶,纤维粘连蛋白(Fibronectin,FN),Hyclone的胰蛋白酶(含EdTA),青链霉素(双抗),Solarbio的磷酸盐缓冲液(Phosphate Buffered Saline,PBS),ScienCell的内皮细胞培养基(ECM),成都埃法生物科技有限公司的灯盏乙素及冰片,北京凯瑞基生物科技有限公司的二甲基亚砜(Dimethyl sulfoxide,DMSO)。
2.2 实验方法
2.2.1 视网膜血管内皮细胞原代培养
先将培养瓶进行FN包被,包被需在正式取材实验前24 h。取纤维粘连蛋白,规格1010 µg·mL-1。解冻后取0.25 mL原液,加入9.75 mL的PBS液,得浓度25 µg·mL-1的FN共计10 mL,一次性滤器过滤后,用移液枪分别装入2个培养瓶,每瓶5 mL纤维粘连蛋白混合液包被。室温状态下静置45 min后,吸出上清液。再将培养瓶密封好后置入2-8℃冰箱冷藏。
取SD大鼠6只,体质量250-280 g,来源于(成都中医药大学动物房),10%水合氯醛麻醉处死后,碘伏棉签消毒眼周和眼球。摘除眼球,浸泡于75%的酒精中10 min,后拿出浸泡于含有4%双抗的PBS液中,反复冲洗3次。沿角巩膜缘剪开,去除眼前段组织,分离视网膜、玻璃体。视网膜置于培养皿内,加入0.1% Ⅱ型胶原酶消化,37℃下消化20 min,加入终止液(含20%胎牛血清的ECM)终止消化。予以200目筛网过滤,收集滤液,按1000 r·min-1,7 min条件下离心。后取出去除上清。加入ECM培养基(含20%胎牛血清,4%双抗,1%的ECGS)混悬。分装两个培养瓶,培养瓶预先已行FN包被,每瓶各细胞悬液8 mL。予以37℃,5% CO2培养箱中培养48 h。48 h后首次换液进行半量换液[8]。此后每两天换液。
2.2.2 视网膜血管内皮细胞传代
当细胞贴壁生长约8天左右,视生长情况予以消化传代。消化传代前,在37℃孵箱内复温所需的胰酶、培养基、PBS等。待原代细胞生长至80%-90%融合时,进行传代。复温所需的胰酶、培养基、PBS后。弃去原有的培养基后,予以PBS洗涤3次,每次用PBS约2 mL。清洗后加入0.25%胰酶(含EDTA)1 mL进行消化,消化约2 min后可见细胞脱落。消化完全时,加入3 mL培养基终止消化。予以离心机1000 r·min-1,离心5 min,去上清。加入完全培养基约5 mL吹打混匀,按每毫升5×104接种于25 cm2培养瓶,1∶1或者1∶2传代,37℃、5% CO2条件下培养。取第四代细胞用于Transwell实验。
2.3 实验结果
2.3.1 视网膜血管内皮形态观察及细胞生长周期
P1内皮细胞培养第6天可见细胞呈梭形生长,部分可见轴突(图7)。培养第9天,细胞层结构生长致密,融合度达到80%-90%(图8)。

图7 内皮细胞P1第6天(100×)

图8 内皮细胞P1第9天(100×)
图9显示细胞融合度较高,呈梭形生长,结构致密。无接触性抑制。原代细胞在生长前期刚贴壁时,其主要呈散在分布,以单层排列为主,主要以梭形,也有三角形或多角形,边界较为清晰,后期生长较为致密,可呈簇状,网状融合分布。一般可在3-5天细胞生长融合。
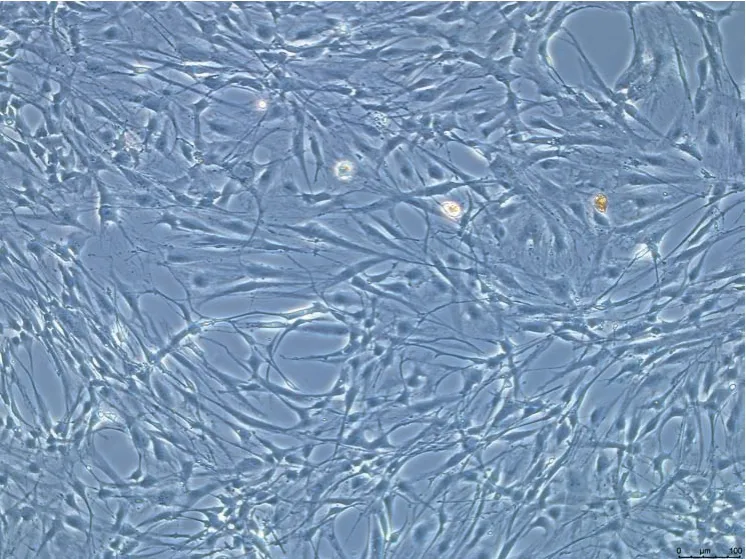
图9 内皮细胞P3(100×)
3 Transwell实验
3.1 建立视网膜血管内皮细胞屏障模型
取内皮细胞培养瓶,吸出瓶内培养基,加入PBS 2 mL吹打冲洗。吸出PBS后加入1 mL胰酶,消化细胞约5 min,加入终止液约3 mL,终止消化,后移入离心管离心,1000 r·min-1,5 min,弃上清,加入约5 mL培养基,重悬。密度约为每毫升5×105。取Transwell(24孔板,0.4 µm),于下室加入600 µL培养基。上室加入约200 µL细胞悬液接种。隔日换液,待细胞贴壁后,每天换液。换液时,先吸出上室液体,再吸出下室液体,然后先加下室培养基600 µL,再加上室培养基200 µL。
3.2 结晶紫染色检测细胞屏障致密度
培养21天,两个模型各随机取出5个小室,用复温后的PBS清洗3次,无水乙醇室温下固定30 min,后再用PBS清洗两次。加入0.1%的结晶紫染色20 min,染色可见单细胞层结构模型形成。
染色结果示视网膜血管内皮细胞胞浆及细胞间连接呈紫色均染,且各组细胞致密度较高,无显著差异。
3.3 冰片及灯盏乙素的药物溶液配制
将所需HBSS、PBS等溶液复温。精密称取灯盏乙素5000 µg,加入50 mL的HBSS溶液,涡旋混匀后得100 µg·mL-1的灯盏乙素溶液。精密称取冰片9600 µg,加入20 µL的DMSO,得浓度480 µg·mL-1的冰片药物母液。再取4 µL含冰片的DMSO母液,加入4 mL含有100 µg·mL-1灯盏乙素的HBSS溶液,充分涡旋后,再用一次性滤器过滤。得含有冰片浓度为480 µg·mL-1,含有灯盏乙素浓度为100 µg·mL-1,DMSO浓度为1/1000的HBSS药物溶液。然后按照不同比例配制含有冰片240 µg·mL-1、120 µg·mL-1、60 µg·mL-1的HBSS溶液。保证其每种浓度下灯盏乙素浓度为100 µg·mL-1,且DMSO浓度小于1/1000,仅仅存在冰片含量的差异性。
3.4 给药取样
取Transwell模型,吸净其上下室培养液,HBSS清洗3次,洗涤细胞单层中可能残留的培养基及附着物。随机编号为A-E。按下列方法处理各个样本(如表8):A孔为阴性对照,上室给含有灯盏乙素100 µg·mL-1的HBSS溶液200 µL,下室给600 µL的纯HBSS。B孔上室给含有冰片浓度为60 µg·mL-1,含有灯盏乙素100 µg·mL-1的HBSS溶液200 µL,下室给600 µL的纯HBSS。C孔上室给含有冰片浓度为120 µg·mL-1,含有灯 盏 乙 素100 µg·mL-1的HBSS溶 液200 µL,下 室给600 µL的纯HBSS。D孔上室给含有冰片浓度为240 µg·mL-1,含有灯盏乙素100 µg·mL-1的HBSS溶液200 µL,下室给600 µl的纯HBSS。E孔上室给含有冰片浓度为480 µg·mL-1,含有灯盏乙素100 µg·mL-1的HBSS溶液200 µL,下室给600 µL的纯HBSS。给药后置于以37℃,5% CO2的孵箱之中。于2 h取下室液体冻存管封存。上室液体全部吸出,冻存管封存于-80℃冰箱保存。
3.5 UPLC-MS/MS检测HBSS中灯盏乙素含量
按照第1部分建立的检测方法进行检测。
3.6 结果
冰片对灯盏细辛透视网膜血管内皮细胞屏障的影响:与阴性对照比较,加入冰片2 h后,灯盏乙素透视网膜血管周内皮细胞屏障到达Transwell下室的浓度升高,提示冰片具备促灯盏乙素透视网膜血管内皮细胞屏障的作用,其效应随冰片浓度加大而增强(图10)。
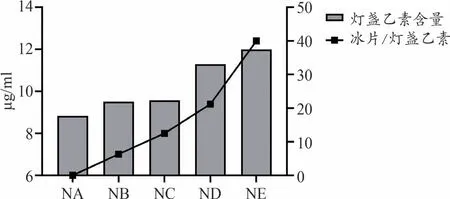
图10 内皮细胞屏障模型中灯盏乙素含量柱状图及冰片与其比值
4 小结与展望
冰片具备促进灯盏乙素透体外血-视网膜内屏障模型的作用,在本实验中上室的冰片药物浓度达到480 µg·mL-1时,灯盏乙素透过体外血-视网膜内屏障模型达到最大药物浓度。冰片外观为一种无色或白色半透明的结晶体。其理化性质中不溶于水。溶于乙醇、氯仿、乙醚、乙酸乙酯、甲醇,极微能溶于水。极易升华,具有类似樟脑的气味。冰片的通透作用,除了外用促透皮作用外,既往在研究血脑屏障时对其研究较多,主要表现在对血脑屏障的开放作用[9],主要表现在通过对内皮细胞间的紧密连接,影响P-糖蛋白(P-gp)功能,以及通过影响P-gp功能,达到开放血脑屏障作用。同时对缺氧模型有保护性作用。此外也有研究显示冰片对血脑屏障有双向调节保护作用[10]。其主要包括通过抑制NF-κB下调P-gp,或以促进血脑屏障胞饮作用方式;此外也可通过抑制IL-1β,MMP-9表达和影响Ca2+-eNOS-NO,VEGF-eNOS-NO等通路方式。在其促透作用方面效果比较确切。对于冰片开放血视网膜屏障,其原理与紧密结构相关,这种紧密连接与蛋白质元素组成的复合物相关,正因为紧密连接的相关蛋白质彼此相互作用,保持了紧密连接的完整性。如果这些蛋白质被破坏,它们将直接影响紧密连接的完整性,从而改变屏障的渗透性。在其促进血视网膜屏障的通透性的机制,可能与减少紧密连接相关蛋白ZO-1表达有关,证实了冰片作为促透剂,能够开放大鼠视网膜血管内皮细胞间的紧密连接,增加血视网膜屏障的通透性[11]。在使用安全性方面,有研究显示天然冰片与合成冰片对兔眼及角膜均不产生刺激性,长期应用亦无毒性伤害,有望作为引经促透剂广泛用于滴眼液配方[12]。
灯盏乙素具有清除氧自由基,提高抗氧化酶活性,减少氧化物产生的作用[13],同时还能抑制细胞焦亡[14]的作用。在既往研究中发现能促进部分阻塞血管的再通,达到再灌注效应[15]。此外也有研究显示灯盏乙素能促进视网膜内血流速度,这对于缺血缺氧内循环的改善有极大帮助[16]。在对于DR中研究显示灯盏花素可能存在降低VEGF的表达作用,从而达到减少血管的新生。这证明无论是青光眼还是糖尿病视网膜病变,灯盏乙素改善血流,对眼底血管的保护性作用巨大。但灯盏乙素存在生物利用度低、半衰期短、稳定性差等问题[17]。在冰片的促透作用下,提高眼内灯盏乙素的药物含量,发挥其保护性作用、保护视神经、提高对视功能,具有重大意义。在实验过程中,如果具备更好实验条件,可将观察时间延长,进一步观察。甚至采用气相色谱对冰片进行浓度测量。如果具备更好的培养基,可否将两种细胞进行进一步培养,建立混合模型,进行进一步的实验观察。如果继续将冰片含量继续提高,促透作用是否会继续加强。这些均有待于我们进一步研究。
