Cr含量对微波烧结ZK30-0.2Cu-Cr合金 组织与性能的影响
2022-03-03徐燕张志珍季洁贾韵熠吴佳妮裴莺萝姬海瑞赵明纯
徐燕,张志珍,季洁,贾韵熠,吴佳妮,裴莺萝,姬海瑞,赵明纯
(中南大学 材料科学与工程学院,长沙 410083)
镁和镁合金具有良好的生物相容性和与人骨相当的弹性模量,是一种具有很大应用潜力的生物可降解植入材料[1−4]。镁合金植入物在人体内被逐渐降解吸收或排泄,在骨骼组织愈合后消失,从而避免二次手术而导致的伤害[5−10]。研究表明,ZK30-Cu合金具有优异的抗菌能力,可满足植入骨材料消炎抗菌的更高要求,但ZK30-Cu合金在生理环境下降解过快[11−14],与骨愈合速率不匹配,导致植入物与周围组织之间形成缝隙[15]。因此,作为人体植入物,必须降低ZK30-Cu合金的降解速率。众所周知,含Cr不锈钢在氧化介质中可形成以Cr2O3为基体的稳定的表面防护膜而产生钝化现象,这种富Cr的氧化膜在很多介质中都具有良好的稳定性,从而提高钢的耐腐蚀性能。根据这一原理,把Cr添加到镁合金中有望提高镁合金的耐腐蚀性能。BUHA[16]采用铸造法制备含微量Cr的Mg-Zn合金,发现Cr固溶至镁基体中,加速析出动力学,从而显著改善Mg-Zn合金的时效硬化响应。黄晓峰等[17]将Cr加入到ZC61镁合金中,未生成新相,但可抑制α-Mg相在较高温度或较长时间下的粗化,从而减小α-Mg的平均晶粒尺寸。VILARIGUES等[18]采用离子注入的方法,分别将中等含量和高含量Cr注入金属Mg的表面,通过浸泡腐蚀发现,注入高含量Cr的镁合金腐蚀速率约为未注入Cr的十分之一,注入中等含量Cr的镁合金腐蚀速率更低。但目前为止,Cr对镁合金耐腐蚀性能的影响还没有明确的定论,对于Cr含量对镁合金植入材料降解性能的影响没有文献报道。本文作者在高效抗菌的ZK30-0.2Cu合金中添加Cr,采用快速高效、节能无污染的微波烧结法制备Cr含量(质量分数)为0~0.40%的ZK30-0.2Cu-Cr合金, 系统研究Cr含量对合金微观结构和力学性能、降解性能、生物相容性与抗菌性能的影响。该研究对于ZK30- 0.2Cu-Cr作为新型抗菌金属材料的临床应用具有重要意义。
1 实验
1.1 ZK30-0.2Cu-Cr合金制备
所用原料ZK30粉末、Cu粉和Cr粉均为高纯度(质量分数为99.9%)粉末,购于河北罗鸿科技有限公司。其中ZK30粉末的平均粒径为40 μm,Cu粉和Cr粉的平均粒径均为20 μm。采用微波烧结法制备w(Cr)分别为0、0.05%、0.10%、0.20%和0.40%的ZK30- 0.2Cu-Cr合金。首先按照合金的名义成分称量原料粉末,通过球磨使粉末混合均匀。用电子万能试验机将混合粉末压制成直径为10 mm、长度为15 mm左右的圆柱体,压力为400 MPa,保压时间120 s。然后用HY-ZG1512型微波管式炉进行微波烧结,升温速率为11 ℃/min,烧结温度为660 ℃,此温度略低于ZK30粉末的熔点,以获得良好的烧结效果,保温时间30 min。为了防止镁合金在高温下发生氧化,烧结过程中通氩气进行保护,气体流量为4~5 L/min。
1.2 组织与性能表征
依次用400#、800#、1 000#、1 500#和2 000#砂纸将ZK30-0.2Cu-Cr合金打磨至表面无明显划痕,每更换一次砂纸型号,将合金样品旋转90°。然后用2.5 μm金刚石抛光膏将合金表面抛光至光亮状态,再用硝酸酒精溶液(硝酸和酒精的体积分数分别为4%和96%)进行腐蚀,腐蚀时间为10~15 s。用Leica DMI 3000K型倒置金相显微镜观察合金的金相组织。采用X射线衍射仪(XRD,D/max 2550)分析合金的物相组成,Cu靶,管电压为40 kV,管电流为30 mA,扫描速度为5 (°)/min,扫描范围为20°~90°。通过扫描电镜(荷兰 PHILIPS公司,Quanta-200)观察合金表面形貌,并用配备的能谱仪(EDS)分析表面的元素分布。
用自动转塔数显显微硬度计(上海皆准仪器设备有限公司,HXD-1000TM/LCD)测定合金的维氏硬度(HV)。负载为2.94 N,保载时间为15 s,随机选取10个点进行测定,计算平均值作为合金的最终硬度。
1.3 耐腐蚀性能
采用浸泡试验、析氢试验和电化学试验评定ZK30-0.2Cu-Cr合金的降解性能。浸泡试验以Hank’s溶液作为模拟体液介质,在(37±1) ℃水浴中进行。Hank’s溶液的成分列于表1。合金表面面积与Hank’s溶液体积的恒定比例设置为1 cm2/30 mL。每浸泡24 h更换一次Hank’s溶液以保证腐蚀溶液的pH值为7.4左右。浸泡72 h后去除合金表面的腐蚀产物,称量合金的质量,按照式(1)[19]计算浸泡腐蚀后的质量损失率(mass loss rate)。然后利用质量损失率和式(2)[16]计算合金的降解速率(degradation rate)。

表1 Hank’s溶液的组成 Table 1 Composition of Hank’s solution
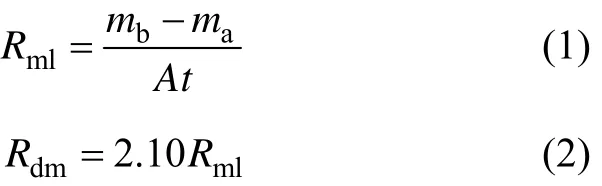
式(1)和式(2)中:Rml为模拟体液中浸泡72 h后的质量损失率,mg/(cm2·d);mb和ma分别为合金浸泡前和浸泡72 h后的质量,mg;A为合金试样与腐蚀液的接触面积,cm2;t为浸泡时间,d;Rdm为合金的降解速率,mm/a。为了确保实验结果可靠,相同Cr含量的合金取3个试样进行浸泡腐蚀实验,取平均值。用XRD对在Hank’s溶液中浸泡72 h后的合金表面腐蚀产物进行物相分析。
析氢实验同样采用Hank’s溶液,浸泡时间为72 h,于不同时间间隔观察析氢体积,根据析氢体积与试样表面积计算出单位面积的析氢量。相同Cr含量的合金取3个试样进行析氢试验,取平均值。通过式(3)将试验得到的析氢速率转换为腐蚀速率[20]。

式中:Rcorr为腐蚀速率,毫米/年(即mm/a);2HV为析氢速率(H2evolution rate),mL/(cm2∙d)。
另外,采用电化学工作站(MUL TI AUTOLAB)对ZK30-0.2Cu-Cr合金的电化学行为进行表征。依据标准的三极体系,用直径和长度分别为10 mm左右和15 mm左右的圆柱体ZK30-0.2Cu-Cr合金作为工作电极(working electrode),尺寸为25 mm×25 mm的铂丝网作为对电极(counter electrode),参比电极为饱和Ag/AgCl(饱和KCl中)。在Hank’s溶液中于37 ℃恒温下测定极化曲线,扫描速率为1 mV/s,根据极化曲线得到自腐蚀电流密度(Jcorr)与腐蚀电位(Ecorr),并用式(4)计算降解速率[20]

式中:Rd为合金的腐蚀速率,mm/a;Jcorr为自腐蚀电流密度,μA/cm2。
1.4 生物相容性
以人骨肉瘤MG63细胞为细胞模型评估ZK30- 0.2Cu-Cr合金的细胞相容性。用环氧树脂封装合金试样,暴露圆柱形试样的一个端面(直径为10 mm的圆形)作为工作表面。将封装后的合金试样放入经Dulbecco’s 改性的Eagle’s 培养基(即DMEM培养基)溶液中(试样的工作表面积与溶液体积之比为1.25 cm2/mL),然后置于含5%CO2(体积分数)湿空气中培养24 h,培养温度为37 ℃。随后取出试样,将溶液离心、过滤,提取上清液作为合金萃取液。将合金萃取液置于4 ℃的环境中冷藏,用于细胞活性实验。将 MG63 细胞用 DMEM以50个细胞/mL的密度在96孔板中培养4 h,随后把各孔中的 DMEM 培养液替换成100 μL的合金萃取液,进一步培养3天,对照组的培养基不含合金萃取液。用荧光显微镜(BX60, Olympus, Tokyo, Japan)观察在不同成分合金萃取液中培养的人骨肉瘤MG63细胞的细胞活性与形态。细胞增殖实验采用同样的方法,用100 μL合金萃取液替换培养基,进一步培养1天、4天和7天,随后在细胞培养板的各孔中添加MTT溶液,在37 ℃下继续培养4 h,然后用二甲基亚砜(DMSO)溶解形成的聚甲醛,用微型平板阅读器(Thermo Scientific Multiscan GO, USA)在 450 nm 波长下测量光学密度(optical density, OD,用符号do表示),光的参考波长为570 nm,用式(5)计算细胞的相对生长率,以表征细胞活性。为保证实验的准确性,每个成分的合金进行3次实验,取平均值。
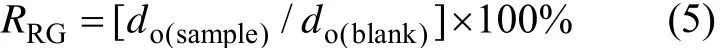
式中:RRG为细胞的相对生长率,%;do(sample)和do(blank)分别为合金组和空白对照组(DMEM培养基)的光 密度。
1.5 抗菌性能
选用的细菌为大肠杆菌(ATCC 25922),采用细菌计数法对ZK30-0.2Cu-Cr合金进行抗菌性能测定。将合金样品放入经过紫外线照射灭菌的Hank’s溶液中,于(37±0.5) ℃温度下浸泡24 h,合金表面积与Hank’s溶液体积之比为1.25 cm2/mL。从Hank’s溶液中取出合金,将溶液离心,提取上清液。将浓度为1×106cfu/mL的细菌悬液与提取液按体积比为1:9混合,置于含5%CO2(体积分数)、37 ℃的湿空气中培养24 h,然后加入磷酸盐缓冲溶液稀释细菌悬液与上清液混合液体至103cfu/mL。取0.1 mL稀释后的混合液,在琼脂平板上均匀铺开,在含5%CO2(体积分数)、37 ℃的湿空气中再培养 24 h,定量计数琼脂平板上的活菌菌落数,用式(6)计算抗菌率。
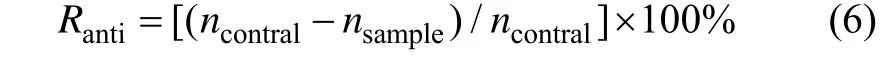
式中:Ranti为抗菌率,%;ncontral和nsample分别为对照组和ZK30-0.2Cu-Cr合金表面的菌落数。
2 结果与分析
2.1 显微组织
图1所示为不同Cr含量的ZK30-0.2Cu-Cr合金金相显微组织照片。从图中看出,粉末颗粒之间发生冶金结合,较大颗粒之间存在微孔,细小颗粒之间结合更好。微波烧结时,在微波电磁场的作用下,通过电导损耗、磁损耗和电介质损耗将吸收的微波场能量转化为热能,使金属粉末升温,粉末颗粒之间逐渐形成烧结颈而发生冶金结合[22]。受Mg的吸波性能较弱、粉末颗粒尺寸较大以及趋肤效应[23]的影响,在微波加热过程中,金属粉末在磁场作用下产生的涡流集中在颗粒表面,阻碍微波的穿透,使得微波作用的深度仅在ZK30粉末颗粒的表层区域,热量由粉末颗粒表面通过热传导、热对流和热辐射的方式传递至粉末颗粒内部。因此,粉末越细小,微波穿透效果越好,粉末之间的冶金结合越充分。大颗粒粉末由于微波穿透深度有限,且冶金结合不充分,更易形成微孔,合金孔隙率较大。

图1 不同Cr含量的ZK30-0.2Cu-Cr合金金相显微组织 Fig.1 Metallographic microstructure of ZK30-0.2Cu-Cr alloy with different w(Cr)
图2所示为ZK30-0.2Cu-Cr合金的XRD谱。从图中观察到所有合金中都含有αMg、MgZnCu和MgZn2相,未发现Cr元素的衍射峰。当被检测物相的含量较低时,受XRD检测技术精度的限制,存在物相检测不出的情况。
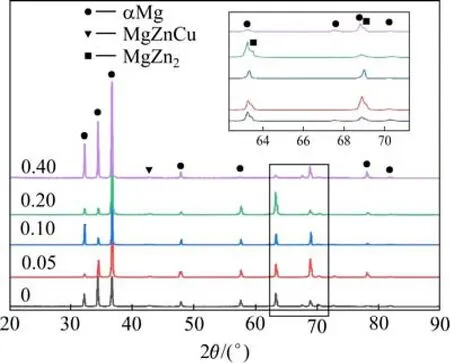
图2 不同Cr含量的ZK30-0.2Cu-Cr 合金的XRD谱 Fig.2 XRD patterns of ZK30-0.2Cu-Cr alloys with different w(Cr)
图3所示为ZK30-0.2Cu-Cr合金形貌的SEM照片,表2所列为图3中相应位置的EDS分析结果。图3与图1所示结果一致,不同Cr含量的合金表面均存在孔洞,大颗粒粉末周围的孔洞数量更多。从表2可知,ZK30-0.2Cu合金的基体中(A点)的w(Cu)为0.12%,表明Cu向基体内发生固相扩散。随Cr含量 增加,Cr在ZK30基体中的固溶度增加,ZK30-0.2Cu- 0.05Cr合金基体中w(Cr)为0.12%;ZK30-0.2Cu-0.4Cr合金基体中w(Cr)增加到0.34%。从图3还看出,在ZK30-0.2Cu-0.2Cr和ZK30-0.2Cu-0.4Cr合金中均存在Cr粉颗粒,后者的Cr颗粒更多,这是由于ZK30粉末对微波的吸收效果较差,冶金结合仅存在于表层一定深度,烧结体内较大颗粒的Cr粉与基体之间冶金结合不充分,Cr的固相扩散不完全,导致残留少部分Cr粉颗粒。

表2 图3中点A、B、C和D的EDS元素组成 Table 2 EDS element composition of point A, B, C and D in Fig.3

图3 ZK30-0.2Cu-Cr合金形貌的SEM图 Fig.3 SEM images of ZK30-0.2Cu-Cr alloys with different w(Cr)
2.2 显微硬度
图4所示为Cr含量对ZK30-0.2Cu-Cr合金维氏硬度(HV)的影响。由图可知,ZK30-0.2Cu的HV为36,添加Cr使ZK30-0.2Cu-Cr合金硬度提高,并且合金硬 度随Cr含量增加而提高,ZK30-0.2Cu-0.4Cr的硬度达到最大值,HV为47.2。这是因为随Cr含量增加,Cr在合金基体中的固溶度增大,固溶强化效果更显著,故合金硬度提高。

图4 Cr含量对ZK30-0.2Cu-Cr合金硬度的影响 Fig.4 Effect of Cr content on hardness of ZK30-0.2Cu-Cr alloys
2.3 耐腐蚀性能
ZK30-0.2Cu-Cr合金浸泡在Hank’s溶液中时,合金表面的Mg与水极易发生反应,生成Mg(OH)2并释放出H2。图5所示为合金浸泡72 h后的质量损失和浸泡过程中析氢量随浸泡时间的变化。从图5(a)看出,ZK30-0.2Cu-0.05Cr合金的质量损失率最大,表明该合金在Hank’s溶液中的耐腐蚀性能最差;ZK30-0.2Cu- 0.2Cr合金的质量损失率最小,合金的耐腐蚀性能最好。浸泡实验过程中的析氢量增加越快,表明合金的腐蚀速率越快。从图5(b)看出,浸泡实验由开始至24 h,析氢量缓慢增加,合金的腐蚀速率较慢,可能是镁合金表面产生的氧化膜对基体存在一定的保护作用。随浸泡时间进一步延长,所有ZK30-0.2Cu-Cr合金的腐蚀速率均加快。原因是溶液中氯离子浓度高,合金表层氧化膜被破坏,合金暴露在溶液中的面积增大,进而腐蚀速率加快。浸泡60 h之后,除了ZK30-0.2Cu- 0.05Cr合金外,其他合金的腐蚀速率放缓,这是由于合金表面被腐蚀产物覆盖,防止镁合金进一步被腐蚀。从图5(b)还看出,ZK30-0.2Cu-Cr合金的腐蚀速率随Cr含量增加呈波动变化。ZK30-0.2Cu-0.1Cr合金的腐蚀速率最慢,ZK30-0.2Cu-0.05Cr合金的腐蚀速率 最快。
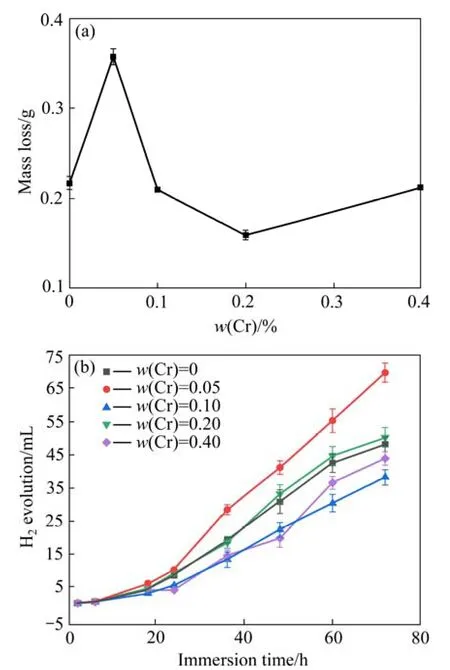
图5 ZK30-0.2Cu-Cr合金的浸泡腐蚀实验结果 Fig.5 Immersion corrosion results of ZK30-0.2Cu-Cr alloy
图6所示为ZK30-0.2Cu-0.4Cr合金在Hank’s溶液中浸泡72 h后的表面XRD谱。从图中看出合金表面的腐蚀产物主要为Mg(OH)2和Cr2O3。基体合金中的Mg元素和溶液中的H2O发生化学反应,生成Mg(OH)2和氢气,Cr元素与溶液中的O2结合生成Cr2O3。Mg(OH)2和Cr2O3覆盖在合金表面,对基体起到保护作用,延缓基体进一步被腐蚀,从而降低腐蚀速率。

图6 ZK30-0.2Cu-0.4Cr合金在Hank’s溶液中 浸泡72 h后的表面XRD谱 Fig.6 Surface XRD pattern of ZK30-0.2Cu-0.4Cr alloy immersed for 72 h in Hank’s solution
图7所示为ZK30-0.2Cu-Cr合金在Hank’s溶液中的电化学极化曲线。ZK30-0.2Cu-Cr合金的阴极极化曲线归因于水被还原析出氢气,而阳极极化曲线则与Mg溶解形成Mg2+有关。通过对极化曲线上Tafel区域的外推法,得到腐蚀电位(Ecorr)和自腐蚀电流密度(Jcorr),列于表3。腐蚀电位用来表征合金的腐蚀趋势,而自腐蚀电流密度则表征腐蚀速率。ZK30-0.2Cu合金的Jcorr为13.50 μA/cm2,ZK30-0.2Cu-0.1Cr和ZK30- 0.2Cu-0.4Cr的Jcorr低于ZK30-0.2Cu的,分别为6.39 μA/cm2和7.62 μA/cm2,表明后两种合金具有较好的耐蚀性能。腐蚀电位具有与自腐蚀电流密度相似的变化趋势。结合浸泡腐蚀实验结果可知,ZK30-0.2Cu- 0.1Cr具有最好的耐蚀性能。
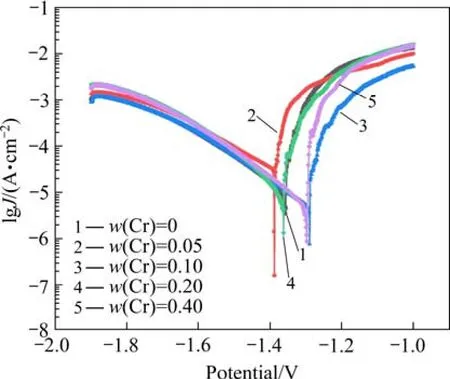
图7 不同Cr含量的ZK30-0.2Cu-Cr合金极化曲线 Fig.7 Polarization curves of ZK30-0.2Cu-Cr alloys with different w(Cr)
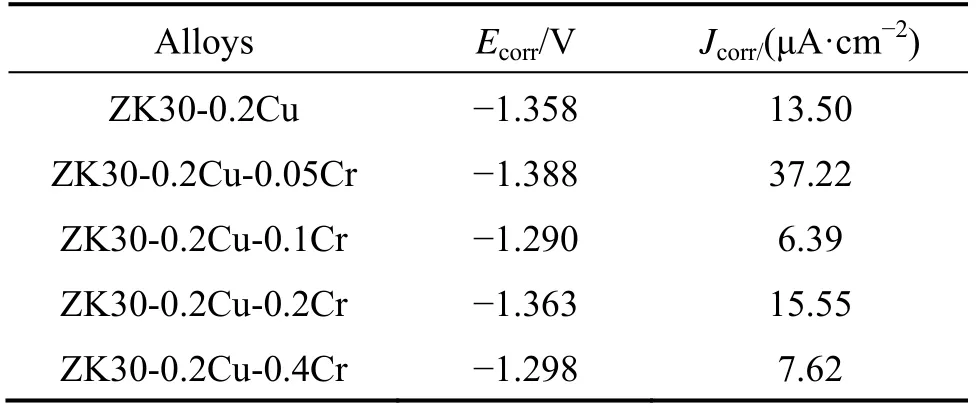
表3 ZK30-0.2Cu-Cr合金在Hank’s溶液中的 极化曲线拟合结果 Table 3 Polarization curve fitting results of ZK30-0.2Cu-Cr alloy in Hank’s solution
镁及其合金的化学性质活泼,并且具有很低的标准电位(−2.37 V),因此其表面很容易形成具有保护作用的Mg(OH)2膜,如式(7)所示,使腐蚀速率降低。但在不同的溶液中,镁合金表现出不同的耐腐蚀性能。体液中存在的各种无机和有机成分,例如氨基酸、蛋白质和氯离子(Cl−)均可影响镁合金的腐蚀行为。从表1可知Hank’s溶液中含有大量氯离子,氯离子将Mg(OH)2转化为MgCl2,如式(8)所示,使合金表面原本不溶的腐蚀层脱落,而导致镁合金的腐蚀速率加快。

另一方面,Cr和氧元素结合生成Cr2O3,在金属表面起到保护作用,提高镁合金的耐蚀性能。在合金的烧结过程中,Cr扩散距离较短,随Cr含量增加,多余的Cr形成富Cr相,如图3(d)和(e)所示,Cr的标准电位−0.41 V,显著高于Mg的标准电位,在镁基体和富Cr相之间形成微电池,发生电偶腐蚀,从而加剧合金的耐蚀。Cr2O3的形成与原电池的形成分别对ZK30-0.2Cu-Cr合金的腐蚀产生阻碍和促进作用,因而腐蚀速率取决于二者中占优势的一方,在这两方面的综合作用下,随Cr含量增加,ZK30-0.2Cu-Cr合金的腐蚀速率不是呈单一的变化趋势,而是随Cr含量增加而波动变化。
表4所列为分别由Hank’s溶液浸泡试验(质量损失率与析氢量)和电化学实验得到的腐蚀速率。由浸泡腐蚀的析氢量和质量损失率得到的腐蚀速率明显大于电化学实验的腐蚀速率。因为极化曲线表征的是合金表面瞬间的腐蚀速率,可反映不同成分合金的腐蚀性能。但由于合金在体液中的降解环境复杂以及表面腐蚀产物的形成,通常需要进行析氢和浸泡试验来表征长时间的平均腐蚀速率。通常用这3种腐蚀速率综合表征合金的抗腐蚀性能,其中ZK30-0.2Cu-0.1Cr合金的抗腐蚀性能最好。
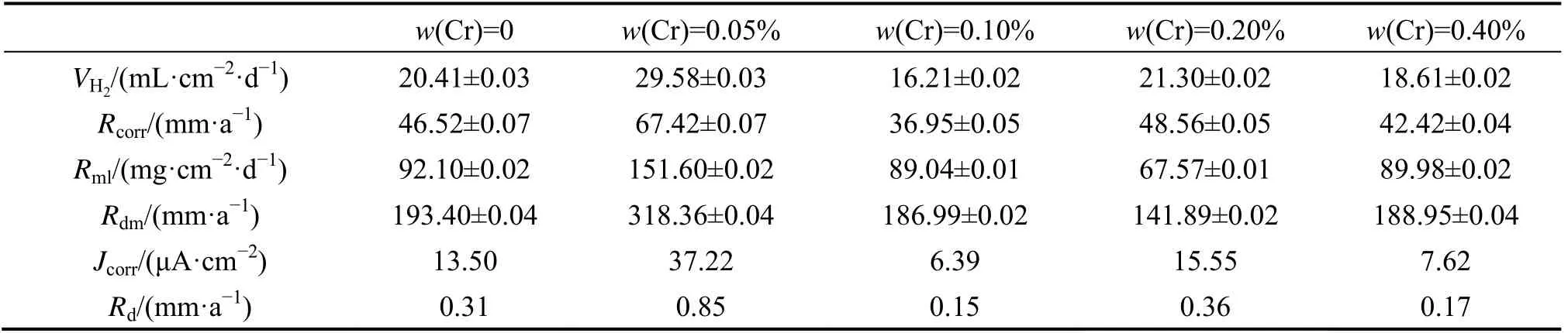
表4 ZK30-0.2Cu-Cr 合金的腐蚀实验结果 Table 4 Corrosion data of ZK30-0.2Cu-Cr alloys
2.4 生物学性能
2.4.1 生物相容性
图8所示为MG63细胞在ZK30-0.2Cu-Cr合金提取液中培养3 d后细胞的生长情况。其中活细胞为绿色,死细胞为红色,可见所有样品的荧光照片中均显示大量活细胞,且不同成分合金培养液培养的活细胞密度无明显差异。细胞的形态为梭形,细胞生长形态良好,表明所有ZK30-0.2Cu-Cr合金均无细胞毒性。
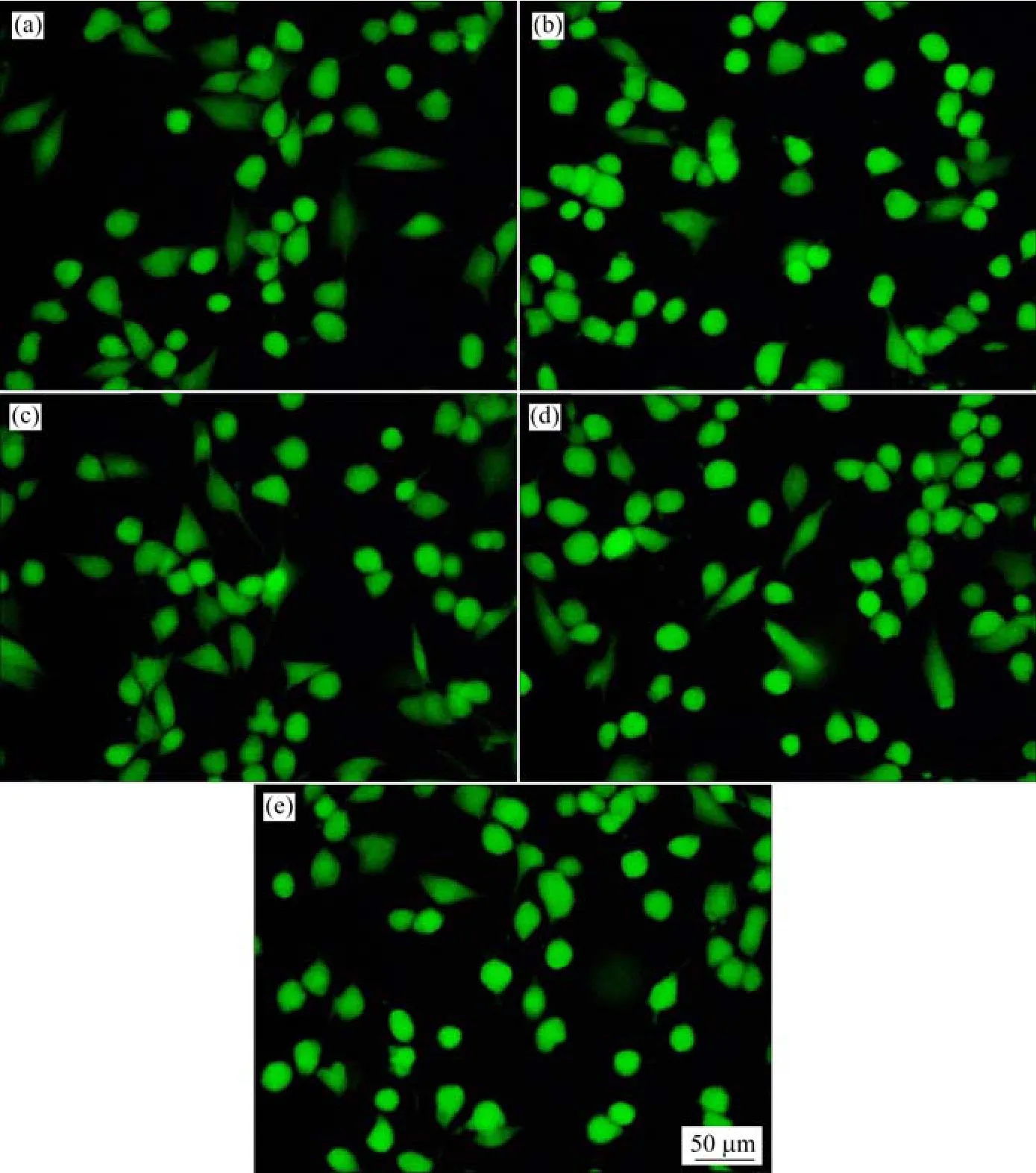
图8 ZK30-0.2Cu-Cr合金提取液培养3 d后 MG63 细胞的荧光形态 Fig.8 Fluorescence morphologies of MG63 cells after 3 d of culture with ZK30-0.2Cu-Cr alloy extract
图9所示为MG63细胞在ZK30-0.2Cu-Cr合金提取液中培养1、4和7 d后细胞的相对增长率(relative grouth rate,RRG)。根据ISO 10993-5规定,当细胞的相对生长率高于75%时,则该种生物材料不具备细胞毒性。由图9可知,培养1 d后,细胞在所有合金提取物中的RGR都超过90%,这表明MG63细胞增殖速度较快,细胞生长较好。其中ZK30-0.2Cu-0.1Cr合金的RGR最高,达到103%。在4 d后,RGR值增加到110%~130%。这表明细胞的生长条件良好。在7 d后,RGR仍高于100%。综上所述,不同Cr含量的ZK30- 0.2Cu-Cr合金均没有细胞毒性,并且具有良好的生物相容性。
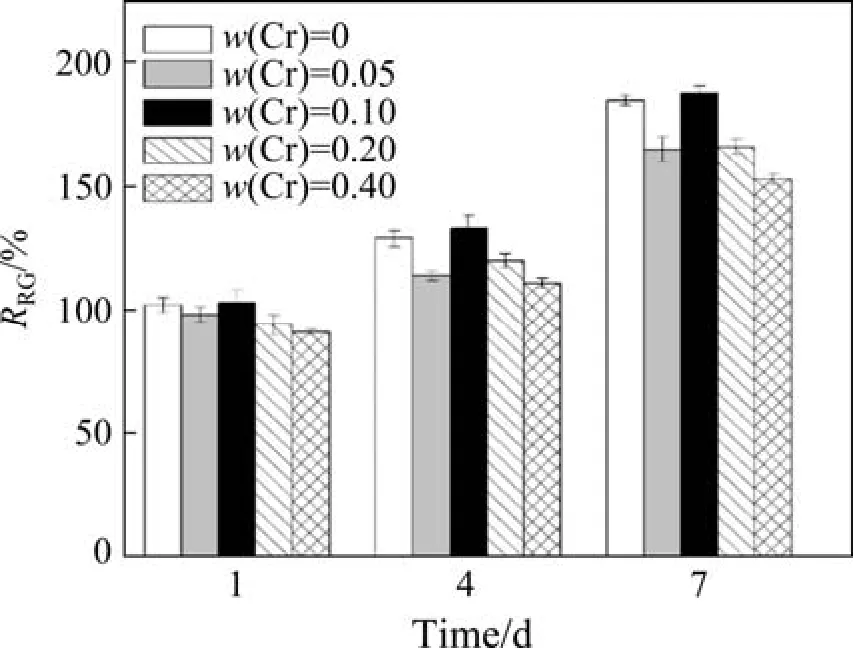
图9 MG63细胞在ZK30-0.2Cu-Cr合金提取液中 培养 1、4、7 d后的相对增长率 Fig.9 The relative growth rate (RRG) of MG63 cells cultured in ZK30-0.2Cu-xCr alloy extract for 1, 4 and 7 d
金属植入物材料在腐蚀过程中释放出金属离子,这些金属离子可能对细胞具有毒性。ZK30-0.2Cu-Cr合金在体液中释放出镁离子、锌离子、铜离子和铬离子等,其中镁离子是形成生物磷灰石的最重要的二价离子之一,它直接影响破骨细胞,并且是影响骨代谢的重要因素。锌是对人类至关重要的元素,与代谢及酶的构成有密切关系,约有160种酶含有锌元素,在锌缺乏症中,几乎所有生理功能都受到强烈干扰[21]。作为人体必需的微量元素之一,铜具有成骨和促进血管生成的功能。铬元素也是人体必需的微量元素之一,在减少应激、提高免疫力、改善胴体品质和提高繁殖性能等方面具有良好的功效。此外,本研究采用微波烧结制备的ZK30-0.2Cu-Cr合金还具有良好的细胞相容性,是具有潜在应用的金属植入物材料。
2.4.2 抗菌性能
图10所示为大肠杆菌在ZK30-0.2Cu-Cr合金提取物中培养24 h后的菌落形貌。从对照组样品上观察到大量的细菌,而用ZK30-0.2Cu合金提取物培养的样品上细菌数量明显减少,ZK30-0.2Cu、ZK30-0.2Cu- 0.05Cr、ZK30-0.2Cu-0.1Cr、ZK30-0.2Cu-0.2Cr和ZK30- 0.2Cu-0.4Cr等5种合金的抗菌率分别为99.08%、99.38%、95.38%、99.08%和93.85%。其中ZK30-0.2Cu- 0.05Cr的抗菌性能最好。ZK30-0.2Cu-Cr抗菌性能来自体液环境中合金降解过程中铜离子的释放。细菌的细胞壁带有负电荷,带正电荷的铜离子吸附在细菌的 细胞壁上,破坏膜的通透性,导致细胞膜萎缩,随后细胞溶解[24]。因此ZK30-0.2Cu-Cr合金的抗菌性能与腐蚀过程中Cu2+的释放相关,腐蚀速率越快的ZK30- 0.2Cu-Cr合金,释放的Cu2+离子越多,抗菌性能越好。耐腐蚀性能最好的ZK30-0.2Cu-0.1Cr合金可以保证Cu离子较长时间持续释放。
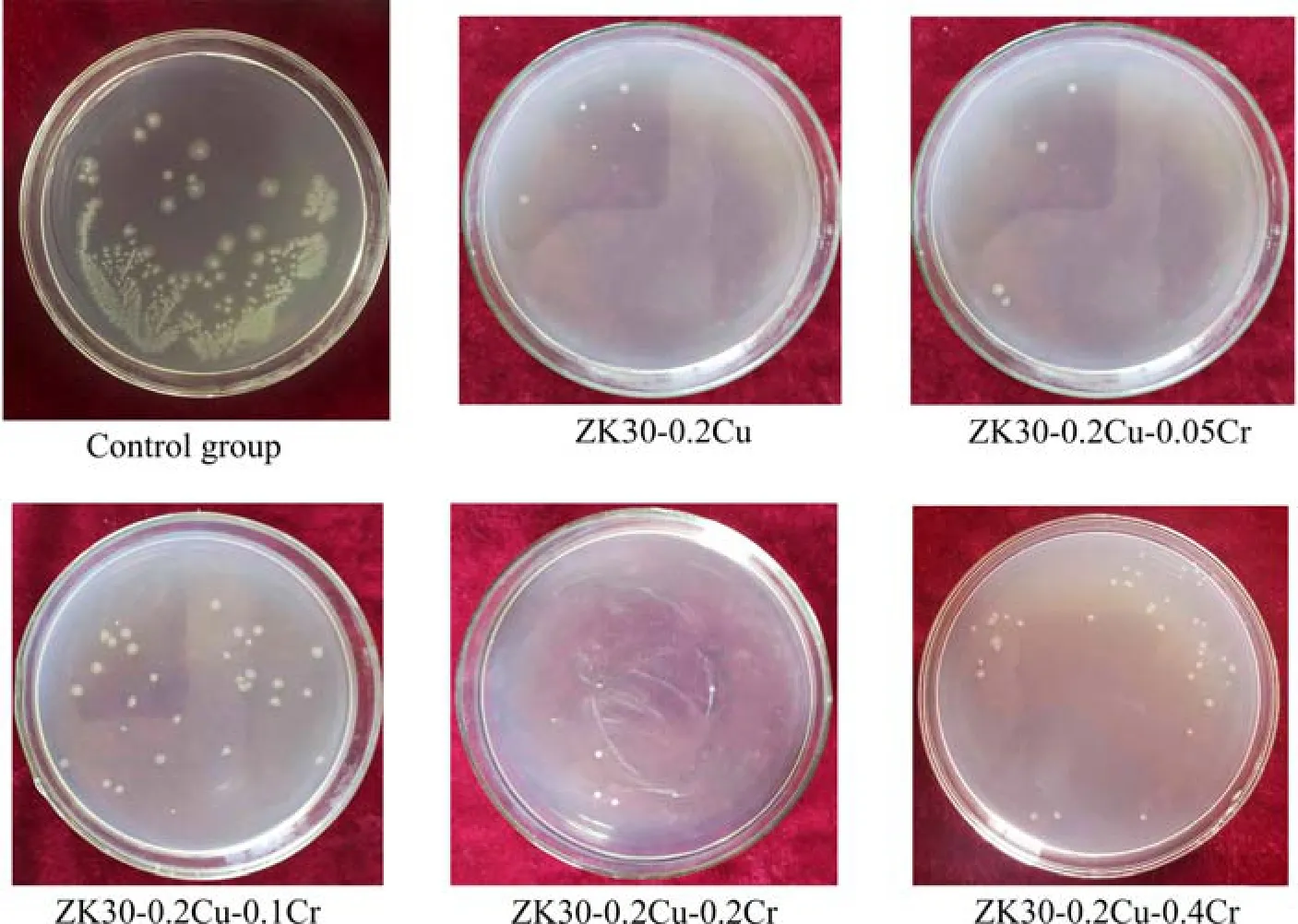
图10 大肠杆菌共培养24 h后琼脂平板上菌落生长的照片 Fig.10 Photographs of colony growth on agar plate after E. coli co-cultivation for 24 h
3 结论
1) 采用微波烧结技术制备ZK30-0.2Cu-Cr合金(Cu的质量分数分别为0、0.05%、0.10%、0.20%和0.40 %),合金中尺寸较小的粉末颗粒之间冶金结合较好,粉末之间空隙较小。随Cr含量增加,有少部分Cr粉末颗粒残留,且孔隙率较大。
2) Cr固溶在ZK30-0.2Cu合金基体中产生固溶强化作用,随Cr含量从0增加至0.2%,合金硬度升高,当Cr含量继续升高时,硬度变化不大。
3) ZK30-0.2Cu-Cr合金浸泡在模拟体液中,体液中的氯离子使镁合金表面氧化膜脱落,加快镁的腐蚀速率。Cr含量较小时,Cr与Mg基体在烧结过程中发生较完全的冶金结合,Cr充分扩散,固溶至镁基体内,形成Cr2O3,可提高镁合金的耐蚀性能;Cr含量过多时,合金基体内形成富Cr相,导致合金的耐蚀性能降低。ZK30-0.2Cu-0.1Cr合金抗腐蚀性能最好。
4) 不同Cr含量的ZK30-0.2Cu-Cr合金提取液培养环境中的活细胞数量无明显差异,且无死细胞,表明该合金无细胞毒性,且有良好的细胞相容性。同时ZK30-0.2Cu-Cr合金具有较好的抗菌性能,抗菌率在93%以上。
