苯甲醛脱氢反应从头算及速率系数不确定度分析
2022-03-02张英佳黄佐华
赵 浩,张英佳,黄佐华
苯甲醛脱氢反应从头算及速率系数不确定度分析
赵 浩,张英佳,黄佐华
(西安交通大学动力工程多相流国家重点实验室,西安 710049)
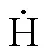
苯甲醛;脱氢反应速率;量子化学从头算;RRKM主方程;不确定度分析
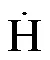
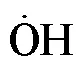
速率系数的不确定度是化学反应机理建模动力学参数优化的重要参考.以往研究中,通常根据量化计算中能量不确定度简单估计速率系数不确定度(一般为2~3).然而,影响速率系数不确定度因素众 多[6],且不同反应体系对能量的敏感程度有较大差异,导致仅通过对单一影响因素的均方求和方法估计速率系数不确定度存在较大误差.为此,本文采用Goldsmith等[7]提出的静态全局不确定评估方法,假定量子化学计算误差呈均匀分布,运用随机采样高维模型获得速率系数概率分布,实现量子化学从头算为始点到主方程为终点的全过程速率系数误差传播评估.
综上,本文工作的目的一是获得苯甲醛与关键自由基的脱氢反应类速率系数,对现有结构化相似类比方法不可靠性给出理论证据;目的二是采用静态全局方法科学评估目标计算体系速率系数的不确定度,为苯甲醛动力学机理建模和模型优化提供依据.
1 计算方法
本文在M06-2X/6-311+g(d,p)理论水平下获得了几何结构优化、谐振频率和零点能;平衡计算耗时和精度要求,在CCSD(T)/cc-pVTZ理论水平下获得了醛基位脱氢反应势能面上的单点能;考虑苯环位脱氢较高能垒和较小反应速率,平衡计算效率和结果可靠性,在DLPNO-CCSD(T)/cc-pVTZ水平获得苯环位脱氢单点能.以上结构的T1诊断值均小于 0.03,故采用单参考态方法可满足目标体系计算要求[8].本文使用ORCA(v4.1.0)程序[9]完成本文 DLPNO-CCSD(T)理论方法计算,使用 Gaussian 09 软件[10]完成其他电子能计算.零点能和频率矫正采用Alecu等[11]的推荐值 0.97.
反应速率系数通过求解RRKM/ME一维主方程获得,计算温度域为300~2000K,压力域为0.1~10MPa.计算过程考虑了范德瓦尔斯势阱,通过相空间理论方法联结反应物和势阱;采用一维受阻振动转子模型描述C6H5COCH3中甲基与苯环的内转动;采用Eckart模型进行量子隧道效应修正;使用MESS软件[12]获得分子结构的几何对称数及反应速率系数.将计算获得的反应速率系数按修正阿伦尼乌斯型关系式拟合.

(1)
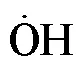
2 脱氢反应速率系数计算
2.1 反应势能面
脱氢反应势能面描述其反应历程包括:反应物进入范德瓦尔斯势阱形成反应物络合物,后越过势垒形成过渡态,再进入范德瓦尔斯势阱形成产物络合物,最终生成稳定产物.对于环上脱氢反应,其邻位(476.1kJ/mol)、间位(474.0kJ/mol)和对位(474.0 kJ/mol)的C—H键解离能几乎相同,使得3个位点有着几乎相同的势能面和反应速率系数.因此,本文统一以邻位脱氢反应为代表,速率系数为苯环总位点数的倍数作为计算标准.
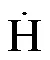
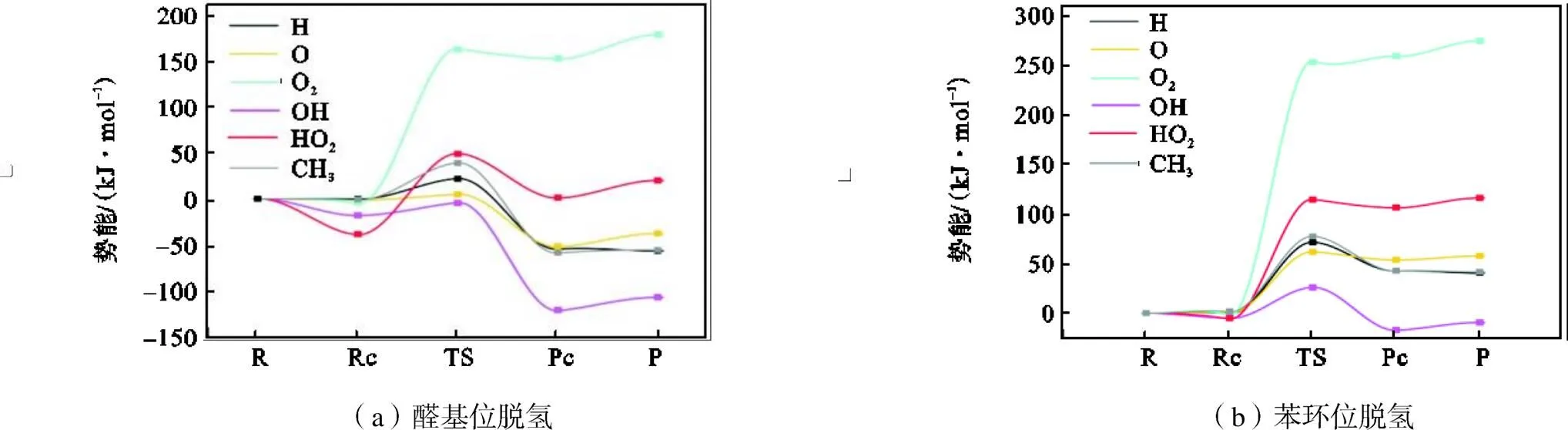
图1 CCSD(T)/cc-pVTZ水平下C6H5CHO+/////O2脱氢反应势能面
2.2 反应速率系数
通过上述详细势能面信息,对主方程求解可获得相应速率系数,以公式(1)拟合的结果见表1.


Tab.1 Calculated rate coefficients of H-abstraction of benzaldehyde attacked by ////O2/ radicals
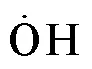

图2 苯甲醛+////O2/脱氢反应速率系数比较
2.3 脱氢反应分支比
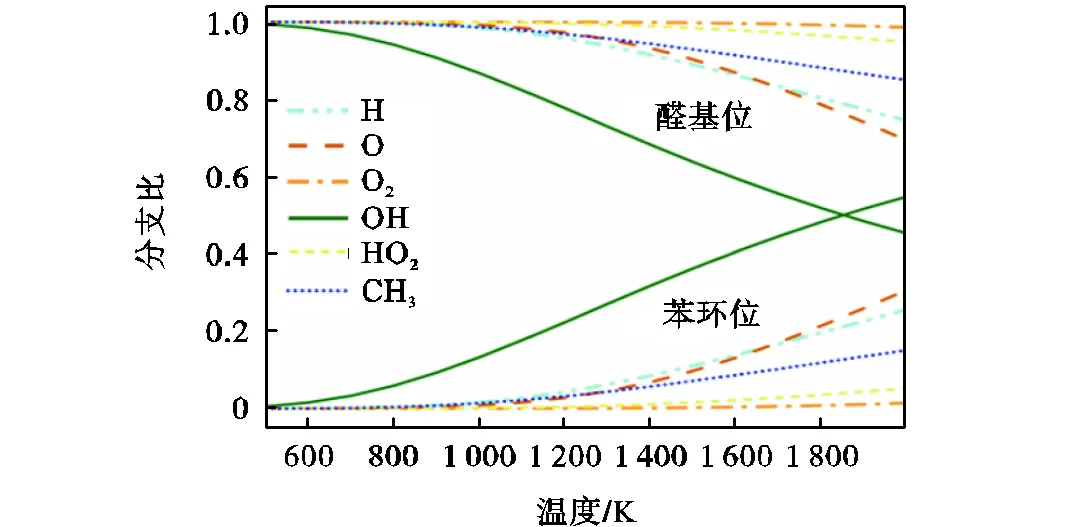
图3 苯甲醛醛基位和苯环位脱氢反应分支比
3 不确定度分析
3.1 不确定度计算
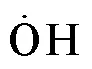
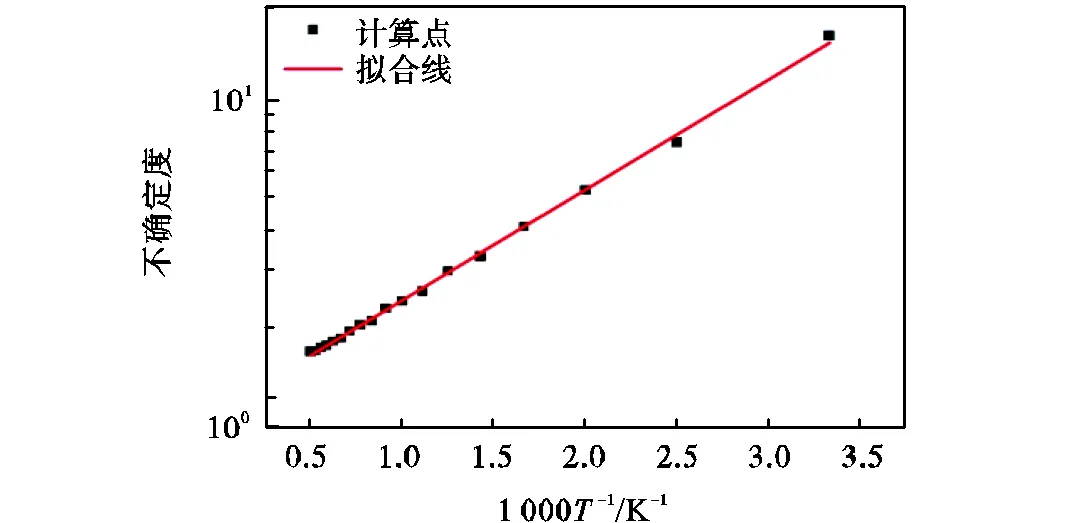
图4 苯甲醛+醛基位脱氢反应不确定度与温度的关系
3.2 速率系数的化学结构类比适用性分析
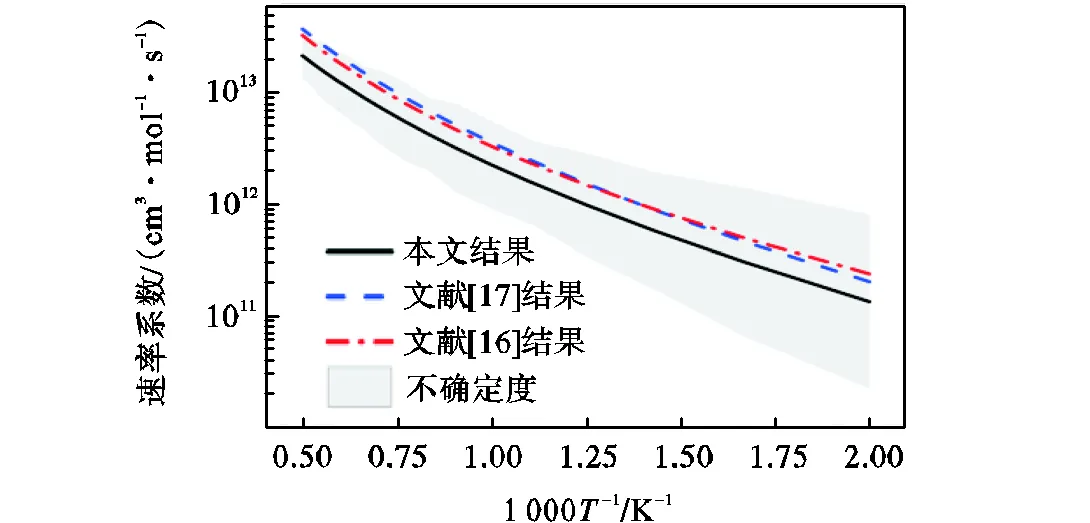
图5 苯甲醛+和乙醛+醛基位脱氢反应速率系数比较
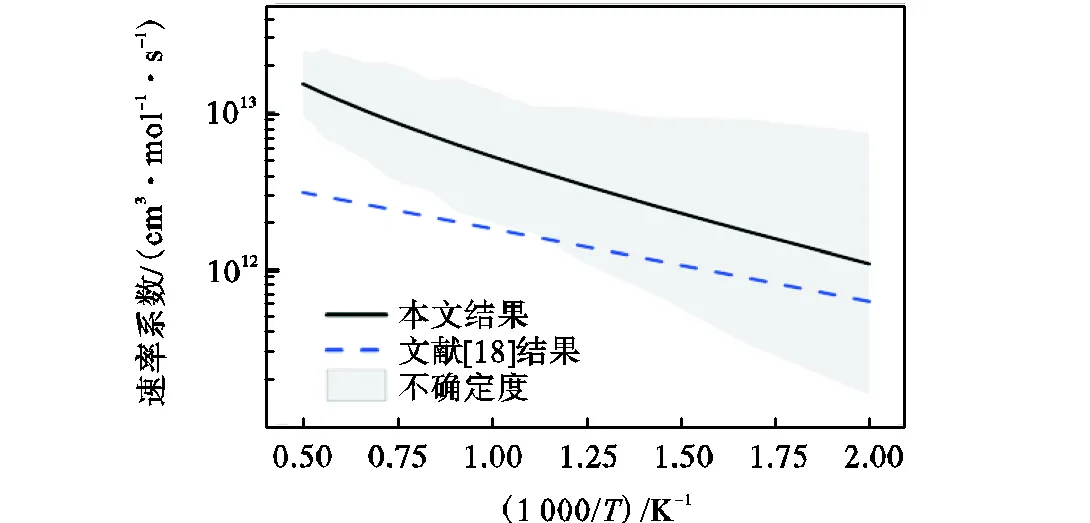
图6 苯甲醛+和乙醛+醛基位脱氢反应速率系数比较
对O2脱氢反应,Baulch等[15]从实验和理论层面系统回顾了乙醛+O2体系速率系数并给出了综合估计值.本文计算结果与该值的比较见图8.可以看出,该类型反应活化能较大,反应速率表现出较强的温度依赖.当温度低于700K时,Baulch等[15]对乙醛脱氢速率系数的推荐值位于误差带内;温度大于700K时,该值溢出误差带.Baulch等[15]给出了600K和1100K下的不确定度分别为3和10,误差随温度变化的趋势与本文计算结果相反.同样地,不建议使用当前乙醛结果分配苯甲醛+O2反应速率系数.
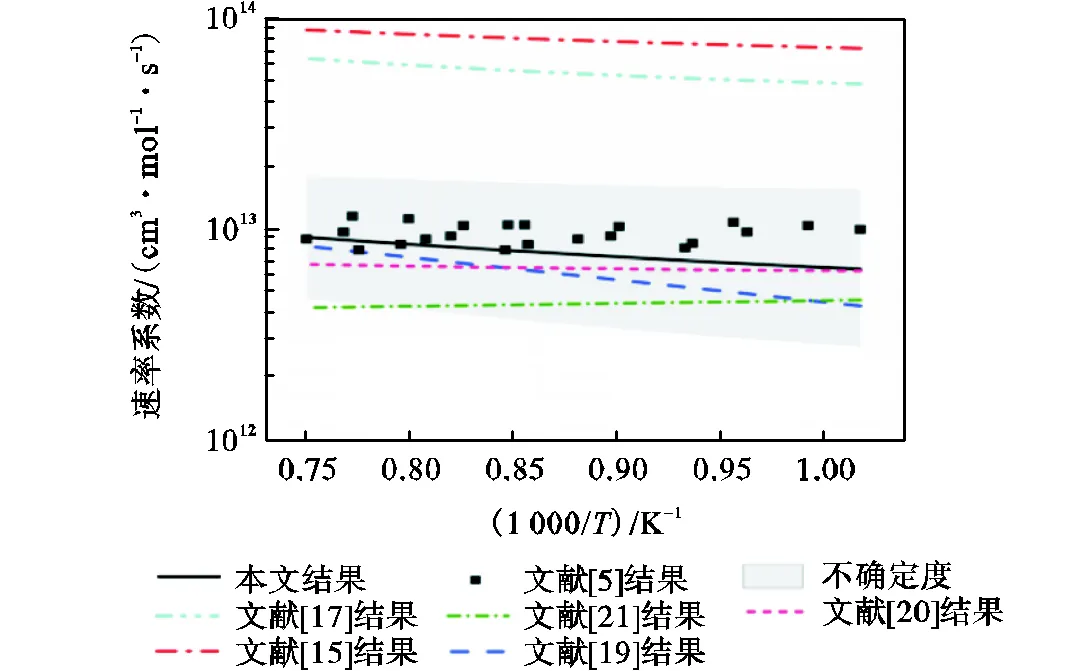
图7 苯甲醛+和乙醛+醛基位脱氢反应速率系数比较


图8 苯甲醛+O2和乙醛+O2醛基位脱氢反应速率系数比较
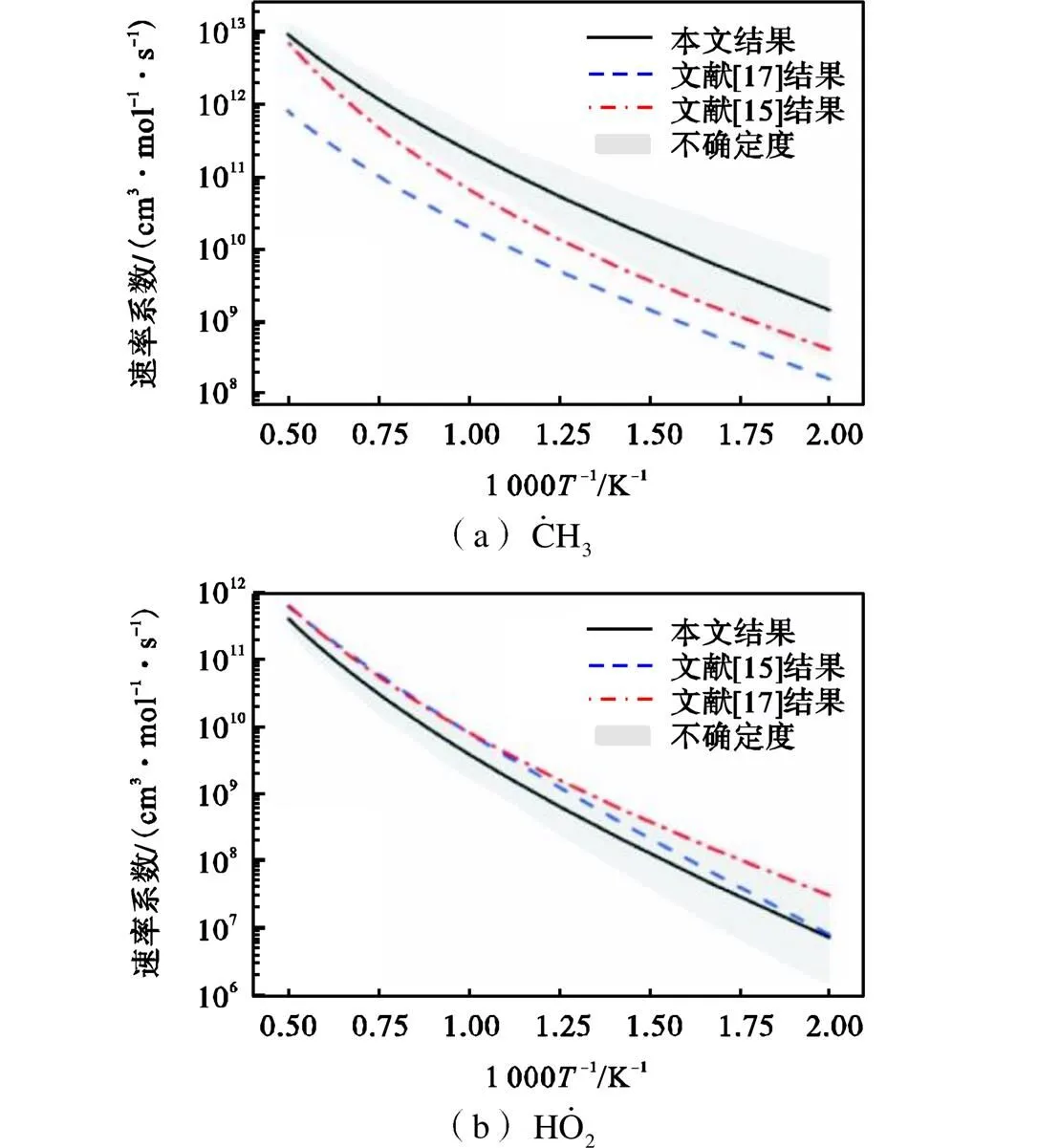
图9 苯甲醛+/和乙醛+/醛基位脱氢反应速率系数比较
4 结 论
(3)分支比结果证明,部分自由基在环位脱氢体现出与醛基位脱氢的竞争,但均在单分子解离主导温度区间(大于1750K),平衡动力学模型尺寸和预测精度,认为苯甲醛动力学建模时可忽略环上脱氢反应过程.
(4) 采用了静态统计学和随机采样方法来科学地评估了目标反应不确定度,并使用速率系数概率分布的2对其进行表征.对于脱氢反应,2000次样本容量可准确估计目标体系速率系数不确定度,误差不超过0.01.结果显示,不确定度的对数与温度倒数表现出近阿伦尼乌斯依赖关系,室温条件下不确定度较高需要依靠实验进行修正.当温度大于500K,脱氢反应不确定度对自由基的种类不敏感,该现象可作为苯甲醛脱氢反应类速率准则构建作参考.
[1] Andrae J C G. Comprehensive chemical kinetic modeling of toluene reference fuels oxidation[J].,2013,107:740-748.
[2] Yuan W,Li Y,Dagaut P,et al. Investigation on the pyrolysis and oxidation of toluene over a wide range conditions(II):A comprehensive kinetic modeling study[J].,2015,162(1):22-40.
[3] Zhang Y,Somers K P,Mehl M,et al. Probing the antagonistic effect of toluene as a component in surrogate fuel models at low temperatures and high pressures. A case study of toluene/dimethyl ether mixtures[J].,2017,36(1):413-421.
[4] Namysl S,Pelucchi M,Maffei L P,et al. Experimental and modeling study of benzaldehyde oxidation[J].,2020,211:124-132.
[5] Wang S K,Davidson D F,Hanson R K. Rate constants of long,branched,and unsaturated aldehydes with OH at elevated temperatures[J].,2017,36(1):151-160.
[6] Metcalfe W K,Dooley S,Dryer F L. Comprehensive detailed chemical kinetic modeling study of toluene oxidation[J].,2011,25(11):4915-4936.
[7] Goldsmith C F,Tomlin A S,Klippenstein S J. Uncertainty propagation in the derivation of phenomenological rate coefficients from theory:A case study of n-propyl radical oxidation [J].,2013,34(1):177-185.
[8] Watts J D,Urban M,Bartlett R J. Accurate electrical and spectroscopic properties of X1Σ+BeO from coupled-cluster methods [J].,1995,90:341-355.
[9] Neese F. The ORCA program system[J].:,2012,2(1):73-78.
[10] Frisch M J,Trucks G W,Schlegel H B,et al.09,. 01[M]. Wallingford C T:Gaussian. Inc,2009
[11] Alecu I,Zheng J,Zhao Y,et al. Computational thermochemistry:Scale factor databases and scale factors for vibrational frequencies obtained from electronic model chemistries [J].,2010,6(9):2872-2887.
[12] Georgievskii Y,Miller J A,Burke M P,et al. Reformulation and solution of the master equation for multiple-well chemical reactions [J].,2013,117(46):12146-12154.
[13] Goodwin D G,Moffat H K,Speth R L. Cantera:An Object-Oriented Software Toolkit for Chemical Kinetics,Thermodynamics,and Transport Processes [EB/OL].https://cantera.org,2019-12-21.
[14] Pelucchi M,Cavallotti C,Cuoci A,et al. Detailed kinetics of substituted phenolic species in pyrolysis bio-oils[J].,2019,4:490-506.
[15] Baulch D,Bowman C,Cobos C,et al. Evaluated kinetic data for combustion modeling:Supplement Ⅱ[J].,2005,34(3):757-1397.
[16] Sivaramakrishnan R,Michael J,Klippenstein S. Direct observation of roaming radicals in the thermal decomposition of acetaldehyde[J].,2010,114(2):755-764.
[18] Warnatz J.C/H/O[M]. New York:Springer-Verlag,1984.
[19] Taylor P H,Yamada T,Marshall P. The reaction of OH with acetaldehyde and deuterated acetaldehyde:Further insight into the reaction mechanism at both low and elevated temperatures[J].,2006,38(8):489-495.
[20] Smith G P,Golden D M,Frenklach M,et al. GRI 3. 0 Mechanism. Gas Research Institute [EB/OL]. http://www.meberkeley.edu/Gri_mech,1999.
[21] Li Y,Zhou C W,Somers K P,et al. The oxidation of 2-butene:A high pressure ignition delay,kinetic modeling study and reactivity comparison with isobutene and 1-butene[J].,2017,36(1):403-411.
Calculation of H-Atom Abstractions of Benzaldehyde and Uncertainty Analysis of Rate Coefficient
Zhao Hao,Zhang Yingjia,Huang Zuohua
(State Key Laboratory of Multiphase Flow in Power Engineering,Xi’an Jiaotong University,Xi’an 710049,China)
benzaldehyde;reaction rate coefficient of H-atom abstraction;calculation;RRKM master equation;uncertainty analysis
TK16
A
1006-8740(2022)01-0078-07
2021-02-28.
国家自然科学基金资助项目(91741115).
赵 浩(1997— ),男,硕士研究生,zhaohaoyx@stu.xjtu.edu.cn.Email:m_bigm@tju.edu.cn
张英佳,男,博士,教授,yjzhang_xjtu@xjtu.edu.cn.
(责任编辑:隋韶颖)
