CaFe2O4基复合光催化剂的制备及性能研究
2022-02-24张春燕刘哲语
张春燕,刘哲语
(1.山西铁道职业技术学院,山西太原 030013; 2.中国科学院山西煤炭化学研究所,山西太原 030128)
工业现代化给人类带来了巨大进步,但也给环境造成了巨大影响。尤其是江河两岸的印染厂、纺织厂等的染料废水若直接排放到江河内,将对水环境造成严重污染。因此,对染料废水进行处理并再利用对减少水环境污染极为重要。近年来,有效的办法是采用半导体光催化技术降解有机染料,从而实现水环境污染治理〔1〕。目前,可实现工业应用的半导体光催化剂主要为二氧化钛和钛酸锶,但带隙宽、仅能响应紫外光的缺点限制了这 2种催化剂在光催化领域的应用〔2-3〕。铁酸钙(CaFe2O4)是一种潜在的光催化剂,它具有带隙窄的优点,在光催化降解有机染料领域具有潜在的应用前景。但该催化剂太阳光利用率较低、电荷迁移和分离效率低,严重限制了它在降解有机废水方面的应用〔4-7〕。
基于能带排列理论构建异质结光催化剂是提高单相光催化剂太阳光利用率、电荷迁移能力和分离效率的有效方法〔8- 11〕。构建的异质结光催化剂具有3种能带排列方式:一种是Ⅰ型能带排列,即一种半导体的导带和价带均位于另一种半导体的内部;另一种是Ⅱ型能带排列,即一种半导体的价带或导带在另一种半导体内部;第三种是Ⅲ型能带排列,即 2种半导体的导带和价带均无交叠。在这3种排列方式中,Ⅰ型能带排列的异质结光催化剂因电荷载流子迁移速率和分离效率高而越来越受到人们的重视。硫酸钙(CaSO4)和三氧化二铁(Fe2O3)是 2种不同类型的半导体,可用于同CaFe2O4一起构建双异质结CaFe2O4/CaSO4/Fe2O3三元复合光催化剂,提高CaFe2O4的太阳光利用率、电荷迁移能力和分离效率,进而提高体系的光催化活性。然而,目前尚未有科研人员制备CaFe2O4/CaSO4/Fe2O3三元复合光催化剂并研究其光催化活性。
本研究采用一步水热法合成CaFe2O4/CaSO4/Fe2O3三元复合光催化剂,研究该催化剂的相纯度、形貌、光吸收能力、电荷转移能力和分离效率以及光催化活性。基于能带排列理论和光催化实验结果,探讨该复合光催化剂的催化机理。
1 实验部分
1.1 催化剂的制备
按物质的量比为n(Ca)∶n(Fe)= 1∶ 2的比例称取适量硝酸钙和硫酸铁,依次缓慢溶解在 20 mL去离子水中,在磁力搅拌器的连续搅拌下,将试剂完全溶解。随后,加入适量硫酸调节溶液酸度。将70 mL配制好的溶液转移至反应釜中,随即密封好反应釜。将反应釜置于干燥箱中,以 10℃/min的升温速率升至 180℃,待温度稳定后恒温48 h。然后以 10℃/min的降温速率降至室温。打开反应釜,取出内胆,将上层清液倒掉。再用去离子水反复清洗产物数次后,在 150℃干燥 24 h,获得CaFe2O4/CaSO4/Fe2O3三元复合光催化剂。
1.2 催化剂的表征
采用Bruker D8型X射线衍射仪(XRD)分析催化剂的相纯度和晶体结构。采用JEOL 6335F型场发射扫描电子显微镜(SEM)观察催化剂的表面形貌。采用UV- 2500型紫外可见分光光度计测量催化剂的紫外可见吸收光谱。采用CST 350型电化学工作站测量催化剂的阻抗谱和光电流密度。
1.3 光催化实验
采用721分光光度计测量CaFe2O4/CaSO4/Fe2O3三元复合光催化剂降解甲基橙前后的浓度。甲基橙初始质量浓度为 20 mg/L,光催化剂的投加量为 15 mg/L,每隔30 min取一次样,经离心后取上层清液测量甲基橙的质量浓度。
采用酒精、苯醌(BQ)和草酸铵(AO)作为猝灭剂,研究它们对甲基橙降解率的影响,进而洞察羟基自由基、空穴和超氧自由基在光催化反应过程中的作用。
2 结果与讨论
2.1 相纯度分析
相结构和纯度是影响光催化剂光催化活性的一个重要因素,通过XRD可表征分析光催化剂的纯度和相结构。为了对比CaFe2O4/CaSO4/Fe2O3三元复合光催化剂与Fe2O3、CaFe2O4和CaSO4晶体结构的区别,采用类似的方法合成了Fe2O3、CaFe2O4(CaSO4外购)。4种物质的XRD见图 1。
LDH检测:空腹采集患者静脉血,不抗凝,离心分离血清。应用LDH检测试剂盒(成都元和华盛股份有限公司产品)和i2000全自动生化分析仪(美国Abbott Laboratories公司产品)检测LDH。正常值参考范围:150~245 U/L。
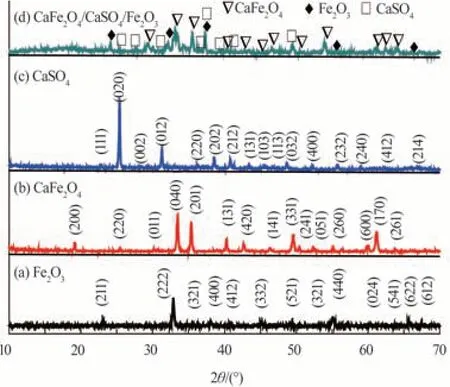
图 1 光催化剂XRDFig.1 XRD of photocatalysts
图 1(a)~(c)分 别 为Fe2O3、CaFe2O4和CaSO4的XRD图,3种物质均为相应的纯相化合物,不含其他杂质,对应的标准PDF卡片号分别为33-0664、32-0168、37-0184。图 1(d)是CaFe2O4/CaSO4/Fe2O3三元复合光催化剂的XRD图,CaFe2O4的XRD衍射峰主要集中在(040)、(201)、(131)、(331)和(170)晶面;除了CaFe2O4的衍射峰外,图 1(d)还存在Fe2O3和CaSO4的衍射峰,且该样品不含其他杂质元素。结果表明,采用一步水热法可成功合成CaFe2O4/CaSO4/Fe2O3三元复合光催化剂。
2.2 形貌分析
采用SEM观察光催化剂的表面形貌,可大致推断光催化剂的比表面积。图 2(a)是CaFe2O4/CaSO4/Fe2O3三元复合光催化剂的SEM照片。采用一步水热法合成的CaFe2O4/CaSO4/Fe2O3三元复合光催化剂呈花状,主要由一些细颗粒黏连而成。花状的细颗粒表明CaFe2O4/CaSO4/Fe2O3三元复合光催化剂具有高的比表面积,是潜在的高效光催化剂。
为进一步证实合成了CaFe2O4/CaSO4/Fe2O3三元复合光催化剂,图 2(b)给出了CaFe2O4/CaSO4/Fe2O3三元复合光催化剂的高分辨TEM(HRTEM)照片。晶面间距0.241 2 nm和0.1476 nm分别对应Fe2O3的(222)和(440)晶面;0.3499 nm对应CaSO4的(020)晶面;0.2675 nm和0.2433 nm分别对应CaFe2O4的(040)和(121)晶面。HRTEM结果进一步确认了采用一步水热法可成功合成CaFe2O4/CaSO4/Fe2O3三元复合光催化剂。

图 2 CaFe2O4/CaSO4/Fe2O3的SEM(a)和HRTEM(b)Fig.2 SEM(a)and HRTEM(b)of CaFe2O4/CaSO4/Fe2O3
2.3 光学性质分析
半导体光催化剂的光学性质可预估它在降解有机废水方面的光催化能力。图3(a)是Fe2O3、CaFe2O4、CaSO4和CaFe2O4/CaSO4/Fe2O3三元复合光催化剂的紫外可见吸收谱图。由图3(a)可知,Fe2O3、CaFe2O4、CaSO4和CaFe2O4/CaSO4/Fe2O3三元复合光催化剂在紫外区域差异较大。Fe2O3和CaFe2O4的紫外吸收峰截止于350 nm,且CaFe2O4的吸收峰最高。CaSO4在 200~420 nm范围内出现了 2个明显的吸收峰。当三者复合后,CaFe2O4/CaSO4/Fe2O3三元复合光催化剂在 200~450 nm范围内出现了强的吸收带,且吸收峰已拓展到可见光区域;在550~800 nm处,CaFe2O4/CaSO4/Fe2O3三元复合光催化剂也具有一定的可见光吸收能力。结果表明,CaFe2O4/CaSO4/Fe2O3三元复合光催化剂具有潜在的紫外可见光催化降解能力。
根据Tauc关系,可将吸收光谱转换为(αhν)2-hν的关系曲线图,如图3(b)~(c)所示。该曲线最陡处的斜率外延至与横坐标的交点的值为光催化剂的带 隙 能(Eg)。基 于 此,Fe2O3、CaFe2O4、CaSO4和CaFe2O4/CaSO4/Fe2O3三元复合光催化剂的Eg分别为 1.83、 1.85、3.69/4.29、 1.35/ 2.64 eV。从CaSO4和CaFe2O4/CaSO4/Fe2O3三元复合光催化剂的(αhν)2-hν的关系曲线图中可以看到这 2种物质均具有 2个Eg,在后续光催化机理分析时需与文献对比,确定CaSO4的Eg。

图3 紫外可见吸收谱(a)和(αhν) 2-hν的关系曲线(b~c)Fig.3 UV-Vis absorption spectrum(a)and the relation curve of(αhν) 2-hν(b~c)
2.4 电化学性质分析
电化学工作站可测量半导体光催化剂的阻抗谱和光电流密度,通过阻抗谱和光电流密度可分析光催化剂的电荷转移和分离效率。图4(a)是CaFe2O4和CaFe2O4/CaSO4/Fe2O3三元复合光催化剂的阻抗谱。从图中可以看出,阻抗谱由一个小的半圆和一条直线组成,高频区的半圆可归因于电极/电解液界面的电荷转移阻抗〔12〕,低频区的直线则可归因于瓦尔堡阻抗〔13〕。与纯的CaFe2O4相比,CaFe2O4/CaSO4/Fe2O3三元复合光催化剂的半圆半径几乎可以忽略,可见CaFe2O4/CaSO4/Fe2O3三元复合光催化剂具有更高的电荷转移能力和分离效率〔13- 15〕。
图4(b)是CaFe2O4和CaFe2O4/CaSO4/Fe2O3三 元复合光催化剂的光电流密度。当氙灯打开时,光电流密度瞬间达到最大值并趋于稳定。当氙灯关闭时,光电流密度瞬间下降到最初值。CaFe2O4/CaSO4/Fe2O3的光电流密度的绝对值接近于0.4μA/cm2,比纯CaFe2O4大了 2倍多〔13〕。该结果也证明CaFe2O4/CaSO4/Fe2O3三元复合光催化剂具有高的电荷转移能力和分离效率,可响应可见光。

图4 阻抗谱(a)和光电流密度(b)Fig.4 Impedance spectroscopy(a)and photocurrent density(b)
2.5 光催化活性分析
选择甲基橙作为目标降解染料,研究CaFe2O4/CaSO4/Fe2O3三元复合光催化剂对有机废水的降解性能。图5(a)是Fe2O3、CaFe2O4、CaSO4和CaFe2O4/CaSO4/Fe2O3三元复合光催化剂在紫外光照射下催化甲基橙降解的曲线。当甲基橙废水在仅紫外光照射而不添加光催化剂条件下辐照 120 min时,甲基橙染料几乎没有降解,表明该染料在自然条件下非常稳定。加入Fe2O3作为光催化剂, 120 min时甲基橙染料的降解率约为39.7%。加入CaFe2O4或CaSO4作为光催化剂,90 min时甲基橙染料几乎被完全降解。加入CaFe2O4/CaSO4/Fe2O3三元复合光催化剂,甲基橙染料的降解率随光照时间的延长而增加,光照时间达到90 min时,甲基橙染料的降解率达到了97.85%。

图5 紫外光照射下的光催化降解曲线(a)和一级动力学曲线(b)Fig.5 Photocatalytic degradation curves(a)and first‑order kinetics curves(b)under UV irradiation
在紫外光照射下可降解有机染料废水的光催化剂有很多,但如果只能在紫外光照射下才降解的话,对太阳光的利用率非常低。根据CaFe2O4/CaSO4/Fe2O3三元复合光催化剂的紫外可见吸收光谱和光电流密度分析可知,该光催化剂具有可见光降解活性。图6(a)给出了Fe2O3、CaFe2O4、CaSO4和CaFe2O4/CaSO4/Fe2O3三元复合光催化剂在可见光照射条件下催化甲基橙降解的曲线。在未添加光催化剂条件下,甲基橙染料在可见光照射下很难降解。当添加Fe2O3、CaFe2O4、CaSO4和CaFe2O4/CaSO4/Fe2O3三元复合光催化剂后,经 180 min可见光照射后,甲基橙染料的降解率分别为37.88%、47.88%、79.89%和94.33%,CaFe2O4/CaSO4/Fe2O3三元复合光催化剂对甲基橙的降解率最高。
图6(b)给出了Fe2O3、CaFe2O4、CaSO4和CaFe2O4/CaSO4/Fe2O3三元复合光催化剂在可见光照射条件下 的 一 级 动 力 学 曲 线。Fe2O3、CaFe2O4、CaSO4和CaFe2O4/CaSO4/Fe2O3三元复合光催化剂的一级动力学常数k分别为0.0024、0.0034、0.008 2、0.0144 min- 1。CaFe2O4/CaSO4/Fe2O3三元复合光催化剂的k约为CaSO4的 1.8倍。由此可知,CaFe2O4/CaSO4/Fe2O3三元复合光催化剂是一种可高效利用可见光的光催化剂。

图6 可见光照射下的光催化降解曲线(a)和一级动力学曲线(b)Fig.6 Photocatalytic degradation curves(a)and first‑order kinetics curves(b)under visible light irradiation
2.6 循环稳定性分析
图7(a)给出了CaFe2O4/CaSO4/Fe2O3三元复合光催化剂的稳定性实验结果。每次光催化实验结束后,光催化剂需经离心、过滤、干燥等步骤后再进行下一次光催化降解实验。经过5次光催化降解实验后,甲基橙染料降解率仅下降了3.8%。
图7(b)是CaFe2O4/CaSO4/Fe2O3三元复合光催化剂在光催化前以及光催化循环5次后的XRD对比图。光催化前后的XRD衍射峰除了强度有变化外,峰的位置几乎没有变化。此外,光催化后半峰宽略微变窄,可能是由于吸附了少量降解产物所致。可见,CaFe2O4/CaSO4/Fe2O3复合光催化剂是一种稳定性好且重复使用效率高的光催化剂。
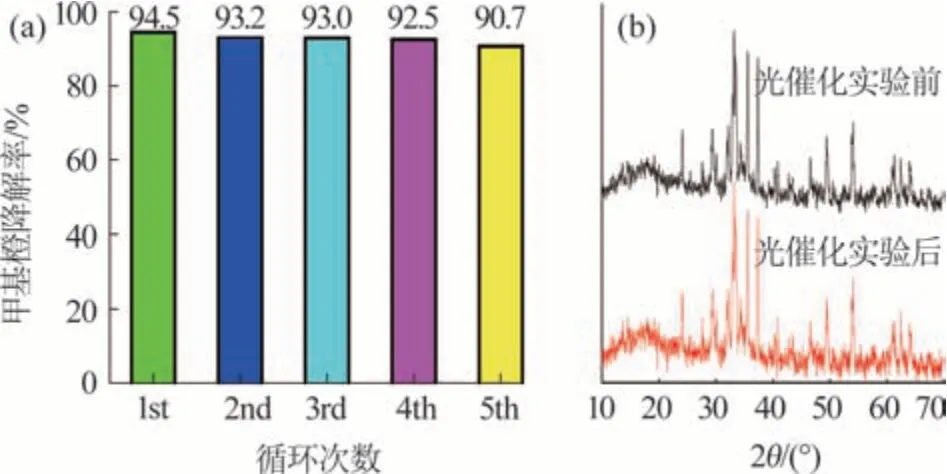
图7 循环实验中CaFe2O4/CaSO4/Fe2O3的稳定性(a)和XRD图(b)Fig.7 Stability(a)and XRD patterns(b)of CaFe2O4/CaSO4/Fe2O3 in cycle experiment
2.7 光催化机理研究
CaFe2O4/CaSO4/Fe2O3三元复合光催化剂具有高的紫外可见光催化降解活性,需通过能带排列理论对其进行分析,洞察电子、空穴、羟基自由基和超氧自由基在光催化降解过程中所起的关键作用。基于式(1)和式(2),可获得CaFe2O4、CaSO4和Fe2O3的导带电位(ECB)和价带电位(EVB)。

式中,Ee=4.5 eV,X是不同金属氧化物的电负性,CaFe2O4、CaSO4和Fe2O3的Eg分 别 为 1.85〔16〕、3.94〔17〕、 1.83 eV〔18〕。本实验获得了上述3种半导体的Eg,CaFe2O4和Fe2O3的Eg值与文献一致,但CaSO4具有 2个Eg,与文献对比,选用前人报道的结果对其光催化机理进行分析。CaFe2O4、CaSO4和Fe2O3的电负性可由式(3)~(5)计算获得。

式中,XCa= 2.2 eV,XFe=4.06 eV,XS=6.22 eV,XO=7.54 eV。根据计算,CaFe2O4、CaSO4和Fe2O3的电负性、Eg、导带和价带电位见表 1。

表 1 CaFe2O4、CaSO4和Fe2O3的E g、电负性和导带、价带电位Table 1 E g,electronegativity,E CB and E VB of CaFe2O4,CaSO4 and Fe2O3
根据计算获得的导带和价带电位,图8给出了CaFe2O4/CaSO4/Fe2O3三元复合光催化剂的光催化机理。根据能带排列理论,CaFe2O4与CaSO4、CaSO4与Fe2O3之间构成Ⅰ型能带排列。当光辐照到CaFe2O4/CaSO4/Fe2O3三元复合光催化剂表面时,位于CaFe2O4、CaSO4和Fe2O3价带上的电子被激发跃迁到导带,在价带留下空穴。

图8 CaFe2O4/CaSO4/Fe2O3的光催化机理Fig.8 Photocatalytic mechanism of CaFe2O4/CaSO4/Fe2O3
由于CaSO4的价带电位比CaFe2O4和Fe2O3更正,位于CaSO4价带上的空穴将会转移到CaFe2O4和Fe2O3的价带,同时由于H2O/·OH和OH-/·OH的氧化还原电位分别为+ 2.72 V和+ 1.89 V,价带上的空穴能与H2O或OH-反应生成羟基自由基(·OH)〔19〕,见式(6)和式(7)。价带的空穴也会直接与染料作用,生成无毒无害的产物。

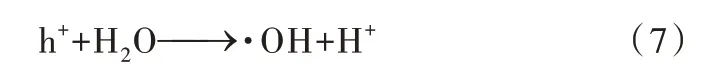
值得注意的是,CaSO4的导带能级最低,在三者形成异质结后,CaSO4导带上的电子会转移到CaFe2O4和Fe2O3的导带上。同时,由于O2/·O2-的氧 化 还 原 电 位 为-0.13 V〔20〕,位于CaFe2O4和Fe2O3导带的电子将与O2反应生成超氧自由基(·O2-),如式(8)所示。

同时,在CaFe2O4和Fe2O3导带将发生如下反应:

无论导带还是价带生成的·OH均会与染料作用,生成无毒无害的降解产物。
酒精、苯醌和草酸铵被用作猝灭剂来分别研究光催化反应液中·OH、·O2-和空穴扮演的角色。图9给出了不同猝灭剂对甲基橙降解率的影响曲线。酒精对光催化活性的抑制作用较大,说明在光催化反应过程中,电子与溶液中的H2O2反应生成·OH活性物种〔21〕。与酒精相比,苯醌对光催化活性的抑制作用较小,说明在反应过程中电子与O2作用生成了·O2-活性物种。而草酸铵加入后,对甲基橙光催化活性的抑制作用最弱,表明空穴在整个光催化反应过程中占据的作用要较·OH和·O2-小。

图9 不同猝灭剂对甲基橙降解率的影响Fig.9 Effect of different quenching agents on degradation rate of methyl orange
根据文献〔21- 23〕,H2O2容易吸附在Fe2O3的表面,进而发生如下反应:


反应式(13)~(15)表明,除了空穴经一系列反应可生成·OH外,铁离子间的反应也能产生大量·OH,故而出现上述现象。由此可知,空穴、·OH和·O2-的协同作用使得CaFe2O4/CaSO4/Fe2O3三元复合光催化剂在降解甲基橙方面具有高的光催化活性。
3 结论
采用一步水热法成功地制备了CaFe2O4/CaSO4/Fe2O3三元复合光催化剂。物相结构分析表明,XRD衍射谱中除CaFe2O4、CaSO4和Fe2O3的衍射峰外,不含其它任何杂质。该复合光催化剂呈花状,主要由细颗粒团聚堆积而成,具有较高的比表面积。在 200~450 nm波长范围具有较高的光吸收能力,其Eg约为 2.64 eV。阻抗谱和光电流密度曲线分析表明,CaFe2O4/CaSO4/Fe2O3三元复合光催化剂具有较高的电荷转移能力和分离效率。通过对比研究,光催化实验证明了该催化剂在降解甲基橙染料方面具有较强的紫外可见光催化活性。降解机理主要是空穴、·OH和·O2-的协同作用。
