应用前段光学相干断层扫描作为角膜缘干细胞缺乏的诊断参数测量干眼患者中央角膜上皮厚度的临床研究
2022-02-22陈粉娜孟繁剑郭斯琴
陈粉娜,孟繁剑,郭斯琴
(佛山市中医院眼科,广东 佛山 528000)
角膜缘干细胞是角膜上皮增殖和移行的动力来源,对于维持角膜上皮的完整性至关重要。角膜缘干细胞缺乏,角膜上皮细胞亦缺乏,黏蛋白即分泌不足。角膜缘干细胞缺乏将引起黏蛋白缺乏型干眼(DE)。目前国内外尚缺乏简单易行的泪液黏蛋白检测方法,故黏蛋白型干眼诊断困难。国际上亦没有角膜缘干细胞缺乏的诊断标准,结膜上皮细胞标记、共聚焦显微镜、印迹细胞学等辅助检查被建议用以辅助诊断。研究表明,用前段光学相干断层扫描(AS-OCT)测量中央角膜上皮厚度(CET)的临界值为46.6 μm,可作为临床怀疑角膜缘干细胞缺乏时的初始诊断试验[1]。故应用AS-OCT作为角膜缘干细胞缺乏诊断参数测量DE患者CET。
1 资料与方法
1.1一般资料:选择2020年4月~2020年10月在佛山市中医院眼科门诊确诊的21例(42眼)DE患者作为观察组年龄20~50岁,另选取20例(40眼)正常人作为对照组,年龄20~50岁。观察组42眼中男17眼,女25眼,对照组40眼中男15眼,女25眼。本研究得到佛山市中医院伦理委员会的批准,遵循赫尔辛基宣言的原则。所有对象均获得知情同意书。DE诊断标准:①主诉干涩感、异物感、烧灼感等眼部不适;②采用德国Oculus公司研发的OCULUS Keratograph眼表综合分析仪检查泪膜破裂时间(BUT)<10 s。正常人组一般选择陪患者就诊人员,其纳入标准:无诉眼部不适,既往无眼部疾病,BUT>10 s。剔除和脱落标准:①纳入后发现有不符合纳入标准者;②实验期间不服从研究,因自身原因有退出计划的。
1.2方法:所有研究对象均在知情同意下进行相关检查。两组患者由同一技师在对其诊断设盲情况下应用AS-OCT测量CET1、CET2和CET3。CET测量:OCT最亮的第一层(泪膜)与前弹力层(第二亮层)之间的厚度。三点法[1]:记录最中央及左右两边间隔1 mm一共3个位置的角膜上皮厚度。CET1为左边角膜厚度,CET2为最中央角膜厚度,CET3为右边角膜厚度。见图1。
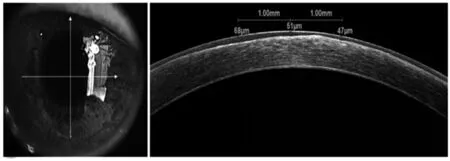
图1 CT测量法及三点法
1.3观察指标:两组的CET1、CET2、CET3分别与临界值46.6 μm比较并组间分别比较。
2 结果
2.1两组一般资料比较:见表1。两组患者性别、年龄通过秩和方差检验,差异无统计学意义(P>0.05),具有可比性。
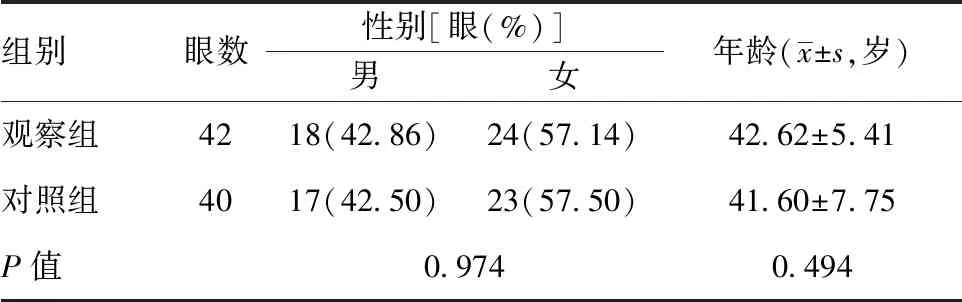
表1 两组对象一般资料比较
2.2两组CET与临界值分别比较:两组CET1、CET2、CET3均与临界值差异有统计学意义(P<0.05),观察组均低于对照组,差异有统计学意义(P<0.05)。

表2 两组CET、CET2、CET3与临界值比较
3 讨论
角膜缘干细胞属于单能干细胞,存在于角膜缘基底细胞层中,人类角膜缘的Vogt栅栏结构即角膜缘干细胞所在区,角膜缘附近丰富的血管网滋养代谢旺盛的干细胞。如果角膜缘干细胞缺乏,上皮创伤将不能愈合,出现持续性的上皮缺损或结膜上皮和新生血管向角膜内生长。角膜缘干细胞是分开角膜和结膜的独特结构,是角膜上皮增殖和移行的动力来源,对于维持角膜上皮的完整性至关重要。角膜缘干细胞缺乏,角膜上皮细胞亦缺乏,黏蛋白即分泌不足。
DE的分类[2]:①水液缺乏型DE:水液性泪液生成不足和(或)质的异常而引起,如Sjogren综合征和许多全身性因素引起的DE;②蒸发过强型DE:由于脂质层质或量的异常而引起,如睑板腺功能障碍、睑缘炎、视屏终端综合征、眼睑缺损或异常引起蒸发增加等;③黏蛋白缺乏型DE:为眼表上皮细胞受损而引起,如药物毒性、化学伤、热烧伤对眼表的损害及角膜缘功能障碍等;④泪液动力学异常型DE:由泪液的动力学异常引起,如瞬目异常、泪液排出延缓、结膜松弛等;⑤混合型DE:是临床上最常见的DE类型,为以上两种或两种以上原因所引起的DE。故角膜缘干细胞缺乏将引起黏蛋白缺乏型DE。
临床上DE的发病率为21%~30%[3],但目前国内外尚缺乏简单易行的泪液黏蛋白检测方法,故黏蛋白缺乏型DE诊断困难。国际上亦没有角膜缘干细胞缺乏的诊断标准,结膜上皮细胞标记、共聚焦显微镜、印迹细胞学等辅助检查被建议用以辅助诊断。Amit Mehtani研究亦表明角膜缘干细胞缺乏患者的角膜和角膜缘上皮厚度比正常人变薄,AS-OCT测量CET可作为诊断角膜缘干细胞缺乏的诊断指标[4]。当DE患者的CET<46.6 μm,可以提示其角膜缘干细胞缺乏,角膜缘干细胞缺乏,角膜上皮细胞亦缺乏,黏蛋白即分泌不足,以此诊断为黏蛋白缺乏型DE。DE与CET两者相辅相成,互相加证,故有此研究。
因为干眼的影响因素包括性别、年龄等。研究过程中发现对检查者要求极高,测量界限相差少许即相差甚远,在层面上下或中间都有差别,在角膜中央及非中央测量均有差别,故要求同一个技师操作,为避免技师存在主观性测量,故对其设盲。
观察组即DE组的中央角膜上皮厚度CET1、CET2、CET3均低于临界值46.6 μm,观察组入组标准为眼干、异物感、烧灼感不适,BUT<10 s,此类患者其实我们不知其DE具体分型,但多半为蒸发过强型DE,因为其BUT<10 s。泪膜由脂质层、水液层及黏蛋白层组成,最里面的黏蛋白层缺乏,即使水液层及脂质层足够,亦不能黏附在黏蛋白层上,泪膜保护层同样缺失,水分仍然蒸发过快,造成DE。所以只要能排除睑板腺功能障碍引起的DE,余BUT<10 s即为黏蛋白缺乏型DE。本研究也证实此类患者有一定程度角膜缘干细胞缺乏,蒸发过强型DE及其黏蛋白缺乏型DE界限难以区别清楚。CET提示角膜缘干细胞缺乏,从另一个角度表示黏蛋白缺乏。
对照组即正常人组的中央角膜上皮厚度CET1、CET2、CET3均高于临界值46.6 μm,再次证明DE患者的中央角膜厚度低。两组间对比直接提示DE患者的中央角膜厚度低,进一步求证CET可作为角膜缘干细胞的诊断参数,辅助诊断黏蛋白缺乏型DE。田潇的综述中表明了AS-OCT测量角膜厚度应用于干眼的诊断,AS-OCT广泛应用于干眼的诊断[5]。
综上所述,AS-OCT CET<46.6 μm可作为角膜缘干细胞缺乏的诊断参数辅助诊断黏蛋白缺乏型DE。但因干眼病因复杂,分型界限较难,特别是蒸发过强型DE及其黏蛋白缺乏型DE缺乏循证区分界限,此研究只是多方位、另角度分析、加证,故黏蛋白缺乏型干眼仍需进一步细节研究。
