牙菌斑pH检测电极技术的研究进展
2022-02-22车会凌胡顺铭林思王瑄黄原源尹伟
牙菌斑生物膜是口腔微生物定植在牙面的形成的口腔微生态,其可引起龋病、牙周病等口腔常见病,因此对牙菌斑的控制是预防龋病的有效途径之一
。牙菌斑环境中多种因子如细菌、糖、酸、钙、氟离子等的检测,都是可以用于其致病力监测的重要途径。牙菌斑原位pH 值是指采用电极直接在牙面菌斑原位测定得到的菌斑pH 值。牙菌斑pH 值与牙硬组织脱矿之间存在着密切的关系,其pH 临界值为5.5 左右
。菌斑原位pH 值检测一直作为其代谢及其个体龋活性检测的有效指标,在龋病预防实践中起重要作用
。体外检测菌斑pH 值准备工作复杂且不能实现连续监测,因此应用牙菌斑pH 检测的电极技术可以有效辅助龋风险的评估。
本文对适用于接触法的牙菌斑原位pH 值检测技术的类别、需求、发展过程、原理、应用进行综述;另外本文将对其他几种非接触法技术进行介绍,为临床龋风险检测技术的选择提供参考。
1 牙菌斑pH 检测电极技术及其发展
牙菌斑pH 检测的电极技术是指在直接测定菌斑pH 值时所采用的pH 电极检测技术
。在近年来在牙菌斑pH 值的动态分析研究中,牙菌斑pH值检测的电极技术作为高效便捷的检测方式被学者们广泛应用。其中,玻璃电极最先被用于菌斑pH 值测定,但其薄弱的玻璃膜在接触法检测牙面pH 值时易损坏,因此相比接触法,该电极多应用于牙菌斑pH 值的体外采样检测以及埋伏电极后的遥感监测
。金属氧化物微电极在使用中可以兼顾性能及强度。氧化锑微电极首先被应用于描述牙菌斑原位pH 值的变化,这之后相继出现氧化钯、氧化铱微电极,但这类电极存在制备工艺复杂、成本较高的问题。离子敏感场效应晶体管灵敏、准确、微小,被广泛应用于埋伏电极法测定牙菌斑pH 值。Sharma 等
研制的牙科pH 光学仪实现了非接触的光学牙菌斑pH 测量,是牙菌斑pH检测技术的一大突破,但该仪器目前的测试结果尚未明确表现其可靠性,应用于研究的案例较少。
现在常用的牙菌斑pH 检测电极已具备响应速度快、测量结果稳定、重现性好、生物无害性以及响应灵敏度高等性能特点,同时这些电极在酸性范围内对pH 值呈线性响应,基本满足应用于人体的电极需求。但牙菌斑的位置、结构特殊,牙邻接点以下等龋易感部位操作空间小,需要体积微小的电极才能实现这些牙菌斑的pH 值检测。然而,缩小体积的同时也存在着技术复杂、成本高昂以及电极易损坏的问题,因此牙菌斑pH 检测电极技术仍旧未能实现在临床上的推广。未来尚需针对这些不足进一步优化电极的制备技术,使牙菌斑pH 值的检测技术的应用不再仅仅局限于实验室,也能辅助临床的龋风险筛查。
2 适用于接触法检测牙菌斑pH 值的电极分类及特点
2.1 微型玻璃电极
微型玻璃电极是最早运用到牙菌斑pH 检测的一种H
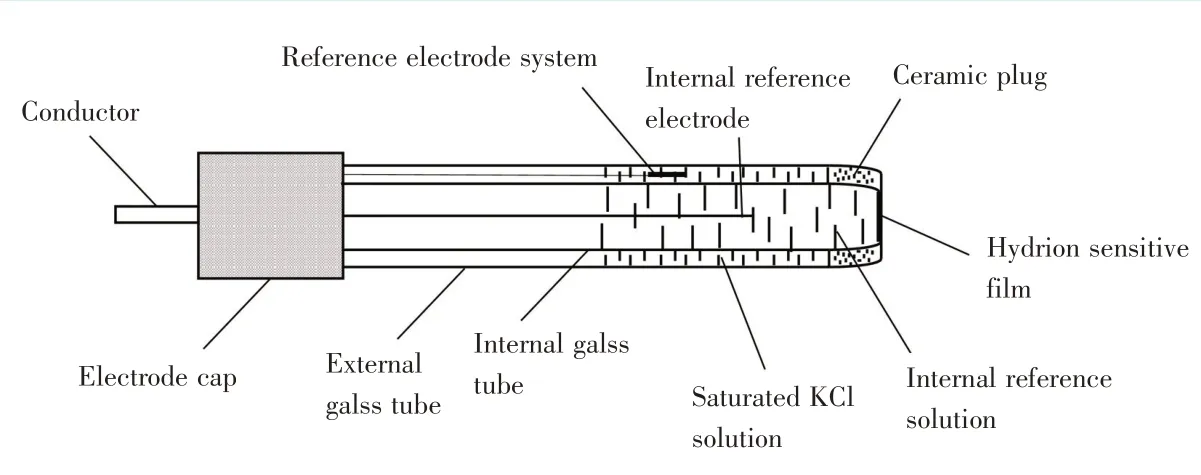
响应性玻璃电极。目前常用的玻璃微电极基本都是复合微电极,不需要额外的参比电极(图1)。该电极主要通过玻璃敏感膜中的Na
与溶液中H
进行交换产生电位差,实现对H
的选择性响应。现有的玻璃微电极线性、敏感性、稳定性较好
,但易折断且响应较慢
。由于在操作中易损,该类电极在检测牙菌斑时主要采用电极埋伏法,而较少应用于接触法
。
从石灰用量对方铅矿矿浆电位影响的试验结果可以得出,随着石灰用量的增加,无论是采用铁介质磨矿,还是瓷介质磨矿,方铅矿矿浆电位都是逐渐上升,但铁介质磨矿时矿浆电位始终低于瓷介质磨矿。这是由于随着CaO用量的增加,方铅矿阳离子水解作用强烈,形成羟基络合物,如公式(2)所示:
金属氧化物电极的制作工艺复杂,其衬底材料的制备主要通过成本较高的高温拉丝技术实现。氧化膜制备方式则主要包括电化学沉积法
、电化学生长
、溅射沉积法
及热处理方法
,其中热处理方法所得电极稳定性最好。为提高电极的性能,复合金属氧化物膜
及复合衬底材料
的制备也成为近年来研究的方向(图3)。
2.2 金属氧化物微电极
该类电极主要利用金属丝表面氧化物对H
的选择性响应产生电位差,从而测量pH 值的大小。以氧化铱微电极为例,氧化铱薄膜对H
的响应方程式如下
:
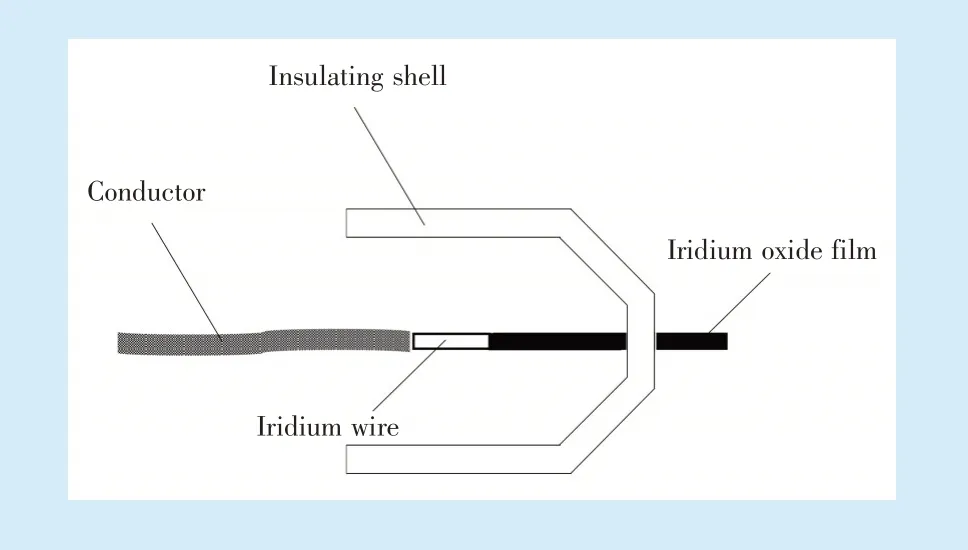
金属氧化物微电极用于弥补微型玻璃电极的强度不足,自20 世纪40 年代初开始被广泛使用。该类电极包括氧化锑、氧化钯和氧化铱电极(图2)。
离子敏感场效应晶体管在检测时需要充分浸入溶液中
,但在应用于接触法检测牙菌斑pH时,该电极的敏感膜无法充分接触菌斑,因此离子敏感场效应晶体管往往通过电极埋伏法监测牙菌斑pH 值的变化(图4)。
离子敏感场效应晶体管通过不同种类的H
离子敏感膜实现对H
的选择性。电解液中的H
可以改变敏感膜的电场分布
,从而实现pH 的测定。由于敏感膜可以替换,该电极也可应用于菌斑中的Na
、K
、Ca
等离子,以及蛋白质
、DNA
等生物大分子的浓度测定。因此,离子敏感场效应晶体管在各个医学领域的推广潜力都极大。
近几年的研究表明,该反应为可逆反应,电极表面氧化膜的均匀性及稳定性可直接影响到该氧化膜与溶液中氢离子的反应速度、反应程度
。现有研究主要致力于制备更加均匀稳定的氧化膜
,以取得更加优良的电极的性能。
由于锑电极会影响到牙菌斑中微生物的正常生长,自氧化钯电极出现后其使用已逐渐减少
。氧化钯微电极灵敏度高、其测试结果不易受干扰,约10 s 左右可响应稳定
。由于氧化铱电极的强度最佳,龋风险检测结果可靠,近几年的相关研究最多。氧化膜均匀的氧化铱电极具有响应较快、线性优良、漂移较小、性能稳定、结果精度优良等优点
。同时铱电极在血液pH 值
、神经电位
测量的领域也表现出优良的性能。
这类电极可以兼顾体积、强度及性能,在龋风险检测技术的临床发展中最具有应用潜力,是近年来研究及发展较为迅速的电极种类。3 种电极中,氧化钯微电极技术最成熟,氧化铱微电极则成为近年来最受欢迎的金属氧化物电极
。虽然该类电极寿命及强度优于微型玻璃电极,但额外需要使用参比电极,以及表面氧化膜易脱落的问题仍局限了该电极的临床推广。因此,金属氧化物电极仍需实现微型复合电极的制备,并增加其氧化膜的结合力。
现有的工艺可实现微米至纳米级的玻璃微电极制备,该电极在心肌
、神经
等的电位测量方面应用较多。但尺寸减小也使电极寿命缩短,许多玻璃微电极只能使用1 次,成本较高,限制了其临床应用。由于其技术相对成熟,目前仅在对pH值精度有较高需求的实验中会有一定的应用。现有研究通过调整敏感膜中的成分
对传统玻璃膜的强度及灵敏性进行改善,也有研究制备材料修饰的玻璃电极
,实现对其性能的改良。
4~7月不同土层土壤温度逐渐升高,5 cm土层深度温度达到30 ℃以上,25 cm土层温度在20 ℃以上,随着土层深度的增加,土壤温度呈下降趋势。5~15 cm土层行间土壤温度明显高于株间温度,20~25 cm行间与株间土壤温度差异较小;7月5 cm土层间作小麦土壤最高温度达到49. 5 ℃,25 cm土层温度达到30℃,高于行间清耕和自然生草,直接影响苹果树根系生长和成活率。

已有关于研究农业机械化水平评价指标的文献中,主要考察的指标是农业机械化程度[3-4]。由于我国畜牧业机械化统计数据的缺失,本文畜牧业机械化水平也通过畜牧机械在畜牧生产过程中的应用程度来反映,因此拟通过加权各家畜种类在畜牧生产过程中的主要关键环节的机械化应用程度来计算其机械化水平。
3 其他非接触法检测牙菌斑pH 值的电极及技术
3.1 离子敏感场效应晶体管
2{[IrO
(OH)
·2H
O]
-·2H
}+2e
+2H
⇋[Ir
O
(OH)
·3H
O]
·3H
+3H
O

排除标准:患者病例资料不完整;接受手术的结肠癌患者为急诊患者;患者有腹部手术史;患者具有家族性多发性息肉;患者合并有肠梗阻;患者具有溃疡性结肠炎;患者合并有其它恶性疾病;患者具有克罗恩病史;对本手术药物过敏或者属于过敏体质的患者。
离子敏感场效应晶体管响应极快,测量值变异系数及漂移程度小
。除此之外,离子敏感场效应晶体管的体积小、可批量制作,其参比电极也集成于同一芯片上,无需额外使用参比电极。这些优势使离子敏感场效应晶体管成为了菌斑pH 值持续监测理想的生物传感器。
离子敏感场效应晶体管目前只能通过埋伏电极法应用于牙面pH 检测。虽然这种监测方式可以灵敏地监测到牙菌斑pH 值波动的数据,但是只能监测单一点位的pH 值,无法在临床上实现对患者全口各个位点的龋风险筛查,因此其临床的推广仍需电极结构及用法的改良。
本栏目主要刊载有关社区医疗、预防、保健、康复、健康教育等方面的学术理论、实践经验、科研成果及学术动态等。按不同的论文格式和内容分为论著、健康管理、医疗实践、综述等子栏目。
3.2 牙科pH 光学仪
Sharma 等
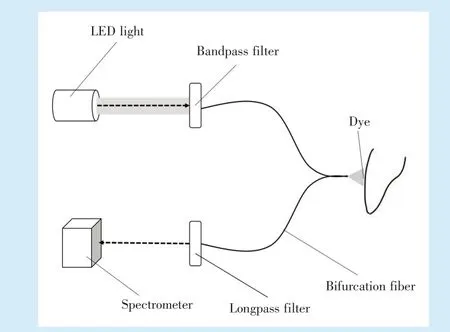
制备的牙科pH 光学仪采用对人体无害的FL 溶液作为染料。该染料中的离子在不同pH 值下发射光谱的不同,可以实现对牙菌斑pH 值的检测。该仪器在口内无接触检测菌斑的pH 值,避免了接触法对菌斑的破坏,并且该仪器在咬合点和缝隙等区域也能测得菌斑pH 值(图5)。牙科pH 光学仪体积小、易操作,可实现多位点测量,值得临床推广。但该种仪器尚处于研发初期,体外测试结果线性较差,染料保留率不足,仍需长期实验以确定该电极可靠性及生物安全性。
“秀花,从咱俩认识到现在将近三年了,这么长的时间,我是个什么样的人,你大概也心里有个数了。你觉得大哥对你够意思吗?”
4 总结与展望
现有的大部分菌斑pH 检测电极技术均存在成本较高、易损坏、工艺复杂等问题,适用于牙菌斑原位pH 检测的电极技术仍需进一步探讨。用于接触法实现牙菌斑原位pH 测量的电极中,由于玻璃电极极易损坏,目前金属氧化物微电极的使用最广泛;离子敏感场效应晶体管微小、灵敏、稳定,适用于埋伏电极法,被应用于遥感监测单一位点的牙菌斑pH 值变化。牙科pH 光学仪作为近年来新诞生的无接触牙菌斑pH 检测技术,在牙菌斑原位pH 检测中应用前景广。未来牙菌斑pH 检测电极技术的主要发展方向包括:进一步提升检测电极的性能,使其微小、耐用、灵敏、稳定;改善牙菌斑pH 检测的操作方式,使其更加便捷、数据化;进一步开发全新的无接触检测技术;另外,现有电极普遍存在的工艺复杂、成本高的问题仍需克服。
Che HL wrote the article. Hu SM, Lin S,Wang X and Huang YY collected the references and revised the article.Yin W reviewed the article. All authors read and approved the final manuscript as submitted.
[1]李雨含,李嘉鑫,张诗铭,等.变异链球菌噬菌体在龋病防治中的研究进展[J]. 口腔疾病防治, 2021, 29(3): 184-188. doi:10.12016/j.issn.2096-1456.2021.03.007.Li YH, Li JX, Zhang SM, et al. Research progress on Streptococcus mutans phages in the prevention of dental caries[J]. J Prev Treat Stomatol Dis, 2021, 29(3): 184 - 188. doi: 10.12016/j.issn.2096-1456.2021.03.007.
[2]Xiao J,Hara AT,Kim D,et al.Biofilm three-dimensional architecture influences in situ pH distribution pattern on the human enamel surface[J]. Int J Oral Sci, 2017, 9(2): 74-79. doi: 10.1038/ijos.2017.8.
[3]Joshi VS, Sheet PS, Cullin N, et al. Real-Time metabolic interactions between two bacterial species using a carbon-based pH microsensor as a scanning electrochemical microscopy probe[J].Anal Chem, 2017, 89(20): 11044-11052. doi: 10.1021/acs.analchem.7b03050.
[4]Garg D, Karuna YM, Srikant N, et al. Evaluation of plaque pH changes following consumption of health drinks by children: a pilot study[J]. J Clin Diagn Res, 2017, 11(5): ZC05-ZC08. doi:10.7860/JCDR/2017/24617.9779.
[5]Wang XL, Cheng CY, Ge CL, et al. Urea rinse effectively neutralises sucrose-induced decrease in plaque pH[J]. Chin J Dent Res,2015,18(3):185-190.
[6]Sharma M, Carson MD, Graham JY, et al. Dental pH Opti-Wand(DpOW): measuring oral acidity to guide enamel preservation[J].Annu Int Conf IEEE Eng Med Biol Soc, 2018: 3738-3741. doi:10.1109/EMBC.2018.8513280.
[7]Nishio Y, Furukawa M, Tateishi I, et al. Development and evaluation of responsive glass for pH electrodes capable of taking measurments from samples as small as 50 μL[J]. Bunseki Kagaku,2019,68(2):103-108.
[8]Smit A, Pollard M, Cleaton-Jones P, et al. A comparison of three electrodes for the measurement of pH in small volumes[J]. Caries Res,1997,31(1):55-59.doi:10.1159/000262375.
[9]Barbic M,Moreno A,Harris TD,et al.Detachable glass microelectrodes for recording action potentials in active moving organs[J].Am J Physiol Heart Circ Physiol, 2017, 312(6): H1248-H1259.doi:10.1152/ajpheart.00741.2016.
[10] Lau PY, Katona L, Saghy P, et al. Long-term plasticity in identified hippocampal GABAergic interneurons in the CA1 area
[J]. Brain Struct Funct, 2017, 222(4): 1809-1827. doi: 10.1007/s00429-016-1309-7.
[11] Sha R,Komori K,Badhulika S.Amperometric pH sensor based on graphene-polyaniline composite[J]. IEEE Sens J, 2017, 17(16):5038-5043.doi:10.1109/JSEN.2017.2720634.
[12] Wang P, Guo T, Zhao T, et al. Effect of oxidization temperatures and aging on performance of carbonate melt oxidized Iridium oxide pH electrode[J]. Sensors (Basel), 2019, 19(21): 4756. doi:10.3390/s19214756.
[13] Zhengwen Zhou et al. pH electrodes based on iridium oxide films for marine monitoring[J]. Trends Environ Anal Chem, 2020, 2020:e00083.doi:10.1016/j.teac.2020.e00083.
[14] Qin Y, Alam AU, Pan S, et al. Low-temperature solution processing of Palladium/Palladium oxide films and their pH sensing performance[J]. Talanta, 2016, 146: 517-524. doi: 10.1016/j.talanta.2015.08.062.
[15] Chaisiwamongkhol K, Batchelor-Mcauley C, Compton RG. Optimising amperometric pH sensing in blood samples: an iridium oxide electrode for blood pH sensing[J].Analyst,2019,144(4):1386-1393.doi:10.1039/c8an02238k.
[16] Cork SC,Eftekhar A,Mirza KB,et al.Extracellular pH monitoring for use in closed-loop vagus nerve stimulation[J]. J Neural Eng,2018,15(1):016001.doi:10.1088/1741-2552/aa8239.
[17] Zhu ZJ, Liu XY, Ye ZN, et al. A fabrication of Iridium oxide film pH micro-sensor on Pt ultramicroelectrode and its application on in-situ pH distribution of 316L stainless steel corrosion at open circuit potential[J]. Sens Actuators B Chemdoi: 10.1016/j.snb,2017(255):1974-1982.
[18] Zhang X, Ye Y, Kan YT, et al. A new electroplated Ir/Ir(OH)xpH electrode and its application in the coastal areas of Newport Harbor, California[J]. Acta Oceanologica Sinica, 2017, 36(5): 99-104.doi:10.1007/s13131-017-1064-5.
[19] Huang F,Wan Z,Jin Y,et al.The effects of cyclic isothermal oxidation on Ir/IrO pH electrode and a method to correct the potential drift of metal oxide electrode[J]. J Electrochem Soc, 2017, 164(13):B632-B640.
[20] Jovic M,Hidalgo-Acosta JC,Lesch A,et al.Large-scale layer-bylayer inkjet printing of flexible iridium-oxide based pH sensors[J].J Electroanal Chem, 2017 (819): 384-390. doi: 10.1016/j.jelechem.2017.11.032.
[21] Zea M, Moya A, Fritsch M, et al. Enhanced performance stability of iridium oxide-based pH sensors fabricated on rough inkjet-printed platinum[J]. ACS Appl Mater Interfaces, 2019, 11(16): 15160-15169.doi:10.1021/acsami.9b03085.
[22] Alam AU,Qin Y,Nambiar S,et al.Polymers and organic materialsbased pH sensors for healthcare applications[J]. Progress Mater Sci,2018,96(3):174-216.doi:10.1016/j.pmatsci.2018.03.008.
[23] Briggs EM,Sandoval S,Erten A,et al.Solid state sensor for simultaneous measurement of total alkalinity and pH of seawater[J].ACS Sens, 2017, 2(9): 1302 - 1309. doi: 10.1021/acssensors.7b00305.
[24] Ma S, Li X, Lee YK, et al. Direct label-free protein detection in high Ionic strength solution and human plasma using dual-gate nanoribbon-based ion-sensitive field-effect transistor biosensor[J].Biosens Bioelectron, 2018, 117: 276 - 282. doi: 10.1016/j.bios.2018.05.061.
[25] Imaizumi Y, Goda T, Schaffhauser DF, et al. Proton-sensing transistor systems for detecting ion leakage from plasma membranes under chemical stimuli[J].Acta Biomater, 2017,50:502-509.doi:10.1016/j.actbio.2016.12.018.
