丹酚酸A对诱导Aβ42聚集的干预作用研究
2022-02-19刘美艳李学波魏鸿潘晓丽
刘美艳 李学波 魏鸿 潘晓丽
(成都中医药大学药学院,成都 611137)
阿尔茨海默病(alzheimer disease,AD)是一种老年痴呆最常见的形式,由于慢性退行性神经系统而导致的疾病,尤其好发于老年人当中[1-3]。AD的病死亡率很高,仅次于心血管疾病和癌症,不仅给患者带来了巨大的伤痛,同时给患者家属带来了沉重的经济负担[4]。然而不幸的是到目前为止,AD的发病原因尚无定论,人们也还未找到治疗AD的特异性药物和方法。目前,关于AD有多种发病机理假说[5-11],很多病理学和基因证据支持淀粉样蛋白假说。AD患者脑内老年斑的主要成分是β-淀粉样蛋白(amyloid β-protein, Aβ) ,其聚集会产生细胞毒性,从而损伤神经细胞,最终导致患者出现认知功能障碍、记忆力衰退等临床现象[12-14]。近年来,通过Aβ为靶点治疗AD已成为研究热点[15]。
科研人员尸检时发现老年斑中金属离子含量异常,其含量远远超过正常人,并且发现金属离子如Zn2+和Cu2+等在体外能促进Aβ的聚集[16-17]。金属离子稳态假说认为大脑中金属离子紊乱会影响AD的病理进程。由于Aβ上具有金属螯合位点, 而AD患者脑内的金属离子含量高于正常人,因此许多金属离子如Fe3+、Cu2+、Zn2+和Al3+等都能与Aβ结合形成Aβ-金属复合物。因此,通过调节脑内金属离子平衡可能成为治疗AD的方向之一[18]。
近年来,丹参作为传统中药,其主要活性成分如醌类和酚酸类或与其他中药配伍的方剂都能明显改善AD症状[19-21]。丹酚酸A是从唇形科鼠尾草属植物丹参(Salvia miltiorrhiza Bunge)中提取分离得到的一种酚酸类活性成分[22]。本文基于淀粉样蛋白联级假说和金属离子稳态假说,利用ThT荧光实验探究金属Zn2+对Aβ聚集的影响,以及丹酚酸A对Zn2+诱导Aβ聚集的干预作用;同时在体外合成丹酚酸A金属配合物,并对其进行结构表征,研究其可能的配位情况。希望通过本研究为探索中药丹参治疗AD的作用机制奠定基础。
1 仪器与试剂
1.1 仪器
TDZ5-WS型多管架自动平衡离心机购自湖南湘仪仪器开发有限公司;BP211D型电子分析天平购自德国Sartorius公司;A560型双光束紫外可见分光光度计购自翱艺仪器有限公司;DF-101S型集热式恒温加热磁力搅拌器购自成都市国伟科技有限公司;全自动酶标仪购自Thermo公司;Tensor-27型傅立叶变换中红外光谱仪购自Bruker公司;DZF型真空干燥箱购自北京科伟永兴仪器有限公司;移液枪、96孔板购自成都胜拓仪器有限公司; AM-600型超导核磁共振购自Bruker公司。
1.2 试剂
六氟异丙醇、乙酸锌、硫黄素T购自上海麦克林生化科技有限公司;氘代DMSO购自上海泰坦科技股份有限公司;Aβ42购自上海吉尔生化有限公司;丹酚酸A购自成都普思生物科技有限公司(纯度大于98%);色谱甲醇购自诺尔施公司;Herpes缓冲液购自北京索莱宝科技有限公司;无水乙醇购自成都科隆有限公司。
2 样品溶液的配制
2.1 Aβ42单体化
将Aβ42溶于六氟异丙醇中配成1 mmol/L清澈透明的溶液,然后置于通风厨内让六氟异丙醇自然挥发12 h,而后真空冷冻干燥4 h后于-20℃储存[23]。
2.2 Aβ42及各待试样品溶液的配制
HFIP处理后的Aβ42用适量的DMSO完全溶解,随后用Herpes缓冲液(0.1 mol/L, pH7.4)稀释至所需浓度;1 mmol/L金属Zn2+和丹酚酸A母液均用DMSO配制;5 mmol/L ThT母液用Herpes缓冲液(0.1 mol/L,pH7.4)配制,避光保存,实验时使用上述Herpes缓冲液稀释。
3 ThT荧光实验
3.1 研究金属Zn2+对Aβ42聚集的影响
配制一系列Aβ42浓度恒定而金属Zn2+浓度不同的溶液。具体步骤:将Aβ42溶液分别与不同浓度的金属Zn2+溶液混合,于37℃恒温箱中共同孵育48 h。
3.2 研究丹酚酸A对Aβ42聚集的影响
配制一系列Aβ42浓度恒定而丹酚酸A浓度不同的溶液。具体步骤:将Aβ42溶液分别与不同浓度的丹酚酸A溶液混合,于37℃恒温箱中共同孵育48 h。
3.3 研究丹酚酸A对金属Zn2+诱导的Aβ42聚集的影响
配制一系列Aβ42和金属Zn2+浓度恒定而丹酚酸A浓度不同的溶液。具体步骤:将Aβ42和金属Zn2+溶液混合,于37℃恒温箱中共同孵育5 min,加入不同浓度的丹酚酸A溶液,继续置于37℃恒温箱中孵育48 h。
3.4 研究丹酚酸A对Aβ42聚集体解聚的影响
配制一系列Aβ42浓度恒定而丹酚酸A浓度不同的溶液。具体步骤:将Aβ42溶液放置于37℃恒温箱中孵育48 h,形成聚集体,随后加入不同浓度的丹酚酸A溶液,继续置于37℃恒温箱中孵育48 h。
3.5 研究丹酚酸A对金属Zn2+诱导的Aβ42聚集体解聚的影响
配制一系列Aβ42和金属Zn2+浓度恒定而丹酚酸A浓度不同的溶液。具体步骤:将Aβ42和金属Zn2+溶液混合,于37℃恒温箱中共同孵育48 h,形成聚集体,随后加入不同浓度的丹酚酸A溶液,继续置于37℃恒温箱中孵育48 h。
上述孵育液孵育好后,取20 μL至黑色96孔板中,加入180 μL硫黄素T溶液(5 μmol/L),同时设置3个复孔。最后,用多功能酶标仪测量荧光吸收值,设定激发波长450 nm,发射波长482 nm,记录5 min末的荧光强度。
4 金属配合物的合成
准确称取丹酚酸A 49.4 mg(0.1 mmol)溶于5 mL无水乙醇中,在磁力搅拌器中溶解,待丹酚酸A完全溶解后滴加含有21.95 mg乙酸锌(0.1 mmol)的无水乙醇溶液,反应液随着乙酸锌溶液的滴加逐渐从淡黄色变为黄绿色,同时反应液变浑浊,继续在室温下搅拌反应1 h,静置一段时间后有沉淀,沉淀离心,再用无水乙醇洗涤数次直至上清液变为无色,产物于35℃真空干燥,得黄绿色粉末状固体产物,称重,W=实际重量,W0=理论重量,计算配合物产率。
产率(%)=W/W0×100%
5 统计学方法
实验所得数据均用SPSS 20.0进行单因素方差分析,并且比较组间差别,当P<0.05判定为有统计学意义。根据Aβ42蛋白的荧光值来描述金属Zn2+和丹酚酸A对Aβ42聚集的影响。
6 结果与讨论
6.1 ThT荧光实验结果
6.1.1 金属Zn2+对Aβ42聚集的影响
本研究结果显示,随着金属Zn2+浓度增加,Aβ42的荧光值逐渐升高。具体结果见图1。
6.1.2 丹酚酸A对Aβ42聚集的影响
本研究结果显示,随着化合物丹酚酸A浓度增加,Aβ42的荧光值逐渐降低。具体结果见图2。
6.1.3 丹酚酸A对金属Zn2+诱导的Aβ42聚集的影响
本研究结果显示,随着化合物丹酚酸A浓度增加,金属Zn2+诱导Aβ42聚集的荧光值逐渐降低。具体结果见图3。
6.1.4 丹酚酸A对Aβ42聚集体解聚的影响
本研究结果显示,随着化合物丹酚酸A浓度增加,Aβ42聚集体的荧光值逐渐降低。具体结果见图4。
6.1.5 丹酚酸A对金属离子诱导的Aβ42聚集体解聚的影响
本研究结果显示,随着化合物丹酚酸A浓度增加,金属Zn2+诱导Aβ42聚集体的荧光值逐渐降低.具体结果见图5。
6.2 配合物的表征
6.2.1 配合物的一般性质
丹酚酸A-Zn(Ⅱ)配合物收率为53.47%。丹酚酸A-Zn(Ⅱ)配合物与丹酚酸A及乙酸锌相比较,外观颜色和性质都发生了显著的变化。丹酚酸A-Zn(Ⅱ)配合物粉末颜色为黄绿色,难溶于丙酮、乙醚、三氯甲烷和乙酸乙酯等极性小的试剂,微溶于甲醇,溶于DMSO。
6.2.2 紫外光谱
本研究结果显示,在200~600 nm范围内对丹酚酸A和丹酚酸A-Zn(Ⅱ)配合物进行UV-vis 扫描分得到紫外吸收光谱(表1)。丹酚酸A的紫外吸收光谱中,205 nm为苯环的E带吸收,289 nm为苯环的K带吸收。丹酚酸A-Zn(Ⅱ)配合物的紫外光谱中仍有2个主要吸收峰。具体结果见表1。

表1 丹酚酸A及其金属配合物的UV(nm)主要数据Tab.1 UV (nm) main data of salvianolic acid A and its metal complexes
6.2.3 红外光谱
本研究结果显示,在400 cm-1~4000 cm-1范围内对丹酚酸A和丹酚酸A-Zn(Ⅱ)配合物进行扫描得到红外光谱主要特征峰。具体结果见表2。
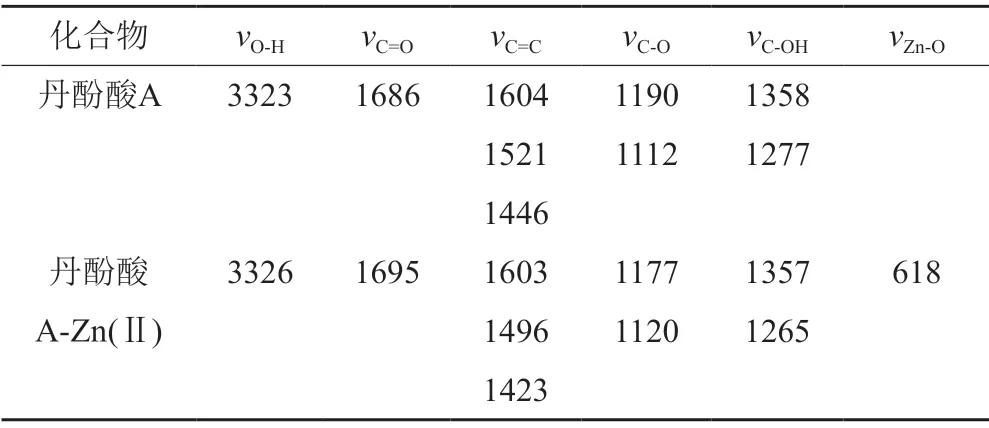
表2 丹酚酸A及其金属配合物的IR(cm-1)主要数据Tab.2 Main data of IR (cm-1) of salvianolic acid A and its metal complexes
6.2.4 核磁共振氢谱
本研究结果显示,丹酚酸A及其金属配合物的核磁共振氢谱(表3)。由数据可见,金属配合物相比于丹酚酸A,其核磁共振氢谱发生了少许变化。具体结果见表3。
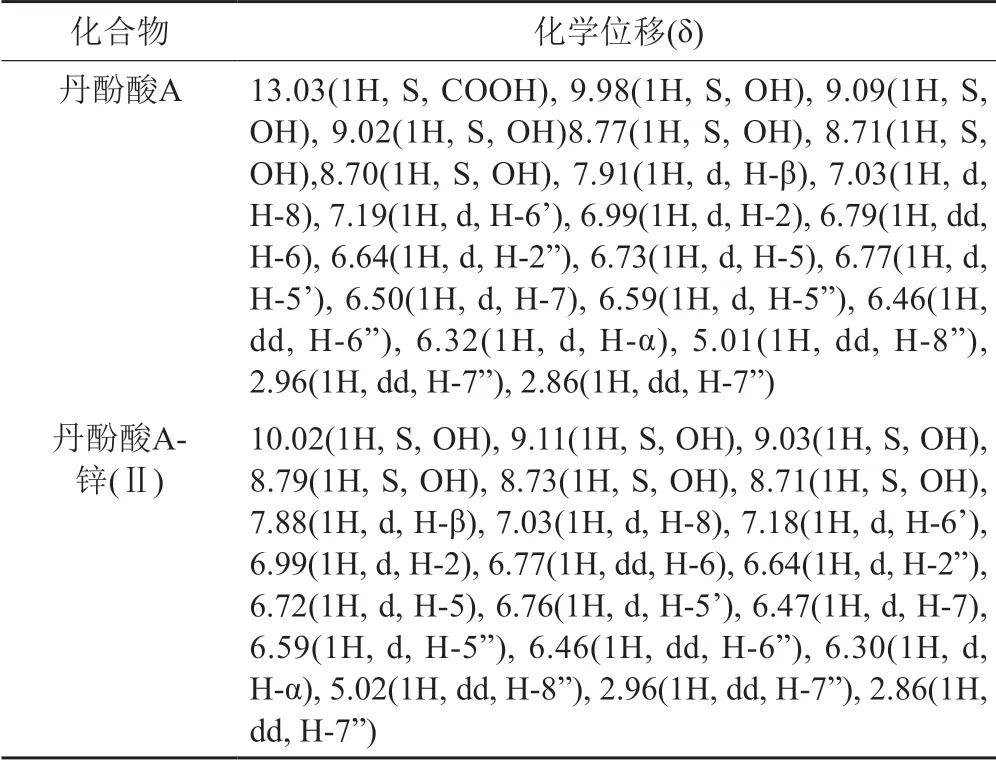
表3 丹酚酸A及其金属配合物的1H NMR 的数据(DMSO-d6)Tab.3 1H NMR data of salvianolic acid A and its metal complexes (DMSO-d6)
由参考文献[24]和以上结构表征结果,可推测金属配合物可能结构式:1分子丹酚酸A与1分子金属Zn2+通过丹酚酸A的羧基和羧基邻位的苯环形成配合物(图6)。
6.3 讨论
许多文献已证明金属离子能加速Aβ的聚集[25-26],通过本次ThT荧光实验的结果,可推断金属Zn2+能快速诱导Aβ42的聚集,并且其促进作用呈现剂量依赖性,符合文献所报道的。许多天然产物如杨梅素、槲皮素等,不仅自身能抑制Aβ的聚集,而且还能和金属离子络合从而抑制金属离子诱导Aβ的聚集,具有双靶点同时抑制作用[27-28]。丹酚酸A为酚酸类天然产物,通过本次ThT荧光实验初步显示丹酚酸A不仅能明显抑制Aβ42的聚集,而且可以明显促进Aβ42聚集体的解聚,并且其抑制作用和解聚作用均呈剂量依耐性;同时,丹酚酸A和Aβ42竞争性的络合金属Zn2+,从而抑制金属Zn2+诱导Aβ42的聚集和促进金属Zn2+诱导Aβ42聚集体的解聚。
紫外吸收峰的形状基本保持不变,但吸收峰的位置发生了一定程度的红移,表明配合物形成的同时没有破坏丹酚酸A的共轭结构[29]。峰位移动的原因可能是:丹酚酸A与金属Zn2+形成配合物后, 整个分子中电子的离域程度增大, 致使电子跃迁时需要的能量降低, 使吸收峰发生红移[30]。
在红外吸收光谱中丹酚酸A-Zn(Ⅱ)配合物的羧酸羰基吸收峰相比于丹酚酸A发生了一定程度的红移,而且吸收强度明显减弱,可能是配合物中配位作用使 C=O键作用力减弱,从而使电子云密度减少,表明羧基参与了配位成键[30]。芳环骨架振动频率为1450 cm-1、1600 cm-1,丹酚酸A和丹酚酸A-Zn(Ⅱ)配合物在此区域内均出现吸收峰。然而丹酚酸A-Zn(Ⅱ)配合物的苯环吸收峰相比丹酚酸A发生了小幅度的蓝移,吸收强度明显减弱 ,并且从参考文献[24]可知分子的空间结构上离配位点最近的苯环或双键是最重要的影响因素,苯环的影响力要大于直链双键,由苯环参与的配位更加稳定,说明苯环参与了配位反应。同时丹酚酸A-Zn(Ⅱ)配合物在低频区600 cm-1左右出现了一个新的弱吸收峰,表明氧原子与金属Zn2+形成了Zn—O配位键[31]。
配合物和丹酚酸A1H NMR 中均有六个酚羟基信号,只是化学位移有不同程度的变化,可能是受配位作用的影响。丹酚酸A1H NMR 中δ13.03(1H,S)为羧基的活泼氢信号[32],然而配合物的氢谱中未见此羧基氢的信号峰,表明羧基参与了配位反应。
因此,通过本次实验得到的结果以及以往的文献,可推测丹酚酸A-Zn(Ⅱ)配合物可能结构式为1分子丹酚酸A与1分子金属Zn2+通过丹酚酸A的羧基和羧基邻位的苯环形成配合物。
7 结论
本实验基于淀粉样蛋白学说和金属离子稳态学说,采用ThT荧光法得出中药丹参药效成分丹酚酸A对Aβ42以及金属Zn2+诱导Aβ42的聚集均有抑制作用,并且对Aβ42以及金属Zn2+诱导Aβ42的聚集体均有解聚作用。体外模拟丹酚酸A和金属Zn2+的络合方式,并采用紫外光谱、红外光谱、核磁共振氢谱对丹酚酸A-Zn(Ⅱ)配合物进行结构表征,研究其可能的配位结构。我们在对丹参大量化合物进行活性筛选的基础上,发现丹酚酸A具有双靶点同时抑制作用,因此希望通过本次实验能为探索中药丹参治疗AD的作用机制奠定基础。
