卵母细胞来源对水牛体细胞核移植胚胎发育潜能的影响
2022-02-15李玲玉郑海英陈明棠唐丽萍尚江华杨春艳
李玲玉,郑海英,陈明棠,唐丽萍,尚江华,杨春艳
(中国农业科学院广西水牛研究所,农业农村部水牛遗传与繁育技术重点实验室,南宁530001)
在过去的10年中,水牛作为一种乳肉兼用的经济型家畜受到了越来越多的关注,尤其是奶水牛产业的发展使水牛的开发和利用迈入了一个新阶段。然而,水牛繁殖周期长、繁育率普遍较低,严重制约了水牛产业的发展。近年来,科学家们尝试使用不同的辅助生殖技术(ART)提高水牛的繁殖效率,包括性别控制、活体采卵(OPU)、体外受精(IVF)、体外胚胎生产(IVEP)、体细胞核移植(SCNT)和徒手克隆[1-4]等技术。其中,SCNT可充分利用丰富的沼泽型水牛卵巢,其卵母细胞可作为核移植的受体,采集并培养具有优良遗传基因的河流型水牛体细胞作为核移植的供体,在短期内可生产大量的优秀河流型水牛[4]。
在家畜上,关于屠宰场(SLH)和活体采卵来源卵母细胞体外受精及体外胚胎生产结果并不完全一致。水牛活体采卵-体外受精胚胎的囊胚率显著高于屠宰场卵巢-体外受精胚胎,但其分裂率无显著差异[5],黄牛活体采卵-体外受精胚胎的囊胚率显著低于屠宰场卵巢组[6]。对山羊的研究发现,活体采卵和屠宰场来源卵母细胞不影响其体外成熟率、受精胚胎的分裂率及囊胚率[7]。此外,在体外胚胎生产研究中发现,囊胚中的E-钙黏蛋白(E-cadherin)可介导细胞黏着和胞外信号到胞质的传递,且作为一种依赖Ca2+的细胞黏连糖蛋白,在早期胚胎发育过程的细胞识别、迁移和组织分化中具有关键作用[8],常被用以预测早期胚胎发育。而转录因子Sox2是胚胎发育的先锋因子,在早期胚胎的内细胞团中表达,因此Sox2标志着早期胚胎发育的发生[9]。目前,SCNT的受体卵母细胞主要来源为屠宰场卵巢,多为淘汰的低繁殖性能或高龄母水牛,其卵母细胞质量较差,而活体采卵技术可反复从适龄的良种河流型水牛体内得到优质的卵母细胞用于SCNT[10]。本实验室已通过SCNT技术先后培育了30余头克隆水牛[11-12]。然而,与屠宰场来源卵巢相比,通过活体采卵技术获得的卵母细胞数量有限,在一定程度上会限制SCNT的应用。因此,本研究拟将屠宰场卵巢和活体采卵来源的卵母细胞体外成熟培养后用于SCNT,比较SCNT重构胚的融合率、分裂率、囊胚率及胚胎发育潜能相关蛋白E-cadherin和Sox2的表达水平,以探明卵母细胞来源对SCNT重构胚发育能力及发育潜能关键蛋白表达水平的影响。
1 材料与方法
1.1 主要试剂及仪器
TCM199、牛血清白蛋白(BSA)、4-羟乙基哌嗪乙磺酸(HEPES)缓冲液、表皮生长因子(EGF)和胎牛血清(FBS)均购自Gibco公司;卵泡刺激素(FSH)、黄体生成素(LH)、雌二醇(E2)、丙酮酸钠、半胱氨酸、细胞松弛素B等均购自Sigma公司;35 mm培养皿、载玻片及盖玻片等耗材均购自Thermo Fisher公司;兔源E-cadherin(ab16505)、鼠源Sox2(ab97959)一抗及Hochest 33342购自Abcam公司;山羊抗兔IgG H&L、山羊抗鼠IgG H&L二抗均购自Bioworld公司。试验需用的主要仪器包括超声波活体采卵仪(2100,TOKYO公司)、集卵杯(CCA-200,富士平公司)、体视显微镜(DM750,莱卡公司)、纺锤体观察仪(CRI,Nikon公司)、倒置显微镜(TE200-S,Nikon公司)、电融合仪(ECM-2001,BTX公司)、二氧化碳培养箱(Heracell VIOS V160i,Thermo公司)、激光共聚焦显微镜(Nikon A1,Nikon公司)。
1.2 卵母细胞的采集
试验共分为2组,分别为活体采卵组(OPU组)和屠宰场卵巢组(SLH组)。OPU组所用10头非泌乳期尼里-拉菲水牛供体来自广西水牛研究所种畜场,年龄、营养状况和饲养条件一致,年龄(6.40±0.65)岁,体重(602.0±80.0)kg。利用B超或内窥镜监测并穿刺水牛卵巢上的可见卵泡,进行活体采卵,具体操作参照Liang等[13]所述方法。SLH组所用屠宰场尼里-拉菲水牛卵巢来自广西南宁屠宰场,当天宰杀取得的新鲜卵巢置于37 ℃生理盐水中保存,2~3 h运回实验室,用连接有10 mL注射器的17号针头抽吸所有3~8 mm卵泡,收集的卵泡液在体视显微镜下挑选包裹3层以上卵丘细胞的卵丘-卵母细胞复合体(COCs)。
1.3 SCNT重构胚的构建
1.3.1 卵母细胞体外成熟 挑选包裹2层及以上卵丘细胞的COCs,每10~20枚COCs放入覆盖石蜡油的40 μL体外成熟培养液(TCM199+10% FBS+5 μg/mL FSH+10 μg/mL LH+0.2 mmol/L丙酮酸钠+1 μg/mL E2+50 μmol/L半胱氨酸+25 ng/mL EGF)微滴中,38.5 ℃、5% CO2、饱和湿度的条件下培养22~24 h。卵母细胞成熟以排出第一极体为标志。
成熟率(%)=排出第一极体卵母细胞数/入孵总卵母细胞数×100%
1.3.2 供体细胞复苏培养 从液氮中取出冻存的水牛耳纤维细胞,37 ℃水浴解冻后,加入2 mL细胞培养液(DMEM+10% FBS)混匀,2 500 r/min离心5 min,细胞沉淀用细胞培养液重悬,接种至40 μL微滴中继续培养,每24 h换液。待细胞长至40%~50%,更换为含0.5% FBS的DMEM培养液进行血清饥饿处理3~5 d,用0.25%胰蛋白酶进行消化,1 500 r/min离心5 min收集细胞用于SCNT。
1.3.3 重构胚的融合和激活 COCs成熟后,用移液枪反复吹吸去除COCs周围的卵丘细胞。挑选具有第一极体的卵母细胞并将其移入去核液(TCM199+10% FBS+7.5 μg/mL细胞松弛素B)中,利用纺锤体观测仪进行精确去核,然后沿着去核时留下的透明带切口将单个供体细胞注入卵母细胞的卵周间隙,使之与卵母细胞紧密接触,获得SCNT重构胚。将SCNT重构胚移至融合液(250 mmol/L山梨醇+0.1 mmol/L醋酸钙+0.5 mmol/L醋酸镁+0.5 mmol/L HEPES+0.1% BSA)中清洗2次后,转入含融合液的1 mm3融合槽内,拨动重构胚使卵母细胞与体细胞的接触面与电流方向垂直,施加2次电脉冲(1 kV/cm,10 μs)进行电融合。电融合后,将重构胚移入胚胎培养液(TCM199+10% FBS)中,在38.5 ℃、5%CO2、饱和湿度条件下的培养箱中培养30 min,体视显微镜下观察卵周隙,未见体细胞则视为融合成功。
融合后的重构胚用5 μmol/L离子霉素激活处理5 min,然后用2 mmol/L的二甲氨基嘌呤(dimethylaminopurine,6-DMAP)培养3~4 h。激活的重构胚转移到含有单层颗粒细胞的40 μL培养液微滴中,在38.5 ℃、5%CO2、饱和湿度条件下培养,每2 d换液1次,培养48 h,观察并统计重构胚的分裂率,5~8 d观察并统计囊胚率。
1.4 E-cadherin和Sox2蛋白免疫荧光检测
发育至7 d的SCNT重构胚用PBS清洗3次,在室温下于4%多聚甲醛溶液中固定30 min,PBST(含0.1% Tween-20的PBS)清洗3次,5 min/次,而后转移到含有0.1% Triton X-100的渗透液中通透30 min,用PBST清洗后移入封闭液(PBST+5% BSA)中室温封闭1 h,PBST清洗后转移到一抗(E-cadherin 1∶250,Sox2 1∶200)中,阴性对照组不孵育一抗,置于湿盒中4 ℃孵育过夜;PBST清洗后转入二抗(山羊抗兔IgG H&L,1∶1 000,山羊抗鼠IgG H&L,1∶1 000)中室温孵育2 h,PBST清洗后移入10 μg/mL的Hoechst 33342中进行核复染15 min,PBST清洗后转入玻片上少量的抗淬灭剂微滴中,用盖玻片覆盖固定,在激光共聚焦显微镜下观察并拍照。利用Image J v1.8.0软件对其荧光强度进行分析,用平均荧光强度半定量表征特异性蛋白E-cadherin及Sox2的表达。
1.5 数据统计与分析
用SPSS 17.0软件进行单因素方差分析(One-Way ANOVA),结果以平均值±标准差表示,P<0.05表示差异显著。
2 结 果
2.1 不同来源卵母细胞体外成熟效果
由表1可知,OPU组卵母细胞体外成熟率显著高于SLH组(P<0.05)。

表1 各组卵母细胞体外成熟率
2.2 不同来源卵母细胞对SCNT重构胚发育潜能的影响
由表2、图1可知,OPU组SCNT重构胚的融合率和分裂率与SLH组相比差异均不显著(P>0.05),囊胚率显著高于SLH组(P<0.05)。

表2 各组SCNT重构胚的融合率、分裂率和囊胚率

图1 各组SCNT重构胚不同发育阶段的状态(200×)Fig.1 State of SCNT reconstructed embryos at different developmental stages in each group (200×)
2.3 不同来源卵母细胞SCNT胚胎E-cadherin和Sox2蛋白表达水平
由图2可知,E-cadherin蛋白定位于细胞膜上,Sox2蛋白分布在细胞核膜及细胞质中。由图3可知,OPU组SCNT胚胎E-cadherin和Sox2蛋白的平均荧光强度均显著高于SLH组(P<0.05)。
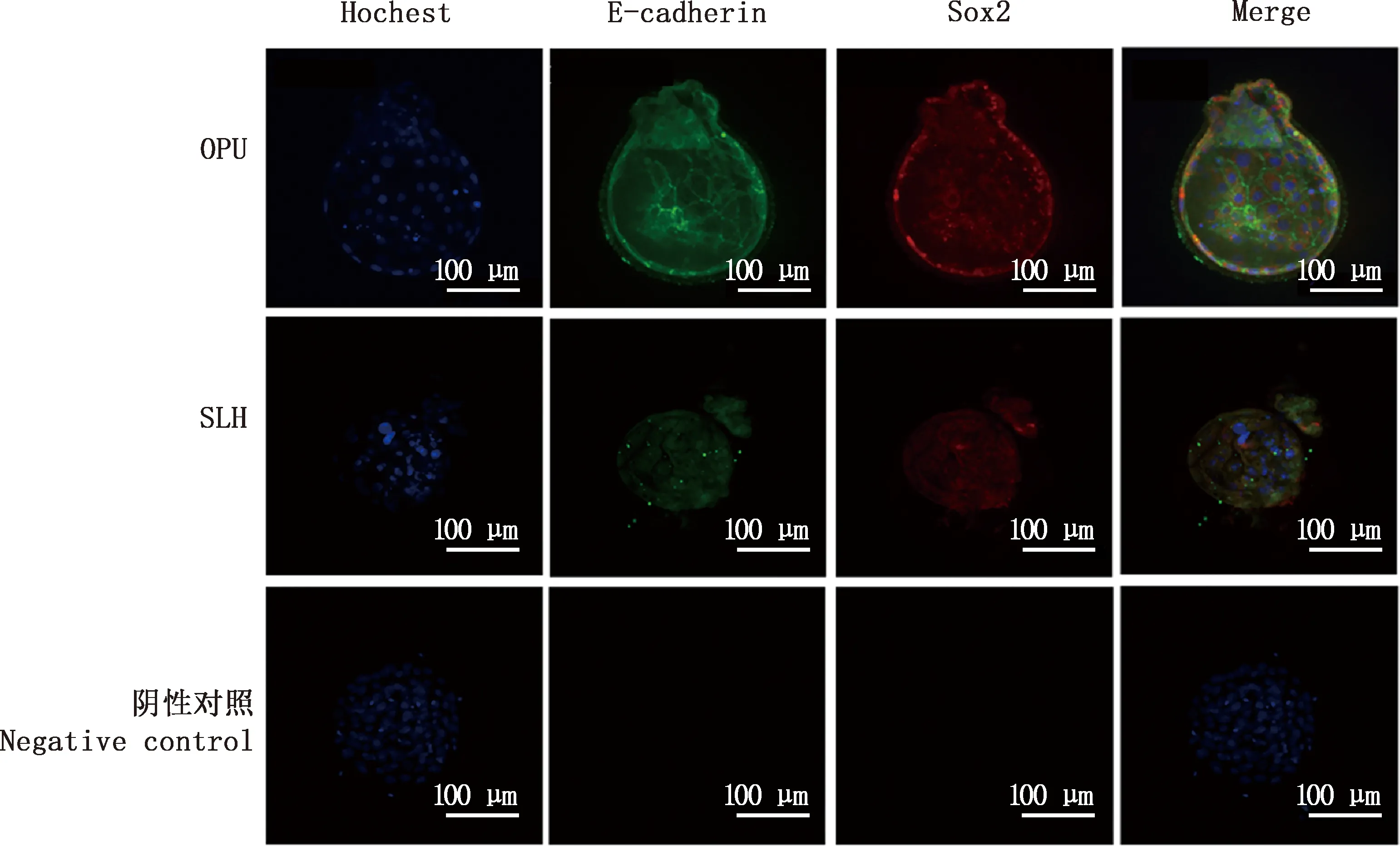
图2 各组SCNT重构胚E-cadherin及Sox2蛋白免疫荧光检测(400×)Fig.2 Imunofluorescence detection of E-cadherin and Sox2 proteins of SCNT reconstructed embryos in each group (400×)
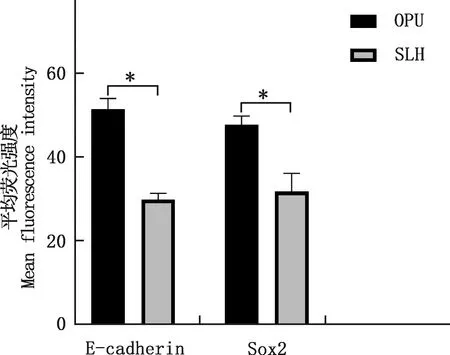
*,差异显著(P<0.05)*,Significant difference (P<0.05)图3 各组SCNT重构胚E-cadherin及Sox2蛋白的平均荧光强度Fig.3 Mean fluorescence intensity of E-cadherin and Sox2 of SCNT reconstructed embryos in each group
3 讨 论
体细胞核移植在科学研究和遗传繁育应用方面均具有重要意义,但目前体细胞克隆效率较低,其应用受到了很大的限制。在体细胞核移植中,卵母细胞作为受体可以为供体核遗传物质的重编程提供材料,同时为胚胎的进一步发育提供所需的营养物质[14-15],因此卵母细胞的质量被认为是影响SCNT效率的一个关键因素。有研究表明,利用活体采卵穿刺母牛卵泡获得的卵母细胞,在体外成熟24 h的成熟率[16]、体外受精后的胚胎分裂率和囊胚率[17]均显著高于屠宰场卵巢卵母细胞。本研究结果显示,OPU组获得的卵母细胞体外成熟率显著高于SLH组,SCNT胚胎的囊胚率也显著高于SLH组,此结果与黄牛不同来源卵母细胞的体外受精胚胎发育效率[8,17]相似。这可能是由于每周2次的活体采卵,致使卵巢卵泡发育波反复重置并增加了卵泡发生波的频率[18-19],使更多的原始卵泡发育成为成熟卵泡,且活体采集操作会在卵泡闭锁前将卵母细胞吸出,减少了成熟卵泡的闭锁,从而提升了活体采集卵母细胞的质量。相比于活体牛卵巢的繁殖性能状态,屠宰场的水牛多为淘汰母牛,卵巢繁殖性能相对低下,且卵巢处于的卵泡发生波阶段不定,导致活体采集卵母细胞的质量高于屠宰场来源卵母细胞,从而影响之后的胚胎发育能力。
本研究利用免疫荧光技术检测了不同来源卵母细胞SCNT胚胎的E-cadherin和Sox2蛋白表达水平,发现OPU组SCNT胚胎中的E-cadherin和Sox2表达水平均高于SLH组SCNT胚胎。E-cadherin蛋白是一种黏附连接蛋白,在细胞与细胞间的黏附连接、紧实连接及细胞核形成中起着关键作用[20-21],且可以作为细胞信号传导的重要调节剂,维持细胞及胚腔结构的完整性[22]。有研究表明,健康囊胚中E-cadherin蛋白大量表达,其低表达水平会导致胚胎在致密化过程中产生极性,抑制胚胎细胞的分化,从而引起胚胎发育能力低下,甚至发育停滞[22-23]。Sox2蛋白是胚胎发育的先锋转录因子,对维持胚胎干细胞(ES)多能状态起关键作用[12]。在哺乳动物早期胚胎发育过程中,Sox2转录因子是内细胞团的形成标志[12,24],也是早期胚胎发育发生的标志。前人的研究发现,Sox2定位于细胞核中,在胚胎发育的2-细胞期合子基因组中表达,且桑椹胚期和囊胚期之间的表达显著增加[25]。利用基因编辑手段全身性敲除Sox2会致死胚胎[12],条件性敲除Sox2会影响胚胎干细胞的特性,同时抑制了胚胎干细胞的增殖[26],而在减数分裂的卵母细胞中敲除Sox2,并不会影响卵母细胞的形成[27],说明Sox2对于卵母细胞成熟不是必需的,但在控制早期胚胎发育及诱导胚胎干细胞的多能分化中具有重要功能。本研究中OPU组SCNT胚胎的Sox2蛋白表达量高,进一步提示了OPU与屠宰场组SCNT重构胚的发育能力差异可能与其胚胎多能性分化能力相关。
本研究中OPU组SCNT重构胚的E-cadherin及Sox2蛋白表达均显著高于SLH组SCNT胚胎,表明OPU组SCNT重构胚细胞间具有更强的黏附能力和胚胎完整性,且高表达的Sox2蛋白可能上调了SCNT胚胎的干细胞向神经或生殖细胞方向分化,滋养层细胞分化后分泌合成更多的促生长发育因子,继而促进SCNT胚胎发育,但具体的信号传导通路仍需要进一步研究探讨。
4 结 论
本研究结果表明,OPU组卵母细胞的体外成熟效率显著高于SLH组的卵母细胞,OPU组SCNT重构胚E-cadherin和Sox2蛋白的表达水平显著高于SLH组SCNT重构胚,初步揭示了SLH组SCNT效率低下的原因。 试验结果进一步解释了屠宰场来源水牛卵母细胞SCNT重构胚低发育潜能的原因,也为研究活体和屠宰场卵巢来源卵母细胞SCNT重构胚的后续发育潜力及相关信号传导提供理论基础。
