柠檬酸改性H-beta催化甲苯和叔丁醇烷基化
2022-02-12王园园宋华苑丹丹孙兴龙柳艳修
王园园,宋华,苑丹丹,孙兴龙,柳艳修
(1 东北石油大学化学化工学院,黑龙江 大庆 163318;2 大庆石化工程有限公司,黑龙江 大庆 163714)
对叔丁基甲苯(PTBT)是一种非常重要的化工原料,其下游产品对叔丁基苯甲醛、对叔丁基苯甲酸、对叔丁基苯乙腈、对叔丁基苄氯等都是十分重要的有机合成中间体,在医药、农药、染料、香料及食品添加剂等领域都具有十分广泛的应用。对叔丁基甲苯的传统合成路线是在HSO、HF、AlCl等催化剂的作用下,通过氯代叔丁烷、异丁烯、叔丁醇等烷基化试剂与甲苯进行Friedel−Crafts 烷基化反应获得,但这些合成过程存在设备腐蚀严重、产物分离困难、环境污染不容忽视等问题,因而工业化生产受到限制。
beta分子筛因其具有丰富的表面酸性,独特的微观孔道结构,在甲苯叔丁基化反应过程中表现出优异的催化活性。但beta 分子筛酸强度分布较宽,大量强酸的存在易引发异构化、过烷基化等副反应发生,造成对位选择性下降,催化活性降低。此外,beta 属于中等孔、高硅沸石分子筛,孔道相对较小,介于ZSM−5 分子筛和Y 分子筛之间。由于孔道的限制,过烷基化、聚合等生成的副产物易造成孔道堵塞,催化剂失活。因此,需要对其进行有效的二次改性处理,通过调变beta分子筛的孔道结构和酸性分布,改善beta分子筛的催化活性和稳定性。当前众多改性方法中,酸脱铝法因其反应条件简单缓和,改性后样品无明显缺陷,具有很强的应用潜力。
酸处理过程最常用的是无机酸,作为小分子酸,空间阻力小,扩散速度快,能有效深入到孔道内部进行脱铝。杨晓光等发现,采用硫酸处理Hβ 分子筛可有效提高其催化活性。刘晓玲等采用盐酸处理HEU−1 分子筛时发现,盐酸只能脱除HEU−1的非骨架铝,调变弱酸中心。但与水热处理结合后,能同时调变HEU−1的酸类型和酸密度,产生介孔。白国义等发现磷酸改性的H−beta分子筛的弱酸含量降低,但中强酸量显著增加,反应活性增强。无机酸酸性过强,易破坏骨架结构,且铝物种易残留在孔道内部无法脱除,应用受到限制。柠檬酸(HCA)是一种三元有机酸,和铝离子具有非常强的络合能力且配合物稳定,利用柠檬酸和铝原子之间强的配位作用,缓慢将分子筛中的铝原子从骨架脱出是提高分子筛硅铝比、丰富孔道、引入介孔同时改善热稳定性的有效方法。
1 材料和方法
1.1 催化剂的制备
Na−beta 分子筛(Si/Al=25),山东立元有限公司;H−beta分子筛按文献[7]方法制备。
取一定量的H−beta分子筛,在固液比为1g/10mL条件下,分别用0.1mol/L、0.25mol/L、0.5mol/L、1.0mol/L 的HCA 溶液在室温下处理24h,过滤、洗涤至中性,120℃烘干12h,550℃焙烧4h后冷却备用。经不同浓度HCA 溶液处理的H−beta 分子筛,记作HCA/H−beta,其中表示HCA 的物质的量浓度。
1.2 催化剂的表征
采用D/max−2200PC X 射线衍射仪(日本Rigaku 公司)对样品的物相结构进行表征,根据样品中2=22.5°处衍射峰的强度计算其相对结晶度;采用ΣIGMA 场发射扫描电子显微镜(德国Zeiss 公司)对样品的微观形貌进行表征;采用JEM−1010型透射电子显微镜(日本JEOL公司)对样品的微观孔道结构进行表征;采用Tensor 27 型红外光谱仪(德国Bruker公司)对样品进行红外表征;采用NOVA2000e 型比表面积及空隙分析仪(美国Quantachrome 公司)对样品的孔结构进行测定,用BET 法计算比表面积,BJH 法计算孔容和孔径分布,t−plot 法计算外表面积和微孔体积;采用Chembet−3000 型全自动化学吸附仪(美国Quantachrome 公司)进行氨气程序升温脱附分析。采用Tensor 27 型FTIR 仪(德国Bruker 公司)进行吡啶吸附测定。
1.3 催化剂的性能评价
催化剂的活性评价在高温高压反应釜中进行。活性评价条件:180℃,自生压力,甲苯10mL(94mmol),叔丁醇27mL(283mmol),催化剂用量为1.0g,溶剂(环己烷)用量60mL。反应产物用GC−14 型气相色谱仪(氢火焰离子检测器)进行分析,色谱分析条件为:SE−30毛细管柱,0.26mm×48m,初始柱温60℃,停留2min,再以15℃/min 的速率升温至200°C,停留10min。
2 结果与讨论
2.1 物理化学表征
图1 为HCA/H−beta 分子筛催化剂的XRD 图。由图1 可知,经HCA 处理后的H−beta 分子筛样品仍然保持了beta 分子筛的骨架结构,说明H−beta分子筛的晶体结构并没有因HCA 处理而发生明显变化。由表1 可知,低浓度HCA 改性后的H−beta衍射峰强度略有增强,而高浓度HCA改性后的H−beta衍射峰强度却明显下降。这是因为低浓度HCA对H−beta 的骨架结构无明显破坏作用,主要脱除非骨架铝和无定形铝,且具有一定的补铝功能,因而结晶度得以保持,甚至略有提高。但高浓度HCA 却因脱除部分骨架铝,导致晶格产生缺陷,结晶度降低。
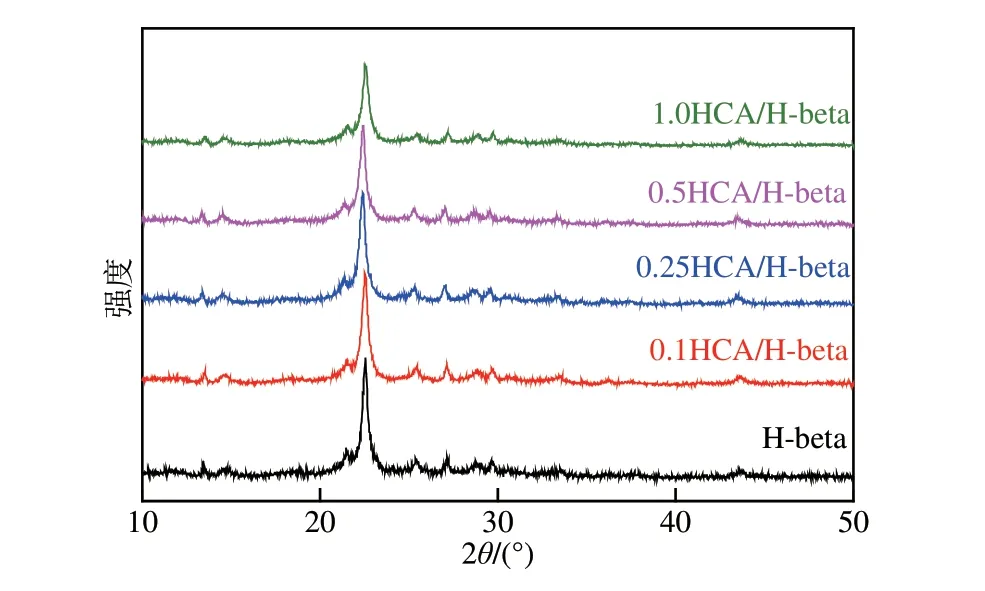
图1 xHCA/H−beta分子筛的XRD谱图
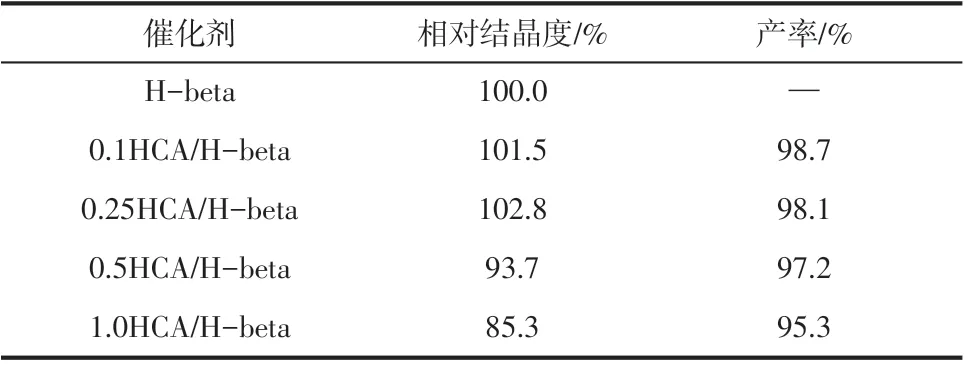
表1 HCA处理对H-beta分子筛结晶度和收率的影响
图2为H−beta和0.25HCA/H−beta分子筛的SEM图和TEM 图。由SEM 图可知,H−beta 分子筛为粒径约为300nm 的球形颗粒结构。HCA 改性后的H−beta分子筛样品的晶粒表面被刻蚀,但整体形貌未发生明显变化。由H−beta 和0.25HCA/H−beta 的TEM 图可知,经0.25mol/L 的HCA 酸处理改性后的H−beta依然保持高度有序的孔道结构。

图2 H−beta和0.25HCA/H−beta的SEM图和TEM图
H−beta、HCA 和HCA/H−beta 分子筛样品的FTIR 谱图见图3。由图3 可知,HCA/H−beta 的吸收振动峰较H−beta 差别不大,说明低浓度HCA 改性未对H−beta 分子筛的骨架结构造成影响,这与XRD 结果相吻合。众所周知,位于1089cm处的吸收峰为四面体内部反对称伸缩振动吸收峰,该峰与H−beta 沸石中骨架铝的含量有关,骨架铝含量增加,该峰向低波数方向移动。当使用0.1mol/L的HCA处理H−beta时,该数值变化很小,表明H−beta 骨架铝含量变化不大。当使用0.25mol/L 的HCA 处 理H−beta 时,该 数 值 从1089cm位 移 至1086cm,表明骨架铝含量有所增加,说明此时出现补铝现象。当采用1.0mol/L 的HCA 处理H−beta时,该数值从1089cm位移至1092cm,说明高浓度HCA处理H−beta时,骨架铝被大量脱除。此外,0.25HCA/H−beta 的红外谱图上没有出现HCA 的C= O伸缩振动吸收峰(1728cm),说明水洗过程可以去除残留的HCA。
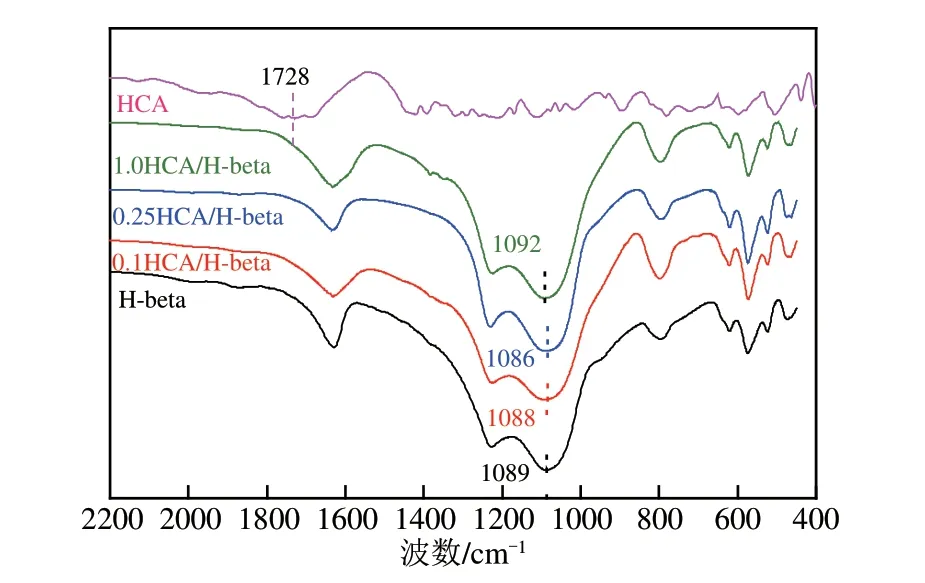
图3 HCA、H−beta及xHCA/H−beta的FTIR谱图
由表2 可知,与未改性H−beta 分子筛相比,HCA/H−beta 样品的比表面积、孔容、孔径较H−beta 样品都有所增加,说明HCA 改性能有效二次成孔,丰富孔道结构。当使用低浓度HCA(≤0.25mol/L)处理H−beta 分子筛时,和同时增大,表明低浓度HCA 处理H−beta 出现了新的微孔。这是因为低浓度的HCA 能优先脱除分子筛孔道内部的非骨架铝和无定形铝,疏通了原来堵塞的孔道,有效增加了微孔含量。颜曦明等则认为,微孔数量的增加源于HCA 处理过程中部分晶内悬挂键重新架键成桥,将部分大孔变成数个微孔。的增加是HCA改性将部分骨架铝以柠檬酸铝的形式脱除,微孔被腐蚀扩充形成介孔所致。上述实验结果表明,低浓度HCA 能够将部分非骨架铝和无定形铝通过酸洗脱除,使孔道更加畅通,改善了分子筛的空间性质。但当HCA 的浓度过高时,大量骨架铝被脱除,孔道结构遭到严重破坏。
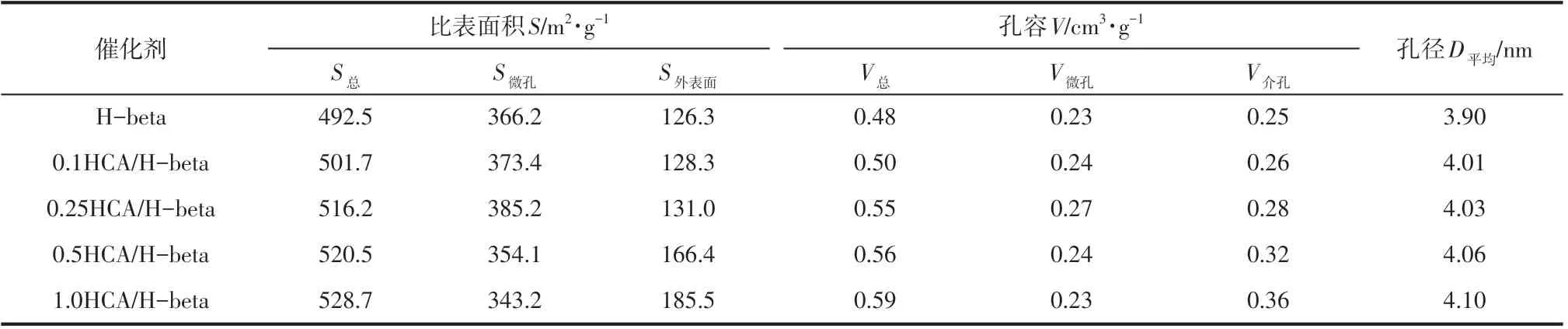
表2 xHCA/H-beta分子筛的结构性质
2.2 酸性表征
HCA/H−beta 样品的NH−TPD 谱图见图4。和未改性H−beta相比,HCA/H−beta的弱酸强度和酸量都呈明显的下降趋势,但强酸强度和酸量的变化却因HCA 浓度的不同而存在差异。当用低浓度HCA 改性处理H−beta 时,弱酸含量减少,强酸含量变化不大,而中强酸量却随着HCA 浓度的增加而增加,在HCA 浓度为0.25mol/L 时达到最大。这是因为低浓度HCA 主要脱除晶格中的弱酸中心,使得弱酸含量明显下降,而中强酸量增加可能因为补铝现象:HCA 中不但含有三个—COOH,还含有一个—OH,—OH的存在会降低脱除的骨架铝与柠檬酸之间的螯合程度,因此,一部分铝物种在溶液中能以Al和Al(OH)等阳离子的形式存在。在H的作用下,Al和Al(OH)水解生成的Al(OH)重新进入H−beta 分子筛骨架内部,实现了补铝。但当用高浓度HCA 改性处理H−beta 时,H−beta 分子筛的弱酸量和强酸量都明显下降,这说明高浓度HCA 还能脱除晶格中的强酸中心,使得H−beta 在高浓度HCA 处理后总酸量大幅下降。Xie 等认为,在HCA 处理H−beta 分子筛的过程中,在脱铝的同时也发生补铝现象。脱铝发生在H−beta分子筛骨架的Si(2Al)位,而补铝发生在Si(0Al)位。不同浓度的HCA 脱铝与补铝位置及数目有所差异,从而导致催化剂样品中酸量和酸强度的不同变化。
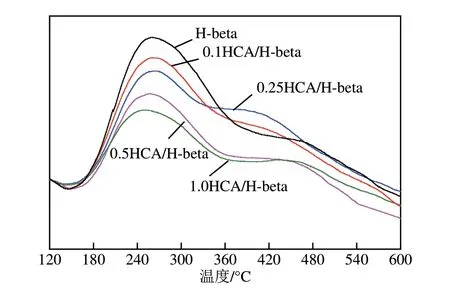
图4 xHCA/H−beta分子筛的NH3−TPD谱图
HCA/H−beta样品的Py−IR分析见图5和表3。其中1450cm附近的吸附峰归属于L酸中心,1540cm附近的吸附峰归属于B酸中心,而1490cm附近的吸附峰为L酸和B酸共同作用的结果。由图5和表3可知,HCA/H−beta 样品的B酸含量随着HCA 浓度的增加呈先增加后降低的趋势,而L酸含量则呈先降低后增加的趋势。这是因为酸处理过程能改变铝的状态和分布,在较低的HCA 下,优先脱除非骨架铝和缺陷位上的铝,L酸量降低,且未对晶体的组织结构造成影响。非骨架铝的脱除更加有利于孔道疏通,更多B酸中心暴露,B酸量增加。Xie 等认为B 酸量增大是H−beta 沸石的Si(1Al)及Si(2Al)配位总数增大导致的。但当HCA 浓度过高时,骨架铝脱除变成非骨架铝,造成B酸中心减少,L酸中心增加。L酸增加也可能是因为较高的焙烧温度下,部分B酸转化为了L酸。
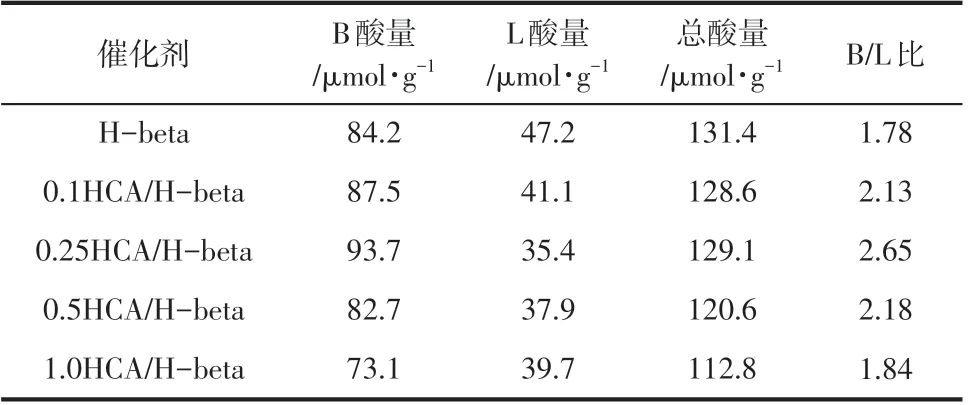
表3 xHCA/H-beta分子筛的酸性特征(Py−IR,150°C)
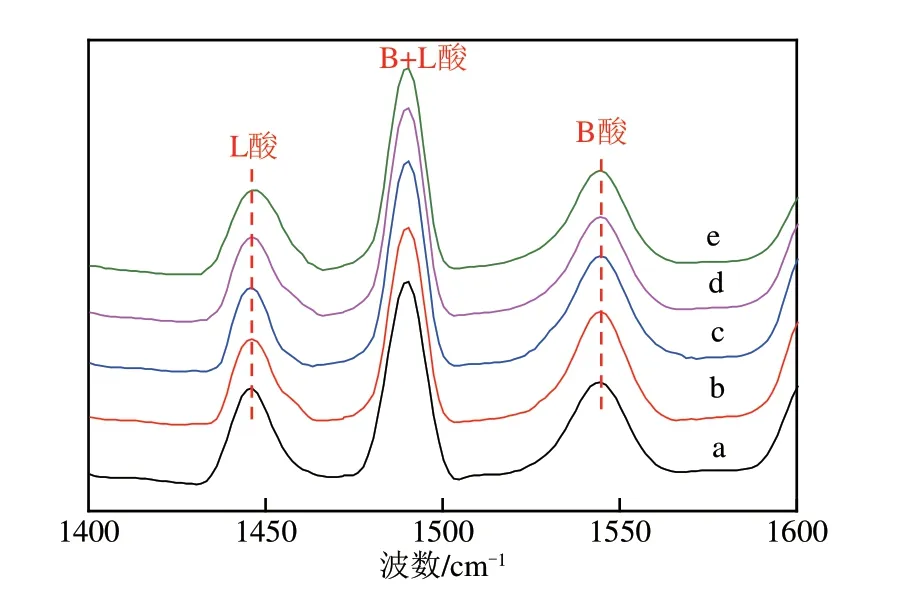
图5 xHCA/H−beta分子筛的Py−IR谱图
2.3 催化性能评价
表4为H−beta和HCA/H−beta分子筛催化剂的性能比较。从产物分布上看,H−beta 和HCA/H−beta分子筛催化甲苯和叔丁醇烷基化产物主要以对叔丁基甲苯(PTBT)为主、间叔丁基甲苯(MTBT)次之,而几乎无邻叔丁基甲苯生成(OTBT)生成。在三种异构化产物中,PTBT 占比最大是合理的。一方面,甲苯和叔丁醇的烷基化反应是芳环上的亲电子取代反应,遵循正碳离子机理,B酸为主要的活性中心。甲基作为邻对位致活基团,使得叔丁基正碳离子主要进攻甲基的邻位和对位。但是由于叔丁基体积较大,受空间位阻的影响,OTBT 很难生成,因而产物主要为PTBT。另一方面,从动力学角度分析来看,β沸石分子筛的12元环直通道的孔道开口尺寸为0.66nm×0.67nm,受择形催化作用的影响,具有线性结构的PTBT(动力学直径0.58nm)比非线性结构的MTBT(动力学直径0.65nm)更易从其孔道中扩散出来。因而,从上述两方面看,产物主要为PTBT。但实际产物分析中还会有一定比例的MTBT 生成,这是因为虽然MTBT 在动力学上不占优势,但MTBT在热力学上却更加稳定,生成的PTBT 会发生异构化反应生成MTBT,且该异构化反应主要发生在强酸中心上。此外,产物中还有微量的3,5-二叔丁基甲苯(3,5-DTBT),该过烷基化产物是PTBT 或MTBT 深度烷基化的结果,由于其分子尺寸较大,主要生成于催化剂的外表面。

表4 xHCA/H-beta分子筛催化甲苯和叔丁醇烷基化性能的比较
由表4还可以看出,不同浓度柠檬酸改性后的H−beta 分子筛催化剂的酸性和孔道结构存在差异,从而表现出不同的催化活性和对位选择性。随着HCA浓度的增加,HCA/H−beta分子筛的催化活性呈先增加后降低的趋势,在HCA 浓度为0.25mol/L时,甲苯转化率达到最大(67.0%)。一方面,由BET 结果可知,低浓度HCA 改性可有效清除孔道中的非骨架铝和无定形铝,增加孔体积和比表面积,减少了孔道阻力,有利于反应原料和产物在孔道中的扩散,提高传质效率;另一方面,由酸性表征可知,低浓度HCA 改性可以改变分子筛的酸性质,使得中强酸和B酸含量增加。中强酸的存在能促进弱酸活性的发挥,B酸的增多有利于催化活性增强。但HCA浓度不宜过高,这是因为浓度过高,酸性太强,分子筛催化剂的骨架铝也会被脱除,导致晶体结构遭到破坏,酸性中心减少,活性降低。此外,适宜的HCA改性也有利于PTBT选择性的提高,这可能是因为强酸含量的降低有效抑制了异构化反应的发生。H−beta和HCA/H−beta催化甲苯和叔丁醇烷基化反应的碳平衡都在94.2%以上。
3 结论
(1)适宜浓度的柠檬酸改性没有破坏H−beta分子筛的骨架结构,且在脱铝的同时兼具补铝功能,不但使得改性后的H−beta 分子筛孔道更加畅通,而且优化了铝在分子筛中的分布,增加中强酸和B酸含量,提高催化剂活性。
(2)催化剂的甲苯叔丁基化活性评价表明,较为适宜的柠檬酸处理浓度为0.25mol/L。在适宜的反应条件下,即催化剂1.0g、甲苯10mL(94mmol)、叔丁醇27mL(283mmol)、环己烷60mL、反应温度180℃、反应时间4h,甲苯转化率为67.0%,PTBT的选择性为80.4%。
