微波萃取–高效液相色谱荧光检测法测定食品包装用纸中11 种荧光增白剂
2022-01-27周良春马俊辉张晓飞文彬羽李双琦杨婷
周良春,马俊辉,张晓飞,文彬羽,李双琦,杨婷
[成都产品质量检验研究院有限责任公司,国家包装产品质量检验检测中心(成都),成都市产品质量监督检验研究院,成都 610100]
荧光增白剂(FWA)是一种能吸收太阳光中不可见的紫外光,再发射出可见蓝紫色荧光的有机化合物[1–2],该过程可淡化产品中的灰白色或微黄色,提高产品的亮度。因此,荧光增白剂在造纸、塑料制品、洗涤剂和化妆品等行业中得到广泛的应用[3–6]。但是,荧光增白剂对人体有害,若长期接触或者摄入会削弱人体免疫力和伤口愈合能力[7],甚至会有致癌的风险[8]。一些生产企业为了提高纸的增白效果,常将其用于纸及其制品(特别是食品包装用纸)中。食品包装用纸中的荧光增白剂可能会迁移至食品中,从而被人体吸收,对消费者的身体健康造成严重的损害。现行国家标准GB 4806.8—2016[9]明确规定食品包装用纸中不得检出荧光性物质。
目前,荧光增白剂的检测方法主要有紫外灯照射法[10]、紫外分光光度法[11]、荧光分光光度法[1,12]、高效液相色谱荧光检测法[2,8,13–17]和超高效液相色谱串联三重四级杆质谱法[18–19]。紫外灯照射法只能定性检测;紫外分光光度法和荧光光度法可以定量,但只能测定荧光增白剂总量;超高效液相色谱串联三重四级杆质谱法灵敏度高,能准确定性和定量,但仪器价格昂贵,检测成本较高,不利于实验室普及,且对预处理后的样品溶液净化要求较高;高效液相色谱法仪器价格相对较低,检测灵敏度较高,操作简便。利用高效液相色谱仪测定食品接触用纸中荧光增白剂含量已有文献报道[3,8,14,16],样品处理均用超声萃取仪。用微波萃取的方法提取食品包装用纸中的荧光增白剂未见报道。
笔者建立一种微波萃取高效液相色谱测定食品包装用纸中11 荧光增白剂含量的方法,缩短了样品萃取时间,提高了检测效率,降低了有机溶剂用量。
1 实验部分
1.1 主要仪器与试剂
高效液相色谱仪:Ultimate 3000 型,配FLD 检测器,赛默飞世尔科技(中国)有限公司。
纯水/超纯水一体化系统:Milli-Q Direct 16 型,美国密理博公司。
电子分析天平:ME204E–02 型,感量为0.1 mg,梅特勒–托利多仪器(上海)有限公司。
密闭式高通量微波消解/萃取仪:JUPITER A型,上海新仪微波化学科技有限公司。
智能酸度计:pHS–4C+型,分辨率可调(0.001,0.01,0.1),成都世纪方舟科技有限公司。
11 种荧光增白剂标准溶液:质量浓度均为100 μg/mL,福州绿川生物科技有限公司,各化合物CAS 号,化学式及代号、生产批号等信息见表1。
甲醇、乙腈和乙醇:均为色谱纯,赛默飞世尔科技(中国)有限公司。
三乙胺:分析纯,成都市科隆化学品有限公司。
四丁基溴化铵:分析纯,天津市科密欧化学试剂有限公司。
乙腈–水溶液:分别量取乙腈40 mL 和超纯水60 mL,将二者混合,再向混合液中准确加入0.6 mL分析纯三乙胺,搅拌,混合均匀。
食品包装纸样品:市售食品包装纸。
实验用水为超纯水。
1.2 标准溶液的配制
分别移取一定体积11 种荧光增白剂标准溶液于50 mL 容量瓶中,用乙腈–水溶液定容,配制成各组分质量浓度均为1 000 μg/L 的混合标准储备液,于4℃保存,有效期为一个月。
用乙腈–水溶液将11 种荧光增白剂混合标准储备液稀释至各组分质量浓度均分别为2、10、20、40、80、100、150 μg/L 的系列混合标准溶液。
1.3 液相色谱条件
色谱柱:Kromasil 100–5 C18柱(250 mm×4.6 mm,5 µm,瑞典Akzo Nobel 公司);柱温:35 ℃;进样体积:20 μL;检测波长:激发波长为362 nm,发射波长为410 nm;流动相:A 为甲醇–乙腈溶液(体积比为3∶2),B 为25 mmol/L 四丁基溴化铵溶液(含体积分数为5%的甲醇,并用三乙胺调节溶液pH 为8.0);流动相流量:1.0 mL/min;梯度洗脱程序如表2 所示。
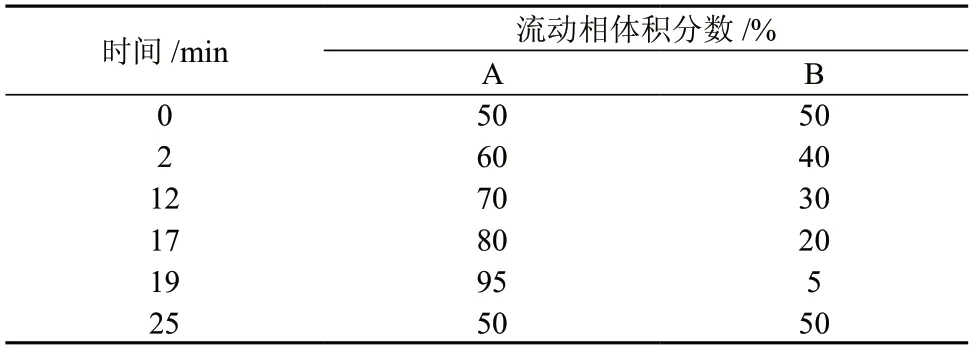
表2 梯度洗涤程序
1.4 实验方法
1.4.1 阳性样品的制备
将食品接触用包装用纸用剪刀剪成约为0.5 cm×0.5 cm 碎片,称取约0.25 g样品(精确至0.1 mg),置于微波萃取罐中,向其中加入一定量的荧光增白剂混合标准溶液,混匀,避光于4 ℃冰箱中存放24 h,待充分吸收后待测。
1.4.2 样品分析
将样品用剪刀剪成约为0.5 cm×0.5 cm 碎片,称取约0.25 g 样品(精确至0.1 mg),加入20 mL 乙腈–水溶液,于80 ℃微波萃取15 min,冷却,将提取液转移至25 mL 容量瓶中,再加入5 mL 上述萃取溶液洗涤,合并提取液,定容至标线,混匀,取2 mL提取液,过孔径为0.45 μm 的滤膜,用高效液相色谱仪测分析测定,以色谱峰面积标准曲线法定量。
2 结果与讨论
2.1 液相色谱条件的选择
2.1.1 激发波长和发射波长
利用液相色谱仪配置的荧光检测器对11 种荧光增白剂混合标准溶液进行光谱扫描,该11 种荧光增白剂的最大激发波长在360~363 nm 范围内,最大发射波长在408~410 nm 范围内。当选择激发波长为362 nm、发射波长为410 nm 时各物质均有较高荧光响应值,11 种荧光增白剂混合标准溶液3D光谱扫描如图1 和图2 所示。
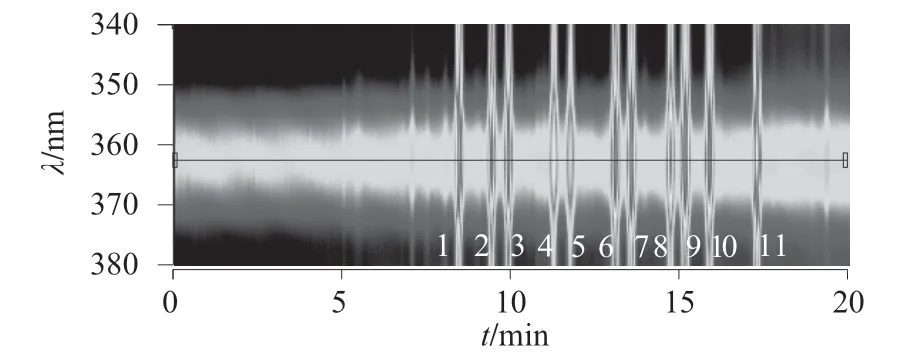
图1 11 种荧光增白剂混合标准溶液的激发光谱图
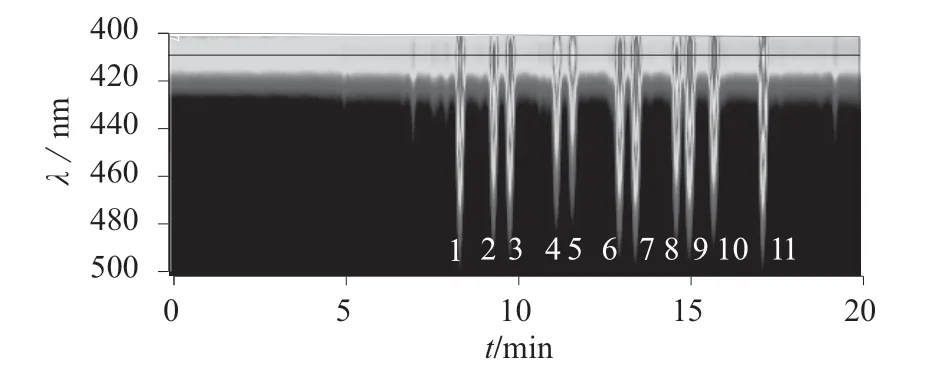
图2 11 种荧光增白剂混合标准溶液的发射光谱图
2.1.2 流动相
选取Kromasil 100–5 C18色谱柱(250 mm×4.6 mm,5 µm)为分析柱,进样体积选择20 μL,流动相流量选择1.0 mL/min。常用柱温为室温,升高柱温可以缩短液相色谱分析时间,提高检测效率。本次目标分析物有11 种,数量较多,当选择柱温为35℃时,各物质均能较好分离,且在18 min 内完全出峰。
甲醇和乙腈是液相色谱仪常用有机流动相。11种荧光增白剂含有磺酸基和苯基,可溶解于有机溶剂与水的混合溶液中,特别是乙腈的水溶液。标准混合溶液溶剂为乙腈水溶液,说明11 种荧光增白剂在乙腈水溶液中能较好的溶解。试验结果表明,若只用40%乙腈水溶液作为流动相,11 种荧光增白剂不能有效分离。参考韩晓鸥等[20]所提出的仪器条件,选择乙腈–甲醇溶液(体积比为3∶2)为流动相A,调节流动相B 进行优化。当流动相B 为体积分数5%的甲醇水溶液时,11 种荧光增白剂完全不能分离开,如图3(a)所示。因为11 种荧光增白剂分子中含有多个磺酸基团,极性较强,在C18柱中保留较差,均在3 min 内全部出峰。为了增强其在C18柱上的保留,加入正离子对试剂四丁基溴化铵(TBA)与磺酸基团结合来减小极性。所以,当流动相B 为10 mmol/L 四丁基溴化铵水溶液(含体积分数为5%的甲醇,并用三乙胺调节溶液pH 为8.0)时,11 种荧光增白剂除FWA 264 和FWA 353 外,其它均能较好分离,如图3(b)所示。当流动相B 中四丁基溴化铵的浓度增加至25 mmol/L 时,11 种荧光增白剂均能够完全分离,如图3(c)所示。同时,该类物质中含有多个磺酸基团,需要在碱性条件下才能确保待测物在与离子对试剂结合前充分离子化。韩晓鸥等[20]研究表明,pH 值为9.5~10 时,色谱峰会出现拖尾现象。本实验结果表明:当pH 为8.0 时,各物质色谱峰均较好。因此,流动相B 选择25 mmol/L四丁基溴化铵水溶液(含体积分数为5%的甲醇,并用三乙胺调节溶液pH 为8.0)。
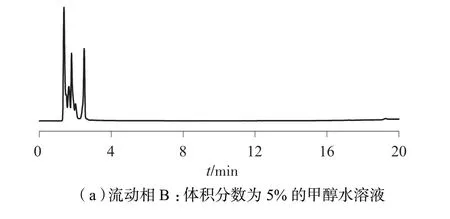
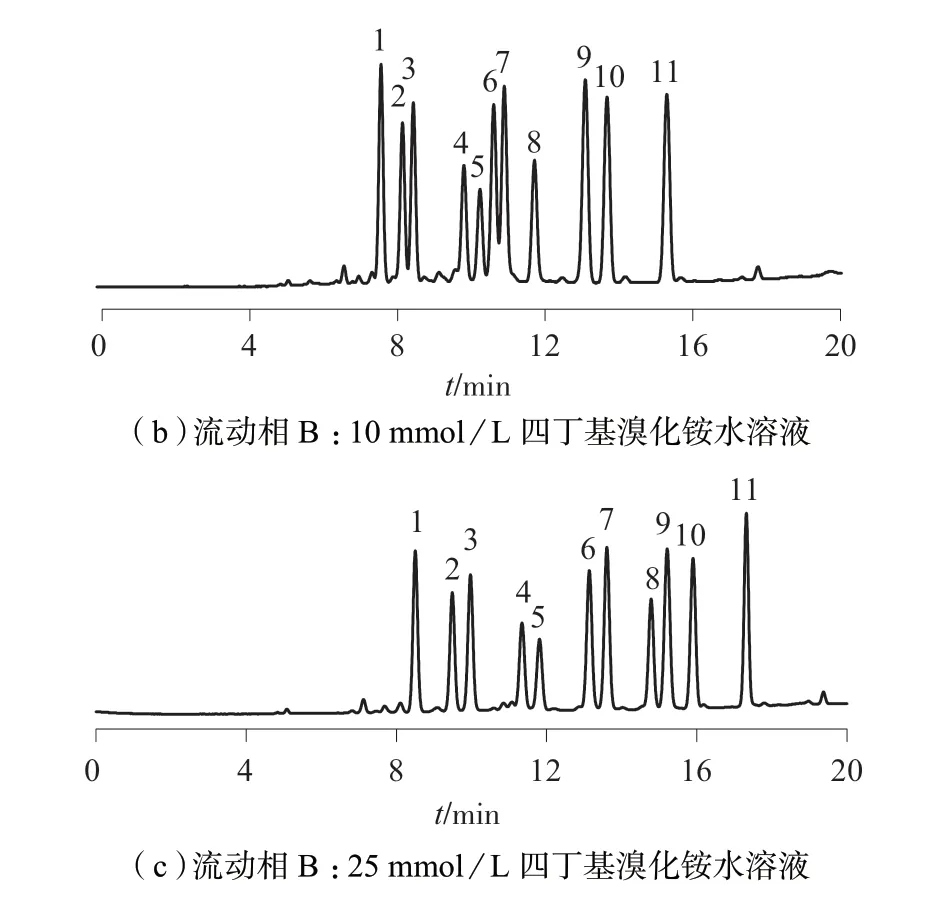
图3 不同流动相对应的11 种荧光增白剂的色谱图
2.2 样品前处理条件的选择
2.2.1 萃取溶剂
11 种荧光增白剂均为阴离子荧光增白剂,含有较多的非水溶性苯环,所以选择有机溶剂与水的混合溶液作为提取试剂。分别选择40%的乙腈–水、甲醇–水、乙醇–水溶液(均含0.6%的三乙胺)和乙腈–水溶液(不含三乙胺)作萃取剂,加入到已知含量的自制阳性样品中,按照1.4.3 的处理方法进行提取,计算各种荧光增白剂的回收率,绘制柱状图如图4 所示。
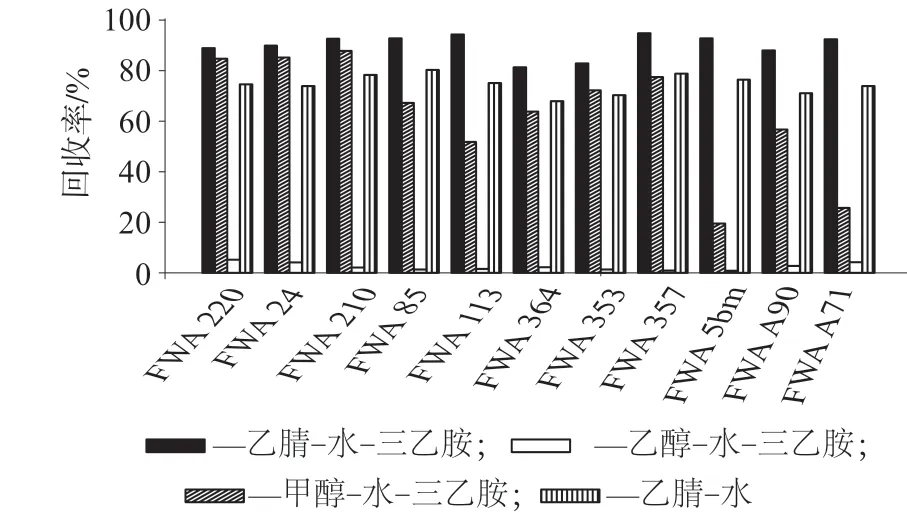
图4 不同混合溶剂提取时11 种荧光增白剂的回收率
由图4 可知,提取效率从大到小依次为:乙腈–水溶液(含三乙胺)>甲醇–水溶液>乙腈–水溶液>乙醇–水溶液。提取效率最好的溶剂为乙腈–水溶液(含三乙胺),这是因为该类阴离子型荧光增白剂在碱性条件下以离子形式存在,更易被提取。乙醇–水–三乙胺体系中的三乙胺使萃取液呈碱性,利于磺酸基以离子形式存在,但是该类化合物中的苯环等疏水基团在乙醇中溶解度很低,使乙醇–水溶液的萃取效率最低。
为了进一步优化萃取溶剂中乙腈与水的混合比例,分别选取乙腈与水的体积比为1∶4、2∶3、3∶2和4∶1(均含有0.6%的三乙胺)对阳性样品进行微波提取,试验结果如图5 所示。由图5 可知,当乙腈与水的体积比为2∶3 时,各种荧光增白剂的回收率均在80%以上,提取效率最高。随着水含量降低,各种荧光增白剂的回收率均迅速减小。这是因为荧光增白剂的磺酸基团为水溶性的,随着萃取剂中水含量降低,溶于萃取剂的荧光增白剂减少。综合考虑,选取乙腈–水的体积比为2∶3(含0.6%的三乙胺)作为萃取溶剂。
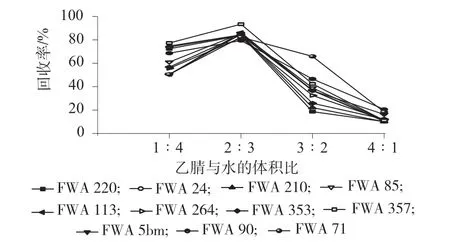
图5 不同配比乙腈和水萃取11 种荧光增白剂的回收率
萃取剂中三乙胺的主要作用是调节pH 值,使溶液呈碱性,以便各物质充分离子化和溶解。考察三乙胺的体积分数分别为0.2%、0.4%、0.6%、0.8%和1.0%时11 种荧光增白剂的荧光响应,结果表明,随着三乙胺含量增大,荧光增白剂FWA 220 的响应值也增大,当三乙胺体积分数为0.6%时,FWA 220的响应值不再变化,其余物质响应无明显变化。因此选择三乙胺体积分数为0.6%。
2.2.2 萃取时间
称取约0.25 g自制阳性样品(4份)于萃取罐中,分别向其中加入20 mL 乙腈–水溶液,于80 ℃分别微波萃取5、10、15 和20 min,考察萃取时间对荧光增白剂回收率的影响,试验结果如图6 所示。
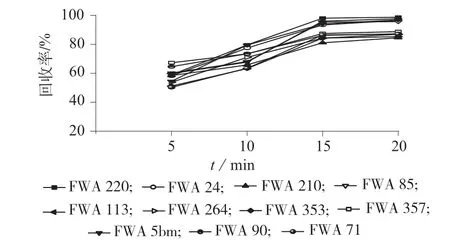
图6 不同萃取时间11 种荧光增白剂的回收率
由图6 可知,当萃取时间为15 min 时,各种荧光增白剂提取效率均达到较高水平(80%以上),萃取时间继续延长,回收率增大不明显。因此选择萃取时间为15 min。
2.2.3 萃取温度
分别选择萃取温度为60、70、80 和90℃,考察萃取温度对各种荧光增白剂回收率的影响。按照1.4.2样品处理方法,对自制阳性样品进行提取和测定,计算各种荧光增白剂的回收率,结果如图7 所示。
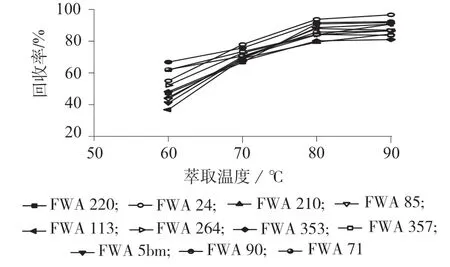
图7 不同萃取温度时11 种荧光增白剂的回收率
由图7 可知,随着萃取温度的升高,各种荧光增白剂的回收率逐渐提高,当萃取温度为80 ℃时,各种荧光增白剂回收率均大于80%,温度继续升高回收率提高不明显。因此选取萃取温度为80 ℃。
2.3 线性范围、相关系数、方法检出限和定量限
按照1.4.1 方法配制11 种荧光增白剂质量浓度均分别为2、10、20、40、80、100、150 μg/L 的系列混合标准溶液,在1.3 条件下测定。以各种荧光增白剂质量浓度为横坐标(X)、色谱峰峰面积为纵坐标(Y),绘制标准曲线,计算线性方程及相关系数。
用空白样品加标的方法,分别以3 倍信噪比和10 倍信噪比对应的标准溶液质量浓度作为各种荧光增白剂的方法检出限和定量限。
11 种荧光增白剂的质量浓度线性范围、线性方程、线性相关系数、检出限和定量限列于表3。由表3 可知,11 种荧光增白剂在2~150 μg/L 的质量浓度范围内,线性相关系数均不小于0.999 6,表明线性关系良好,满足测试要求。当称样量为0.25 g、定容体积为25 mL 时,样品中11 种荧光增白剂的检出限为0.1~0.2 mg/kg,定量限为0.3~0.6 mg/kg。
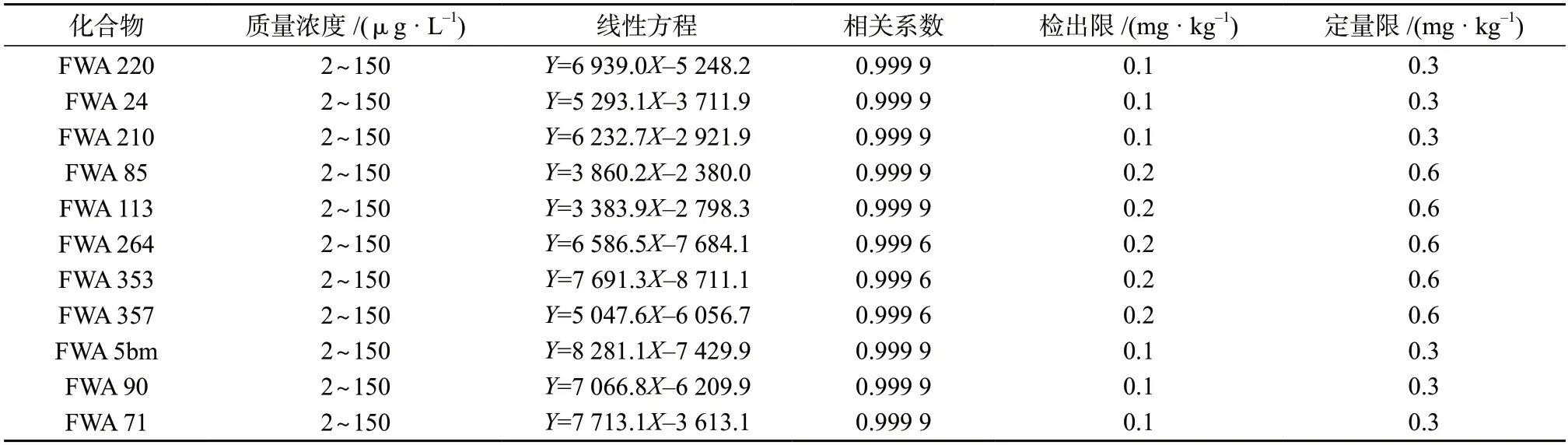
表3 11 种荧光增白剂质量浓度线性范围、线性方程、相关系数、检出限和定量限
2.4 加标回收和精密度试验
采用向阴性样品中加入标准溶液的方式进行加标回收试验。选择未检出荧光增白剂的食品接触用纸作为阴性样品,分别添加2.0、20.0 和100.0 μg/L 低、中、高3 个浓度水平的11 种荧光增白剂混合标准溶液,每个加标水平平行测定6 次,11 种荧光增白剂测定值、回收率和测定结果的相对标准偏差列于表4。
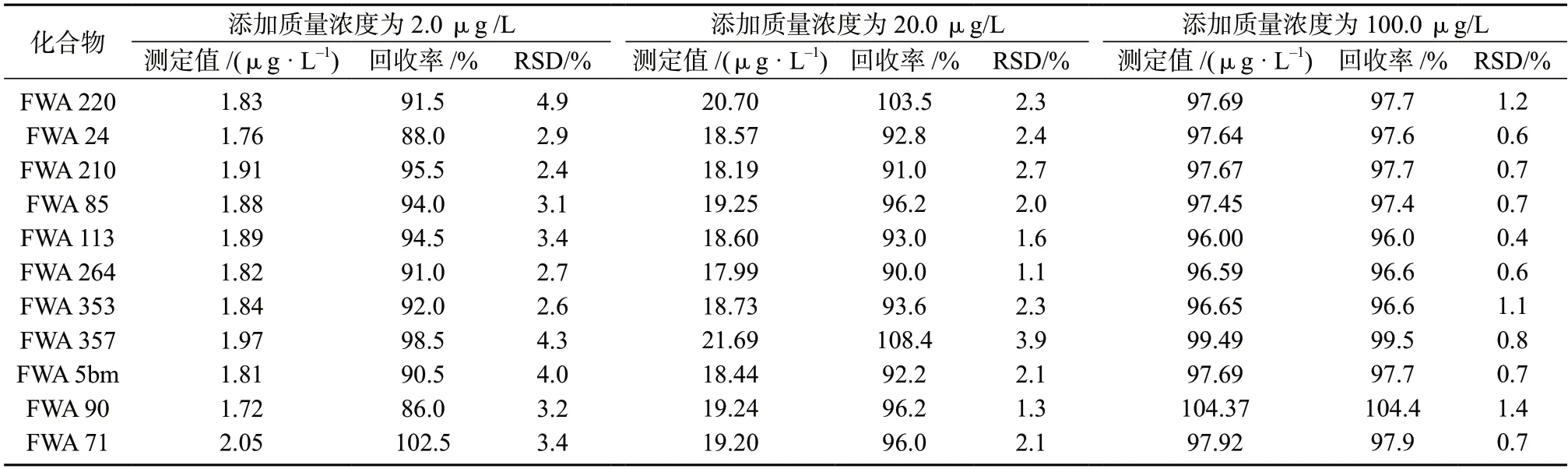
表4 加标回收和精密度试验结果(n=6)
由表4 可知,11 种荧光增白剂的加标回收率为86.0%~108.4%,相对标准偏差为0.4%~4.9%(n=6),表明该方法准确度和精密度良好,可用于食品接触用纸制品中荧光增白剂的检测。
3 结语
建立了检测食品包装用纸中11 种荧光增白剂的微波萃取高效液相色谱方法。该法样品处理快速、简便,使用有机溶剂少。该方法具有干扰小、分离效果好、灵敏度高、定量准确、重现性好等优点。
