曲妥珠单抗辅助治疗HER2阳性晚期胃癌的安全性及对患者血清肿瘤标志物的影响研究
2022-01-24史长山
李 红,史长山
(辽宁省健康产业集团铁煤总医院消化内科,辽宁 铁岭 112700)
胃癌为临床消化道常见恶性肿瘤之一,发病率、病死率均较高,早期无典型临床症状,诊断难度较高,早期确诊率低,易错过最佳手术治疗时期[1]。研究[2]指出,约11%的晚期胃癌患者在发生发展过程中可见人表皮生长因子受体2(HER2)阳性表达。目前,临床治疗HER2阳性晚期胃癌患者的主要疗法为药物化疗,常用药物为卡培他滨片+顺铂注射液,容易受到药物耐受、药品不良反应等因素的影响,影响化疗效果[3]。曲妥珠单抗为胃癌一线药物之一,其结合卡培他滨片+顺铂注射液方案对HER2阳性晚期胃癌的效果及安全性尚未完全明确[4]。本研究以200例HER2阳性晚期胃癌患者为研究对象进行前瞻性研究,旨在进一步分析曲妥珠单抗辅助治疗HER2阳性晚期胃癌的安全性及对患者血清肿瘤标志物的影响。报道如下。
1 资料与方法
1.1 一般资料
前瞻性选取2017年6月-2020年6月于辽宁省健康产业集团铁煤总医院消化内科就诊的HER2阳性晚期胃癌患者200例为研究对象,患者均知情同意,采用随机数表法将其分为曲妥珠单抗辅助组与常规组,各100例。曲妥珠单抗辅助组,男54例,女46例;TNM分期[5],III期60例,IV期40例;年龄40~75岁,平均(58.37±2.14)岁;发病位置,胃底部58例,胃体、胃窦部42例。常规组,男57例,女43例;TNM分期,III期62例,IV期38例;年龄42~75岁,平均(58.40±2.13)岁;发病位置,胃底部55例,胃体、胃窦部45例。2组一般资料比较,无统计学差异(P>0.05),具有可比性。
1.2 纳入与排除标准
纳入标准,1)HER2阳性晚期胃癌诊断符合《HER2阳性晚期胃癌分子靶向治疗的中国专家共识(2016版)》[6]中相关标准,并经超声胃镜、病理检查等确诊者;2)初治,依从性好者;3)有明确的病灶,TNM分期为III、IV期者;4)心电图、肝、肾功能及血常规等均在正常范围,但不具备手术指征者;5)预计生存期长于6个月者等。排除标准,1)伴有感染或组织创伤者;2)免疫力低下、有放疗史或激素替代治疗超过1个月者;3)胃癌分期存在分歧者;4)伴其他类型的恶性肿瘤者;5)伴有胃腺瘤样息肉、慢性胃炎等其他胃部疾病者;6)无法耐受曲妥珠单抗、顺铂、卡培他滨方案者等。
1.3 方法
常规组予以卡培他滨片(成都苑东生物制药股份有限公司,国药准字H20203570,0.5 g)+顺铂注射液(云南生物谷药业股份有限公司,国药准字H20043888,6 mL:30 mg)方案化疗:第1天以115 mg·m-2顺铂注射液静脉滴注,第1天~第14天口服1 000 mg·m-2卡培他滨片。曲妥珠单抗辅助组在常规组基础上予以8 mg·kg-1注射用曲妥珠单抗(上海复宏汉霖生物制药有限公司,国药准字S20200019,150 mg)静脉滴注,第1天使用。2组均以21 d为1个治疗周期,共治疗6个周期。
1.4 观察指标
1.4.1 临床疗效 参考《实体瘤治疗疗效评价标准-RECIST》[7]拟定。将2组治疗6个周期后的疗效分为疾病进展(PD)、疾病稳定(SD)、部分缓解(PR)、完全缓解(CR)。PD:基线病灶最大径之和增加高于20%,或出现新病灶;SD:基线病灶最大径之和缩小低于30%,或增加高于20%;PR:基线病灶最大径之和至少缩小高于30%,并维持1个月以上;CR:病灶均消失,并维持1个月以上;疾病控制率(DCR)=(CR+PR+SD)例数/总例数×100%;缓解率(RR)=(CR+PR)例数/总例数×100%。
1.4.2 血清肿瘤标志物 采集2组治疗前后的空腹静脉血3 mL,离心15 min(3 500 r·min-1),分离血清,以电化学发光法检测血清癌胚抗原(CEA)、糖类抗原724(CA724)、糖类抗原199(CA199)水平,检测仪为MPI-E电致化学发光检测仪(西安瑞迈分析仪器有限责任公司)。
1.4.3 血生化指标 血样采集及血清制备同1.4.2,以酶联免疫吸附试验检测2组血清N端脑钠肽前体(NT-proBNP)水平,试剂盒由武汉默沙克生物科技有限公司提供;以AU 5800全自动生化分析系统[贝克曼库尔特商贸(中国)有限公司]检测2组血清天冬氨酸转氨酶(AST)、血尿素氮(BUN)、丙氨酸转氨酶(ALT)、肌酐(Cr)水平。
1.4.4 不良反应发生情况 记录2组治疗期间肝功能损害、恶心呕吐、手足综合征、骨髓抑制等不良反应的发生情况。
1.4.5 生活质量评分 以生活质量核心问卷量表[8]评估2组治疗前后生活质量,包括认知功能、躯体功能、情绪功能、角色功能、社会功能,各项均为0~100分,得分越高提示生活质量越佳。
1.5 统计学方法
使用SPSS 21.0软件分析数据,计量资料以均数±标准差(±s)表示,组内比较使用配对t检验,组间比较使用独立样本t检验,计数资料以例(%)表示,χ2检验;以P<0.05表示差异有统计学意义。
2 结果
2.1 2组临床疗效结果比较
见表1。

表1 2组临床疗效结果比较(n= 100) 例
2.2 2组治疗前后血清肿瘤标志物水平比较
见表2。
表2 2组治疗前后血清肿瘤标志物比较(±s,n = 100)

表2 2组治疗前后血清肿瘤标志物比较(±s,n = 100)
注:与治疗前比较,# P<0.05;与常规组比较,△P<0.05
组别 时间 CEA/(ng·mL-1) CA724/(U·mL-1) CA199/(U·mL-1)曲妥珠单抗辅助组 治疗前 47.97±2.92 53.85±5.47 89.64±9.84治疗后 13.64±1.31#△ 24.76±2.25#△ 37.46±4.23#△常规组 治疗前 48.19±2.94 53.79±5.51 89.72±9.90治疗后 18.29±1.46# 36.83±4.40# 54.58±5.84#
2.3 2组治疗前后血生化指标比较
见表3。
表3 2组治疗前后血生化指标比较(±s,n = 100)
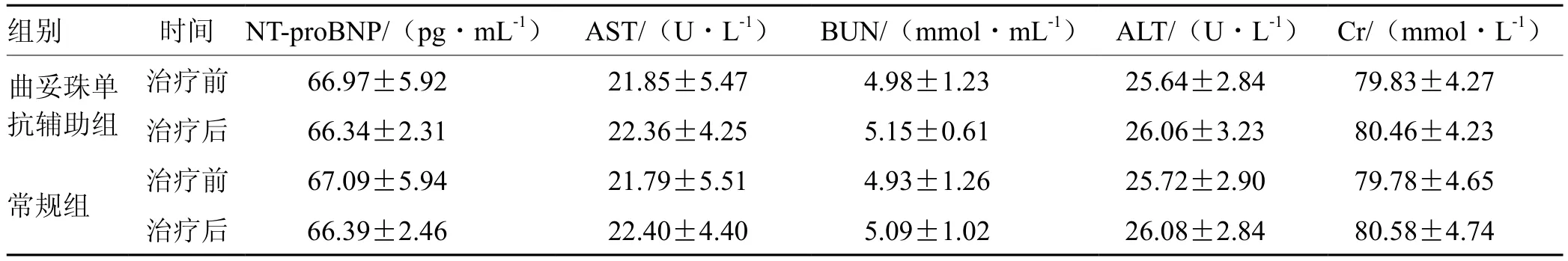
表3 2组治疗前后血生化指标比较(±s,n = 100)
组别 时间 NT-proBNP/(pg·mL-1) AST/(U·L-1) BUN/(mmol·mL-1) ALT/(U·L-1) Cr/(mmol·L-1)曲妥珠单抗辅助组治疗前 66.97±5.92 21.85±5.47 4.98±1.23 25.64±2.84 79.83±4.27治疗后 66.34±2.31 22.36±4.25 5.15±0.61 26.06±3.23 80.46±4.23常规组 治疗前 67.09±5.94 21.79±5.51 4.93±1.26 25.72±2.90 79.78±4.65治疗后 66.39±2.46 22.40±4.40 5.09±1.02 26.08±2.84 80.58±4.74
2.4 2组治疗前后生活质量比较
见表4。
表4 2组治疗前后生活质量比较(±s,n = 100) 分
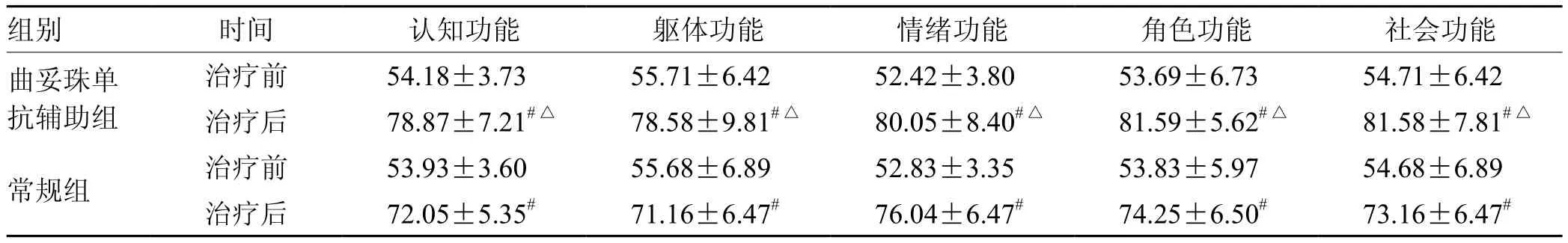
表4 2组治疗前后生活质量比较(±s,n = 100) 分
注:与治疗前比较,# P<0.05;与常规组比较,△P<0.05
组别 时间 认知功能 躯体功能 情绪功能 角色功能 社会功能曲妥珠单抗辅助组治疗前 54.18±3.73 55.71±6.42 52.42±3.80 53.69±6.73 54.71±6.42治疗后 78.87±7.21#△ 78.58±9.81#△ 80.05±8.40#△ 81.59±5.62#△ 81.58±7.81#△常规组 治疗前 53.93±3.60 55.68±6.89 52.83±3.35 53.83±5.97 54.68±6.89治疗后 72.05±5.35# 71.16±6.47# 76.04±6.47# 74.25±6.50# 73.16±6.47#
2.5 2组不良反应发生情况比较
见表5。
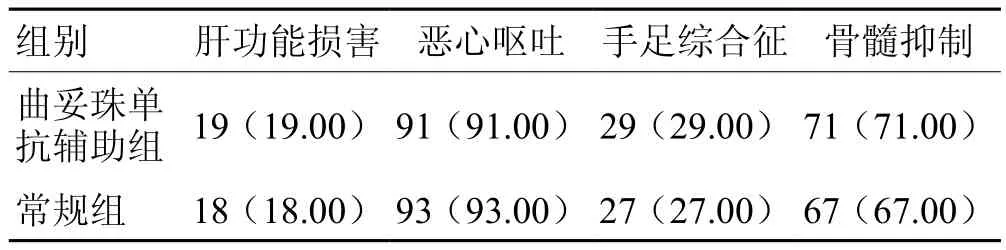
表5 2组不良反应发生情况比较(n= 100) 例(%)
3 讨论
目前尚无HER2阳性晚期胃癌相关的标准化疗方案[9-10]。卡培他滨片+顺铂注射液方案化疗,可有效降低HER2阳性晚期胃癌患者肿瘤细胞活性,控制其癌细胞生长、扩散,该方案虽起效迅速且持久,但化疗不良反应仍较为严重,容易对机体免疫功能产生一定的抑制作用[11-12]。近年来,随着分子生物学研究不断深入,HER2阳性晚期胃癌患者的分子靶向治疗已逐渐成为研究热点[13]。本研究采用靶向药物曲妥珠单抗辅助治疗HER2阳性晚期胃癌取得了较好的治疗效果。
HER2属于原癌基因之一,由1 382个胞嘧啶、922个腺嘌呤、880个胸腺嘧啶、1 346个鸟嘌呤组成,为表皮生长因子受体家族成员之一,有酪氨酸蛋白激酶活性,可参与调节细胞分裂、分化、增殖,促进肿瘤细胞增殖并抑制其凋亡,有助于增加肿瘤细胞的侵袭力,促进肿瘤血管、淋巴管新生促进病情进展,故HER2阳性晚期胃癌患者多预后较差[14-15]。曲妥珠单抗属于免疫球蛋白G抗体,由重组脱氧核糖核酸衍生所得人源化单克隆抗体,治疗HER2阳性乳腺癌疗效显著,可通过选择性作用于HER2阳性细胞的细胞外部分抑制HER2活性,进而抑制肿瘤细胞的生长[16]。本研究结果显示,治疗6个周期后,曲妥珠单抗辅助组DCR、RR分别为78.00%、49.00%,高于常规组的54.00%、27.00%,提示曲妥珠单抗辅助治疗HER2阳性晚期胃癌可提高临床疗效。
CEA、CA724、CA199均为临床常见肿瘤标志物。CEA为恶性肿瘤临床诊断的标志性抗原分子;CA724为新发现的一种高分子质量糖蛋白,诊断胃癌的灵敏性、特异性均较高;CA199为临床常用于胃肠道肿瘤筛查的糖蛋白;三者水平越高提示胃癌的恶性程度、胃癌细胞活力越高,且其水平升高可促进患者病情进展[17]。本研究结果显示,治疗6个周期后,曲妥珠单抗辅助组血清CEA、CA724、CA199水平低于常规组,生活质量各项评分(认知、躯体、情绪、角色、社会功能)均显著高于常规组,提示曲妥珠单抗辅助治疗HER2阳性晚期胃癌可降低患者血清肿瘤标志物水平,抑制病情进展,有助于提高患者生活质量。分析原因可能为曲妥珠单抗作为生物靶向治疗药物,结合常规化疗药物治疗HER2阳性晚期胃癌,可对HER2所介导的生物学效应产生抑制作用,有效杀灭肿瘤细胞,抑制血清肿瘤标志物水平异常升高[18]。研究[19-21]指出,曲妥珠单抗辅助治疗HER2阳性晚期胃癌可降低患者血清肿瘤标志物水平。本研究还发现,治疗6个周期后,2组血清NT-proBNP、AST、BUN、ALT、Cr水平及肝功能损害、恶心呕吐、手足综合征、骨髓抑制等不良反应发生情况比较差异无统计学意义,提示曲妥珠单抗的临床安全性良好,不会加重心、肝、肾功能紊乱,亦不会增加不良反应发生,但2组不良反应发生率均较高,进一步说明如何降低不良反应发生率仍为HER2阳性晚期胃癌患者治疗中需要重点关注的问题。研究[22-24]指出,曲妥珠单抗辅助治疗HER2阳性晚期胃癌患者安全、有效,不会加重心、肝、肾功能损伤。
综上所述,曲妥珠单抗辅助治疗HER2阳性晚期胃癌可降低患者血清肿瘤标志物水平,抑制病情进展,临床疗效显著,安全性良好,有助于提高患者生活质量。
