MSCT 对动脉导管依赖型肺动脉闭锁合并室间隔缺损患者的肺血管发育情况的评估及其与血氧饱和度的关系△
2022-01-23张丽丽
罗 纯,席 悦,张丽丽,蒋 骏
[1.佛山市第一人民医院影像科,广东佛山 528000;2.广东省人民医院(广东省医学科学院)放射科,广州 510080;3.深圳市第二人民医院(深圳大学第一附属医院)医学影像科,广东深圳 518000]
肺动脉闭锁合并室间隔缺损(pulmonary atresia complicated with ventricular septal defect,PA/VSD)是一种少见的发绀型先天性心脏复杂畸形,自然死亡率极高,临床症状严重程度取决于心外体动脉支供应肺动脉血流的多少[1-4]。目前对于PA/VSD的分型与外科治疗策略尚未统一,Castaneda分型根据有无肺动脉主干、左右肺动脉汇合部及肺部血流供应来源分成4 型,动脉导管依赖型(包括Castaneda Ⅰ型及Ⅱ型)肺血流主要由未闭动脉导管供应[2,5]。不同于Castaneda Ⅲ型及Ⅳ型由于侧支血管的参与,循环及肺血的变化及影响较为复杂,动脉导管依赖型PA/VSD 患者固有肺动脉均存在,且主要由未闭动脉导管供血,对于这类患者,一般推荐新生儿期即应手术介入[6-7],手术的目的是建立肺动脉的前向血流,促进肺动脉及其分支的生长发育[3];但是也有很多学者认为对于一些危重患儿,存在许多不稳定因素,也不应一味的强求根治手术[8];所以术式的选择仍存在很多争议[1,6,8]。本研究回顾性纳入和分析了在广东省人民医院的先天性心脏病数据库中有完整临床及影像资料的99 例动脉导管依赖型PA/VSD 患儿,测量患儿术前多层螺旋计算机断层扫描(multi-slice computed tomography,MSCT)对肺血管评估的相关指标,并分析各项指标与手术策略及患儿术前血氧饱和度的关系。
1 材料和方法
1.1 一般资料
2007 年1 月至2015 年1 月于广东省人民医院接受MSCT 检查并最终手术确诊为动脉导管依赖型PA/VSD 患儿共99 例,男64 例(64.6%),女35 例(35.4%),年龄(706.15±141.09)d,体质量6.5(2.3~50.0)kg;根据Castaneda 分型,Ⅰ型PA/VSD 61 例,Ⅱ型PA/VSD 38 例;姑息手术36 例,根治手术63 例。99 例患者中12 例发生院内死亡,3 例因患者情况不佳进行二次根治术,2 例患者情况不佳,家属强行出院。所有患者临床及MSCT 影像资料完整。
1.2 心脏计算机断层扫描检查方案
患者术前心脏计算机断层扫描(computed tomography,CT)均在接受手术前4 周内进行。采用GE LightSpeed VCT 64 层CT 或Philips iCT 256 层CT 扫描仪进行扫描。在患儿自由呼吸状态下进行心脏CT 扫描,扫描范围自胸廓入口至左膈下2 cm。其中21 例采用回顾性心电门控扫描,78 例采用前瞻性心电触发扫描;对不能配合检查者给予镇静(口服水合氯醛,0.1 mg/kg)。对比剂采用非离子型对比剂(碘必乐,300 mgI/mL),剂量2 mL/kg,以高压注射器注入,流率0.2~2.0 mL/s。应用对比剂跟踪技术自动触发扫描。具体扫描参数详见文献[3]。
1.3 心脏计算机断层扫描图像评估及数据分析
图像数据均传至GE AW4.3 后处理工作站进行图像处理、测量及分析,重建方法包括多平面重建(multiplanar reformation,MPR)、最大密度投影(maximum intensity projection,MIP)及容积再现(volume rendering,VR)。如Nakata 等所描述的一样,本研究对患者左、右肺动脉大小的测量点选择在其分出第一个分支肺动脉之前。侧支的定义为从主动脉或分支发出的直径大于2 mm 的血管,测量点选择在近开口处的狭窄部位或近开口5 mm。肺静脉大小的测量点选择在左心房入口之前[9]。在经多平面重组后的图像上对相应血管截面进行ROI 手动绘制或直线测量,从而获得相应血管的断面面积和直径,具体测量如图1 所示。McGoon 比值(McGoon ratio,M 率)、肺动脉指数(pulmonary arterial index,PA;Nakata)、总的新肺动脉指数(total neopulmonary arterial index,TNPAI)及肺静脉指数(pulmonary vein index,PVI)的计算方法如下:M 率=(右肺动脉直径+左肺动脉直径)/隔水平处降主动脉直径;PAI=(右肺动脉面积+左肺动脉面积)/体表面积(body surface areas,BSA);TNPAI=(左肺动脉横截面积+右肺动脉横截面积+侧支横截面积)/BSA[3,5];PVI=所有肺静脉横截面积之和/BSA[4,9-10]。BSA 的计算采用Stevenson 公式:BSA=0.0 061×身高+0.0 128×体质量-0.1 529[4]。

图1 患者CT 各评价指标的测量示意图(①显示右肺动脉直径及横截面积的测量使用正交法于分出第一个分支肺动脉之前测量;②显示左下肺静脉直径及横截面积的测量使用正交法于左心房入口之前测量)
1.4 统计学分析
采用SPSS 19.0 统计分析软件。计量数据以()表示,采用t检验或U检验。对于分类变量以[n(%)]表示,采用卡方(χ2)检验或Pearson′s 确切概率法;采用Pearson 相关性分析分析各个影像评价指标与术前血氧饱和度(blood oxygen satura⁃tion,SaO2)之间的相关性。以P<0.05 为差异有统计学意义。
2 结果
2.1 不同手术方式患者的基线资料比较
在99 例患者中,合并畸形包括房间隔缺损30 例,永存左上腔静脉15 例,冠状动脉起源异常4 例,迷走左/右锁骨下动脉5 例,主动脉右弓右降3 例,镜面右位心1例,主动脉弓下左无名静脉1例,右心室肥厚1例及左主支气管动脉导管压迫至狭窄1例。姑息手术组与根治手术组患儿的年龄、性别比较,差异无统计学意义[(1.15±2.44)dvs.(2.38±4.41)d,P=0.128;男:63.9%(23/36)vs.65.1%(41/63),P=0.905];两组患者的体质量比较,差异有统计学意义[(6.46±4.3)kgvs.(9.64±8.41)kg,P=0.038]。
2.2 心脏计算机断层扫描检查结果
所有患者均诊断为PA/VSD,且心脏CT 图像均对畸形有良好的显示,并与手术结果完全符合。MSCT 对患儿的室间隔缺损,闭锁的肺动脉及动脉导管未闭(patent ductus arteriosus,PDA)及参与肺段供血的侧支均能够清楚显示(如图2),所有患儿肺动脉与右心室之间无直接连接,其中61例存在肺动脉主干,38例无明确的肺动脉主干。根治手术组与姑息手术组Castaneda 分型、是否有肺动脉主干及是否含有PDA 以外的侧支血管比较,差异无统计学意义[55.6%(20/36)vs.65.1%(41/63),P=0.349;19.4%(7/36)vs.17.4%(11/63),P=0.806]。姑息手术组与根治手术组患者的M 率、PAI、TNPAI、PVI 及SaO2比较,差异均有统计学意义(P<0.001),见表1。M率、PAI、TNPAI及PVI与术前SaO2有显著的正弱相关(P=0.009,r=0.261;P=0.036,r=0.210;P=0.006,r=0.272;P=0.004,r=0.286),且相关系数PVI >TNPAI >M 率>PAI,见图3。

图2 MSCT 显示患儿闭锁的肺动脉、未闭动脉导管及参与肺段供血的侧支的图像(①显示患者的左、右肺动脉;②显示未闭动脉导管,该患者PDA 汇入左、右肺动脉汇合部处明显狭窄;③显示降主动脉发出一条稍粗的侧支血管供应右上肺,侧支血管未见明确狭窄)

图3 M 率、PAI、TNPAI 和PVI 与术前SaO2的相关性分析散点图
表1 根治手术和姑息手术患儿的血氧和各影像评价指标的比较 [n,]
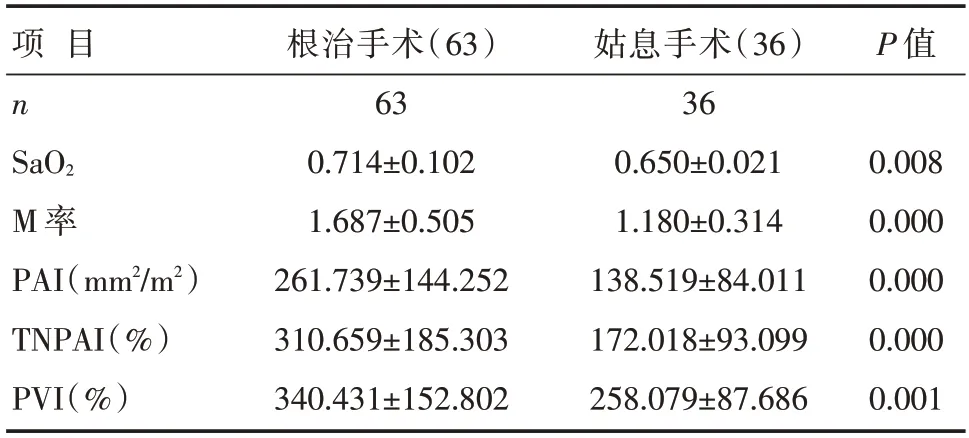
表1 根治手术和姑息手术患儿的血氧和各影像评价指标的比较 [n,]
3 讨论
PA/VSD 是临床少见的先天性心脏病复杂畸形,患儿自然病死率高,如不治疗,动脉导管依赖型患儿依旧有50%死于出生后6 个月[6]。近年来,针对PA/VSD 患儿的姑息及根治手术均广泛应用于临床。姑息手术包括右心室肺动脉连接术及体肺分流术,体肺分流术因可避免体外循环更为常见,室间隔缺损多维持开放;姑息手术目的是促进肺动脉及其分支的生长发育,手术难度较低,短期预后更佳;但有研究显示分流手术不能改善肺血管的发育,且分流管大小固定,与患儿发育不匹配,分流相关的并发症也是导致患儿多次手术及死亡的主要原因之一[1,8]。根治手术(右心室流出道重建加关闭室间隔缺损)较姑息手术难度明显增加,术后病死率增高,但是由于导管依赖型患儿全部或大部分的肺血流是由固有肺动脉供给,肺动脉往往发育较好,拥有较好的解剖学基础,且术后患儿的缺氧改善明显高于姑息手术,对患儿的症状及远期生长发育的改善更明显,也可避免多次手术带来的额外干预负担及持续的室间隔缺损分流,也更利于右心室流出道的重建;一些学者甚至认为当动脉导管依赖型患儿SaO2不低于75%~80%,而并不会导致右心室压力高于左心室,即可进行根治手术[1,6,11]。
本组患儿中,根治手术组与姑息手术组Cas⁃taneda 分型不同(是否存在肺动脉)、是否存在侧支血管比较,差异没有统计学意义(P=0.349,P=0.407,P=0.806)。动脉导管型PA/VSD 患儿侧支几乎不存在或仅存在一些细小侧支,对于肺动脉发育的影响较小,即使手术一般也不会造成局部肺血流过多的情况[1,7];另外随着术者经验的积累,肺动脉切开/下拉补片越来越多应用在PA/VSD 患儿,手术经验的积累使得肺动脉流出道重建术难度慢慢减低,对于动脉导管依赖型PA/VSD 患儿是否存在主肺动脉及侧支不再成为根治手术及姑息手术的选择因素;肺血管发育状况才是影响预后和治疗方案选择的主要因素。
目前MSCT被公认是PA/VSD患儿的常规检查,能够清楚地显示固有肺动脉发育情况,未闭动脉导管的位置或狭窄及周围结构关系,参与双肺供血的体肺侧支数量、起源及形态特点。肺血管床的发育程度和肺血流量反映了整个肺血管的功能情况,对PA/VSD 患儿治疗决策和预后判断有重要意义[11];一直以来,肺动脉的大小被用来判断肺血管床的发育情况,从而反映肺血流,用于定量评估适应证并制定PA/VSD 患儿的手术计划[2,3,5,12-13]。目前常用的评估肺血流量指标包括M 率和PAI 及TNPAI,2020 先天性心脏病外科治疗中国专家共识中也明确对于动脉导管依赖型PA/VSD 患儿,一期矫治术的手术适应证包括M 率≥1.2~1.5 及术前PAI 指数≥150 mm2/m2[3,5,11];本研究的MSCT 均良好地显示了患儿的畸形,且根治手术组患儿的M 率、PAI 及TNPAI 与姑息手术患儿比较,差异均有统计学意义(P<0.001,P<0.001,P<0.001),这也符合既往研究及专家共识[2,11]。虽然动脉导管依赖型PA/VSD 患者合并侧支较少,且肺血供还是主要由未闭动脉导管供应,但本研究发现还是有一些患者会合并一些小的侧支血管。虽然这些侧支较小,但是他们仍然参与肺的血供,相对于PAI,TNPAI 对这类患者肺血管床的评估应该更准确。
本研究中根治手术组患儿的术前经皮SaO2明显高于姑息手术组患儿(P=0.008),M 率、PAI、TN⁃PAI 及PVI 与术前SaO2有正向的弱相关。表明患儿SaO2在一定程度上与肺血管发育相关。单纯的肺动脉解剖预测的局限性在于肺动脉的解剖不一定与肺动脉功能完全统一相关[10-11];虽然M 率、PAI 及与TNPAI 是重要的解剖信息,临床结果具有一定的相关性[11],但也有人对这些动脉性指标是否能够真正反映肺血管床功能提出异议。Reddy等[11]研究认为TNPAI 能够更好地反映PA/VSD 合并侧支患儿肺血管床的发育情况;Honjo等[14]发现,TNPAI 与术后右心室收缩压并无显著关系,并不能很好地预测患者的预后。近年来,对于肺静脉是否能更好地反映肺血管床的发育也越来越引起学者的讨论,李渝芬等[9]的研究表明,PA/VSD 以及单心室的患儿左右肺静脉横截面积分别与左、右肺循环流量呈正相关;而在肺动脉,这种单侧的相关性不存在,说明肺动脉和肺静脉均反映肺循环流量和肺血管床发育,但肺静脉比肺动脉可能更有优势。Kawahira 等[10]的研究发现,在正常人和法洛四联症患儿的肺静脉面积与肺血流的相关性要优于肺动脉,特别对于PA/VSD 患儿,肺动脉往往发育不良,存在局限性狭窄及窄后扩张的情况,肺静脉指数的优势更明显,并且他们认为单侧肺血管发育情况可能与左、右肺血管发育不平衡的关系更密切;Jia 等[4]的研究结果也提示,PVI 似乎是肺血流更有用的形态学指标,有助于Ⅲ及Ⅳ型PA/VSD 患者的手术预后预测。本研究中,根治手术组与姑息手术组患儿的PVI 比较,差异均有统计学意义(P=0.001),且当与术前SaO2进行比较发现,相关系数PVI >TNPAI >M 率>PAI,PVI 与SaO2的相关性系数最高;虽然差异不大,但是否提示PVI 可以提供关于先天性心脏病患儿中肺组织血流量与血管阻力差异更重要信息?是否能够更好地反映肺血管床功能?
本研究的局限性:本研究尚需要更大宗的病例证明MSCT 得出的指标与SaO2的深层关系;本研究未对患儿的长期预后进行随访,这些影像指标与术后的血氧改善及患儿长期预后还需要进一步研究;对于左右肺血管发育不平衡目前尚没有比较完善的评估方法,还需要进一步研究其与患儿预后的关系。
综上所述,MSCT 能够很好地显示及评估动脉导管依赖型的PA/VSD 患儿的肺血管发育状况,及显示其他畸形;虽然目前主要仍然使用M 率、PAI指数指导临床手术方案的选择,但是本研究发现PVI 指数与患儿SaO2的相关性较动脉性指标更高,虽然差异不大,但是相关系数呈现的趋势可能说明肺静脉的评估可能较肺动脉更有意义。
