儿童患者西罗莫司血药浓度监测及临床应用分析
2022-01-18王漪檬马爱玲赵宁民马培志河南省人民医院郑州450003
王漪檬,马爱玲,赵宁民,马培志 (河南省人民医院,郑州 450003)
西罗莫司(sirolimus,SRL)是一种大环内酯类抗菌药物,起初作为低毒性的抗真菌药物被发现,后作为免疫抑制剂上市,主要适用于移植患者,预防器官排斥。既往研究表明,西罗莫司作为哺乳动物雷帕霉素靶蛋白(mammalian target of rapamycin,mTOR)的特异性抑制剂,可干扰细胞异常的生长和增殖,与肿瘤发生、血管生成密切相关[1-4]。故近年来临床也将西罗莫司用于治疗结节性硬化症、血管瘤、淋巴管畸形、白血病和蓝色橡皮疱痣综合征等[4-9]。
西罗莫司的治疗窗较窄,个体差异大,其治疗效果、不良反应的发生和严重性与其血药浓度相关,为了进一步完善临床合理用药,对西罗莫司进行血药浓度监测(therapeutic drug monitoring,TDM)是有意义且必要的[10-13]。目前临床对于儿童患者使用西罗莫司后的血药浓度研究数据严重不足,儿童临床试验开展困难,药动学行为个体差异较大[14-15],且年龄越小各种药代动力学参数越不稳定[16]。本研究回顾性分析了54例儿童患者应用西罗莫司后的血药浓度与相关的实验室指标,旨在为西罗莫司的合理应用提供参考。
1 资料和方法
1.1 仪器与试剂
西门子全自动生化分析仪Viva-E(Emit 2000均相酶免疫法)。雷帕霉素试剂盒(批号8S01953816),样本萃取液(批号8S079UL),雷帕霉素质控品(290),甲醇为色谱纯,SCILOGEX MX-S旋涡混合器,SC-3610低速离心机,LG16-A高速离心机。
1.2 临床资料
选取我院2019年12月1日至2020年12月1日使用西罗莫司的儿童患者(≤18岁),进行西罗莫司血药浓度监测共54例次。其中男37例(68.5%),女17例(31.5%);平均年龄为6.4岁(4个月~18岁)。
1.3 血样的采集与测定
首次取样应在给予起始负荷剂量后4日,即患儿体内药量达到稳态后,于当日清晨给药前,取静脉血约2 mL置于EDTAK2真空管中,上下颠倒混匀样本5~10次后,使用移液器吸取200 μL全血样品至离心管中,依次加入200 μL甲醇和50 μL样本萃取液,涡旋混匀至无血块,15 000 r/min离心5 min,取上清液至样品杯中,置于全自动生化分析仪中检测。
1.4 统计学方法

2 结果
2.1 西罗莫司血药浓度监测结果活体分析
西罗莫司血药浓度为1.8~35.0(8.7±5.9)ng/mL,其中血药浓度个体差异可达约20倍。我院54例患儿的西罗莫司血药浓度监测结果见图1。将西罗莫司血药浓度结果分为低(<4.0 ng/mL)、中(4.0~12.0 ng/mL)、高(>12.0 ng/mL)浓度三组,不同浓度患儿例数及中位血药浓度结果见表1。

图1 患儿西罗莫司血药浓度监测结果

表1 西罗莫司血药浓度
2.2 不同性别、不同年龄段患儿西罗莫司血药浓度
患儿性别、年龄与西罗莫司的血药浓度见表2。

表2 患儿性别、年龄和西罗莫司血药浓度比较
2.3 西罗莫司治疗不同疾病时血药浓度监测结果分析
51.9%的患儿采用西罗莫司治疗结节性硬化症,与治疗其他疾病相比,治疗该疾病时其西罗莫司血药浓度最低,为4.6(3.9)ng/mL。治疗血管瘤时,西罗莫司血药浓度最高,为11.5(4.7)ng/mL。可见使用西罗莫司治疗不同疾病时,临床实际监测到的血药浓度结果差异较大,见表3。

表3 西罗莫司血药浓度与疾病的情况
2.4 西罗莫司治疗结节性硬化症时血药浓度分析
结节性硬化症的患儿多合并癫痫症状,其中60.7%的患儿存在联合使用抗癫痫药物的情况,且有25.0%的患儿存在联合使用2种以上抗癫痫药物。其中联合使用丙戊酸的比例最高(57.1%),这种情况下,西罗莫司的血药浓度为6.3(5.5)ng/mL,丙戊酸的血药浓度为66.0(50.0)μg/mL,两者均在各自的治疗窗范围内。
2.5 西罗莫司血药浓度与实验室指标的统计分析
查阅文献,选择考察患者的天冬氨酸氨基转移酶(AST)、丙氨酸氨基转移酶(ALT)和中性粒细胞计数(NEU)等实验指标情况。结果显示,AST和西罗莫司全血谷浓度(CSRL)在0.01水平上呈正相关(r=0.458,P<0.05),即随着CSRL的升高,AST数值也随之升高,见表4。
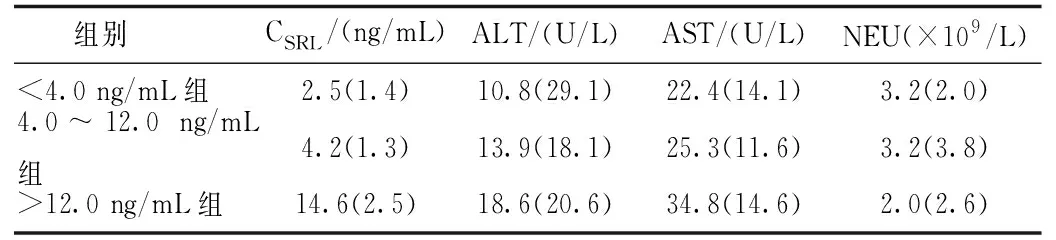
表4 儿童患者西罗莫司血药浓度-实验室指标情况
随着血药浓度的升高,ATL、AST和NEU的结果异常率也随之直线上升,即过高的血药浓度会导致肝功能和中性粒细胞异常率显著提升,见表5。

表5 西罗莫司血药浓度-实验室指标的异常率情况
3 讨论
3.1 西罗莫司血药浓度监测治疗窗的选择
关于西罗莫司治疗窗的确定,研究结论众多。如用于移植患者,全血药物浓度应根据免疫风险、转化时间和其他免疫抑制药物的使用,为5.0~15.0 ng/mL[10];用于结节性硬化合并癫痫的患者为5.0~10.0 ng/mL[14];用于蓝色橡皮疱痣综合症患者为2.5~12.0 ng/mL[9]。因此,本研究将西罗莫司血药浓度4.0~12.0 ng/mL作为治疗窗,并将患儿分为低(<4.0 ng/mL)、中(4.0~12.0 ng/mL)、高(>12.0 ng/mL)三组进行比较分析。
3.2 实验室指标的选择
西罗莫司主要经肝脏代谢,肝功能可直接影响血药浓度[11,17]。但是,西罗莫司又会对患儿产生肝毒性[13],包括全血谷浓度升高(即超过治疗浓度水平)后出现致命性肝坏死。另外,肝功能异常和NEU减少症都是儿童患者使用西罗莫司后常见的不良反应[1]。因此,本研究将ALT、AST和NEU与血药浓度结合进行分析。结果显示,使用西罗莫司的患儿中,25.9%出现了肝功能异常,22.2%出现了NEU减少。特别是在高浓度组中,45.5%的患儿出现ALT、AST或NEU异常的情况。在进行实验室指标与血药浓度的相关性的统计分析中也发现,AST与血药浓度呈正相关(r=0.458,P<0.01),此现象在接受肾移植的成年患者中也有过报道[18],但在儿童患者中为首次发现。综合肝功能异常率和NEU减少率,提示临床使用西罗莫司时不仅要注意用药剂量,定期监测其血药浓度,还要同时注意相关实验室指标异常的出现。
3.3 影响西罗莫司血药浓度的因素
遗传因素如基因型可影响西罗莫司的血药浓度[19-21]。基因(CYP3A4、ABCB1等)多态性可改变药物的体内处置状态,使血药浓度随之变化,从而影响治疗效果,如CYP3A4可参与西罗莫司的体内代谢过程。*3/*3 基因型患者与*1/*1和*1/*3患者相比,其西罗莫司的体内代谢较慢,可适当降低给药剂量。
非遗传因素如食物也可影响西罗莫司的血药浓度[22]。西罗莫司口服后可快速吸收,绝对生物利用度约15%,但变异度较高,饮食可显著影响其生物利用度,如葡萄柚汁可升高其浓度;高脂饮食可使其平均总暴露量(AUC)增加23%~35%[13]。另有文献报道[22],将使用西罗莫司的患者从喂养状态切换到禁食状态后,其血药浓度突然下降。
联合用药与西罗莫司的血药浓度也密切相关。经肝药酶CYP3A4代谢并抑制CYP3A4活性的药物如环孢素、红霉素、伏立康唑等可抑制西罗莫司的代谢,使其血药浓度增加,易出现不良反应。另外,一些肝药酶诱导剂如利福平[22]、苯妥英钠、丙戊酸钠、卡马西平等均能降低西罗莫司的血药浓度,从而导致监测结果偏低。
患者的感染状态也会影响西罗莫司的血药浓度[22]。有病例报道当患者出现发热咳嗽等流感症状时,西罗莫司血药浓度会突然升高。
虽然影响西罗莫司血药浓度结果的影响因素较多,但本研究将重点放于对血药浓度结果的回顾性分析和将之与实验室指标相结合,希望为临床使用西罗莫司提供参考。
西罗莫司血药浓度监测结果个体差异较大,其中37.1%的患儿血药浓度结果在治疗窗之外。与西罗莫司治疗白血病和血管瘤相比,治疗结节性硬化症时其血药浓度最低,这是与其疾病因素有关,因为结节性硬化症多合并癫痫,而多数抗癫痫药物(如苯巴比妥、苯妥英钠、卡马西平等)为肝药酶诱导剂或抑制剂,当西罗莫司与抗癫痫药物联合使用时,必将直接影响其血药浓度。这一现象与已有研究结果相符合[23-24]。
由于使用西罗莫司的患儿较少,本研究纳入的样本量有限,需在今后的工作中进一步进行更深入的研究。
